绿脓杆菌
| 绿脓杆菌 | |
|---|---|
| |
| 科学分类 | |
| 域: | 细菌域 Bacteria |
| 门: | 假单胞菌门 Pseudomonadota |
| 纲: | γ-变形菌纲 Gammaproteobacteria |
| 目: | 假单胞菌目 Pseudomonadales |
| 科: | 假单胞菌科 Pseudomonadaceae |
| 属: | 假单胞菌属 Pseudomonas |
| 种: | 绿脓杆菌 P. aeruginosa
|
| 二名法 | |
| Pseudomonas aeruginosa (Schroeter, 1872) Migula, 1900
| |
| 模式菌株 | |
| RH 815 = ATCC 10145 = ATCC 10145-U = CCEB 481 = CCUG 551 = CCUG 28447 = CCUG 29297 = CFBP 2466 = CIP 100720 = DSM 50071 = IBCS 277 = IFO (now NBRC) 12689 = JCM 5962 = LMG 1242 = NCCB 76039 = NCIB (now NCIMB) 8295 = NCTC 10332 = NRRL B-771 = VKM B-588 | |
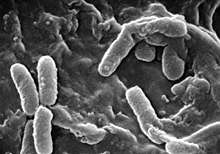
绿脓杆菌,又称铜绿假单胞菌(学名:Pseudomonas aeruginosa),是一种革兰氏阴性菌、好氧、呈长棒形的细菌,只有单向的运动性。[1]牠是一种机会性感染细菌,且对植物亦是机会性感染的。[2]
与其他假单胞菌属的细菌一样,绿脓杆菌分泌多种的色素,包括绿脓菌素(呈青色)、萤光素(呈萤光黄色)及绿脓菌红素(呈啡红色)。假单胞菌属培养基P就是用作增加绿脓菌素及绿脓菌红素的生产,而假单胞菌属培养基F就是加强萤光素的生成。[3]

绿脓杆菌的特征是牠那如珠母般的外形及在试管内的葡萄气味。临床确认绿脓杆菌的方法是在于绿脓菌素及萤光素的生成,且在42℃的环境下生长的能力。绿脓杆菌在柴油及航空燃料中仍能生长,更被称为“氢碳分解菌”,能引发微生物腐蚀作用。牠会产生一种暗色的凝胶垫,一般被误解为藻类。
名称由来
[编辑]绿脓杆菌的学名是Pseudomonas aeruginosa,当中的Pseudomonas是由希腊语的pseudo及monas所组成,意即虚假的单元,是早期微生物学用作描述病菌的。而Aeruginosa则是铜绿(即铜的氧化物),正好表达了这种细菌所产生的青色色素。绿脓菌素的生物合成是以群体效应来调控,就像充满囊肿性纤维化病人肺部绿脓杆菌的生物膜一样。
病因
[编辑]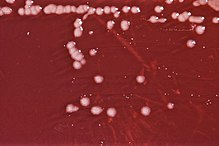
绿脓杆菌是一种令免疫受损的机会性感染病原,一般影响肺部及泌尿道,或造成烧伤、伤口及其他血液感染,如败血病。[4]虽然很不常有,但绿脓杆菌亦会造成肺炎。[5]在隐形眼镜清洁不完全的状况下也有机会造成眼睛角膜感染。在很多与呼吸器有关的肺炎研究中指出,绿脓杆菌是其中一种需要隔绝的细菌。[6]绿脓菌素(pyocyanin)-一种蓝绿色的有毒代谢物,就是绿脓杆菌的致病因子之一,且在氧化应激下能使秀丽隐杆线虫死亡,但是有研究指水杨酸能抑制绿脓菌素的生成。[7] 10%在医院感染的病症都是由绿脓杆菌所引致的。囊肿性纤维化病人的肺部是最先感染绿脓杆菌的一群。在缺乏适当处理食水质素下,牠亦是引致皮肤炎的其中一种细菌。牠也是造成烧伤感染最普遍的细菌。
- 绿脓菌素(Pyocyanin):抑制纤毛活动,且可扩散至细胞内导致氧化应激,使细胞死亡。
- 脂多糖(Lipopolysaccharide, LPS):促发炎细胞激素产生(TLR4感知),可导致血管内皮损伤甚至弥漫性血管内凝血(DIC)。
- 弹性蛋白酶(Elastase):分解组织胶原蛋白,破坏间隙促进细菌扩散。
- 磷脂酶C(Phospholipase C):水解细胞膜磷脂酰胆碱(Phosphatidylcholine),使细胞破裂,可导致β溶血(β-Hemolysis)。
- 外毒素A(Exotoxin A):最主要致病因子,属于A-B毒素,B亚基结合目标细胞表面HB-EGF内吞后,A亚基将NAD的ADP-Ribose转移至真核延伸因子-2 (Eukaryotic Elongation Factor-2)上(也就是ADP-核糖基化),使tRNA无法将氨基酸接至胜肽链上,阻止蛋白质合成,最终导致细胞死亡。
实验室检测
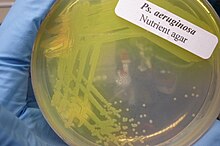
[编辑]绿脓杆菌的黏液菌株最常由囊性纤维化患者的肺组织中分离出来。绿脓杆菌可以在多种培养基上培植出黄绿或黄棕色的菌落,包括非选择性的血琼脂和选择性的马康基氏琼脂(只能培植革兰氏阴性菌)。检测绿脓杆菌主要是基于一系列的生化及诊断学测试。绿脓杆菌常带特征性水果味,此可作为实验室及临床诊断绿脓杆菌感染的线索。[9]
绿脓杆菌会产生抑制细胞蛋白质的合成作用的外毒素A(exotoxin A),并且会产生损害人类鼻纤毛功能和破坏呼吸道上皮的绿脓菌素(pyocyanin),这种蓝色色素也是吞噬细胞的促炎因子之一。此外,绿脓杆菌还会产生其他三种可溶性蛋白──细胞毒素(25kDa),又称为杀白细胞素(leucocidine)〉和两种溶血素,一个是磷脂酶(phospholipase),另一个是卵磷脂酶(lecithinase)。绿脓杆菌产生的黏液外多糖(mucoid exopolysaccharide)称为藻酸盐(alginate),其黏液会形成生物膜,协助细菌附着,使宿主的防御机制无法攻击细菌,如淋巴细胞、巨噬细胞、呼吸道的纤毛作用、抗体或补体作用。藻酸盐也是甘露糖醛酸(mannuronic acid)和葡萄糖醛酸(glucuronic acid)的重复聚合物[10]。
而目前已知不带毒力作用的萤光嗜铁素Pyoverdine和绿脓菌素(Pyocyanin)结合,在紫外光(Woods light)激发下,
出现绿脓杆菌特异性的亮绿色萤光,培养基所含的Cetrimide具选择性
可抑制部分G(+)及G(-)菌生长,而氯化镁和硫酸钾可帮助Pyoverdine产生。[11]
目前在临床上,也可使用MALDI-TOF-MS进行快速鉴定。[12]
治疗
[编辑]绿脓杆菌经常会从有菌的环境(如口腔棉棒、痰或其他)下,虽不是感染,但只是定植。从这些有菌的环境中隔离绿脓杆菌须特别小心,而在进行前须得微生物学家或传染病学专家的意见。一般来说治疗是不需要的。
当绿脓杆菌从无菌环境(血液或骨骼)中隔离时,须小心地处理,及差不多每次也需要接受治疗。
绿脓杆菌天生对大部分抗生素有抗药性,而且能快速地产生抗药性突变。一般结合两种抗生素(氨基糖苷类抗生素,β-内酰胺类抗生素或喹诺酮类抗生素)采用进取的抗菌治疗。[9] 一般治疗须由实验室敏感性协助治疗,而非只凭经验选择抗生素的种类。若已经使用了抗生素,其繁殖情况必须尽力了解及经常检讨抗生素的效用。
能有效对抗绿脓杆菌的抗生素包括:
- 氨基糖苷类抗生素(庆大霉素、丁胺卡那霉素、妥布霉素、阿米卡星等)
- 部分喹诺酮类抗菌药(环丙沙星及左氧氟沙星,但不包括莫西沙星)
- 部分第三代(头孢哌酮、头孢他啶)及第四、第五代头孢菌素(头孢吡肟、头孢洛林等)以及头孢菌素复方制剂(头孢哌酮舒巴坦钠)
- 哌拉西林、替卡西林、羧苄西林、磺苄西林、阿洛西林、美洛西林、阿帕西林、卡茚西林、卡非西林(绿脓杆菌本质上能抵抗所有其他的青霉素类抗生素)
- 碳青霉烯(多利培南、美罗培南、亚胺培南、亚胺培南/西司他汀、帕尼培南、比阿培南,但不包括厄他培南)
- 氨曲南、卡芦莫南
- 多粘菌素类抗生素
- 磺胺嘧啶银(仅局部皮肤用药)
由于临床上绿脓杆菌全身感染患者(尤其是重症患者)一般为混合感染,故一般治疗全身感染时优先使用头孢菌素复方制剂(如头孢哌酮舒巴坦钠)或碳青霉烯(如亚胺培南/西司他汀)来确保抗菌谱能覆盖大部分致病菌,若样本检测出耐药绿脓杆菌菌株,则加用氨基糖苷类抗生素(一般是阿米卡星)或喹诺酮类(一般采用环丙沙星),若仍然耐药,则改用多粘菌素B。单环β内酰胺类抗生素和抗绿脓杆菌青霉素类则应用于局部轻症感染(如泌尿系统感染等)。
参考
[编辑]- ^ Ryan KJ; Ray CG (editors). Sherris Medical Microbiology 4th ed. McGraw Hill. 2004. ISBN 978-0-8385-8529-0.
- ^ Iglewski BH. Pseudomonas. In: Baron's Medical Microbiology (Barron S et al, eds.) 4th ed. Univ of Texas Medical Branch. 1996. (via NCBI Bookshelf) ISBN 978-0-9631172-1-2.
- ^ King EO, Ward MK, Raney DE. Two simple media for the demonstration of pyocyanin and fluorescin.. J Lab Clin Med. 1954, 44 (2): 301–7. PMID 13184240.
- ^ Todar's Online Textbook of Bacteriology. [2006-10-13]. (原始内容存档于2006-10-09).
- ^ Fine; et al. Prognosis and outcomes of patients with community-acquired pneumonia. A meta-analysis. JAMA. 1996, 275: 134.
- ^ Diekema DJ; et al. Trends in antimicrobial susceptibility of bacterial pathogens isolated from patients with bloodstream infections in the USA, Canada and Latin America. Clin Infect Dis. 1999, 29: 595.
- ^ Prithiviraj B, Bais H, Weir T, Suresh B, Najarro E, Dayakar B, Schweizer H, Vivanco J. Down regulation of virulence factors of Pseudomonas aeruginosa by salicylic acid attenuates its virulence on Arabidopsis thaliana and Caenorhabditis elegans.. Infect Immun. 2005, 73 (9): 5319–28. PMID 16113247.
- ^ Newman, John W.; Floyd, Rachel V.; Fothergill, Joanne L. The contribution of Pseudomonas aeruginosa virulence factors and host factors in the establishment of urinary tract infections. FEMS Microbiology Letters. 2017-08-15, 364 (15) [2019-11-03]. ISSN 0378-1097. doi:10.1093/femsle/fnx124. (原始内容存档于2019-11-16) (英语).
- ^ 9.0 9.1 Harvey, R.A. Champe P.C., Fisher B.D.(2007). Microbiology Lippincott's Williams & Wilkins
- ^ {吴俊忠、吴雪霞、周以正、周如文、胡文熙、洪贵香、孙培伦等十七人. 临床微生物学 细菌与霉菌学 第七版第一次印刷.台北市: 五南图书出版股份有限公司.2019年10月: 198. ISBN 978-957-763-609-6}
- ^ Oxoid - Product Detail. www.oxoid.com. [2019-11-03]. (原始内容存档于2019-11-11).
- ^ Cabrolier, Nadège; Sauget, Marlène; Bertrand, Xavier; Hocquet, Didier. Matrix-Assisted Laser Desorption Ionization–Time of Flight Mass Spectrometry Identifies Pseudomonas aeruginosa High-Risk Clones. Journal of Clinical Microbiology. 2015-04-01, 53 (4): 1395–1398 [2019-11-03]. ISSN 0095-1137. PMID 25653397. doi:10.1128/JCM.00210-15. (原始内容存档于2019-11-03) (英语).
