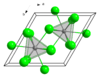
氯化钆
| 氯化钆 | |||
|---|---|---|---|
| |||

| |||
| 别名 | 三氯化钆 | ||
| 识别 | |||
| CAS号 | 10138-52-0 19423-81-5 (hexahydrate) | ||
| PubChem | 61486 | ||
| ChemSpider | 55406 | ||
| SMILES |
| ||
| InChI |
| ||
| InChIKey | MEANOSLIBWSCIT-DFZHHIFOAP | ||
| ChEBI | 37288 | ||
| 性质 | |||
| 化学式 | GdCl3 | ||
| 摩尔质量 | 263.61 g/mol g·mol⁻¹ | ||
| 外观 | 吸湿性的白色固体 | ||
| 密度 | 4.52 g/cm3 | ||
| 熔点 | 609 °C | ||
| 沸点 | 1580 °C | ||
| 溶解性(水) | 可溶 | ||
| 相关物质 | |||
| 其他阴离子 | 氧化钆 | ||
| 其他阳离子 | 氯化铕, 氯化铽 | ||
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |||
氯化钆是一种无机化合物,化学式为GdCl3,它是一种无色的、有吸湿性的固体,可溶于水。
制备[编辑]
氯化钆通常用氯化铵法制备,这中间包括初始合成的(NH4)2[GdCl5],这种物质的制备需要在230℃和氧化钆反应而得:[1]
- 10 NH4Cl + Gd2O3 → 2 (NH4)2[GdCl5] + 6 NH3 + 3 H2O
或者利用六水合氯化钆或金属钆和氯化铵的反应制得(NH4)2[GdCl5]:
- 4 NH4Cl + 2 GdCl3∙6H2O → 2 (NH4)2[GdCl5] + 12 H2O
- 10 NH4Cl + 2 Gd → 2 (NH4)2[GdCl5] + 6 NH3 + 3 H2
第二步,让(NH4)2[GdCl5]在300℃分解:
- (NH4)2[GdCl5] → GdCl3 + 2 NH4Cl
分解过程中,会产生中间体NH4[Gd2Cl7]。
氯化铵法是最常见的,并且比其他方法廉价。此外,金属钆在600℃与氯化氢气流作用,也能得到氯化钆:[2]
- Gd + 3 HCl → GdCl3 + 3/2 H2
氧化钆在红热时与氯气和二氯化二硫的混合气体作用,或和光气作用,也能得到无水氯化钆。[3]
2 Gd2O3+6 Cl2->4 GdCl3+3 O2[來源請求]
氯化钆可以形成六水合物(GdCl3∙6H2O),这个六水合物由可以氧化钆(III)溶于浓盐酸后,蒸发结晶出来。[4][3]
参考资料[编辑]
- ^ Meyer, G. The Ammonium Chloride Route to Anhydrous Rare Earth Chlorides-The Example of YCl3. Inorganic Syntheses. 1989, 25: 146–150. ISBN 978-0-470-13256-2. doi:10.1002/9780470132562.ch35.
- ^ Corbett, John D. Trichlorides of the Rare Earth Elements, Yttrium, and Scandium. Inorganic Syntheses. 1983, 22: 39–42. ISBN 978-0-470-13253-1. doi:10.1002/9780470132531.ch8.
- ^ 3.0 3.1 《无机化合物制备手册》.化学工业出版社.朱文祥 主编.P119. 【Ⅲ-169】三氯化钆(Gadolinium chloride)
- ^ Quill, L. L.; Clink, George L. Preparation of Lanthanide Chloride Methanolates Using 2,2-Dimethoxypropane. Inorganic Chemistry. 1967, 7 (7): 1433–1435. doi:10.1021/ic50053a032.
扩展阅读[编辑]
- Gadolinium. Magnetic Resonance TIP-MRI Database. [February 22, 2006]. (原始内容存档于2014-07-14).
- Gadolinium. Webelements. [February 22, 2006]. (原始内容存档于2008-04-19).
| |||||||