超临界流体
超临界流体(英语:Supercritical fluid, SCF)是一种物质状态,当物质在超过临界温度及临界压力以上,气体与液体的性质会趋近于类似,最后会达成一个均匀相之流体现象。超临界流体类似气体具有可压缩性,可以像气体一样发生泻流,而且又兼具有类似液体的流动性,密度一般都介于0.1到1.0g/ml之间。
接近临界点时,压力或者温度的小变化会使密度发生很大变化,因此使得超临界流体的许多特性可以被“精细调整”。超临界流体适合作为工业和实验室过程中的溶剂,而且可以取代许多有机溶剂。二氧化碳和水是最常用的超临界流体,分别被用于去除咖啡因和发电与萃取。
特性
[编辑]总体而言,超临界流体的属性介于气体和液体之间。在表1显示,显示一些常用作超临界流体的化合物之临界性质。
| 物质 | 分子质量 | 临界温度 | 临界压力 | 临界密度 |
|---|---|---|---|---|
| 克/摩尔 | K | 百万帕(标准大气压) | g/cm3 | |
| 二氧化碳(CO2) | 44.01 | 304.1 | 7.38 (72.8) | 0.469 |
| 水(H2O,依IAPWS资料) | 18.015 | 647.096 | 22.064 (217.755) | 0.322 |
| 甲烷(CH4) | 16.04 | 190.4 | 4.60 (45.4) | 0.162 |
| 乙烷(C2H6) | 30.07 | 305.3 | 4.87 (48.1) | 0.203 |
| 丙烷(C3H8) | 44.09 | 369.8 | 4.25 (41.9) | 0.217 |
| 乙烯(C2H4) | 28.05 | 282.4 | 5.04 (49.7) | 0.215 |
| 丙烯(C3H6) | 42.08 | 364.9 | 4.60 (45.4) | 0.232 |
| 甲醇(CH3OH) | 32.04 | 512.6 | 8.09 (79.8) | 0.272 |
| 乙醇(C2H5OH) | 46.07 | 513.9 | 6.14 (60.6) | 0.276 |
| 丙酮(C3H6O) | 58.08 | 508.1 | 4.70 (46.4) | 0.278 |
表2示出了典型的液体,气体和超临界流体的密度,扩散系数和粘度。
| 密度(kg/m3) | 黏度(µPa∙s) | 扩散系数(mm²/s) | |
|---|---|---|---|
| 气体 | 1 | 10 | 1–10 |
| 超临界流体 | 100–1000 | 50–100 | 0.01–0.1 |
| 液体 | 1000 | 500–1000 | 0.001 |
在超临界流体中没有液体及气体之间的相界限,因此不存在表面张力,借由改变流体的压力和温度,可以微调超临界流体的特性,使其更类似液体或是气体。物质在流体中的溶解度即为重要特性之一,在固定温度条件下,溶解度会随流体密度增加而增加。由于密度也是随压力增加而增加,因此在压力增加时,溶解度也会增加。溶解度和温度的关系比较复杂,在固定密度条件下,溶解度会随温度增加而增加,但靠近临界点时,温度轻微的增加会造成密度的大幅下降。因此靠近临界点时,随着温度上升,溶解度会先下降,然后再上升[2]。
二种以上的超临界流体,只要温度及压力超过其临界点,二者均可以混溶,形成单一相的混合物。二元混合物的临界点可以用二超临界流体的临界温度及临界压力,再配合加权平均求得:
- Tc(mix) = (A的摩尔分数)x A的Tc + (B的摩尔分数)x B的Tc
若要有更高的准确度,临界点可以用像是彭-罗宾逊物态方程之类的状态方程求得,或是用基团贡献(group contribution)法求得,像密度之类的其他性质,也可以用状态方程来计算[3]。
相图
[编辑]
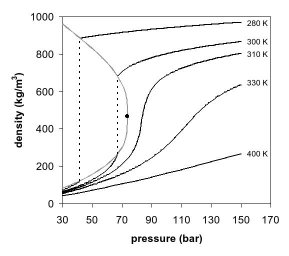
图1是二氧化碳的相图,在压力-温度的相图中,液态和气态为不同的二相,但若超过临界点,液态和气态的相态都消失了,变成单一相态的超临界流体。图2是二氧化碳密度-压力的相图,其中也可以看到类似的现象,当温度远低于临界温度280K时,随着压力的增加,气体会被压缩,最后(约40巴压力时)会凝结成密度高很多的液体,因此相图中有表示不连续的垂直虚线。此系统包括高密度的液体及低密度的气体,二者达到平衡状态。随着温度的升高,气体的密度会增加,而液体的密度会减少。在临界点304.1 K及7.38 MPa(73.8巴)时,液体和气体的密度相同,因此变成一均匀相(超临界二氧化碳)。
温度高于临界温度的气体无法单纯用加压的方式液化。若温度略高于临界温度(310K),压力在临界压力附近时,密度对压力的曲线几乎是垂直线,因此微小的压力变化就会使超临界流体的密度有很大的改变。像黏度、相对电容率及溶剂强度等物理量都和密度有关,在临界点附近这些物理量也会随压力有很大的变化。在温度更高时,超临界流体的行为开始类似气体,当温度到400K时,随着压力的变化,密度几乎呈线性的变化。
许多压缩气体其实都是超临界流体。例如氮的临界点是126.2 K(- 147 °C)及3.4 MPa(34巴),因此若压力容器中的氮气压力及温度大于临界点,氮气就已变为超临界流体。在室温下,氮气和氧气的温度远高于临界点,因此其特性类似气体。不过这些气体除非冷却到其临界温度以下,否则是无法液化的。
自然界的超临界流体
[编辑]海底火山
[编辑]
海底火山常见于海底的地表。有些在较浅海域的海底活火山会释放蒸汽及岩石碎片,而且喷出至较海平面高很多的高度。但许多海底火山在很深的海域,巨大的海水压力使蒸汽和气体无法爆炸性释放。例如深度超过3000米的海域,其压力到300个大气压,已超过临界压力的218大气压,而且喷口的水温也会超过374.2℃(≒374.15℃),因此喷口最热的水会变成超临界流体。
行星大气
[编辑]金星大气层含有96.5%的二氧化碳和3.5%的氮。金星表面压力为9.3百万帕(93巴),表面温度为735 K,压力及温度都高于主要成分的临界点,因此使金星表面大气成为超临界流体。
太阳系中的气态巨行星内部大气的主要成分是氢与氦,其温度远远高于临界点。木星和土星的大气,在星球表面为气态,往星球内部逐渐变为液体。但海王星和天王星上,这种转变还不太为人所了解。太阳系外行星巨蟹座55e和格利泽876d的理论模型,二者都沉积了以超临界水形式存在的海洋,底部是一层高压冰。
用途
[编辑]超临界流体萃取
[编辑]因为超临界流体具有低粘度和高扩散系数,因此相较于一般的液体萃取,超临界流体萃取可以有较快的萃取速度。借由调整超临界流体的密度,可以进行选择性的萃取,而且在不加压的情形下,超临界流体会蒸发,残留溶剂的量非常少,甚至没有残留。二氧化碳是最常用的超临界流体溶剂,大量用在生咖啡豆的去咖啡因制程,或是在啤酒制造中用来萃取啤酒花中的成分[4],或是从植物中提炼精油及药品。许多实验室的测试方法已将超临界流体萃取作为萃取的方式之一,取代使用传统溶剂的萃取法[5][6][7]。
超临界流体分解
[编辑]利用超临界水可气化生物质的特性,可以进行生物质的分解。[8] 这种生物质的气化可以用来制造烃类燃料,用在高效的燃烧装置中,或用于产生燃料电池所需要的氢气。在后者的应用,由于在水蒸汽转化过程中,水也可以参与反应,提供氢原子,因此氢气产量可以远高于生物质中的氢含量。
干洗
[编辑]超临界二氧化碳可以代替干洗中的四氟乙烯等传统有机溶剂,传统溶剂会污染环境,而超临界二氧化碳溶剂对环境友好,对健康无害,易于循环利用。超临界二氧化碳用于干洗的一缺点是,泄压过程中会对钮扣、拉链等造成损害。[9] 溶于超临界二氧化碳的清洁剂可以提高超临界二氧化碳的溶解能力。[10]
超临界流体色谱
[编辑]超临界流体色谱兼有气相色谱和高效液相色谱的优点。超临界流体色谱可以分析易挥发和热不稳定的分析物(气相色谱无法做到),还可以分析火焰离子化检测器(液相色谱无法做到),超临界流体色谱另外一个优点是能够产生比较窄的峰。不过实务上超临界流体色谱还不能完全取代广泛使用的气相色谱和液相色谱,只有在像手性分离及高分子量碳水化合物分析才会使用超临界流体色谱[11]。 制造业上已经有了模拟移动床装置。[12] 最终产物的纯度非常高,但成本也非常高,只适用于制备如药物等高价值的材料。
化学反应
[编辑]改变反应溶剂的条件,可以使反应体系为均匀相,便于反应进行,或者使体系发生相分离,以便分离反应产物。快速扩散能加快扩散控制型反应的进行。温度及压力可以调整反应依特定的反应路径进行,以产生特定的手性异构体[13]。超临界流体对环境的影响也比传统的有机溶剂要小。
制备药物共晶
[编辑]超临界流体是制备活性药物成分的新异晶体结构——药物共晶的新介质。药物共晶粒子可以通过超临界流体技术一步合成,这是传统方法很难甚至不可能做到的。超临界流体的多种性质(如超临界二氧化碳强溶解性、抗溶剂效应、雾化增强)可用于制备纯的和干燥的新药物共晶——由活性药物成分、由一种或多种晶格构象异构体组成的结晶分子络合物。[14][15]
制备纳米和微米粒子
[编辑]制备窄分布粒径的小粒子是制药业和其他工业技术上非常重要的过程。应用超临界流体可以有多种方法使溶质快速超过饱和点,比如通过稀释、减压,或二者兼而用之。这些过程在超临界流体里要比在通常的液体里发生得更快,使成核或失稳相分离压过晶体生长,产生非常小的、粒径均匀的粒子。超临界流体可以制出粒径大小在5—2000纳米范围内的粒子[16]。
超临界干燥
[编辑]超临界干燥是一种去除溶剂并且不引起表面张力效应的方法。随着液体的蒸发,表面张力会拖拽固体中的小结构,造成固体扭曲或收缩。在超临界条件下,不存在表面张力,清除超临界流体不会影响固体形状。超临界干燥用于制造气凝胶,干燥一些易被破坏的材料,如考古样品或是用于电子显微镜实验的样品[17]。
超临界水氧化
[编辑]超临界水氧化以超临界水作为介质,氧化危险废物和清除有毒燃烧产物。
超临界流体发电
[编辑]热机的热效率和高低温热源之间的温度差有关。若要调高发电厂的效率就需要调高工作温度。若用超临界的水做为工作流体,现在的技术可提升热机效率,由非临界条件下的39%提高到45%。[18] 超临界水反应堆是一种很有发展性的核系统,也可以依类似原理提高热效率,核系统中也可以使用超临界二氧化碳,有类似的效果。[19]。燃煤发电的超临界机组已经非常常见,比传统的火电厂效率提高很多。
历史
[编辑]1822年,卡尼亚尔·德·拉·图尔男爵在进行实验时发现超临界流体的特性,他将炮管密封,其中加入不同温度的流体,再放入燧石的小球,球在炮管中滚动时会有声音的不连续变化;但当温度超过临界温度时,声音的不连续变化消失了,炮管的流体中液体和气体的密度变得相同,变成一个超临界流体的相,因此也没有二相之间的相界限[20]。
参看
[编辑]参考资料
[编辑]- ^ Edit Székely. Supercritical Fluid Extraction. Budapest University of Technology and Economics. [2007-11-20]. (原始内容存档于2007-10-24).
- ^ Supercritical Fluid Extraction, Density Considerations. [2007-11-20]. (原始内容存档于2021-04-28).
- ^ A.A. Clifford. Calculation of Thermodynamic Properties of CO2 using Peng Robinson equation of state.. Critical Processes Ltd. 2007-12-04 [2007-11-20]. (原始内容存档于2008-05-05).
- ^ The Naked Scientist Interviews. [2007-11-20]. (原始内容存档于2015-04-16).
- ^ U.S.EPA Method 3560 Supercritical Fluid Extraction of Total Recoverable Hydrocarbons. http://www.epa.gov/SW-846/pdfs/3560.pdf Archive-It的存档,存档日期2008-12-17
- ^ U.S.EPA Method 3561 Supercritical Fluid Extraction of Polycyclic Aromatic Hydrocarbons. http://www.epa.gov/SW-846/pdfs/3561.pdf
- ^ Use of Ozone Depleting Substances in Laboratories. TemaNord 2003:516. 存档副本 (PDF). [2011-03-28]. (原始内容 (PDF)存档于2008-02-27).
- ^ Supercritical water gasification of biomas. Iowa Energy Center. [201-11-17]. (原始内容存档于2015-03-25).
- ^ 侯爱芹 戴瑾瑾. 二氧化碳在纺织领域应用的研究进展. 纺织导报. 2004, (2): 67–80.
- ^ Science News Online. [2007-11-20]. (原始内容存档于2013-05-09).
- ^ Bart, C. J. Chapter 4: Separation Techniques. Additives in Polymers: industrial analysis and applications. John Wiley and Sons. 2005: 212. ISBN 978-0-470-01206-2. doi:10.1002/0470012064.ch4.
- ^ Simulated Moving Bed Theory (PDF). [2007-11-20]. (原始内容 (PDF)存档于2004-08-29).
- ^ R. Scott Oakes, Anthony A. Clifford, Keith D. Bartle, Mark Thornton Pett and Christopher M. Rayner. Sulfur oxidation in supercritical carbon dioxide: dramatic pressure dependent enhancement of diastereoselectivity for sulphoxidation of cysteine derivatives. Chemical Communications. 1999, (3): 247–248. doi:10.1039/a809434i.
- ^ L. Padrela, M.A. Rodrigues, S.P. Velaga, H.A. Matos and E.G. Azevedo (2009). "Formation of indomethacin–saccharin cocrystals using supercritical fluid technology". European Journal of Pharmaceutical Sciences. 38, pp. 9–17. doi:10.1016/j.ejps.2009.05.010
- ^ L. Padrela, M.A. Rodrigues, S.P. Velaga, H.A. Matos and E.G. Azevedo (2009). "Screening for pharmaceutical cocrystals using the supercritical fluid enhanced atomization process". Journal of Supercritical Fluids. article in press, corrected proof. doi:10.1016/j.supflu.2010.01.010
- ^ Sang-Do Yeob and Erdogan Kirana. Formation of polymer particles with supercritical fluids: A review. The Journal of Supercritical Fluids. 2005, 34 (3): 287–308. doi:10.1016/j.supflu.2004.10.006.
- ^ http://dx.doi.org/10.1016/j.cemconres.2017.05.005
- ^ Supercritical steam cycles for power generation applications (PDF). [2007-11-20]. (原始内容 (PDF)存档于2008-12-17).
- ^ Dostal, M.J. Driscoll, P. Hejzlar. A Supercritical Carbon Dioxide Cycle for Next Generation Nuclear Reactors (PDF). MIT-ANP-TR-100. MIT-ANP-Series. [2007-11-20]. (原始内容 (PDF)存档于2010-12-27).
- ^ Berche, Bertrand; Henkel, Malte; Kenna, Ralph. Critical phenomena: 150 years since Cagniard de la Tour. Journal of Physical Studies. 2009, 13 (3): 3001–1–3001–4 [2013-03-19]. (原始内容存档于2021-04-17).
外部链接
[编辑]- Handy calculator for density, enthalpy, entropy and other thermodynamic data of supercritical CO2
- Food Product Design
- CO2 as a natural refrigerant - FAQs
- animated presentation describing what a supercritical fluid is
- NewScientist Environment FOUND:The hottest water on Earth (页面存档备份,存于互联网档案馆)

