鉛化合物

鉛化合物是含鉛元素的化合物,在這些化合物中,鉛主要呈現+2和+4價,其中+2價更穩定。無機的四價鉛化合物是強氧化劑。[1]鉛的含氧酸鹽大都是無色或白色的,低價氧化物和碘化物有着鮮艷的顏色,二氧化鉛和硫化鉛都是黑色的固體。



鉛化合物的化學性質
[編輯]多種鉛化合物能夠很容易地被還原為單質。如一氧化鉛(PbO)在加熱的時候可以被溫和的有機還原劑(如葡萄糖)還原。一氧化鉛和硫化鉛共熱,也能得到金屬鉛。[2]
- 2 PbO + PbS → 3 Pb + SO2
金屬鉛暴露於空氣中,表面會形成一層緻密的薄膜(含氧化鉛和鹼式碳酸鉛)以阻止向金屬內部的進一步氧化反應。鉛在硫酸和鹽酸中較為穩定,但是能溶於硝酸,形成硝酸鉛並放出一氧化氮:
- 3 Pb + 8 H+ + 8 NO−
3 → 3 Pb2+ + 6 NO−
3 + 2 NO + 4 H2O
鉛和鹼金屬硝酸鹽共熱,可以產生一氧化鉛(俗稱密陀僧),硝酸鹽則被還原為亞硝酸鹽。一氧化鉛可溶於硝酸和乙酸,形成的溶液能夠沉澱出微溶或難溶於水鹵化物、硫化物、硫酸鹽、碳酸鹽和鉻酸鹽。在鹵化物中,碘化物的溶解性比溴化物小,溴化物的溶解性比氯化物小。[3]
Pb+NaNO3–>PbO+NaNO2
氧化鉛溶解在鹼金屬氫氧化物溶液中,形成亞鉛酸鹽。亞鉛酸鹽和氯氣反應,可以得到二氧化鉛,其中鉛為+4價:[2]
- PbO + 2 OH− + H2O → Pb(OH)2−
4 - Pb(OH)2−
4 + Cl2 → PbO2 + 2 Cl− + 2 H2O
二氧化鉛是+4價鉛化合物的一個代表,它是一種強氧化劑。而+4價鉛的氯化物PbCl4則很不穩定,容易分解為PbCl2並放出氯氣。+4價鉛的溴化物和碘化物仍屬未知。[3]二氧化鉛溶解在鹼金屬氫氧化物溶液中,形成相應的鉛酸鹽。[2]
- PbO2 + 2 OH− + 2 H2O → Pb(OH)2−
6
鉛的另一種氧化物四氧化三鉛(Pb3O4)是混合價態氧化物,同時含有+2和+4價鉛。
1:1的鉛鈉合金可以和鹵代烴反應,產生有機鉛化合物,如四乙基鉛。[4]
氧化物和硫化物
[編輯]
鉛有多種氧化物,其中PbO、Pb3O4和PbO2是最常見的三種氧化物。PbO有兩種結構:α-PbO和β-PbO,這兩種氧化鉛都具有層狀結構,鉛原子都是四配位的。α-PbO是紅色固體,Pb–O鍵長為230 pm;β-PbO是黃色固體,Pb–O的鍵長為221和249 pm(不對稱的結構產生了兩種鍵長)。[5]由於兩種結構的相似性,它們都能在標準狀態下存在(其中β-PbO含有痕量(10−5)的雜質,如Si、Ge、Mo等)。PbO和酸反應形成鹽,和鹼反應生成[Pb(OH)3]−和[Pb(OH)4]2−。[6]
二氧化鉛可以由鉛鹽和鹵素作用產生。α型屬於三方晶系,β型屬於四方晶系。[6]兩種形態均是棕褐色固體,含有無法失去的水,加熱二氧化鉛會使其分解為一氧化鉛或四氧化三鉛。二氧化鉛是一種強氧化劑,可以氧化鹽酸和硫酸,分別放出氯氣和氧氣。它和強鹼反應,生成羥基鉛(IV)酸鹽,和鹼性氧化物反應,生成鉛(IV)酸鹽。[6]
鉛和硫或硫化氫反應,生成硫化鉛。硫化鉛屬於NaCl晶型,簡單立方結構,因而有着高熔點(1114℃)。在空氣中加熱硫化鉛,會得到一氧化鉛和硫酸鉛。[7]硫化鉛難溶於水、弱酸、硫化銨或多硫化銨溶液,這使得它在無機定性分析中和錫、砷、銻等元素分離。硫化鉛可溶於硝酸和濃鹽酸,分別生成硫和硫化氫。[7]硫化鉛和一氧化鉛共熱,可以得到金屬鉛:[2]
- 2 PbO + PbS → 3 Pb + SO2↑
鉛是ⅣA族中唯一能形成穩定的硫醇鹽的元素,硫醇(R−SH)和鉛(II)鹽反應,可以生成黃色的硫醇鉛沉澱。硫醇鉛易被氧化:[8]
- (RS)2Pb + I2 → R2S2 + PbI2
鹵化物
[編輯]

在氟化氫中加熱碳酸鉛,可以得到氟氫化物,熔融時產生氟化鉛。氟化鉛是白色晶體,比碘化鉛更易溶,但比氯化鉛和溴化鉛難溶。氟化鉛不能形成氟配位的化合物(PbF+陽離子除外)。[9]四氟化鉛是黃色晶體粉末,不穩定。
其它二鹵化物可以由鉛(II)鹽和其它金屬的鹵化物共熱得到,沉澱法或單質化合法亦可。這些鹵化物屬於正交晶系,其溶解度隨着溫度的升高而變大,向溶液中加入鹵化物會先降低其溶解度,之後由於形成配合物(最大配位數為6),溶解度再次增高。配合物的種類取決於離子濃度、鹵化物中鹼金屬的原子序數、鹵化物的種類、反應溫度及離子強度等因素。[10]四氯化鉛可以由二氧化鉛溶於濃鹽酸得到,易分解。氫溴酸和氫碘酸與二氧化鉛反應,只會得到二鹵化物及氧化產生的鹵素單質。[11]二砹化鉛也有報道。[12]
氯配合物
[編輯]鉛可以形成一系列的氯配合物,25 °C時,它們的平衡常數如下:[13]
- Pb2+ + Cl− → PbCl+, K1 = 12.59
- PbCl+ + Cl− → PbCl2, K2 = 14.45
- PbCl2 + Cl− → PbCl3−, K3 = 3.98 ×10−1
- PbCl3− + Cl− → PbCl42−, K4 = 8.92 × 10−2
甲胺鹽酸鹽和氯化鉛反應,可以得到甲銨氯鉛酸鹽([CH3NH3][PbCl3])。溴與碘的配合物也已製得。[14]
含氧酸鹽
[編輯]
鉛與硫酸或鹽酸無明顯作用,但是可以溶解在硝酸中,生成硝酸鉛(Pb(NO3)2)並放出一氧化氮。[9]硝酸鉛易溶於水,但在硝酸溶液中的溶解度較低。硝酸鉛於相應的陰離子反應,可以沉澱出鹵化鉛、硫酸鉛、鉻酸鉛、碳酸鉛或鹼式碳酸鉛等物質。[3]硝酸鉛於1597年首次在文獻中被描述,德國人安德烈亞斯·利巴菲烏斯在文獻中稱之為「甜蜜的鉛」,這源於硝酸鉛嘗起來的味道。[15]
乙酸鉛(Pb(CH3COO)2)又稱醋酸鉛、鉛糖,鉛糖一名也源於其甜味,過去曾作為甜味劑,後來人們發現食入乙酸鉛會導致鉛中毒,政府便禁止了這一添加劑。[16]乙酸鉛和硫化氫反應,可以產生黑色的硫化鉛,根據這一性質,乙酸鉛製作為試紙被用於檢測硫化氫的存在。
鹼式碳酸鉛(Pb3(OH)2(CO3)2)又稱鉛白、C.I.顏料白1,曾在19世紀被當作白色顏料使用。[17]由於鉛白具有毒性,這一白色顏料逐漸被鈦白(TiO2)替代。[18]另一種含鉛顏料是鉻黃,成分是鉻酸鉛(PbCrO4)。鉻酸鉛可由鉻酸鈉和硝酸鉛反應,沉澱得到。它最早於19世紀20年代作為黃色顏料使用。[19]這種物質的缺點除了有毒外,它在空氣中會變暗[20],後來被另一種稱作「鎘黃」的顏料所代替。[21]
鉛化合物扮演的另一個角色便是炸藥,除了硝酸鉛合劑外,苦味酸鉛是又一知名的爆炸品。它由苦味酸鹽和可溶性鉛鹽反應,沉澱得到。苦味酸鉛對撞擊敏感,2 kg的物體從2 cm高處落下即可引爆。[22]
有機鉛化合物
[編輯]最著名的有機鉛化合物是鉛烷衍生物四甲基鉛(TML)和四乙基鉛(TEL),而六乙基二鉛(HEDL)的穩定性就較差,這些化合物中含Pb(IV),Pb–C鍵為共價鍵。因此它們是典型的有機鉛化合物。[23]
鉛和鈉形成1:1的合金,與烷基鹵化物反應,生成有機鉛化合物,如四乙基鉛。[24]在四甲基鉛和四乙基鉛中的Pb–C鍵鍵能分別只有167和145 kJ/mol,數據表明這些化合物受熱分解。四乙基鉛在100 °C(373 K)開始分解,熱解產物是單質鉛和烷基自由基,它們的相互作用可以產生六乙基二鉛。[23]這些化合物在日光或紫外線下也能分解。[25]在氯的存在下,烷基可以被氯取代;在HCl的存在下(前者反應的副產物),R2PbCl2可以完全轉變為無機物PbCl2。烷基鉛和溴的反應類似。[25]四甲基鉛和二氧化硫在水的存在下反應,生成(CH3)2PbSO3;和三氧化硫在潮濕的1,2-二氯乙烷中反應,生成(CH3)2PbSO4;和四氧化二氮在戊烷中反應,生成(CH3)3PbNO3,但在三氯甲烷中反應,生成[(CH3)2Pb(cis-(CH3NO)2)](NO3)2。[26]
環戊二烯基鈉和硝酸鉛反應,生成鉛的環戊二烯配合物二茂鉛,它可溶於苯、丙酮、乙醚等有機溶劑,難溶於水,但在冷水中穩定。[27]
四乙酸鉛和芳香烴反應,可以直接得到有機鉛化合物,如和苯甲醚的反應:[28]
四苯基鉛是一種白色固體,難溶於水,可由格氏試劑(苯基溴化鎂)和氯化鉛在乙醚中反應得到:[29]
- C6H5MgBr + 2 PbCl2 → Pb(C6H5)4 + Pb + 4 MgBrCl
四苯基鉛和鹽酸反應,生成氯化三苯基鉛和二氯化二苯基鉛。[30]四苯基鉛和硫在150°C以上發生爆炸:[31]
- Pb(C6H5)4 + 3 S → PbS + (C6H5)2S
有機硫化物(C2H5)3Pb-S-Pb(C2H5)3可以由四乙基鉛和硫反應得到。硒化物(如(CH3)3Pb-Se-R)、碲化物(如(C6H5)3Pb-Te-Pb(C6H5)3)也有報道。[8]
溶解度相圖
[編輯]硫酸鉛難溶於水,如圖所示,向含0.1 mol/L的Pb2+溶液中滴加SO42−溶液。溶液的pH為4.5,在此pH之上,Pb2+的濃度不會超過0.1 mol/L,這是因為偏高的pH會促進Pb(OH)2的生成。從圖中可以看出,在SO42−的濃度為0.1 mol/L時,Pb2+的溶解度下降了10000倍。

|

|
| 溶液中溶解的Pb2+與SO42−的關係圖[32] | 含鉛物種在硫酸鹽介質中的電位-pH圖[32] |
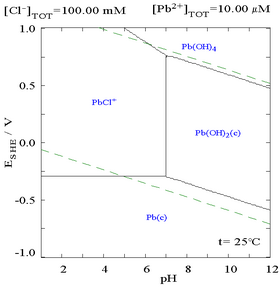
向含有Pb2+的溶液中滴加Cl−,鉛的溶解度變小,當Cl−濃度變得較大時,因形成氯配合物,溶解度再次變大。

|
|
| 溶液中Pb(II)與總氯含量的關係圖[32] | 含鉛物種在氯化物介質中的電位-pH圖[32] |
參考文獻
[編輯]- ^ Polyanskiy 1986,第14–15頁.
- ^ 2.0 2.1 2.2 2.3 Pauling, Linus. General Chemistry. W.H. Freeman. 1947. ISBN 978-0-486-65622-9.
- ^ 3.0 3.1 3.2 Brady, James E.; Holum, John R. Descriptive Chemistry of the Elements. John Wiley and Sons. 1996. ISBN 978-0-471-13557-9.
- ^ Windholz, Martha. Merck Index of Chemicals and Drugs, 9th ed., monograph 8393. Merck. 1976. ISBN 978-0-911910-26-1.
- ^ Polyanskiy 1986,第21頁.
- ^ 6.0 6.1 6.2 Polyanskiy 1986,第22頁.
- ^ 7.0 7.1 Polyanskiy 1986,第28頁.
- ^ 8.0 8.1 郝潤蓉 等. 無機化學叢書 第三卷 碳 硅 鍺分族. 科學出版社, 1998. pp. 528. 3. 有機鉛的硫族化合物 ISBN 7-03-000129 X/O·40
- ^ 9.0 9.1 Polyanskiy 1986,第32頁.
- ^ Polyanskiy 1986,第33頁.
- ^ Polyanskiy 1986,第34頁.
- ^ Zuckerman, J. J.; Hagen, A. P. Inorganic Reactions and Methods, the Formation of Bonds to Halogens. John Wiley & Sons. 1989: 426. ISBN 978-0-471-18656-4.
- ^ Ward, C. H.; Hlousek, Douglas A.; Phillips, Thomas A.; Lowe, Donald F. Remediation of Firing Range Impact Berms. CRC Press. 2000. ISBN 1566704626.
- ^ Saidaminov, Makhsud I.; Abdelhady, Ahmed L.; Murali, Banavoth; Alarousu, Erkki; Burlakov, Victor M.; Peng, Wei; Dursun, Ibrahim; Wang, Lingfei; He, Yao; MacUlan, Giacomo; Goriely, Alain; Wu, Tom; Mohammed, Omar F.; Bakr, Osman M. (2015). "High-quality bulk hybrid perovskite single crystals within minutes by inverse temperature crystallization". Nature Communications. 6: 7586. PMC 4544059 . PMID 26145157. doi:10.1038/ncomms8586.
- ^ Libavius, Andreas. Alchemia Andreæ Libavii. Francofurti: Iohannes Saurius. 1595.
- ^ Stoeppler, M. (1992), Hazardous Metals in the Environment, Techniques and Instrumentation in Analytical Chemistry, 12, Elsevier, p. 60, ISBN 9780080875606, From the results achieved so far it is obvious that the purity law for lead in wines in the last two centuries was frequently ignored.
- ^ Engel, Gustave (1879). Les produits chimiques à l』Exposition Universelle de Paris en 1878, examinés plus spécialement au point de vue de l』industrie des toiles peintes, Bulletin de la Société Industrielle de Mulhouse. 49 :53-83
- ^ Laver, M. Titanium Dioxide Whites, in Fitzhugh, E.W. (Ed), Artists' Pigments, Vol 3, Oxford university Press, 1997, p. 309
- ^ Kühn, H. and Curran, M., Chrome Yellow and Other Chromate Pigments, in Artists』 Pigments. A Handbook of Their History and Characteristics, Vol. 1, L. Feller, Ed., Cambridge University Press, London 1986, p. 187 – 204, pp 188-190
- ^ Pichon, A. Pigment degradation: Chrome yellow’s darker side. Nature Chemistry, 5(11), 2013, 897–897. doi:10.1038/nchem.1789
- ^ Gettens, Rutherford John; Stout, George Leslie (1966). "Painting Materials: A Short Encyclopaedia". Courier Dover Publications: 106. ISBN 978-0-486-21597-6.
- ^ Urbanski, T.: Chemistry and Technology of Explosives, Vol. 1, Pergamon Press – PWN Polish Scientific Publishers, 1964, S. 525.
- ^ 23.0 23.1 Polyanskiy 1986,第43頁.
- ^ Windholz, Martha. Merck Index of Chemicals and Drugs, 9th ed., monograph 8393. Merck. 1976. ISBN 0-911910-26-3.
- ^ 25.0 25.1 Polyanskiy 1986,第44頁.
- ^ Gmelin Handbook of Inorganic Chemistry (8th Edition). Pb - Organic Compounds Part 1. Springer-Verlag Berlin Heidelberg GmbH, 1987. 1.1.1.1.4.6 With Nonmetal Compounds. pp 140
- ^ Fischer, E. O.; Grubert, H. (1956). "Über Aromatenkomplexe von Metallen. IV. Di-cyclopentadienyl-blei". Zeitschrift für anorganische und allgemeine Chemie. 286 (5–6): 237. doi:10.1002/zaac.19562860507.
- ^ Robert P. Kozyrod and John T. Pinhey (1990). "The C-arylation of β-dicarbonyl compounds". Org. Synth.; Coll. Vol., 7, p. 229
- ^ P. Pfeiffer, P. Truskier: Zur Darstellung organischer Blei- und Quecksilber-Verbindungen. In: Berichte der deutschen chemischen Gesellschaft. Band 37, Nr. 1, Januar 1904, S. 1125, doi:10.1002/cber.190403701183.
- ^ P. Pfeiffer, P. Truskier: Zur Darstellung organischer Blei- und Quecksilber-Verbindungen. In: Berichte der deutschen chemischen Gesellschaft. Band 37, Nr. 1, Januar 1904, S. 1125, doi:10.1002/cber.190403701183.
- ^ Max Schmidt, Herbert Schumann: Spaltungsreaktionen metallorganischer Verbindungen mit Chalkogenen. Reaktionen von Schwefel mit silicium-, germanium- und bleiorganischen Verbindungen. In: Zeitschrift für anorganische und allgemeine Chemie. Band 325, Nr. 3-4, Oktober 1963, ISSN 0044-2313, S. 130, doi:10.1002/zaac.19633250305.
- ^ 32.0 32.1 32.2 32.3 Puigdomenech, Ignasi. Hydra/Medusa Chemical Equilibrium Database and Plotting Software. KTH Royal Institute of Technology. 2004. (原始內容存檔於2007-09-29).
參考書目
[編輯]Polyanskiy, N. G. Fillipova, N. A , 編. Аналитическая химия элементов: Свинец [Analytical Chemistry of the Elements: Lead]. Nauka. 1986 (俄語).

