氟化氢
此条目需要补充更多来源。 (2021年3月19日) |
| 氟化氢 | |
|---|---|
| |

| |
| IUPAC名 Hydrogen fluoride | |
| 识别 | |
| CAS号 | 7664-39-3 |
| ChemSpider | 14214 |
| SMILES |
|
| InChI |
|
| InChIKey | KRHYYFGTRYWZRS-UHFFFAOYAC |
| ChEBI | 29228 |
| RTECS | MW7875000 |
| KEGG | C16487 |
| 性质 | |
| 化学式 | HF |
| 摩尔质量 | 20.0063 g·mol⁻¹ |
| 外观 | 无色气体 |
| 密度 | 0.818 g/L |
| 熔点 | −83.38 C (189.77 K) |
| 沸点 | 19.54 °C (293.15 K) |
| pKa | 3.17(水) 15(DMSO)[1] |
| 危险性 | |
| 欧盟危险性符号 | |
| 警示术语 | R:R26/27/28-R35 |
| 安全术语 | S:S1/2-S7/9-S26-S36/37/39-S45 |
| 主要危害 | 剧毒、腐蚀性 |
| NFPA 704 | |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
氟化氢(化学式:)是氢的氟化物,有强烈的腐蚀性,有剧毒。它是无色的气体,在空气中,只要超过3ppm就会产生刺激的味道。
氢氟酸是氟化氢的水溶液,可以透过皮肤黏膜、呼吸道及肠胃道吸收。若不慎暴露于氢氟酸,应立即用六氟灵(Hexafluorine)冲洗,若现场无六氟灵,则先以大量清水冲洗20至30分钟,然后以葡萄糖酸钙软膏或药水涂抹,并紧急送医处理[2];若不小心误饮,则要立即喝下大量的高钙牛奶,并需紧急送医处理。
异常特性
[编辑]氟化氢相对于其他卤素氢化物具有一些异常的物理特性和化学特性。
高熔点及沸点
[编辑]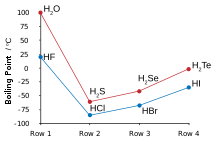
由于氟原子电负性很大,所以会与氢原子形成氢键,所以沸点较氯化氢、溴化氢、碘化氢等为高。
弱酸性
[编辑]氢氟酸之水溶液是一种弱酸。一方面由于氟原子半径小,电荷密度高,对氢原子的束缚较大,另一方面由于H-F共价键高度极性,故氟化氢具有分子间氢键,使得氟化氢具有高度化学稳定性,离解度非常低。因此,离解生成之水合氢离子浓度较低,使酸度常数Ka较低。由此氟化氢为弱酸。
酸度变化
[编辑]其他卤化氢于水中浓度增加,酸度会下降。
对于一般氢卤酸,卤化氢浓度上升至某个程度,每单位体积溶液中之含水量急剧下降,令此反应之平衡位置趋向左边,使离解度下降,酸性下降。但在较浓的氟化氢水溶液中,酸度反而会增加。此现象是由于氟离子之一个反应:
对于氢氟酸,若氟化氢浓度增加,以上反应之平衡位置趋向右边,使氟离子浓度上升。
根据勒沙特列原理,此化学平衡之平衡位置趋向右边以倾向增加氟离子之浓度,故此离解度上升,酸性上升。
侵蚀玻璃性
[编辑]氢氟酸本身对硅酸盐(硅)及二氧化硅有极强的侵蚀能力。 故可腐蚀玻璃(主要成分是二氧化硅及硅酸盐),是可腐蚀玻璃的酸,所以日常贮存要使用塑料瓶或铅制容器。
作为溶剂
[编辑]氟化氢是强酸性溶剂,在氟化氢中:
与硝酸反应:HNO3+2HF→H2NO3++HF2-
与硫酸反应:H2SO4+3HF→HSO3F+H3O++HF2-
- 高氯酸显两性。
显碱性时:HClO4+2HF⇌H2ClO4++HF2-
显酸性时:HClO4+HF⇌H2F++ClO4-
一价的氟化物均易溶于氟化氢;二价的氟化物、、溶解度稍大,、、溶解度稍小;三价的氟化物溶解度稍小;其余二至四价金属的氟化物均难溶。
一些低价过渡金属的氟化物可以将溶剂还原,如和,将溶剂还原,放出氢气,自身被氧化为和。
在酸性环境下,氢氟酸非常危险,因为氢离子在酸性环境下会腐蚀皮肤,而氟离子则会将体内的钙,镁离子溶出,将严重破坏生理平衡。
参考文献
[编辑]- ^ pKa's of Inorganic and Oxo-Acids. D. H. Ripin, D. A. Evans. [2020-03-09]
- ^ 六氟靈使用法則. 永百实业股份有限公司. [2019-08-29]. (原始内容存档于2019-08-29).





















