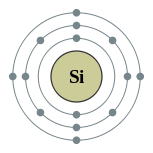
硅
| 「Silicon」的各地常用名稱 | |
|---|---|
| 中国大陸 | 硅 |
| 臺灣 | 矽 |
| 港澳 | 矽 |
| 新加坡 | 矽 |
| 馬來西亞 | 硅 |

硅是外观帶著灰藍色金屬光澤且堅硬易碎的晶體,亦是一種四價的類金屬半導體。矽為週期表第十四族元素之一[8]:碳在其排序之上,其下依序為鍺、錫、鉛和鈇[註 1]。由於它對於氧的高親和力,直至在西元1823年才第一次被永斯·贝采利乌斯成功純化[9]。它的熔點和沸點分別為攝氏1414度及3265度,且分別在金屬和非金屬中排名第二,僅次於硼。矽在宇宙中最常見元素中排名第八,但以元素型態分佈在地殼是非常罕見的。它常以二氧化矽或矽酸鹽等多樣的形式廣泛分佈於土壤、沙和小行星和行星中。地殼的組成超過九成是矽酸鹽類物質,使得矽成為地殼中含量第二的元素,僅次於氧。
元素矽也在世界經濟上有很大的影響,矽通常會與天然礦物一起加工,其用途廣泛:包括建築業使用的粘土、矽砂和石頭。波特蘭水泥中的砂漿和灰泥組成也含有矽酸鹽,可與硅砂和礫石混合成混凝土,用於走道、地基、道路上。它們還用於白色陶瓷,像是瓷器,也可用於製造傳統的石英鈉鈣玻璃和許多其他特殊玻璃。矽最廣為人知的用途是去合成以聚矽氧聚合物為基礎的合成聚合物。有些矽的化合物,像是碳化矽可用作研磨物或高強度陶瓷元件。大多數游離的矽被用於鍊鋼、鑄鋁和高質量的化工業上(通常是製造氣相二氧化矽)。更顯著的是,半導體電子業運用極少部分的高純度矽(小於10%),而高純度矽在積體電路上是一種必要的元素,大部分的電腦、手機及現代科技都依靠它。
雖然動物通常對於矽的需求是微量的,但在生物學裡,矽是一種必要的元素。在多種的海綿動物門及微生物裡,像是矽藻及放射蟲會分泌由二氧化矽組成的骨骼物質。二氧化矽亦通常沉澱於植物組織中。
性質[编辑]
物理性質[编辑]
结晶型的硅是暗蓝色的,很脆,是典型的半导体。
化學性質[编辑]
硅的化学性质非常稳定,常与氧元素形成化合物,如SiO2等。[10]存在于地表的硅几乎总以含氧化合物的形式存在,尤以包含4个配位键的结构居多,少有例外。[11]每1个硅元素搭配4个氧元素的组合可以单独形成基团,也可以形成链、带、环、层等复杂结构。[11]在常温下,除氟化氢以外,很难与其他物质发生反应。
固态硅单质不太活泼,不易與气体或液体试剂反应;液态硅单质则相反,能与多数金属发生反应。[12]
同素异形体[编辑]
同素异形体有两种,一种为暗棕色无定形粉末,用镁使二氧化硅还原而得,性质比较活泼,能够在空气中燃烧,称无定形硅;另一种为性质稳定的晶体(结晶硅),是用炭在电炉中使二氧化硅还原而得。

发现[编辑]
1787年,拉瓦锡首次发现硅存在于岩石中。然而在1800年,汉弗里·戴维将其错认为一种化合物。1811年,盖-吕萨克和路易·特纳可能已经通过将单质钾和四氟化硅混合加热的方法制备了不纯的无定形硅。1823年,硅首次作为一种元素被贝采利乌斯发现,并于一年后提炼出了无定形硅,其方法与盖-吕萨克使用的方法大致相同。他随后还用反复清洗的方法将单质硅提纯。
名称由来[编辑]
英文中的silicon一词,来自拉丁文的silex, silicis,意思为燧石(即火石,富含硅元素)。在1831年,苏格兰化学家托马斯·汤姆森創造了這個名詞[10]。
在1823年純化出來後,瑞典化学家永斯·贝采利乌斯利用新拉丁文規則造出silicium這個單字,再加上-ium字根,以代表它是一種金屬。歐洲許多國家都採用silicium這個名稱,但英文名稱最終採用了在1817年提出的silicon這個拼法,去除了代表金屬的-ium字根,因為它的物理特性更接近於碳(carbon)與硼(boron)這一類元素[10]。
汉字[编辑]
1837年,日本第一部西方化学译著,宇田川榕庵的《舍密開宗》首先以「珪土」作为硅元素的名称。该书术语譯自荷兰语词汇,由于当时荷兰语硅的元素名为「keiaarde」,是「keisteen-aarde」(燧石土)的缩略,日本就专门找了一个玉字旁的同音字「珪」(平假名:けい kei,漢語:guī,是「圭」的异体字)来音译「kei」。因此「keisteen」就译成「珪石」,作为SiO2的名称;由于当时荷兰语中的镁、铝、硅、钡等元素都是以「-aarde」(土)结尾,因此日语也分别照译成苦土、礬土、珪土、重土[13]。后来日本摒弃了源自荷兰语的「土」,改译为「珪素」,在19世纪后期又出现了「硅素」的写法[14],不过19世纪末日本规定以「珪素」为准。「珪/硅」进入中国是20世纪初,由于它属于固态非金属元素,所以中国采用了石字旁的写法[15]。
在中國,清朝徐寿在1871年出版的《化學鑑原》中,創造「矽」字作為silicon的音译[16]。在中華民國成立後,中華民國教育部於1933年公布《化學命名原則》,採用「矽」為正式譯名,音读为「si(t),夕(入)」,其中写道「Silicon舊譯一作硅,一作矽,硅由日名珪素孳演而成,因爲固體,故改王旁爲石;於義旣無可取,不如用諧聲之矽。」[15][註 2]台灣以此為標準譯名。
中華人民共和國成立後,中国科学院于1953年2月在北京组织召开了一次全国性的化学物质命名扩大座谈会。会议邀集全国各地的化学专家以及从事文字改革工作的学者参加。据会议纪要显示,当日会场上围绕矽字等同音字是否需要变更有着两种不同的看法。一派是以顾翼东、方柏容、刘泽先三位先生为代表,主张改;另一派则以符绶玺、侯毓汾二位先生为代表,主张不改[21]。座谈会结束后不久,《化学通报》连载了化学名词审查小组成员陶坤的文章——《化学新字的读音》上、下两篇。在下篇中,陶文宣布将矽字改为硅字,在注解中,他陈述了更改的理由:“矽音夕,与硒、烯、醯、锡不易分辨。[22]”真正全国性的统一变更是在1957年。这一年,中国科学院编译出版委员会名词室下发《关于几个化学名词订名问题的通知》,正式宣布废矽改硅的决定。这一通知中提到了审定理由和过程:“1953年化学名词审查小组建议将‘矽’改为‘硅’,1955年,无机化合物名词审查小组认为此项建议甚为正确,在征求全国各有关单位意见后,决议将‘矽’改为‘硅’。[23]”不过,在一些术语中,如医学术语“矽肺”、工业术语“矽钢片”中,中国大陆仍然保留了矽字[24](在中國大陸讀作xī[25])。在香港,兩用法皆有,但「矽」較通用。
分布[编辑]
硅主要以含氧化合物的形式,作为仅次于氧的最丰富的元素存在于地壳中,约占地表岩石的四分之一,广泛存在于硅酸盐和硅石中。
制备[编辑]
工业上,通常是在电炉中由高纯度碳还原二氧化硅(常见于石英或沙子)而制得:[11]
这样制得的硅纯度为97~98%,[26]叫做粗硅。再将它融化后重结晶,用酸除去杂质,得到纯度为99.7~99.8%的純硅。如要将它做成半导体用硅,还要将其转化成易于提纯的液体或气体形式,再经蒸馏、分解过程得到多晶硅。如需得到高纯度的硅,则需要进行进一步的提纯处理。
同位素[编辑]
已发现的硅的同位素共有12种,包括硅25至硅36,其中只有硅28,硅29,硅30是稳定的,其他同位素都带有放射性。
用途[编辑]
硅是一种半导体材料,可用于制作半导体器件、太陽能電板、光纖和積體電路。还可以合金的形式使用(如硅铁合金),用于汽车和机械配件。也与陶瓷材料一起用于金属陶瓷中。还可用于制造玻璃、混凝土、砖、耐火材料、矽氧烷、硅烷。與鐵結合,可以成為矽鋼,這是一種耐磨的鋼件,常用在各種工具上。此外,矽也是不鏽鋼的主成分之一,用來使不鏽鋼具有耐磨的特性。
重要化合物[编辑]
- 碳化矽,耐磨耐热,[27]用於半導體、避雷針、電路元件、高溫應用、紫外光偵檢器、結構材料、天文、碟剎、離合器、柴油微粒濾清器、細絲高溫計、陶瓷薄膜、裁切工具、加熱元件、核燃料、珠寶、鋼、護具、觸媒擔體等領域。
- 二氧化矽,是沙和石英的主要成分。在半導體和太陽能板等應用中,是目前主要的原料。
- 矽烷,在醫學和工業領域有著廣泛的應用。
- 四氯化矽,應用在半導體工業和光電池中。
参见[编辑]
参考资料[编辑]
註腳[编辑]
引用资料[编辑]
- ^ Prohaska, Thomas; Irrgeher, Johanna; Benefield, Jacqueline; Böhlke, John K.; Chesson, Lesley A.; Coplen, Tyler B.; Ding, Tiping; Dunn, Philip J. H.; Gröning, Manfred; Holden, Norman E.; Meijer, Harro A. J. Standard atomic weights of the elements 2021 (IUPAC Technical Report). Pure and Applied Chemistry. 2022-05-04. ISSN 1365-3075. doi:10.1515/pac-2019-0603 (英语).
- ^ Weeks, Mary Elvira. The discovery of the elements: XII. Other elements isolated with the aid of potassium and sodium: beryllium, boron, silicon, and aluminum. Journal of Chemical Education. 1932, 9 (8): 1386–1412.
- ^ Voronkov, M. G. Silicon era. Russian Journal of Applied Chemistry. 2007, 80 (12): 2190. doi:10.1134/S1070427207120397.
- ^ Ram, R. S.; et al. Fourier Transform Emission Spectroscopy of the A2D–X2P Transition of SiH and SiD (PDF). J. Mol. Spectr. 1998, 190: 341–352. PMID 9668026. (原始内容 (PDF)存档于2012-02-09).
- ^ Magnetic susceptibility of the elements and inorganic compounds 互联网档案馆的存檔,存档日期2012-01-12., in Lide, D. R. (编), CRC Handbook of Chemistry and Physics 86th, Boca Raton (FL): CRC Press, 2005, ISBN 0-8493-0486-5
- ^ Physical Properties of Silicon (页面存档备份,存于互联网档案馆). New Semiconductor Materials. Characteristics and Properties. Ioffe Institute
- ^ 7.0 7.1 7.2 7.3 [1] (页面存档备份,存于互联网档案馆) Hopcroft, et al., "What is the Young's Modulus of Silicon?" IEEE Journal of Microelectromechanical Systems, 2010
- ^ 矽 - 長庚大學電子工程系網頁. elec.cgu.edu.tw. [2022-08-06]. (原始内容存档于2022-11-04) (中文(臺灣)).
- ^ Silicon - Element information, properties and uses | Periodic Table. www.rsc.org. [2022-08-06]. (原始内容存档于2022-10-23).
- ^ 10.0 10.1 10.2 见Greenwood 1984,第516頁(位于上册第9章“硅”第1节“导论”)。
- ^ 11.0 11.1 11.2 11.3 见Greenwood 1984,第518頁(位于上册第9章“硅”第2节“硅元素”)。
- ^ 见Greenwood 1984,第524頁(位于上册第9章“硅”第2节“硅元素”)。
- ^ 宇田川榕菴. 舎密開宗. 1837.
- ^ 太田泰弘; 孙丽平. 关于“珪素、硅素”的溯源. 中国科技术语. 2013, 15 (3): 58–59.
- ^ 15.0 15.1 國立編譯館. 化學命名原則. 國立編譯館. 1933.
- ^ 徐壽. 化學鑑原. 1871.
- ^ 邵靖宇. 硅字的来历和变迁. 中国科技术语. 2008, 10 (1): 46–48 [2008-12-23]. (原始内容存档于2009-05-22).
- ^ 18.0 18.1 黄河清; 侯迁; 邵靖宇. 关于“硅”和“矽”来历的补充. 中国科技术语. 2008, 10 (4): 64.
- ^ 吴国庆. 硅作为元素名一开始就读作gui而不读作xi. 中国科技术语. 2010, 12 (4): 59–62. ISSN 1673-8578. doi:10.3969/J.ISSN.1673-8578.2010.04.012. Wikidata Q87817714 (中文)., Wikidata Q87817714
- ^ 教育部異體字典-砉. [2008-12-23]. (原始内容存档于2009-06-28).
- ^ 王力. 废矽改硅:避免中译化学名词同音字的一次选择. 中国科技术语. 2013, 15 (3): 56–57 [2016-09-07]. (原始内容存档于2016-09-19).
- ^ 陶坤. 化学新字的读音(下). 化学通报. 1953, (8): 359.
- ^ 中国科学院编译出版委员会名词室. 关于几个化学名词订名问题的通知. 化学通报. 1957, (1): 70.
- ^ “硅”字的来历和变迁. [2023-03-18]. (原始内容存档于2023-03-31).
- ^ 中国社会科学院语言研究所词典编辑室. 新华字典 第11版. 商务印书馆. 2010. ISBN 978-7-100-06959-5.
- ^ 见Greenwood 1984,第519頁(位于上册第9章“硅”第2节“硅元素”)。
- ^ 见Greenwood 1984,第525頁(位于上册第9章“硅”第2节“硅元素”)。
补充来源[编辑]
- Norman Neill Greenwood; Alan Earnshaw. Chemistry of the Elements [元素化学]. 曹庭礼 (翻译与编辑); 夏鲁惠 (翻译与编辑); 耿承延 (翻译与编辑) 1. 北京: 高等教育出版社. 1984 (中文(中国大陆)).
外部链接[编辑]
| 维基共享资源上的相关多媒体资源:硅 |
- 元素硅在洛斯阿拉莫斯国家实验室的介紹(英文)
- EnvironmentalChemistry.com —— 硅(英文)
- 元素硅在The Periodic Table of Videos(諾丁漢大學)的介紹(英文)
- 元素硅在Peter van der Krogt elements site的介紹(英文)
- WebElements.com – 硅(英文)
| 元素周期表(类金属) | |||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| IA 1 |
IIA 2 |
IIIB 3 |
IVB 4 |
VB 5 |
VIB 6 |
VIIB 7 |
VIIIB 8 |
VIIIB 9 |
VIIIB 10 |
IB 11 |
IIB 12 |
IIIA 13 |
IVA 14 |
VA 15 |
VIA 16 |
VIIA 17 |
VIIIA 18 | ||||||||||||||||||||
| 1 | H | He | |||||||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | |||||||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |||||
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |||||
| |||||||||||||||||||||||||||||||||||||
| ||||||||||||