氯化釔
外觀
| 氯化釔 | |
|---|---|
| |
| IUPAC名 氯化釔(III) Yttrium(III) chloride | |
| 識別 | |
| CAS號 | 10361-92-9 |
| ChemSpider | 59696 |
| SMILES |
|
| InChI |
|
| InChIKey | PCMOZDDGXKIOLL-DFZHHIFOAW |
| RTECS | ZG3150000 |
| 性質 | |
| 化學式 | YCl3 |
| 摩爾質量 | 195.26 g·mol⁻¹ |
| 外觀 | 白色固體 |
| 密度 | 2.67 g/cm3 |
| 熔點 | 721 °C |
| 沸點 | 1507 °C[1] |
| 溶解性(水) | 82 g/100 mL |
| 溶解性 | 60.1 g/100 mL乙醇 (15°C) 60.6 g/100 mL吡啶 (15°C)[2] |
| 結構 | |
| 晶體結構 | Monoclinic, mS16 |
| 空間群 | C12/m1, No. 12 |
| 危險性 | |
| 歐盟編號 | 未列出 |
| 閃點 | 不可燃 |
| 相關物質 | |
| 其他陰離子 | 氧化釔 |
| 其他陽離子 | 氯化鈧 氯化鑭 氯化錒 |
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |
氯化釔是一種無機化合物,化學式為YCl3,易溶於水。
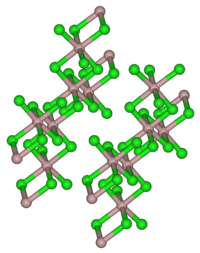
結構
[編輯]固體氯化釔有和AlCl3一樣的結構。
製備和反應
[編輯]無水氯化釔通常由氯化銨和水合氯化釔、氧化釔、或氯氧化釔反應[3][4][5]首先得到(NH4)2[YCl5]:
- 10 NH4Cl + Y2O3 → 2 (NH4)2[YCl5] + 6 NH3 + 3 H2O
- YCl3·6H2O + 2 NH4Cl → (NH4)2[YCl5] + 6 H2O
然後將(NH4)2[YCl5]加熱,使之分解:
- (NH4)2[YCl5] → 2 NH4Cl + YCl3
在分解的過程中,會產生中間體(NH4)[Y2Cl7]。
如果用鹽酸作用於Y2O3,只會得到水合物(YCl3·6H2O),它不能通過直接加熱得到無水物,因為在加熱的過程中會水解,產生氯氧化釔。
參考資料
[編輯]- ^ Yttrium & Compounds, United States Occupational Safety and Health Administration, 2007-01-11 [2008-05-29], (原始內容存檔於2013-03-02)
- ^ Spencer, James F., The Metals of the Rare Earths, New York: Longmans, Green, and Co: 135, 1919 [2008-05-29]
- ^ , Meyer, G. The Ammonium Chloride Route to Anhydrous Rare Earth Chlorides-The Example of YCl3. Inorganic Syntheses. 1989, 25: 146–150. ISBN 978-0-470-13256-2. doi:10.1002/9780470132562.ch35.
- ^ Edelmann, F. T.; Poremba, P. Herrmann, W. A. (ed.) , 編. Synthetic Methods of Organometallic and Inorganic Chemistry VI. Stuttgart: Georg Thieme Verlag. 1997. ISBN 3-13-103021-6.
- ^ Taylor, M.D.; Carter, C.P. Preparation of anhydrous lanthanide halides, especially iodides. Journal of Inorganic and Nuclear Chemistry: 387–391. doi:10.1016/0022-1902(62)80034-7.
