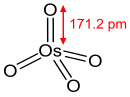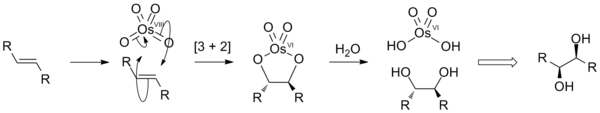四氧化鋨
| 四氧化鋨 | |||
|---|---|---|---|
| |||

| |||
| IUPAC名 Osmium tetraoxide | |||
| 識別 | |||
| CAS號 | 20816-12-0 | ||
| PubChem | 30318 56370778((monopotassiate)) 75811001((monoquinuclidiniate)) 53113021((monotemediate)) | ||
| ChemSpider | 28158 | ||
| SMILES |
| ||
| InChI |
| ||
| InChIKey | VUVGYHUDAICLFK-UHFFFAOYSA-N | ||
| UN編號 | UN 2471 | ||
| EINECS | 244-058-7 | ||
| ChEBI | 88215 | ||
| RTECS | RN1140000 | ||
| MeSH | Osmium+tetroxide | ||
| 性質 | |||
| 化學式 | OsO4 | ||
| 摩爾質量 | 254.23 g·mol⁻¹ | ||
| 外觀 | 無色或淺黃色半透明固體 | ||
| 密度 | 4.9 g/cm³ (固) | ||
| 熔點 | 40.25 °C | ||
| 沸點 | 130 °C | ||
| 危險性 | |||
| 歐盟危險性符號 | |||
| 警示術語 | R:R26/27/28, R34 | ||
| 安全術語 | S:S1/2, S7/9, S26, S45 | ||
| NFPA 704 | |||
| 相關物質 | |||
| 其他陽離子 | 四氧化釕、二氧化鋨 | ||
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |||
四氧化鋨,又稱氧化鋨(VIII),是化學式為OsO4的化合物,常溫下為無色固體,但大多數樣本呈現黃褐色[1],可能是由於其中存在棕黃色二氧化鋨(OsO2)雜質所致。[2]四氧化鋨具有一些不同於大多數金屬氧化物的特殊性質,例如具有揮發性和高毒性。
儘管四氧化鋨有劇毒且鋨元素罕見且昂貴,該化合物仍有很多用途,例如其與脂質結合的特性使其在生物學中廣泛用作電子顯微鏡樣本的染色劑。
物理性質
[編輯]純四氧化鋨是無色的,但因通常混有少量二氧化鋨(OsO2)而呈黃褐色。OsO4可溶於四氯化碳(CCl4),微溶於水,與水反應生成鋨酸(見下文)。OsO4具有揮發性,常溫下易升華。氣味與臭氧相似。鋨的名稱即起源於希臘文的「osme」,意思是「臭味」。[3]
| 溶劑 | 溶解度 | 溫度(℃) |
|---|---|---|
| 水 | 7.24 | 25 |
| 四氯化碳 | 250 | 20 |
結構和電子排布
[編輯]鋨(VIII)是d0金屬離子,因此當Os(VIII)的配位數為四時,其形狀應是四面體構型。還有MnO4−和CrO42−也是四面體構型。
OsO4中鋨的化合價為+8,這是過渡金屬的最高化合價。鋨原子有8個價電子。如果假設每個Os-O鍵都提供兩個電子,則該絡合物總共有16個電子,與高錳酸根離子和鉻酸根離子一樣。
合成
[編輯]粉末狀的鋨在常溫下與O2緩慢反應,生成OsO4。塊狀的鋨則須加熱至670 K才能被氧氣氧化。[5]
- Os + 2 O2 → OsO4
反應
[編輯]氧氟化物
[編輯]- 鋨有很多種氧氟化物,都對潮濕非常敏感。
在77K的低溫下,四氧化鋨與二氟化氪在氫氟酸溶液中反應,生成紫色的 順式-OsO2F4。[6]
- OsO4 + 2 KrF2 → cis-OsO2F4 + 2 Kr + O2
- OsO4與F2反應,生成黃色的OsO3F2:
- 2 OsO4 + 2 F2 → 2 OsO3F2 + O2
- OsO4在常溫下與等摩爾的[Me4N]F反應,在253K的溫度下則與兩倍的物質的量的[Me4N]F反應:[5]:
- OsO4 + [Me4N]F → [Me4N][OsO4F]
- OsO4 + 2 [Me4N]F → [Me4N]2[cis-OsO4F2]
烯烴的氧化
[編輯]- OsO4能催化烯烴與過氧化氫水溶液之間的反應。化學方程式為:
- R2C=CR2 + H2O2 → R2C(OH)-C(OH)R2.
反應中OsVIIIO4先與烯烴R2C=CR2發生加成反應,生成環"酯" R4C2O2OsVIO2,然後再水解,生成二醇和六價鋨化合物(OsVI)[來源請求]:
其它反應
[編輯]- OsO4溶於鹼溶液,生成高鋨酸鹽並分解得到鋨(VI)酸鹽:
- OsO4 + 2 NaOH → Na2[cis-OsO4(OH)2]
- Na2[cis-OsO4(OH)2]+H2O→Na2[OsO2(OH)4]+½O2
- OsO4 + NH3 + KOH → K[Os(N)O3] + 2 H2O
[Os(N)O3]−離子是OsO4的等電子體,且結構相同。與伯胺t-BuNH2[(CH3)3C-NH2]反應得到相應的亞氨基化合物:
- OsO4 + 4 Me3CNH2 → Os(NCMe3)4 + 4 H2O
- 在400K和200個大氣壓下,OsO4在甲醇溶液中與一氧化碳發生"還原性羰基化反應",生成三角形的Os3(CO)12:
此反應中鋨的化合價從+8下降到0。
- 四氧化鋨也可以被碳還原:
- OsO4 + 2 C → Os + 2 CO2[4]
用途
[編輯]有機合成
[編輯]
在有機合成領域中,OsO4廣泛用作把烯烴順式氧化成鄰二醇的氧化劑。參見以上反應機理。此反應既可以是催化反應(厄普約翰雙羥基化反應、勒米厄-約翰遜氧化反應),也可以是不對稱反應(夏普萊斯不對稱雙羥基化反應)。
生物染色
[編輯]OsO4由於含有重金屬鋨原子,對電子的阻擋性較佳,故廣泛用作穿透式電子顯微鏡組織標本的染劑,能增強影像的對比度。[8]OsO4的強氧化性使其能與未飽和碳-碳鍵反應,從而連接脂質。因此在染色的同時,它還會固定生物膜,從而使樣本結構特徵不被破壞,也能快速殺死原生動物等會移動的活體樣本。
鋨礦石精煉
[編輯]OsO4是從礦石中提取鋨的中間產物。將含鋨殘留物用過氧化鈉(Na2O2)處理,形成可溶的Na2[OsO4(OH)2]。該鹽與氯反應形成OsO4。在精煉的最後步驟,粗製的OsO4溶解在NaOH醇中形成Na2[OsO2(OH)4],用氯化銨(NH4Cl)處理後得到(NH4)4[OsO2Cl2]。將此鹽在氫氣中還原,即可得到鋨。[9]
藥物
[編輯]四氧化鋨唯一已知的臨床用途是治療關節炎。[10]由於缺乏有關局部施用四氧化鋨的長期副作用的報告,說明鋨本身可能具有生物相容性,儘管這取決於所施用的鋨化合物種類。2011年,有報告指出鋨(VI)[11]和鋨(II)[12]化合物在體內具抗癌活性,顯示使用鋨化合物作為抗癌藥物具有廣闊的前景。[13]
安全性
[編輯]
四氧化鋨的揮發性很高,能輕易穿透皮膚,且經吸入、進食和皮膚接觸後都是毒物。[14]如果空氣中含有低濃度四氧化鋨,會造成肺淤血及皮膚和眼部損害,人眼接觸四氧化鋨後會對角膜進行不可逆的染色,從而導致失明。因涉及四氧化鋨的實驗必須在通風櫃內操作。[15]四氧化鋨的容許暴露限值(8小時時間加權平均值)為2 µg/m3。[16]由於四氧化鋨可以穿透塑膠和食品包裝,因此必須在玻璃容器中冷藏保存。[17]
外部連結
[編輯]- 國際化學安全卡 0528(頁面存檔備份,存於互聯網檔案館)
- NIOSH Pocket Guide to Chemical Hazards(頁面存檔備份,存於互聯網檔案館)
- BBC report on bomb plot(頁面存檔備份,存於互聯網檔案館)
- BBC 什麼是四氧化鋨(頁面存檔備份,存於互聯網檔案館)
- 四氧化鋨: 本月的化合物(頁面存檔備份,存於互聯網檔案館)
- 化學反應(頁面存檔備份,存於互聯網檔案館)
參考文獻
[編輯]- ^ Girolami, Gregory. Osmium weighs. Nature Chemistry. 2012, 4 (11): 954. Bibcode:2012NatCh...4..954G. PMID 23089872. doi:10.1038/nchem.1479
 .
.
- ^ Cotton and Wilkinson, Advanced Inorganic Chemistry, p.1002
- ^ Dr. M Thomson, Osmium tetroxide (OsO4). [1] (頁面存檔備份,存於互聯網檔案館)
- ^ 4.0 4.1 《無機化學叢書》.張青蓮 主編.第九卷.P439. 3.2.2氧化物
- ^ 5.0 5.1 Housecroft & Sharpe. Inorganic Chemistry. (ed 2, 2005). p 671-673
- ^ Christe et al. "Osmium tetrafluoride dioxide, cis-OsO2F4". J. Am. Chem. Soc. 1993, 115. doi:11279-11284
- ^ Housecroft & Sharpe. Inorganic Chemistry. (ed 2, 2005). p 672,710
- ^ Bozzola, J. J.; Russell, L. D. Specimen Preparation for Transmission Electron Microscopy. Electron Microscopy: Principles and Techniques for Biologists. Sudbury, MA: Jones and Bartlett. 1999: 21–31. ISBN 978-0-7637-0192-5.
- ^ Thompson, M. Osmium tetroxide (OsO4). Bristol University. [2012-04-07]. (原始內容存檔於2013-09-22).
- ^ Sheppeard, H.; D. J. Ward. Intra-articular osmic acid in rheumatoid arthritis: five years' experience. Rheumatology. 1980, 19 (1): 25–29. PMID 7361025. doi:10.1093/rheumatology/19.1.25.
- ^ Lau, T.-C; W.-X. Ni; W.-L. Man; M. T.-W. Cheung; et al. Osmium(vi) complexes as a new class of potential anti-cancer agents. Chem. Commun. 2011, 47 (7): 2140–2142. PMID 21203649. S2CID 1851467. doi:10.1039/C0CC04515B.
- ^ Sadler, Peter; Steve D. Shnyder; Ying Fu; Abraha Habtemariam; et al. Anti-colorectal cancer activity of an organometallic osmium arene azopyridine complex (PDF). Med. Chem. Commun. 2011, 2 (7): 666–668 [2023-11-06]. doi:10.1039/C1MD00075F. (原始內容存檔 (PDF)於2023-07-15).
- ^ Fu, Ying; Romero, María J.; Habtemariam, Abraha; et al. The contrasting chemical reactivity of potent isoelectronic iminopyridine and azopyridine osmium(II) arene anticancer complexes (PDF). Chemical Science. 2012, 3 (8): 2485–2494 [2023-11-06]. doi:10.1039/C2SC20220D. (原始內容存檔 (PDF)於2023-01-17).
- ^ Luttrell, William E.; Giles, Cory B. Toxic tips: Osmium tetroxide. Journal of Chemical Health and Safety. 2007, 14 (5): 40–41. doi:10.1016/j.jchas.2007.07.003.
- ^ Mager Stellman, J. Osmium. Encyclopaedia of Occupational Health and Safety. International Labour Organization. 1998: 63.34. ISBN 978-92-2-109816-4. OCLC 35279504.
- ^ Osmium tetroxide (as Os). Documentation for Immediately Dangerous to Life or Health Concentrations (IDLHs). Centers for Disease Control. 2 November 2018 [2023-11-06]. (原始內容存檔於2023-05-30).
- ^ Hayat, M. A. Principles and Techniques of Electron Microscopy: Biological Applications. Cambridge University Press. 2000: 45–61. ISBN 0-521-63287-0.
- Cotton, S. A. "Chemistry of Precious Metals," Chapman and Hall (London): 1997. ISBN 0-7514-0413-6.
- Berrisford, D. J.; Bolm, C.; Sharpless, K. B., "Ligand Accelerated Catalysis", Angewandte Chemie, International Edition English, 1995, volume 34, pp. 1059-1070.