半胱亚磺酸
外观
| 半胱亚磺酸 | |
|---|---|
| |
| |
| IUPAC名 3-亚磺基-2-氨基丙酸 2-amino-3-sulfinopropanoic acid | |
| 别名 | L-半胱亚磺酸、L-半胱氨酸亚磺酸 |
| 识别 | |
| CAS号 | 1115-65-7 2381-08-0 |
| PubChem | 1549098 |
| ChemSpider | 1266065 |
| SMILES |
|
| InChI |
|
| InChIKey | ADVPTQAUNPRNPO-REOHCLBHBM |
| ChEBI | 16345 |
| DrugBank | DB02153 |
| KEGG | C00606 |
| MeSH | cysteine+sulfinic+acid |
| IUPHAR配体 | 5447 |
| 性质 | |
| 化学式 | C3H7NO4S |
| 摩尔质量 | 153.15698 g·mol⁻¹ |
| 外观 | 白色固体 |
| 溶解性(水) | 可溶于水 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
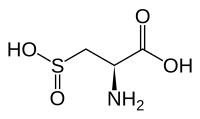
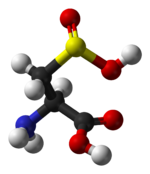
半胱亚磺酸(英語:Cysteine sulfinic acid)又称半胱氨酸亚磺酸,是一种有机化合物,结构式为HO2SCH2CH(NH2)CO2H。半胱亚磺酸为一种带有亚磺酸基团的罕见天然氨基酸。其为白色固体,且可溶于水。和许多天然氨基酸一样,其具有手性,且自然界中仅存在L型体。在中性溶液中为两性离子的形式。半胱亚磺酸是生物牛磺酸代谢过程的中间体,其为非编码氨基酸,但可在翻译后修饰过程中产生。含有半胱亚磺酸的肽是半胱亚磺酸还原酶的反应底物[1]。
半胱亚磺酸在生物体内由半胱氨酸得到。胱硫醚经过胱硫醚γ裂合酶得到半胱氨酸,半胱氨酸要么经过半胱氨酸裂合酶或胱硫醚γ裂合酶降解,要么被半胱氨酸双加氧酶氧化形成半胱亚磺酸。进入半胱亚磺酸途径后,经半胱亚磺酸脱羧酶脱羧形成亚牛磺酸,随后亚牛磺酸被亚牛磺酸脱氢酶氧化成牛磺酸[2]。
同时,在一些腈水合酶的活性位点中发现了含有半胱亚磺酸残基结构的蛋白质[3]。

参考文献
[编辑]- ^ Akter, Salma; Fu, Ling; Jung, Youngeun; Conte, Mauro Lo; Lawson, J. Reed; Lowther, W. Todd; Sun, Rui; Liu, Keke; Yang, Jing; Carroll, Kate S. Chemical proteomics reveals new targets of cysteine sulfinic acid reductase. Nature Chemical Biology. 2018, 14 (11): 995–1004. PMC 6192846
 . PMID 30177848. doi:10.1038/s41589-018-0116-2.
. PMID 30177848. doi:10.1038/s41589-018-0116-2.
- ^ Sumizu K. Oxidation of hypotaurine in rat liver. Biochim. Biophys. Acta. 1962, 63: 210–212. PMID 13979247. doi:10.1016/0006-3002(62)90357-8.
- ^ Isao Endo, Masaki Nojiri, b, Masanari Tsujimura, Masayoshi Nakasako, Shigehiro Nagashima, Masafumi Yohda, Masafumi Odaka "Focused Review: Fe-type nitrile hydratase"Journal of Inorganic Biochemistry 2001, Volume 83, Issue 4, February 2001, Pages 247–253. doi:10.1016/S0162-0134(00)00171-9
