α粒子
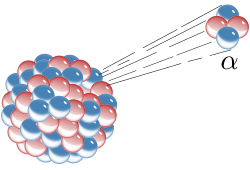 | |
| 组成 | 两个质子及两个中子 |
|---|---|
| 系 | 玻色子 |
| 符号 | α, α2+, He2+ |
| 质量 | 6.644657230(82)×10−27 kg[1] 4.001506179127(63) u |
| 电荷 | +2 e |
| 自旋 | 0[2] |
| CAS号 | 12587-46-1 |
α粒子(英语:Alpha particle),也被称作α射线或α辐射,是由两个质子及两个中子组成的粒子,其与氦-4的原子核相同。它以第一个希腊字母α命名,可以写作α或α2+,通常在α衰变中产生。因为α粒子与氦原子核相同,有时也会写成He2+
或4
2He2+
以代表+2价(失去两个电子)的氦离子。当α粒子从环境中得到电子,它就会变成一般(电中性)的氦原子4
2He。
α粒子的自旋为0。由于标准α放射性衰变的机制,α粒子一般会有大约5 MeV的动能以及相当于4%光速的速度。(见下方“#能量与吸收”)。它是具高电离性的粒子辐射,通常(当其由放射性α衰变产生时)有较小的穿透深度(可以被数公分的大气层,或人类皮肤阻挡)。
然而,由三元裂变产生的所谓长射程α粒子能量及穿透深度都是原本的三倍。比起核裂变过程所产生的氦原子核,组成10~12%宇宙射线的氦原子核通常也有较大的能量,能够穿透人体及数米的固体屏障,而少部分由粒子加速器制造的高能氦原子核也具有相同的能量。
名称
[编辑]有些科学作家会把“双电离氦原子核(He2+
)”和“α粒子”当作相同的术语,但这个命名法并非定义良好。和β、γ粒子/射线一样,粒子的名字都隐含了它的制造过程及所含能量,但这些都没有被严格地应用。[3] 因此,当所指的是恒星的核聚变反应(例如3氦过程),甚至是宇宙射线的一部分时,"α粒子"可以适当地作为术语使用,比α衰变所产生的还要高能的α是一种不常发生的核裂变-三元裂变的常见产物。然而,由粒子加速器(回旋加速器、同步加速器等)所制造的氦原子核比较不能够被称为“α粒子”。
α粒子的来源
[编辑]α衰变
[编辑]

α粒子广为人知的来源为重原子(>106 u)的α衰变。当原子在α衰变中放出α粒子,原子的质量数会因为失去α粒子的四个核子而减少四,原子序会因为失去两个质子而减少二,该原子会变成新的元素。例如:铀衰变成钍、镭衰变成氡即为这类由α衰变进行的核嬗变。
α粒子容易从所有具高放射性的原子放出,如铀、钍、锕、镭以及超铀元素。与其他衰变不同的是,α衰变必须要有一个最小的原子核以完成这一过程。迄今为止发现能够协助此过程的最小原子核为铍-8以及碲元素中最轻的核素,其质量数介于104到109之间。α衰变有时会把原子核留在激发态,而原子核会放出γ射线以释出多余的能量。
α衰变的反应机制
[编辑]和β衰变相比,α衰变中包含的基本相互作用是电磁力与核力的平衡。带正电的原子核与α粒子之间的库仑静电力[2]促使α衰变发生,而核力则会抑制它发生。在经典物理学中,α粒子并没有足够的能量脱离原子核内部强力形成的势能井。
然而,量子隧穿效应使α粒子能够在能量不足的情况克服核力。物质波的性质允许α粒子在距离原子核较远的区域停留,此时电磁力能够抵销核力。因此α粒子能够逃脱。
三元裂变
[编辑]核裂变过程中若发生相对稀有(数百分之一)的三元裂变,会产生特别高能的α粒子。在此过程中,比起一般过程的两个,它会生成三个高能粒子,其中最小的粒子有90%的概率为α粒子,由于此类α粒子的能量高达16 MeV,它们被称为长射程α粒子,能量比起α衰变产生的α粒子还高出许多。中子诱发核裂变(发生在核反应堆的核反应)或是可裂变物质及可裂变锕系元素的核素(也就是可进行核裂变的重原子)进行自发核裂变(一种放射性衰变)时都可能发生三元裂变。无论是诱发或自发裂变,较重的原子核使长射程α粒子能够有比起α衰变产生的α粒子有更高的能量。
加速器
[编辑]高能氦原子核(氦离子)可以从回旋加速器、同步加速器等粒子加速器制造。传统上我们一般不会将其称为α粒子。
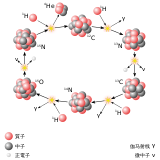
太阳的核反应
[编辑]氦原子核可能参与星体的核反应,历史上我们偶尔会将其视为α反应(参见3氦过程)。
宇宙射线
[编辑]组成宇宙射线10~12%的超高能氦原子核有时会被当成α粒子,宇宙射线生成的机制目前仍争论不休。
能量与吸收
[编辑]
α衰变放出的α粒子的能量有少部分和放射过程的半衰期有关,盖格-纳托法则表明半衰期时间在位数上的差异对能量的影响小于50%。
放出的α粒子所拥有的能量不同,虽然较大的原子核会放出较高能量的α粒子,但大部分α粒子的能量会介于3~7 MeV (兆电子伏特),其上下限对应到放射半衰期极短和极长的核素放出的α粒子。能量与波长的关系使其可以用α光谱测定法识别特定核素。
拥有5 MeV 动能的典型α粒子其速度为15,000 km/s,相当于光速的5%。对单一粒子来说这个能量相当高,但高质量代表它比起其他辐射(例如β粒子、中子辐射)来说速度较小[注 1]
因为它的带电及质量,α粒子可以轻易地被材料吸收,它也只能在空气中移动数公分,它可以被卫生纸或人类的皮肤吸收,通常可以穿透皮肤40微米,相当于数个细胞的深度。
对生物的影响
[编辑]由于α粒子的吸收范围短且无法穿透皮肤表层,除非直接摄入或吸入会放射α粒子的物质,否则α粒子一般不会对生命造成危害。[5]因为其高质量及强吸收,若放出α粒子的放射性同位素进入人体(吞入、摄入或注射,1950年前二氧化钍悬浮液曾被当作X光的显影剂使用),它是电离辐射中电离性最强、最具破坏性的,可能引起任何种类的辐射中毒。估计同剂量α粒子对染色体的影响比β、γ辐射高出10到1000倍,平均为20倍。一项关于内暴露在钚和铀的α辐射,与欧洲核工人的有关研究发现,当相对生物效应为20时,其致癌率(以肺癌为例)与外部暴露在γ辐射一样。也就是说,摄入一单位的α粒子,其危险性与暴露在20单位的γ辐射相同。[6]强α放射物钋-210(1 mg的210Po每秒放出的α粒子与4.215 g的226Ra相同)被怀疑与肺癌和膀胱癌有关(烟草的成分之一)。[7]钋-210曾被用来杀死俄罗斯反政府人士,2006年被用于毒害前俄罗斯联邦调查局中校亚历山大·瓦尔杰洛维奇·利特维年科。[8]
α粒子放射性同位素被吞入时,它的危险度会远胜于预计的半衰期与衰变速率,因为其高相对生物效应会对生物造成伤害。比起同等活性的β或γ放射性同位素,α粒子的危险性在平均上高出20倍,若摄入α放射物则会提高到1000倍。[9]
α粒子的历史
[编辑]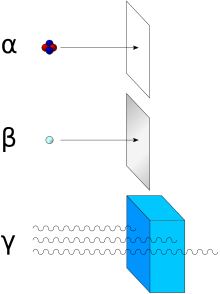


在1899年,物理学家拉赛福(在加拿大蒙特利尔的麦基尔大学工作)与维拉尔(在巴黎工作)以穿透性与在磁场中的偏折把辐射分类成三种,拉赛福将其命名为α、β与γ。[10]拉赛福将α定义为对一般物体穿透力最低的辐射。
拉赛福的工作也包含了测量α粒子的质荷比,让他有了α粒子是+2价氦离子的猜想(之后发现是氦原子核)。[11]1907年,拉赛福和托马斯终于证明α粒子确实是氦离子。[12]他们让α粒子粒子穿过一个真空管的玻璃薄壁,之后管中捕捉到大量的粒子。随后,他们让管中产生电火花,由光谱确认捕捉到的粒子为氦离子,并证实α粒子就是氦离子。
因为α粒子能自然产生,又带有能够参与核反应的高能量,因此对α粒子的研究可以带来早期的核物理学知识。拉赛福用溴化镭放出的α粒子推断汤姆孙的梅子布丁模型在根本上有瑕疵。在拉赛福的学生盖革和马士登进行的α粒子金箔散射实验中,一束α粒子被制造并射向金箔(几百个原子薄)。以硫化锌硫化锌当作光屏,α粒子撞上时会产生光线,拉赛福认为若原子的梅子布丁模型是正确的,则均匀分布的正电荷应只会让带正电的α粒子轻微偏转。
实验发现有些α粒子偏折的幅度比预期的大(在拉赛福的建议下进行确认),有些甚至几乎反弹回来,拉赛福认为若梅子布丁模型是正确的,则被反弹的粒子就像是15吋的炮弹射向卫生纸,但炮弹却被弹开一样。只有当原子的正电荷集中在中心时,才能将α粒子弹开,也就是原子核。
在这之前,没有人知道α粒子自己就是原子核,也不知道质子和中子。这次实验后,汤姆孙的的梅子布丁模型被遗弃,之后出现了玻尔模型以及现代的波动力学模型。
在1917年,拉赛福意外地用α粒子进行了核嬗变。1901年之后一个元素转换成另一个元素被认为是自然的放射性衰变,但当拉赛福将α衰变产生的α粒子射入空气时,产生了新的辐射,后来被确认是氢离子(拉赛福命名为质子)。之后的实验发现质子是由空气中的氮气产生,而这个反应被推定是氮转变成氧的核嬗变。
- 14N + α → 17O + p
这是第一个被发现的核反应。
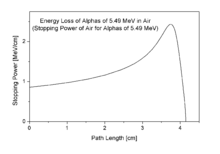
在右边的布拉格曲线中,可看见α粒子在末段失去较多能量。[13]
反α粒子
[编辑]2011年,STAR的成员在美国能源部的布鲁克黑文国家实验室中,利用相对论性重离子对撞机发现了氦原子核的反物质,也被称作反α。[14]该实验将金离子以接近光速对撞以产生反粒子。[15]
应用
[编辑]- 电离烟雾探测器里面会有少量的α放射物镅-241。α粒子会电离空气让电流通过。火焰引起的烟雾粒子会使电流降低,进而使警报响起。此同位素无论是吸入或摄入都非常危险,但只要保持密封就可以将伤害最小化。许多美国直辖市已经计划收集并回收老旧的烟雾探测器以避免它们进入一般的垃圾处理管道。
- 科学家正尝试利用α放射性同位素的破坏性,以少量同位素破坏肿瘤。
α粒子用于治疗癌症
[编辑]α放射性同位素可以用三种方式根除恶性肿瘤:针对特定组织进行不熔放射性治疗(镭-223),作为放射源置入肿瘤(镭-224)和作为肿瘤指向分子的连结物(比如抗体与抗原(肿瘤)的关系)。
镭-223
[编辑]- 注入循环系统的放射性核素可以抵达有血管的地方。然而,这也代表对于内部并未血管化(里面几乎没有血流通过)的大型肿瘤来说,无法有效地以辐射来根除。
- 烟雾探测器带有作为能量来源的镭元素。
镭-224
[编辑]- 镭-224是放射性原子,作为新型癌症治疗方式DaRT(扩散α放射性治疗)的α辐射来源。
- Alpha DaRT由数个以镭-224浸泡的不锈钢圆型管线组成。每个镭-224会产生6个衰变产物,放出4个α粒子。α粒子的射程仅有100微米,不足以处理大部分的肿瘤,然而镭-224的衰变产物可以在组织内2~3毫米的范围内扩散,借此产生有足够的辐射的"死区"以清除肿瘤(当管线设置恰当时)。[17]
- 镭-224的半衰期足够短(3.6天),可以有快速的临床效果而避免长期暴露在辐射下,引起伤害。同时,它的半衰期够长,让它可以有足够的时间从世界上的任何地方送到癌症治疗中心。
α标靶治疗
[编辑]- 针对实体肿瘤的α标靶治疗包含连接α放射性同位素到肿瘤指向分子上(就像抗体一样),可以用静脉注射的方式治疗癌症病人。
α辐射与DRAM错误
[编辑]1978年,Intel的DRAM(动态随机存取记忆体)芯片的"软性错误"被发现与α粒子有关。之后该公司借由严格控制半导体材料中的放射性元素包装解决了这项错误。[18]
参见
[编辑]注释
[编辑]参考资料
[编辑]- ^ CODATA Value: Alpha particle mass. NIST. [15 September 2011]. (原始内容存档于2022-03-04).
- ^ 2.0 2.1 Krane, Kenneth S. Introductory Nuclear Physics. John Wiley & Sons. 1988: 246–269. ISBN 978-0-471-80553-3.
- ^ Darling, David. Alpha particle. Encyclopedia of Science. [7 December 2010]. (原始内容存档于14 December 2010).
- ^ Firestone, Richard B. Table of isotopes. Coral M. Baglin 8th ed., 1999 update with CD-ROM. New York: Wiley. 1999. ISBN 0-471-35633-6. OCLC 43118182.
- ^ Christensen, D. M.; Iddins, C. J.; Sugarman, S. L. Ionizing radiation injuries and illnesses. Emergency Medicine Clinics of North America. 2014, 32 (1): 245–65. PMID 24275177. doi:10.1016/j.emc.2013.10.002.
- ^
Grellier, James; et al. Risk of lung cancer mortality in nuclear workers from internal exposure to alpha particle-emitting radionuclides. Epidemiology. 2017, 28 (5): 675–684. PMC 5540354
 . PMID 28520643. doi:10.1097/EDE.0000000000000684.
. PMID 28520643. doi:10.1097/EDE.0000000000000684.
- ^ Radford, Edward P.; Hunt, Vilma R. Polonium-210: A Volatile Radioelement in Cigarettes. Science. 1964, 143 (3603): 247–249. Bibcode:1964Sci...143..247R. PMID 14078362. S2CID 23455633. doi:10.1126/science.143.3603.247.
- ^ Cowell, Alan. Radiation Poisoning Killed Ex-Russian Spy. The New York Times. 24 November 2006 [15 September 2011]. (原始内容存档于2019-06-19).
- ^ Little, John B.; Kennedy, Ann R.; McGandy, Robert B. Effect of Dose Rate on the Induction of Experimental Lung Cancer in Hamsters by α Radiation. Radiation Research. 1985, 103 (2): 293–9. Bibcode:1985RadR..103..293L. JSTOR 3576584. PMID 4023181. doi:10.2307/3576584.
- ^ Rutherford distinguished and named α and β rays on page 116 of: E. Rutherford (1899) "Uranium radiation and the electrical conduction produced by it," (页面存档备份,存于互联网档案馆) Philosophical Magazine, Series 5, vol. 47, no. 284, pages 109–163. Rutherford named γ rays on page 177 of: E. Rutherford (1903) "The magnetic and electric deviation of the easily absorbed rays from radium," Philosophical Magazine, Series 6, vol. 5, no. 26, pages 177–187.
- ^ Hellemans, Alexander; Bunch, Bryan. The Timetables of Science. Simon & Schuster. 1988: 411. ISBN 0671621300.
- ^ E. Rutherford and T. Royds (1908) "Spectrum of the radium emanation," Philosophical Magazine, Series 6, vol. 16, pages 313–317.
- ^ Magazine "nuclear energy" (III/18 (203) special edition, Volume 10, Issue 2 /1967.
- ^
Agakishiev, H.; et al. (STAR collaboration). Observation of the antimatter helium-4 nucleus. Nature. 2011, 473 (7347): 353–6. Bibcode:2011Natur.473..353S. PMID 21516103. S2CID 118484566. arXiv:1103.3312
 . doi:10.1038/nature10079.. See also Erratum. Nature. 2011, 475 (7356): 412. S2CID 4359058. arXiv:1103.3312
. doi:10.1038/nature10079.. See also Erratum. Nature. 2011, 475 (7356): 412. S2CID 4359058. arXiv:1103.3312  . doi:10.1038/nature10264.
. doi:10.1038/nature10264.
- ^ Antihelium-4: Physicists nab new record for heaviest antimatter. PhysOrg. 24 April 2011 [15 November 2011]. (原始内容存档于2012-01-04).
- ^ Parker, C; Nilsson, S; Heinrich, D. Alpha emitter radium-223 and survival in metastatic prostate cancer. New England Journal of Medicine. 18 July 2013, 369 (3): 213–23 [2022-03-02]. PMID 23863050. doi:10.1056/NEJMoa1213755
 . (原始内容存档于2022-06-17).
. (原始内容存档于2022-06-17).
- ^ Arazi, L; Cooks, T; Schmidt, M; Keisari, Y; Kelson, I. Treatment of solid tumors by interstitial release of recoiling short-lived alpha emitters. Phys Med Biol. 21 August 2007, 52 (16): 5025–42 [2022-03-02]. Bibcode:2007PMB....52.5025A. PMID 17671351. doi:10.1088/0031-9155/52/16/021. (原始内容存档于2022-08-05).
- ^ May, T. C.; Woods, M. H. Alpha-particle-induced soft errors in dynamic memories. IEEE Transactions on Electron Devices. 1979, 26 (1): 2–9. Bibcode:1979ITED...26....2M. S2CID 43748644. doi:10.1109/T-ED.1979.19370.
延伸阅读
[编辑]- Tipler, Paul; Llewellyn, Ralph. Modern Physics 4th. W. H. Freeman. 2002. ISBN 978-0-7167-4345-3.