α粒子
 | |
| 組成 | 兩個質子及兩個中子 |
|---|---|
| 系 | 玻色子 |
| 符號 | α, α2+, He2+ |
| 質量 | 6.644657230(82)×10−27 kg[1] 4.001506179127(63) u |
| 電荷 | +2 e |
| 自旋 | 0[2] |
| CAS號 | 12587-46-1 |
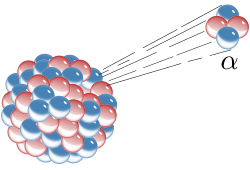
α粒子(英語:Alpha particle),也被稱作α射線或α輻射,是由兩個質子及兩個中子組成的粒子,其與氦-4的原子核相同。它以第一個希臘字母α命名,可以寫作α或α2+,通常在α衰變中產生。因為α粒子與氦原子核相同,有時也會寫成He2+
或4
2He2+
以代表+2價(失去兩個電子)的氦離子。當α粒子從環境中得到電子,它就會變成一般(電中性)的氦原子4
2He。
α粒子的自旋為0。由於標準α放射性衰變的機制,α粒子一般會有大約5 MeV的動能以及相當於4%光速的速度。(見下方「#能量與吸收」)。它是具高游離性的粒子輻射,通常(當其由放射性α衰變產生時)有較小的穿透深度(可以被數公分的大氣層,或人類皮膚阻擋)。
然而,由三元分裂產生的所謂長射程α粒子能量及穿透深度都是原本的三倍。比起核分裂過程所產生的氦原子核,組成10~12%宇宙射線的氦原子核通常也有較大的能量,能夠穿透人體及數公尺的固體屏障,而少部分由粒子加速器製造的高能氦原子核也具有相同的能量。
名稱
[編輯]有些科學作家會把「雙游離氦原子核(He2+
)」和「α粒子」當作相同的術語,但這個命名法並非定義良好。和β、γ粒子/射線一樣,粒子的名字都隱含了它的製造過程及所含能量,但這些都沒有被嚴格地應用。[3] 因此,當所指的是恆星的核融合反應(例如3氦過程),甚至是宇宙射線的一部分時,"α粒子"可以適當地作為術語使用,比α衰變所產生的還要高能的α是一種不常發生的核分裂-三元分裂的常見產物。然而,由粒子加速器(迴旋加速器、同步加速器等)所製造的氦原子核比較不能夠被稱為「α粒子」。
α粒子的來源
[編輯]α衰變
[編輯]

α粒子廣為人知的來源為重原子(>106 u)的α衰變。當原子在α衰變中放出α粒子,原子的質量數會因為失去α粒子的四個核子而減少四,原子序會因為失去兩個質子而減少二,該原子會變成新的元素。例如:鈾衰變成釷、鐳衰變成氡即為這類由α衰變進行的核轉換。
α粒子容易從所有具高放射性的原子放出,如鈾、釷、錒、鐳以及超鈾元素。與其他衰變不同的是,α衰變必須要有一個最小的原子核以完成這一過程。迄今為止發現能夠協助此過程的最小原子核為鈹-8以及碲元素中最輕的核素,其質量數介於104到109之間。α衰變有時會把原子核留在激發態,而原子核會放出γ射線以釋出多餘的能量。
α衰變的反應機制
[編輯]和β衰變相比,α衰變中包含的基本交互作用是電磁力與核力的平衡。帶正電的原子核與α粒子之間的庫侖靜電力[2]促使α衰變發生,而核力則會抑制它發生。在古典物理學中,α粒子並沒有足夠的能量脫離原子核內部強力形成的位能井。
然而,量子穿隧效應使α粒子能夠在能量不足的情況克服核力。物質波的性質允許α粒子在距離原子核較遠的區域停留,此時電磁力能夠抵銷核力。因此α粒子能夠逃脫。
三元分裂
[編輯]核分裂過程中若發生相對稀有(數百分之一)的三元分裂,會產生特別高能的α粒子。在此過程中,比起一般過程的兩個,它會生成三個高能粒子,其中最小的粒子有90%的機率為α粒子,由於此類α粒子的能量高達16 MeV,它們被稱為長射程α粒子,能量比起α衰變產生的α粒子還高出許多。中子誘發核分裂(發生在核反應爐的核反應)或是可裂變物質及可裂變錒系元素的核素(也就是可進行核分裂的重原子)進行自發核分裂(一種放射性衰變)時都可能發生三元分裂。無論是誘發或自發分裂,較重的原子核使長射程α粒子能夠有比起α衰變產生的α粒子有更高的能量。
加速器
[編輯]高能氦原子核(氦離子)可以從迴旋加速器、同步加速器等粒子加速器製造。傳統上我們一般不會將其稱為α粒子。
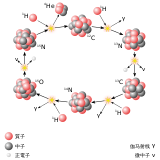
太陽的核反應
[編輯]氦原子核可能參與星體的核反應,歷史上我們偶爾會將其視為α反應(參見3氦過程)。
宇宙射線
[編輯]組成宇宙射線10~12%的超高能氦原子核有時會被當成α粒子,宇宙射線生成的機制目前仍爭論不休。
能量與吸收
[編輯]
α衰變放出的α粒子的能量有少部分和放射過程的半衰期有關,蓋格-納托法則表明半衰期時間在位數上的差異對能量的影響小於50%。
放出的α粒子所擁有的能量不同,雖然較大的原子核會放出較高能量的α粒子,但大部分α粒子的能量會介於3~7 MeV (兆電子伏特),其上下限對應到放射半衰期極短和極長的核素放出的α粒子。能量與波長的關係使其可以用α光譜測定法識別特定核種。
擁有5 MeV 動能的典型α粒子其速度為15,000 km/s,相當於光速的5%。對單一粒子來說這個能量相當高,但高質量代表它比起其他輻射(例如β粒子、中子輻射)來說速度較小[註 1]
因為它的帶電及質量,α粒子可以輕易地被材料吸收,它也只能在空氣中移動數公分,它可以被衛生紙或人類的皮膚吸收,通常可以穿透皮膚40微米,相當於數個細胞的深度。
對生物的影響
[編輯]由於α粒子的吸收範圍短且無法穿透皮膚表層,除非直接攝入或吸入會放射α粒子的物質,否則α粒子一般不會對生命造成危害。[5]因為其高質量及強吸收,若放出α粒子的放射性同位素進入人體(吞入、攝入或注射,1950年前二氧化釷懸浮液曾被當作X光的顯影劑使用),它是游離輻射中游離性最強、最具破壞性的,可能引起任何種類的輻射中毒。估計同劑量α粒子對染色體的影響比β、γ輻射高出10到1000倍,平均為20倍。一項關於內暴露在鈽和鈾的α輻射,與歐洲核工人的有關研究發現,當相對生物效應為20時,其致癌率(以肺癌為例)與外部暴露在γ輻射一樣。也就是說,攝入一單位的α粒子,其危險性與暴露在20單位的γ輻射相同。[6]強α放射物釙-210(1 mg的210Po每秒放出的α粒子與4.215 g的226Ra相同)被懷疑與肺癌和膀胱癌有關(菸草的成分之一)。[7]釙-210曾被用來殺死俄羅斯反政府人士,2006年被用於毒害前俄羅斯聯邦調查局中校亞歷山大·瓦爾傑洛維奇·利特維年科。[8]
α粒子放射性同位素被吞入時,它的危險度會遠勝於預計的半衰期與衰變速率,因為其高相對生物效應會對生物造成傷害。比起同等活性的β或γ放射性同位素,α粒子的危險性在平均上高出20倍,若攝入α放射物則會提高到1000倍。[9]
α粒子的歷史
[編輯]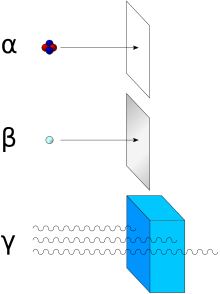


在1899年,物理學家拉賽福(在加拿大蒙特婁的麥基爾大學工作)與維拉爾(在巴黎工作)以穿透性與在磁場中的偏折把輻射分類成三種,拉賽福將其命名為α、β與γ。[10]拉賽福將α定義為對一般物體穿透力最低的輻射。
拉賽福的工作也包含了測量α粒子的質荷比,讓他有了α粒子是+2價氦離子的猜想(之後發現是氦原子核)。[11]1907年,拉賽福和托馬斯終於證明α粒子確實是氦離子。[12]他們讓α粒子粒子穿過一個真空管的玻璃薄壁,之後管中捕捉到大量的粒子。隨後,他們讓管中產生電火花,由光譜確認捕捉到的粒子為氦離子,並證實α粒子就是氦離子。
因為α粒子能自然產生,又帶有能夠參與核反應的高能量,因此對α粒子的研究可以帶來早期的核物理學知識。拉賽福用溴化鐳放出的α粒子推斷湯木生的梅子布丁模型在根本上有瑕疵。在拉賽福的學生蓋革和馬士登進行的α粒子金箔散射實驗中,一束α粒子被製造並射向金箔(幾百個原子薄)。以硫化鋅硫化鋅當作光屏,α粒子撞上時會產生光線,拉賽福認為若原子的梅子布丁模型是正確的,則均勻分布的正電荷應只會讓帶正電的α粒子輕微偏轉。
實驗發現有些α粒子偏折的幅度比預期的大(在拉賽福的建議下進行確認),有些甚至幾乎反彈回來,拉賽福認為若梅子布丁模型是正確的,則被反彈的粒子就像是15吋的砲彈射向衛生紙,但砲彈卻被彈開一樣。只有當原子的正電荷集中在中心時,才能將α粒子彈開,也就是原子核。
在這之前,沒有人知道α粒子自己就是原子核,也不知道質子和中子。這次實驗後,湯木生的的梅子布丁模型被遺棄,之後出現了波耳模型以及現代的波動力學模型。
在1917年,拉賽福意外地用α粒子進行了核轉換。1901年之後一個元素轉換成另一個元素被認為是自然的放射性衰變,但當拉賽福將α衰變產生的α粒子射入空氣時,產生了新的輻射,後來被確認是氫離子(拉賽福命名為質子)。之後的實驗發現質子是由空氣中的氮氣產生,而這個反應被推定是氮轉變成氧的核轉換。
- 14N + α → 17O + p
這是第一個被發現的核反應。
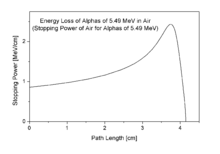
在右邊的布拉格曲線中,可看見α粒子在末段失去較多能量。[13]
反α粒子
[編輯]2011年,STAR的成員在美國能源部的布魯克黑文國家實驗室中,利用相對論性重離子對撞機發現了氦原子核的反物質,也被稱作反α。[14]該實驗將金離子以接近光速對撞以產生反粒子。[15]
應用
[編輯]- 游離煙霧探測器裡面會有少量的α放射物鎇-241。α粒子會游離空氣讓電流通過。火焰引起的煙霧粒子會使電流降低,進而使警報響起。此同位素無論是吸入或攝入都非常危險,但只要保持密封就可以將傷害最小化。許多美國直轄市已經計畫收集並回收老舊的煙霧探測器以避免它們進入一般的垃圾處理管道。
- 科學家正嘗試利用α放射性同位素的破壞性,以少量同位素破壞腫瘤。
α粒子用於治療癌症
[編輯]α放射性同位素可以用三種方式根除惡性腫瘤:針對特定組織進行不熔放射性治療(鐳-223),作為放射源置入腫瘤(鐳-224)和作為腫瘤指向分子的連結物(比如抗體與抗原(腫瘤)的關係)。
鐳-223
[編輯]- 注入循環系統的放射性核素可以抵達有血管的地方。然而,這也代表對於內部並未血管化(裡面幾乎沒有血流通過)的大型腫瘤來說,無法有效地以放射線來根除。
- 煙霧探測器帶有作為能量來源的鐳元素。
鐳-224
[編輯]- 鐳-224是放射性原子,作為新型癌症治療方式DaRT(擴散α放射性治療)的α輻射來源。
- Alpha DaRT由數個以鐳-224浸泡的不鏽鋼圓型管線組成。每個鐳-224會產生6個衰變產物,放出4個α粒子。α粒子的射程僅有100微米,不足以處理大部分的腫瘤,然而鐳-224的衰變產物可以在組織內2~3毫米的範圍內擴散,藉此產生有足夠的輻射的"死區"以清除腫瘤(當管線設置恰當時)。[17]
- 鐳-224的半衰期足夠短(3.6天),可以有快速的臨床效果而避免長期暴露在輻射下,引起傷害。同時,它的半衰期夠長,讓它可以有足夠的時間從世界上的任何地方送到癌症治療中心。
α標靶治療
[編輯]- 針對實體腫瘤的α標靶治療包含連接α放射性同位素到腫瘤指向分子上(就像抗體一樣),可以用靜脈注射的方式治療癌症病人。
α輻射與DRAM錯誤
[編輯]1978年,Intel的DRAM(動態隨機存取記憶體)晶片的"軟性錯誤"被發現與α粒子有關。之後該公司藉由嚴格控制半導體材料中的放射性元素包裝解決了這項錯誤。[18]
參見
[編輯]註釋
[編輯]參考資料
[編輯]- ^ CODATA Value: Alpha particle mass. NIST. [15 September 2011]. (原始內容存檔於2022-03-04).
- ^ 2.0 2.1 Krane, Kenneth S. Introductory Nuclear Physics. John Wiley & Sons. 1988: 246–269. ISBN 978-0-471-80553-3.
- ^ Darling, David. Alpha particle. Encyclopedia of Science. [7 December 2010]. (原始內容存檔於14 December 2010).
- ^ Firestone, Richard B. Table of isotopes. Coral M. Baglin 8th ed., 1999 update with CD-ROM. New York: Wiley. 1999. ISBN 0-471-35633-6. OCLC 43118182.
- ^ Christensen, D. M.; Iddins, C. J.; Sugarman, S. L. Ionizing radiation injuries and illnesses. Emergency Medicine Clinics of North America. 2014, 32 (1): 245–65. PMID 24275177. doi:10.1016/j.emc.2013.10.002.
- ^
Grellier, James; et al. Risk of lung cancer mortality in nuclear workers from internal exposure to alpha particle-emitting radionuclides. Epidemiology. 2017, 28 (5): 675–684. PMC 5540354
 . PMID 28520643. doi:10.1097/EDE.0000000000000684.
. PMID 28520643. doi:10.1097/EDE.0000000000000684.
- ^ Radford, Edward P.; Hunt, Vilma R. Polonium-210: A Volatile Radioelement in Cigarettes. Science. 1964, 143 (3603): 247–249. Bibcode:1964Sci...143..247R. PMID 14078362. S2CID 23455633. doi:10.1126/science.143.3603.247.
- ^ Cowell, Alan. Radiation Poisoning Killed Ex-Russian Spy. The New York Times. 24 November 2006 [15 September 2011]. (原始內容存檔於2019-06-19).
- ^ Little, John B.; Kennedy, Ann R.; McGandy, Robert B. Effect of Dose Rate on the Induction of Experimental Lung Cancer in Hamsters by α Radiation. Radiation Research. 1985, 103 (2): 293–9. Bibcode:1985RadR..103..293L. JSTOR 3576584. PMID 4023181. doi:10.2307/3576584.
- ^ Rutherford distinguished and named α and β rays on page 116 of: E. Rutherford (1899) "Uranium radiation and the electrical conduction produced by it," (頁面存檔備份,存於網際網路檔案館) Philosophical Magazine, Series 5, vol. 47, no. 284, pages 109–163. Rutherford named γ rays on page 177 of: E. Rutherford (1903) "The magnetic and electric deviation of the easily absorbed rays from radium," Philosophical Magazine, Series 6, vol. 5, no. 26, pages 177–187.
- ^ Hellemans, Alexander; Bunch, Bryan. The Timetables of Science. Simon & Schuster. 1988: 411. ISBN 0671621300.
- ^ E. Rutherford and T. Royds (1908) "Spectrum of the radium emanation," Philosophical Magazine, Series 6, vol. 16, pages 313–317.
- ^ Magazine "nuclear energy" (III/18 (203) special edition, Volume 10, Issue 2 /1967.
- ^
Agakishiev, H.; et al. (STAR collaboration). Observation of the antimatter helium-4 nucleus. Nature. 2011, 473 (7347): 353–6. Bibcode:2011Natur.473..353S. PMID 21516103. S2CID 118484566. arXiv:1103.3312
 . doi:10.1038/nature10079.. See also Erratum. Nature. 2011, 475 (7356): 412. S2CID 4359058. arXiv:1103.3312
. doi:10.1038/nature10079.. See also Erratum. Nature. 2011, 475 (7356): 412. S2CID 4359058. arXiv:1103.3312  . doi:10.1038/nature10264.
. doi:10.1038/nature10264.
- ^ Antihelium-4: Physicists nab new record for heaviest antimatter. PhysOrg. 24 April 2011 [15 November 2011]. (原始內容存檔於2012-01-04).
- ^ Parker, C; Nilsson, S; Heinrich, D. Alpha emitter radium-223 and survival in metastatic prostate cancer. New England Journal of Medicine. 18 July 2013, 369 (3): 213–23 [2022-03-02]. PMID 23863050. doi:10.1056/NEJMoa1213755
 . (原始內容存檔於2022-06-17).
. (原始內容存檔於2022-06-17).
- ^ Arazi, L; Cooks, T; Schmidt, M; Keisari, Y; Kelson, I. Treatment of solid tumors by interstitial release of recoiling short-lived alpha emitters. Phys Med Biol. 21 August 2007, 52 (16): 5025–42 [2022-03-02]. Bibcode:2007PMB....52.5025A. PMID 17671351. doi:10.1088/0031-9155/52/16/021. (原始內容存檔於2022-08-05).
- ^ May, T. C.; Woods, M. H. Alpha-particle-induced soft errors in dynamic memories. IEEE Transactions on Electron Devices. 1979, 26 (1): 2–9. Bibcode:1979ITED...26....2M. S2CID 43748644. doi:10.1109/T-ED.1979.19370.
延伸閱讀
[編輯]- Tipler, Paul; Llewellyn, Ralph. Modern Physics 4th. W. H. Freeman. 2002. ISBN 978-0-7167-4345-3.