三硫化二砷
外观
| 三硫化二砷 | |
|---|---|

| |
| |
| IUPAC名 Arsenic trisulfide | |
| 别名 | 硫化砷(III)、雌黄 |
| 识别 | |
| CAS号 | 1303-33-9 |
| PubChem | 4093503 |
| ChemSpider | 21241348 |
| SMILES |
|
| InChI |
|
| InChIKey | OUFDYFBZNDIAPD-UHFFFAOYAM |
| EINECS | 215-117-4 |
| RTECS | CG2638000 |
| 性质 | |
| 化学式 | As2S3 |
| 摩尔质量 | 246.04 g·mol−1 |
| 外观 | 橙色晶体 |
| 密度 | 3.43 g cm−3 |
| 熔点 | 310 °C(583 K) |
| 沸点 | 707 °C(980 K) |
| 结构 | |
| 空间群 | P21/n (No. 11) |
| 晶格常数 | a = 1147.5(5) pm, b = 957.7(4) pm, c = 425.6(2) pm |
| 晶格常数 | α = 90°, β = 90.68(8)°, γ = 90° |
| 配位几何 | As:角锥型 |
| 危险性 | |
| H-术语 | H300, H331, H400, H411 |
| NFPA 704 | |
| PEL | [1910.1018] TWA 0.010 mg/m3 |
| 相关物质 | |
| 其他阴离子 | 三氧化二砷 三硒化二砷 |
| 其他阳离子 | 三硫化二磷 硫化锑 硫化铋 |
| 相关化学品 | 四硫化四砷 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
三硫化二砷是一种无机化合物,化学式为As2S3。三硫化二砷在自然界以雌黄矿物的形式存在。[1]
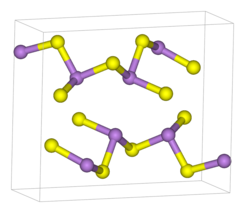
结构
[编辑]三硫化二砷存在晶体和无定形体。[2]单斜的As2S3是层状结构,每个As和3个S成键,As-S为224pm,∠S-As-S 99°;而其蒸气以二聚体As4S6的形式存在,结构与As4O6类似。[3]
属性
[编辑]它是一种半导体,直接的能隙为2.7 eV[4]。 宽的能隙使它对于620 nm至11 µm的红外线透明。
制备
[编辑]三硫化二砷可由单质化合得到,或者从As(III)的溶液中由H2S沉淀。[5]
- 2 As + 3 S → As2S3
化学性质
[编辑]- 2 As2S3 + 9 O2 → 2 As2O3 + 6 SO2
它可以被硫化钠转化为三硫代亚砷酸钠,被多硫化钠转化为四硫代砷酸钠:
- As2S3 + 3 Na2S → 2 Na3AsS3
- As2S3 + 3 Na2S2 → 2 Na3AsS4
而在和氢氧化钠溶液的反应中,会同时产生亚砷酸盐和硫代亚砷酸盐:
- As2S3 + 6 NaOH → Na3AsO3 + Na3AsS3 + 3 H2O
此溶液在经过脱硫、还原等操作可以制得三氧化二砷。[6]当溶液中OH-不足时,则产生偏亚砷酸盐和硫代偏亚砷酸盐:[7]
- 2 As2S3 + 4 NaOH → NaAsO2 + 3 NaAsS2 + 2 H2O
和碳酸钠溶液反应,得到同样的砷化合物:
- 2 As2S3 + Na2CO3 → NaAsO2 + 3 NaAsS2 + 2 CO2↑
- As2S3 + 6 Cl2 → (AsCl3)2·3SCl2
- As2S3 + 3 I2 → 2 AsI3 + 3 S
和氯化亚铜、氯化银等金属氯化物共热,均会产生三氯化砷:[7]
- 3 As2S3 + 6 CuCl —200~300℃→ Cu6As4S9 + 2 AsCl3 (CuCl过量则产生Cu4As2S5)
- 2 As2S3 + 3 AgCl —170℃→ 3 AgAsS2 + AsCl3
- 2 As + 3 Hg2Cl2 → 2 AsCl3 + 6 Hg
- 2 As + 3 HgCl2 → 2 AsCl3 + 3 Hg
用途
[编辑]三硫化二砷可以用于制备砷单质[8]及三氧化二砷[9]、砷酸盐[10]等其它砷化合物。
此外,三硫化二砷还能用作防腐剂,或在医药领域有所应用。[11]
安全
[编辑]As2S3不溶于水,因此毒性低。 老化的样品中可能含有大量的砷氧化物,这些氧化物是可溶的,因此具有剧毒。
自然界的发生
[编辑]在火山环境中发现了雌黄,通常与其他硫化砷(主要是雄黄)一起被发现。 有时会在低温热液脉中发现它,以及一些其他硫化物和亚硫酸盐矿物。
参考文献
[编辑]- ^ 1.0 1.1 武汉大学 吉林大学等. 无机化学(第三版)下册. 高等教育出版社, 2011. pp 704-706. ISBN 978-7-04-004880-3
- ^ Wells, A.F. (1984). Structural Inorganic Chemistry, Oxford: Clarendon Press. ISBN 0-19-855370-6.
- ^ 无机化学丛书. 第四卷 氮 磷 砷分族. 科学出版社. pp 408. 三硫化二砷
- ^ Arsenic sulfide (As2S3). [2020-06-11]. (原始内容存档于2018-10-07).
- ^ Справочник химика. Редкол.: Никольский Б.П. и др.. (3-е изд.). испр. — Л.: Химия, 1971. Т. 2. pp 1168.
- ^ 郑雅杰, 刘万宇, 白猛. 采用硫化砷渣制备三氧化二砷工艺. 中南大学学报:自然科学版, 2008. 39(6): 1157-1163
- ^ 7.0 7.1 7.2 陈寿椿. 重要无机化学反应. 上海科学技术出版社, 1994
- ^ 侯汉娜, 陈甜甜. 硫化砷渣全湿法制备单质砷的研究. 环境保护科学, 2014(6):42-45
- ^ 孟文杰, 施孟华, 李倩 等. 硫化砷渣湿法制取三氧化二砷的处理技术现状. 贵州化工, 2008, 33(5):26-28
- ^ 赖建林, 李勤. 用硫化砷渣制取砷酸铜. 有色金属:冶炼部分, 2001, 1(2):42-44
- ^ 曹梦晔, 巩江, 高昂 等. 雌黄药学研究概况. 辽宁中医药大学学报, 2011(3):54-56
外部链接
[编辑]- (英文)UK Poison Information Document(页面存档备份,存于互联网档案馆)
- (英文)WHO Food Additives Series 24(页面存档备份,存于互联网档案馆)
- (英文)JECFA Evaluation: Arsenic(页面存档备份,存于互联网档案馆)
- (英文)Arsenic trisulfide
| ||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

