一氧化碳
| 一氧化碳 | |||
|---|---|---|---|
| |||
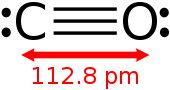
| |||
| IUPAC名 carbon monoxide 一氧化碳 | |||
| 別名 | 煙道氣(flue gas) carbonous oxide | ||
| 識別 | |||
| CAS編號 | 630-08-0 | ||
| PubChem | 281 | ||
| ChemSpider | 275 | ||
| SMILES |
| ||
| InChI |
| ||
| InChIKey | UGFAIRIUMAVXCW-UHFFFAOYAT | ||
| Beilstein | 3587264 | ||
| Gmelin | 421 | ||
| UN編號 | 1016 | ||
| EINECS | 211-128-3 | ||
| ChEBI | 17245 | ||
| RTECS | FG3500000 | ||
| KEGG | D09706 | ||
| MeSH | Carbon+monoxide | ||
| 性質 | |||
| 化學式 | CO | ||
| 莫耳質量 | 28.0101 g·mol⁻¹ | ||
| 外觀 | 無色無味氣體 | ||
| 密度 | (液)0.789 g/cm³ 0 °C 1 atm, 1.250 g/L 25 °C 1 atm, 1.145 g/L | ||
| 熔點 | -205 °C | ||
| 沸點 | -192.5 °C | ||
| 溶解性(水) | 0.0026 g/100 mL(20 °C) | ||
| 溶解性 | 易溶於氯仿,乙酸,乙酸乙酯,乙醇,氨水 | ||
| 偶極矩 | 0.112 D(3.74×10−31 C·m) | ||
| 結構 | |||
| 混成軌域 | 氧和碳各形成兩個sp混層軌域 | ||
| 危險性 | |||
| 歐盟危險性符號 | |||
| 警示術語 | R:R12-R26-R33-R48-R61 | ||
| 安全術語 | S:S9-S16-S33-S45-S53-S63 | ||
| NFPA 704 | |||
| 閃點 | −191 °C | ||
| 自燃溫度 | 609 °C | ||
| 相關物質 | |||
| 相關氧化物 | 二氧化碳,二氧化三碳,一氧化二碳,三氧化碳 | ||
| 附加數據頁 | |||
| 結構和屬性 | 折射率、介電係數等 | ||
| 熱力學數據 | 相變數據、固、液、氣性質 | ||
| 光譜數據 | UV-Vis、IR、NMR、MS等 | ||
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |||
一氧化碳(英語:Carbon monoxide),分子式為CO,是無色、無臭、無味的無機化合物氣體,比空氣略輕。在水中的溶解度甚低,但易溶於氨水。空氣混合爆炸極限為12.5%~74%。 一氧化碳是含碳物質不完全燃燒的產物。也可以作為燃料使用,煤和水在高溫下可以生成水煤氣(一氧化碳與氫氣的混合物)。有些現代技術,如煉鐵,還是會產生副產品的一氧化碳。一氧化碳是可用作身體自然調節炎症反應的三種氣體之一(其他兩種是一氧化氮和硫化氫)。
由於一氧化碳與體內血紅蛋白的親和力比氧與血紅蛋白的親和力大200-300倍,而碳氧血紅蛋白較氧合血紅蛋白的解離速度慢3600倍,當一氧化碳濃度在空氣中達到35ppm,就會對人體產生損害,會造成一氧化碳中毒(又稱煤氣中毒)。
雖然一氧化碳有毒,但動物代謝亦會產生少量一氧化碳,並認為有一些正常的生理功能。
歷史
[編輯]古代希臘人和羅馬人曾經用一氧化碳進行處決。11世紀一位西班牙醫生第一次描述了這種氣體。
最早製備一氧化碳的是法國化學家 de Lassone(1776年)。他通過加熱氧化鋅和碳製得了一氧化碳。但由於一氧化碳燃燒時產生了與氫氣類似的藍色火焰,de Lassone錯誤地認為他製得的是氫氣。在1800年英國化學家William Cruikshank才證明一氧化碳是由碳元素和氧元素組成的化合物。
最早對一氧化碳的毒性進行徹底研究的是法國的生理學家Claude Bernard。在1846年,他讓狗吸入這種氣體,發現狗的血液「變得比任何動脈中的血都要鮮紅」。現在我們知道血液變成「櫻桃紅色」是一氧化碳中毒的症狀。
由於一氧化碳可以使血液變得非常鮮紅的特點,一些肉品商人用一氧化碳處理鮮肉,可以使生肉不被氧化變色,甚至可以在10℃的溫度下保存28天還如同新屠宰的肉,並因此引起非議。美國消費者協會認為即使這種處理沒有害處,也會掩蓋肉不新鮮的狀態,即使肉品處於即將腐爛狀態,消費者也不知情。
據報導,一氧化碳也用在納粹大屠殺名為T4「安樂死」計劃,納粹由海烏姆諾透過貨車運送氣體。
性質
[編輯]一氧化碳的莫耳質量是28.0,它比空氣的莫耳質量28.8略輕。燃燒一氧化碳時會產生藍色火焰。
製備
[編輯]工業用製備
[編輯]在工業上,通常採取二氧化碳在高溫條件下與碳反應的原理製取:
實驗室製備
[編輯]其他
[編輯]有機物在氧氣不足夠的環境下燃燒,會發生不完全燃燒,會生產一氧化碳。例如丙烷的不完全燃燒:
毒性
[編輯]
一氧化碳是無色、無臭、無味氣體,但吸入對人體有十分大的傷害。它會結合血紅蛋白生成碳氧血紅蛋白,碳氧血紅蛋白不能提供氧氣給身體組織。這種情況被稱為血缺氧。濃度低至667ppm可能會導致高達50%人體的血紅蛋白轉換為碳合血紅蛋白,可能會導致昏迷和死亡或變植物人。而香菸中亦含有一氧化碳。 最常見的一氧化碳中毒症狀包括頭痛、噁心、嘔吐、頭暈、疲勞和虛弱,另外還包括視網膜出血,以及異常櫻桃紅色的血。 暴露在一氧化碳中可能嚴重損害心臟和中樞神經系統,會有後遺症。一氧化碳可能令孕婦胎兒產生嚴重的不良影響。
在封閉的環境中,一氧化碳的濃度可以很容易達到造成致命的濃度。平均而言,每年在美國就有170人因一氧化碳而死。然而,根據佛羅里達州衛生署資料「每年有500多名美國人死於一氧化碳意外接觸,美國各地的有數千人因一氧化碳中毒需要緊急醫療照顧」 這些可能產生一氧化碳的產品包括故障的燃料燃燒機器,如爐,爐灶,熱水器和室內加熱器。美國毒物控制中心協會(AAPCC)報告於2007年有39人死於一氧化碳中毒。2005年,美國消費品安全委員會報告有94宗因發電機而導致相關的一氧化碳中毒死亡。一氧化碳也是菸草燃燒產生煙霧的次要成分。 在台灣,根據內政部消防署的統計,2009-2013年間,居家一氧化碳中毒意外事件共計197件,造成 55 人死亡及 471 人受傷。多數原因皆為熱水器安裝不適當所致。[1]
存在
[編輯]一氧化碳存在於各種自然和人造環境中,以「PPM」來度量的典型濃度如下:
| ppmv: 百萬分率 by volume (note: 體積分數 is equal to 莫耳分率 for 理想氣體 only, see 體積 (熱力學)) | |
| 濃度 | 來源 |
|---|---|
| 0.1 ppmv | 大氣中污染的水準(MOPITT)[3] |
| 0.5–5 ppmv | 居家中的平均水準[4] |
| 5–15 ppmv | 居家的火爐、加熱器附近,現代汽車排放的廢氣[5] |
| 17 ppmv | 金星的大氣 |
| 100–200 ppmv | 墨西哥市中心地區的汽車排放[6] |
| 700 ppmv | 火星大氣層 |
| 5,000 ppmv | 家中木材燃燒的排放[7] |
| 7,000 ppmv | 沒有觸媒轉化器的汽車,未經稀釋的暖車尾氣排放[5] |
大氣中的一氧化碳
[編輯]
目前在大氣中,一氧化碳是少量存在的氣體,主要由火山活動產生,但也會因自然和人為的火災(如森林大火,焚燒秸稈和甘蔗以驅趕甘蔗園裏的蚊蟲)所產生。燃燒化石燃料也會產生大量一氧化碳。
而一氧化碳最主要的天然來源是由對流層中的光化學反應而產生,每年產生約5 x 1012千克一氧化碳。
天文物理
[編輯]在地外的星際介質中,一氧化碳十分常見,其分佈之廣,僅次於氫分子,排名第二。由於一氧化碳的分子不對稱,其輻射出的譜線遠比氫分子明亮,因而更容易偵測到。1970年,電波望遠鏡首次在星際空間中偵測到一氧化碳。由於氫分子只能用紫外線檢測,過程中必須使用太空望遠鏡,時至今日,一氧化碳已成為在星系中檢測分子時,最常用的示蹤物。恆星形成過程大多發生於分子雲內,科學家觀測一氧化碳後,對分子雲的認識大有增長[8]。
2021年合成蛋白質爭議
[編輯]中國農業科學院飼料研究所和北京首鋼朗澤新能源科技有限公司於2021年10月30日發布消息稱,中華人民共和國已在國際上首次掌握乙醇梭菌途逕自一氧化碳到蛋白質的規模化生物合成技術,並實現了工業化應用,標誌著中華人民共和國在乙醇梭菌生物合成蛋白質技術領域的重大進步。該消息引致多個中華人民共和國從上至下包括幾乎所有中央級媒體在內的極多媒體的強烈關注和集中報道,此後在被一些生物化學相關領域的科學從業人士了解後引起了廣泛討論和爭議。
參見
[編輯]參考資料
[編輯]- ^ 行政院災害防救辦公室. 行政院災害防救辦公室週報(102 年 12 月 19 日至 102 年 12 月 25 日) (PDF). 2013-12-25 [2015-01-16]. (原始內容 (PDF)存檔於2016-03-08) (中文(繁體)).
- ^ Source for figures: Carbon dioxide, NOAA Earth System Research Laboratory (頁面存檔備份,存於網際網路檔案館), (updated 2010.06). Methane, IPCC TAR table 6.1 (頁面存檔備份,存於網際網路檔案館), (updated to 1998). The NASA total was 17 ppmv over 100%, and CO2 was increased here by 15 ppmv. To normalize, N2 should be reduced by about 25 ppmv and O2 by about 7 ppmv.
- ^ Committee on Medical and Biological Effects of Environmental Pollutants. Carbon Monoxide. Washington, D.C.: National Academy of Sciences. 1977: 29. ISBN 0-309-02631-8.
- ^ Green W. An Introduction to Indoor Air Quality: Carbon Monoxide (CO). United States Environmental Protection Agency. [2008-12-16]. (原始內容存檔於2008-12-18).
- ^ 5.0 5.1 Gosink, Tom. What Do Carbon Monoxide Levels Mean?. Alaska Science Forum. Geophysical Institute, University of Alaska Fairbanks. 1983-01-28 [2007-12-01]. (原始內容存檔於2008-12-25).
- ^ Singer, Siegfried Fred. The Changing Global Environment. Springer. 1975: 90. ISBN 9027704023.
- ^ Gosink T. What Do Carbon Monoxide Levels Mean?. Alaska Science Forum. Geophysical Institute, University of Alaska Fairbanks. January 28, 1983 [December 16, 2008]. (原始內容存檔於2008-12-25).
- ^ Combes, Françoise. Distribution of CO in the Milky Way. Annual Review of Astronomy and Astrophysics. 1991-09-01, 29 (1): 195–237 [2021-04-27]. ISSN 0066-4146. doi:10.1146/annurev.aa.29.090191.001211. (原始內容存檔於2021-04-29).
| ||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||
| ||||||||||||









