组织工程学
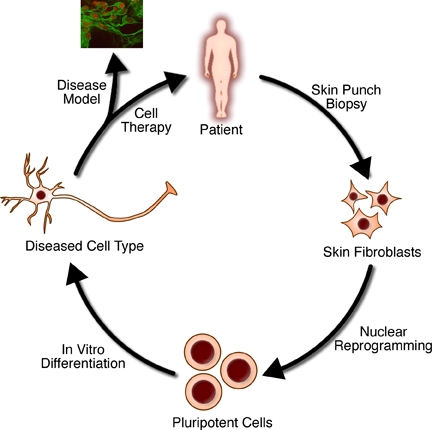
组织工程学(Tissue engineering),是指利用生物活性物质,通过体外培养或构建的方法,再造或者修复器官及组织的技术。这个概念由美国国家科学基金委员会在1987年提出,在此后的二十多年间快速发展。
组织工程学涉及到生物学,材料学和工程学等多学科;目前已经能够再造骨、软骨、皮肤、肾、肝、消化道及角膜、肌肉、乳房等组织器官。
综述[编辑]

目前被普遍运用的组织工程学的定义,是由 Langer 和 Vacanti 所提出的:
组织工程是结合了工程学以及自然科学为一体的综合性学科,致力于发展生代材料以修复,替代,提高人体器官及其功能。[1]
組織工程也被定義為理解組織生長的原理,並生產具備功能性以供替代原先組織的臨床使用。另一個描述接著說,組織工程的基本假設是,利用該系統的生物將在更換,維修,保養,和/或增強組織功能的治療策略下取得更大的效益。
組織工程再多領域多層面的研究下,已經發展出一套對於原料與材料之間的應用有著組織性並且十分新穎的策略,例如生物材料科學的進步,幹細胞應用,特殊生長和轉化因子(differentiation factors)的應用,模擬獨特的仿生環境(biomimetic environments),或是利用物理或化學工程改造的細胞外基質(支架的製程),細胞和生物活性分子之間的組合製備等等。而組織工程目前所遇到的困難主要是如何穩定培養更具複雜性的組織以及如何有效利用實驗室培養出的組織進行移植以及新生組織在生物力學穩定性。
組織工程的持續發展將增長從工程和組織基礎研究同時也會增進組織(tissue)、基質(matrix)、生長因子(growth factor)、幹細胞(stem cell)和發育生物學(developmental biology)、材料科學(materials science)和生物信息學(bioinformatics)的這些學科的融合與應用。
组织工程学的三个要素[编辑]
细胞[编辑]
细胞是一切生物组织最基本的结构单位。干细胞是人体内一种有潜力能够分化为其他类型细胞的特别的细胞,也是生物工程广泛研究和利用的一种手段。
細胞收集與純化[编辑]
從液體組織,例如血液,通常會利用離心或單採血液成分萃取(apheresis)出目標細胞後再進行細胞增生。而從固體組織,純化困難程度較高。通常將組織切碎,然後用胰蛋白酶(trypsin)消化酶或膠原蛋白酶(collagenase)以除去細胞外基質(extracellular matrix)以方便保存的細胞。此時細胞是自由浮動的,之後利用離心法或單採血液成分萃取。
胰蛋白酶作用對溫度敏感性高。在較高的溫度下分解胞外基質速度快,但高溫下相對對細胞的傷害較大。膠原酶作用對溫度敏感性低,對細胞的傷害也較少,但需要更長的時間進行反應,期間會消耗大量昂貴的試劑。
使用細胞的種類[编辑]
一般會利用細胞的來源作為分類依據
- 自體細胞(Autologous cells)是從同一個人的細胞取出後重新植入目標區進行組織再生,自體細胞移植具有最少的問題,像是免疫排斥或是病原體的傳播,但是,在某些情況下可能不可用。例如,有遺傳性疾病的自體細胞不可使用,或者是很患部病灶嚴重的患者(例如:嚴重燒傷)或年長者,可能沒有足夠數量的自體細胞建立有用的細胞株。此外,由於這一類的細胞必須從患者體內採集,此時也需要顧慮在執行這樣的手術操作是否會導致供體部位(donor site)的感染或慢性疼痛,而這兩者間的取捨必須經過縝密評估後再進行抉擇。
由於這類細胞株要從採集到的樣品中進行培養後才能使用,十分花費時間。最近出現了傾向使用來自骨髓和脂肪間葉幹細胞在進行分化(包括骨骼、軟骨、脂肪和神經)的方法,能利用誘導的方式大量分化並產生所需要的細胞。
支架[编辑]
支架是用于支撑细胞成长为一个完整的组织的框架材料。
生长信息[编辑]
用于引导和协调组织内细胞活动的各种方法,目前已知的能够影响细胞活动的生长信息包括各种蛋白质因子和电信号。
组织工程学的医疗应用情况[编辑]
骨骼缺损修复[编辑]
传统临床使的植骨材料主要分为自体骨、同种异体骨、经特殊处理的异种骨和人工骨材料等,这些手段但都存在适用性和并发症等缺陷。随着组织工程学技术的发展,改变了治疗骨缺损的传统治疗模式。而通过组织工程学手段体外培养骨骼组织作为修复材料,则没有其它手段的各种缺点,可以达到理想的效果。
角膜[编辑]
通过体外培养角膜,再移植回人体,让因为角膜缺失或损坏而失明的人士恢复视力。
皮肤[编辑]
对于被烧伤、炎症等因素损害的皮肤,通过体外培养皮肤组织移植人体,达到修复皮肤的外形和功能的目的。
血管[编辑]
心血管疾病包括冠狀動脈閉塞、外周動脈疾病、和其他血管損傷等是急需應用人造血管的例子。不同類型的人造血管已透過許多不同血管組織工程的方法研發出來。 可作血管移植人造血管的例子包括預先種植細胞的人造血管、[2] 由脫細胞血管或用合成生物材料製成的血管。[3]
牙齒[编辑]
參見[编辑]
引用[编辑]
- ^ Langer, R & Vacanti JP, Tissue engineering. Science 260, 920-6; 1993.
- ^ Naegeli, Kaleb M.; Kural, Mehmet H.; Li, Yuling; Wang, Juan; Hugentobler, Emmanuelle A.; Niklason, Laura E. Bioengineering Human Tissues and the Future of Vascular Replacement. Circulation Research. 2022-06-24, 131 (1) [2023-08-13]. ISSN 0009-7330. PMC 9213087
 . PMID 35737757. doi:10.1161/CIRCRESAHA.121.319984. (原始内容存档于2023-08-13) (英语).
. PMID 35737757. doi:10.1161/CIRCRESAHA.121.319984. (原始内容存档于2023-08-13) (英语).
- ^ Chang, William G.; Niklason, Laura E. A short discourse on vascular tissue engineering. npj Regenerative Medicine. 2017-03-27, 2 (1) [2023-08-13]. ISSN 2057-3995. doi:10.1038/s41536-017-0011-6. (原始内容存档于2023-06-25) (英语).
參考文獻[编辑]
- Davis, M.E., et al., Injectable Self-Assembling Peptide Nanofibers Create Intramyocardial Microenvironments for Endothelial Cells. Circulation 111:442-450 (2005).
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||
