噁唑
外觀
| 㗁唑 | |
|---|---|
| |
| IUPAC名 1,3-oxazole 1,3-㗁唑 | |
| 英文名 | Oxazole |
| 識別 | |
| CAS號 | 288-42-6 |
| PubChem | 9255 |
| ChemSpider | 8898 |
| SMILES |
|
| InChI |
|
| InChIKey | ZCQWOFVYLHDMMC-UHFFFAOYAD |
| EINECS | 206-020-8 |
| ChEBI | 35597 |
| MeSH | D010080 |
| 性質 | |
| 化學式 | C3H3NO |
| 摩爾質量 | 69.06 g·mol⁻¹ |
| 密度 | 1.050 g/cm3 |
| 沸點 | 69-70 °C |
| pKa | 0.8 (其共軛酸) [1] |
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |
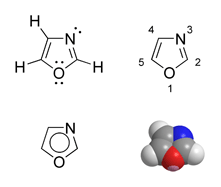
㗁唑(Oxazole)是一大類有機雜環化合物的母體,含有一個氧雜原子和一個氮雜原子。[2]
生物化學
[編輯]在生物化學中,由絲氨酸和蘇氨酸非核糖體多肽環化然後氧化就可以得到噁唑。
在生物體內,噁唑並不像噻唑那樣普遍,後者是噁唑的類似物,用硫原子取代噁唑中的氧原子。
性質
[編輯]噁唑是一個芳香性化合物,但是其芳香性不及噻唑。噁唑也是一個弱鹼,其共軛酸的pKa值是0.8,相比而言,咪唑的共軛酸的pKa是7。
有機合成
[編輯]對於噁唑,經典的有機合成方法有以下幾種:
- Robinson-Gabriel合成:對2-酰氨酮脫水得到噁唑。
- 費歇爾噁唑合成:通過氰醇和醛合成噁唑。
- Bredereck反應:α-鹵代酮與甲酰胺合成噁唑。
- 其他文獻上提到過的方法:
- 噁唑也能夠通過某些炔丙基胺的環化異構化生成。 在一個實驗中[3] ,化學家使用一次性合成法合成了噁唑,過程是首先用炔丙基胺與苯甲酰氯縮合形成酰胺,然後經過一個端基炔的Sonogashira偶聯反應,然後再加入同樣當量的苯甲酰氯,最後由對甲基苯磺酸催化完成環化異構化形成產物。
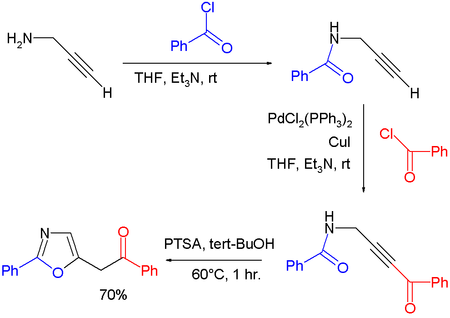

有機反應
[編輯]- 在C2位置對噁唑進行去質子化常常伴隨着異腈化合物的開環。
- 在有活化基的情況下可以在C5發生親電芳香取代反應。
- 若C2位置有離去集團,則可以發生親核芳香取代反應。
- 由噁唑雙烯發生狄爾斯-阿爾德反應,然後脫去氧原子形成嘧啶。
- 4-酰基噁唑的康福斯重排是一個熱重排反應,酰基部分和C5發生重排。
- 多種氧化反應。其中一例 [5]是對4,5-二苯基噁唑的氧化。將其與三當量的硝酸鈰銨反應生成甲酰胺與苯甲酸:

在平衡的半反應中可以看出,對於一當量的噁唑,該反應消耗了三當量的水,產生了四個質子和四個電子,後者是來自CeIV。
參見
[編輯]- 異噁唑,氮在2位的類似物。
- 咪唑,氧被氮取代了的類似物。
- 噻唑,氧被硫取代了的類似物
- 苯並噁唑,噁唑於其他環相連。
- 吡咯,沒有氧原子的一個類似物。
- 呋喃,沒有氮原子的一個類似物。
- 噁唑啉,其中一個雙鍵被還原。
- 噁唑烷,兩個雙鍵均被還原。
- 芳香環
參考文獻
[編輯]- ^ Zoltewicz, J. A. & Deady, L. W. Quaternization of heteroaromatic compounds. Quantitative aspects. Adv. Heterocycl. Chem. 22, 71-121 (1978).
- ^ Heterocyclic Chemistry TL Gilchrist, The Bath press 1985 ISBN 0-582-01421-2
- ^ A new consecutive three-component oxazole synthesis by an amidation–coupling–cycloisomerization (ACCI) sequence Eugen Merkul and Thomas J. J. Müller Chem. Commun., 2006, 4817 - 4819, doi:10.1039/b610839c
- ^ Fully Automated Continuous Flow Synthesis of 4,5-Disubstituted Oxazoles Marcus Baumann, Ian R. Baxendale, Steven V. Ley, Christoper D. Smith, and Geoffrey K. Tranmer Org. Lett.; 2006; 8(23) pp 5231 - 5234; (Letter) doi:10.1021/ol061975c
- ^ Ceric Ammonium Nitrate Promoted Oxidation of Oxazoles David A. Evans, Pavel Nagorny, and Risheng Xu Org. Lett.; 2006; 8(24) pp 5669 - 5671; (Letter) doi:10.1021/ol0624530

