超臨界流體:修订间差异
| 第106行: | 第106行: | ||
{{主|地熱能}} |
{{主|地熱能}} |
||
超臨界二氧化碳流體可以替代水作为[[工質|工作流體]]將熱量轉送至地熱發電廠,然后抽取其能量或推動[[渦輪機]]發電。 |
超臨界二氧化碳流體可以替代水作为[[工質|工作流體]]將熱量轉送至地熱發電廠,然后抽取其能量或推動[[渦輪機]]發電。 |
||
==歷史== |
|||
1822年時法國[[Cagniard de la Tour]][[男爵]]在進行實驗時發現超臨界流體的特性,他將炮管密封,其中加入不同溫度的流體,再放入[[燧石]]的小球,球在炮管中滾動時會有聲音的不連續變化,但當溫度超過臨界溫度時,聲音的不連續變化消失了,炮管的流體中液體和氣體的密度變得相同,變成一個超臨界流體的相,因此也沒有二相之間的不連續界面<ref>{{cite journal |last1=Berche |first1=Bertrand |last2=Henkel |first2=Malte |last3=Kenna |first3=Ralph |year=2009 |title=Critical phenomena: 150 years since Cagniard de la Tour |work=Journal of Physical Studies |volume=13 |number=3 |pages=3001-1-3001-4 |url=http://arxiv.org/abs/0905.1886/}}</ref>。 |
|||
==参看== |
==参看== |
||
2013年3月19日 (二) 15:41的版本
| 此條目需要擴充。 (2010年12月21日) |
超臨界流體(英語:Supercritical fluid, SF)是一種物質狀態,當物質在超過臨界溫度及臨界壓力以上,氣體與液體的性質會趨近於類似,最後會達成一個均勻相之流體現象。 超臨界流體類似氣體具有可壓縮性,而且又兼具有類似液體的流動性,密度一般都介於0.1到1.0g/ml之間。由於其具有液體般的溶解能力,故超臨界流體可定義為具有可控制溶解能力的沉重氣體,或是一種無法區分液體、氣體的物質狀態。
接近臨界點時,壓力或溫度的小變化會導至密度上的大變化,因此使得超臨界流體的許多特性可被「精細調整」。超臨界流體適合作為工業和實驗室過程中的溶劑,而且可以取代许多有機溶劑。二氧化碳和水是最常用的超臨界流體,分別可被用於脫除咖啡因和發電。
特性
總體而言,超臨界流體的屬性介於氣體和液體之間。在表1中,顯示一些常用作超臨界流體的化合物之臨界性質。
| 物质 | 分子质量 | 临界温度 | 临界压力 | 临界密度 |
|---|---|---|---|---|
| 克/摩尔 | K | 百萬帕(标准大气压) | g/cm3 | |
| 二氧化碳(CO2) | 44.01 | 304.1 | 7.38 (72.8) | 0.469 |
| 水(H2O,依IAPWS資料) | 18.015 | 647.096 | 22.064 (217.755) | 0.322 |
| 甲烷(CH4) | 16.04 | 190.4 | 4.60 (45.4) | 0.162 |
| 乙烷(C2H6) | 30.07 | 305.3 | 4.87 (48.1) | 0.203 |
| 丙烷(C3H8) | 44.09 | 369.8 | 4.25 (41.9) | 0.217 |
| 乙烯(C2H4) | 28.05 | 282.4 | 5.04 (49.7) | 0.215 |
| 丙烯(C3H6) | 42.08 | 364.9 | 4.60 (45.4) | 0.232 |
| 甲醇(CH3OH) | 32.04 | 512.6 | 8.09 (79.8) | 0.272 |
| 乙醇(C2H5OH) | 46.07 | 513.9 | 6.14 (60.6) | 0.276 |
| 丙酮(C3H6O) | 58.08 | 508.1 | 4.70 (46.4) | 0.278 |
表2示出了典型的液體,氣體和超臨界流體的密度,擴散係數和粘度。
| 密度(kg/m3) | 粘度(µPa∙s) | 擴散係數(mm²/s) | |
|---|---|---|---|
| 氣體 | 1 | 10 | 1–10 |
| 超臨界流體 | 100–1000 | 50–100 | 0.01–0.1 |
| 液體 | 1000 | 500–1000 | 0.001 |
在超臨界流體中沒有液體及氣體之間的相界限,因此不存在表面張力,藉由改變流體的壓力和溫度,可以微調超臨界流體的特性,使其更類似液體或是氣體。物質在流體中的溶解度即為重要特性之一,在固定壓力下,溶解度會隨流體密度增加而增加,由於密度也是隨壓力增加而增加,因此在壓力增加時,溶解度也會增加。溶解度和溫度的關係比較複雜,在固定密度下,溶解度會隨溫度增加而增加,但靠近臨界點時,溫度輕微的增加會造成密度的大幅下降。因此靠近臨界點時,隨著溫度上昇,溶解度會先下降,然後再上昇[2]。
二種以上的超臨界流體,只要溫度及壓力超過其臨界點,二者均可以混溶,形成單一相的混合物。二元混合物的臨界點可以用二超臨界流體的臨界溫度及臨界壓力,再配合加權平均求得:
- Tc(mix) = (A的莫耳分率)x A的Tc + (B的莫耳分率)x B的Tc
若要有更高的準確度,臨界點可以用像是彭-羅賓遜物態方程式之類的状态方程求得,或是用基团贡献(group contribution)法求得,像密度之類的其他性質,也可以用状态方程來計算[3]。
相圖

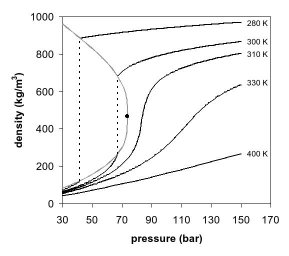
图1是二氧化碳的相圖,在壓力-溫度的相圖中,液態和氣態為不同的二相,但若超過臨界點,液態和氣態的相態都消失了,變成單一相態的超臨界流體。圖2是二氧化碳密度-压力的相圖,其中也可以看到類似的現象,當溫度遠低於臨界溫度280K時,隨著壓力的增加,氣體會被壓縮,最後(約40巴壓力時)會凝結成密度高很多的液體,因此相圖中有表示不連續的垂直虛線。此系統包括高密度的液體及低密度的氣體,二者達到平衡狀態。隨著溫度的昇高,氣體的密度會增加,而液體的密度會減少。在臨界點304.1 K及7.38 MPa(73.8 bar)時,液體和氣體的密度相同,因此變成一均勻相。
溫度高於臨界溫度的氣體無法單純用加壓的方式液化。若溫度略高於臨界溫度(310K),壓力在臨界壓力附近時,密度對压力的曲線幾乎是垂直線,因此微小的壓力變化就會使超臨界流體的密度有很大的改變。像黏度、相对电容率及溶劑強度等物理量都和密度有關,在臨界點附近這些物理量也會隨壓力有很大的變化。在溫度更高時,超臨界流體的行為開始類似氣體,當溫度到400K時,隨著壓力的變化,溫度幾乎呈線性的變化。
許多壓縮氣體其實都是超臨界流體。例如氮的臨界點是126.2 K(- 147 °C)及3.4 MPa(- 34 °C),因此若壓力容器中的氮氣壓力及溫度大於臨界點,氮氣就已變為超臨界流體。在室溫下,氮氣和氧氣的溫度遠高於臨界點,因此其特性類似氣體。不過這些氣體除非冷卻到其臨界溫度以下,否則是無法液化的。
自然界的超臨界流體
海底火山

海底火山常見於海底的地表。有些在較淺海域的海底活火山會釋放蒸汽及岩石碎片,而且噴出至較海平面高很多的高度。但許多海底火山在很深的海域,巨大的海水壓力使蒸汽和氣體無法爆炸性釋放。例如深度超過3000公尺的海域,其壓力到300個大氣壓,已超過臨界壓力的218大氣壓,而且噴口的水溫也會超過攝氏375度,因此噴口最熱的水會变成超臨界流體。
行星大气
金星大氣層含有96.5%的二氧化碳和3.5%的氮。金星表面壓力為9.3兆帕(93巴),表面溫度為735 K,壓力及溫度都高於主要成分的臨界點,因此使金星表面大氣成为超臨界流體。
用途
超臨界流體萃取
因為超臨界流體具有低粘度和高擴散係數,因此相較於一般的液體萃取,超臨界流體萃取可以有較快的萃取速度。
超臨界流體分解
利用超臨界水可氣化生物質的特性,可以進行生物質的分解。[4] 這種生物質的氣化可以用來製造烴類燃料,用在高效的燃燒裝置中,或用於產生燃料電池所需要的氫氣。在後者的應用,由於在水蒸汽轉化過程中,水也可以參與反應,提供氫原子,因此氫氣產量可以遠高於生物質中的氫含量。
乾洗
超臨界流體發電
超臨界二氧化碳流體可以替代水作为工作流體將熱量轉送至地熱發電廠,然后抽取其能量或推動渦輪機發電。
歷史
1822年時法國Cagniard de la Tour男爵在進行實驗時發現超臨界流體的特性,他將炮管密封,其中加入不同溫度的流體,再放入燧石的小球,球在炮管中滾動時會有聲音的不連續變化,但當溫度超過臨界溫度時,聲音的不連續變化消失了,炮管的流體中液體和氣體的密度變得相同,變成一個超臨界流體的相,因此也沒有二相之間的不連續界面[5]。
参看
參考資料
- ^ Edit Székely. Supercritical Fluid Extraction. Budapest University of Technology and Economics. [2007-11-20].
- ^ Supercritical Fluid Extraction, Density Considerations. [2007-11-20].
- ^ A.A. Clifford. Calculation of Thermodynamic Properties of CO2 using Peng Robinson equation of state.. Critical Processes Ltd. 2007-12-04 [2007-11-20].
- ^ Supercritical water gasification of biomas. Iowa Energy Center. [201-11-17].
- ^ Berche, Bertrand; Henkel, Malte; Kenna, Ralph. Critical phenomena: 150 years since Cagniard de la Tour. Journal of Physical Studies. 2009, 13 (3): 3001–1–3001–4.
連結
- Handy calculator for density, enthalpy, entropy and other thermodynamic data of supercritical CO2
- Food Product Design
- CO2 as a natural refrigerant - FAQs
- animated presentation describing what a supercritical fluid is
- NewScientist Environment FOUND:The hottest water on Earth
| ||||||||||||||||||||||||||||||||||||||||||||

