桥本氏甲状腺炎
此條目翻譯品質不佳。 (2014年9月25日) |
| 橋本氏甲状腺炎 | |
|---|---|
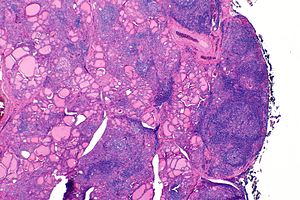 | |
| 橋本氏甲狀腺炎患者的甲狀腺在低倍率顯微鏡下所呈現的影像 | |
| 症状 | 抗甲狀腺自體抗體 |
| 类型 | 自身免疫性甲狀腺炎[*] |
| 分类和外部资源 | |
| 醫學專科 | 內分泌學 |
| ICD-11 | 5A03.20 |
| ICD-10 | E06.3 |
| ICD-9-CM | 245.2 |
| OMIM | 140300 |
| DiseasesDB | 5649 |
| MedlinePlus | 000371 |
| eMedicine | med/949 |
| MeSH | D050031 |
橋本氏甲状腺炎(Hashimoto's thyroiditis)也称慢性淋巴细胞性甲状腺炎(chronic lymphocytic thyroiditis)、橋本氏病(Hashimoto's disease),是甲状腺被一系列细胞或抗体介导免疫过程攻击,所导致的自體免疫性疾病[1][2]。
此症初期可能並無徵狀,甲狀腺會漸漸腫大並形成不會疼痛的甲状腺肿(goiter)。某些患者最終會發展成甲狀腺功能減退症,並導致體重增加、倦怠、便秘、情緒低落以及全身疼痛。患病多年後,一般而言甲狀腺的體積會縮小[1]。此症的潛在併發症包括淋巴癌在內[3]。
此症通常認為是先天基因與後天環境因素的共同影響所造成[4]。危險因子包含家族有無此症或是其他自體性免疫疾病的病史。診斷方式則是測試血液中的促甲状腺激素(TSH)、甲状腺激素(T4)以及甲状腺球蛋白抗体的數值[1]。其他可能引發類似症狀的疾病包含葛瑞夫茲氏症(Graves' disease)以及非毒性結節性甲狀腺腫(nontoxic nodular goiter)等[5]。
此症通常可用左旋甲狀腺素(Levothyroxine)加以治療[1][6],但若患者尚未出現甲狀腺功能減退的症狀時,則可能會建議無需治療或仍可服藥以縮小腺腫[1][7]。患者應避免攝取大量的碘,但適量的攝取仍有必要,尤其當患者在孕期中時[1]。甲狀腺腫則幾乎不需以手術加以移除[5]。
在美國,有5%的人在一生中的某個時點會受此症[4],通常始發於30至50歲間,在女性身上遠多於男性[1][8],且患病率似乎有上升的趨勢[5]。此症是人类发现的第一种自體免疫性疾病,於1912年由日本醫師橋本策在德國首次指明[9][10],並於1957年被認定為屬於自體免疫性疾病之一[11]。
症状和指征
[编辑]桥本氏甲状腺炎(桥本病)有多种症状表现。最常见的有以下症状:疲劳、体重增加、脸色苍白,感觉冷,关节和肌肉疼痛、便秘、头发干燥纤细,重型月经或月经不调、抑郁、心率减慢,受孕和怀孕困难。
女性患有桥本氏甲状腺炎的概率大约是男性的七倍,在青少年中也可能出现,但是最常见的发病是在中年人中,尤其对于男性。患者的家庭通常有甲状腺疾病史和自體免疫疾病史。桥本氏病的患者有时会患有其它自體免疫性疾病,如:
- 白癜风,这是一种消灭产生皮肤色素细胞的疾病。
- 类风湿性关节炎,一种影响全身关节的疾病。
- 愛迪生氏病,一种影响肾上腺的疾病,肾上腺对于身体维持血压,水盐平衡有重要作用。
- 1型糖尿病,一种使血糖浓度上升的疾病。
- 葛瑞夫茲氏病,一种使甲状腺分泌过量甲状腺素的疾病。
- 恶性贫血,一种阻碍身体吸收维生素B12,无法产生足量的血红细胞的疾病。
- 红斑性狼疮,一种伤害身体多个部分,如关节,皮肤,血管和其它器官的疾病。[12]
桥本氏甲状腺炎患者的甲状腺可能变得大而僵硬,并且呈分叶状,但甲状腺的变化也可能无法被触诊观察到。[13]甲状腺肿大是由淋巴细胞浸润和纤维变形造成的,不是由组织增生所导致。
从生理学角度上看,桥本氏甲状腺炎是由甲状腺过氧化物酶抗体(TPO)或甲状腺球蛋白抗体逐渐损伤甲状腺中的甲状腺滤泡造成的。所以可以通过检测血液中的抗体来对该病进行诊断。也可以通过白细胞,特别是T细胞对甲状腺的入侵进行诊断。淋巴瘤特别是非霍奇金淋巴瘤是罕见并且很复杂的情况。[14]
危险因素
[编辑]在桥本氏甲状腺炎患者中,常见家族甲状腺机能紊乱病史。在英国,HLA-DR5 基因的出现与发病有3级的强相关性。并且桥本氏病可能与CTLA-4 (细胞毒性T淋巴细胞抗原-4) 基因多态导致的基因产物表达功能缺失,进而导致T细胞负调控有关。[15]受下调基因多态影响的CTLA4基因与I型糖尿病的发展也有关。[16]在同卵双胞胎的研究中,基因的强相关一致性达到38-55%,对于无临床症状表现的循环甲状腺抗体相关一致性高达80%,这两个情况在异卵双胞胎实验中均没有被观察到,由此证明此病病因有高遗传性。[17]
可预防的环境因素,包括碘摄入量高,缺硒,传染病,某些药物,可以使桥本氏病基因易感人群发病。[18]在不同民族的基因变化会导致以下染色体疾病发病增加,包括特纳综合症,唐氏综合症,克氏综合症等与甲状腺球蛋白抗体和甲状腺过氧化物酶抗体相关的疾病。 持续的损耗这些细胞,例如细胞毒性免疫会有较高可能性引发甲状腺机能减退症,表现为甲状腺素T4T3缺乏,对应的促甲状腺激素TSH水平升高。
最近的研究显示HHV-6(可能是A型)基因在触发桥本氏甲状腺炎中有潜在的作用。[19]
病理
[编辑]桥本氏甲状腺炎的发展有多种可能的病理机制。(待补充)
可能存在多种抗体对抗甲状腺过氧化物酶, 甲状腺球蛋白和TSH受体,尽管小部分患者体内没有这些抗体的存在。一系列双胞胎实验显示,百分之一的人群中可能存在上述抗体但是并没有表现出桥本氏甲状腺炎的症状。然而,与抗体相关的细胞介导的细胞毒作用仍然是桥本氏甲状腺炎导致的细胞凋亡的主要因素。受助T细胞(CD4+ T-cells)激活的作用,激活的毒性T细胞(CD8+ T-cells)是甲状腺损伤的核心因素。作为IV型过敏反应type IV hypersensitivities的特征,巨噬细胞通过助T细胞的激活Th1在甲状腺组织内产生炎症细胞因子,进而存进巨噬细胞在甲状腺内的活动和迁移。[來源請求]
甲状腺发生肉眼可见的变化,看上去产生结核状和不规则的增大,但不是弥漫性的类似于甲亢一样的增大。虽然隔膜完好,腺体本身仍然和周围组织相隔离开,显微检查可以看到更明显的损伤迹象。[20]
从组织学来说,弥漫性的淋巴浸润可以看作过敏反应,特别是血浆B细胞plasma B-cells,可以看作二级淋巴滤泡(生发中心, 不要与正常的胶体填充的甲状腺滤泡follicles相混淆。萎缩的胶体在何氏细胞Hürthle cells傍边排列。何氏细胞具有大量的嗜酸性eosinophilic, 粒状细胞质, 由构成甲状腺滤泡的正常的立方上皮细胞发生变形产生。 严重的甲状腺萎縮通常伴随在甲状腺囊范围内出现胶原蛋白构成的致密纤维带。[21]
诊断
[编辑]通过检测血清中的甲状腺过氧化物酶抗体水平上升来确诊。
由于表现出甲减早期的不明显的症状,桥本氏甲状腺炎经常被误诊为抑郁症,循环性精神病、经前期综合征经前综合症、慢性疲劳综合征、纤维肌痛和勃起功能障碍或焦虑症。肉眼观察,通常表现为硬化的甲状腺肿,触摸无痛感;[20]并且有其它的甲减症状,如框周粘液水肿,根据病情的进展表现为相关的甲减临床症状。检测促甲状腺激素TSH,甲状腺激素游离态T4游离态T3,甲状腺球蛋白抗体(anti-Tg), 甲状腺过氧化物酶抗体 (anti-TPO) and 抗微粒体抗体可以帮助获得准确诊断。[22]由于甲状腺内部的炎症导致甲状腺储存甲状腺球蛋白的囊被破坏,对病人的早期评估可能表现出甲状腺球蛋白水平升高,出现短期的甲亢症状; 由于垂体试图环节T4的水平下降,分泌大量TSH,导致TSH水平升高。[來源請求]

身体内出现大量的原先各自孤立的甲状腺酶被认为是免疫耐受的恶化,会在后期的疾病中表现出更明显的症状。甲状腺细胞相关组织上发生的淋巴浸润通常意味着甲状腺腺体内发现组织学上来说的生发中心(germinal center)的发育。
表现出狂躁症状的桥本氏病患者称作普拉萨德综合症Prasad's syndrome由精神病学家Ashok Prasad命名。[23]
治疗
[编辑]调节激素水平
[编辑]桥本氏甲状腺炎引起的甲状腺机能减退症通常使用甲状腺激素替代的方法进行治疗,常见的替代激素物质有左旋甲状腺激素, 三碘化甲腺胺酸 or 脱水甲状腺提取物. 每天服用一次的药片可以将甲状腺激素维持在正常水平。绝大多数病例需要终生服药。对于由桥本氏甲状腺炎引起的甲状腺机能减退症,建议维持TSH水平在3.0以下。[24]
硒
[编辑]尽管现有的成人甲状腺机能减退症医学指导没有指出需要补充硒,[25]一个46人参与的一年期实验表明每天补充80μg硒可以减缓许多疾病进展相关的指标。[26]另一项88名女患者参与的为期9个月的实验表明,在服用左旋甲状腺素的同时两组患者分别补充100μg 和200μg硒,服用200μg组更有效。[27]2013年,一份更系统的报告显示还没有足够证据支持或者否定硒对于桥本氏甲状腺炎的作用,并且呼吁进行更多临床实验来证实治疗效果。[28]
作为食物补充,FDA建议成人每天补充至少55μg的硒,每天补充上限不超过400μg.[29]
低水平激光疗法
[编辑]根据2013年发表的一项研究显示, 近红外 低水平激光疗法在II期临床实验中能够有效提升甲状腺功能。[30]
无麸质饮食
[编辑]早期的研究显示桥本氏甲状腺炎与脂泻病相关。[31]有一些没有被严格研究的零星报告说无麸质饮食可能会减少自體免疫对甲状腺退化的影响。[32]2012年一月一份以确诊为脂泻病的病人为实验组,健康人为对照组,进行了一年的无麸质饮食实验的报告发表。[33]实验结果表明,经过一年的无麸质饮食脂泻病组有更高的甲状腺炎发病率,但是他们的TPO抗体水平没有下降,甲状腺功能没有提升或甲状腺激素水平没有上升。研究报告指出他们的结果与其它研究结果相矛盾,例如2000年8月发表的90个脂泻病患者在无麸质饮食后,血清中的甲状腺相关抗体出现下降。[34]
病情预测
[编辑]显性甲减是最常见的并发症,每年大概有5%的患有温和甲减和桥本氏病的病人发展成显性甲减。有些情况发展成周期性甲亢,较罕见发展成甲亢型心脏病Basedow-Graves disease表现出甲状腺眼病orbitopathy (眼球突出,红肿). 罕见纤维性自體免疫甲状腺炎表现出严重的呼吸短促和吞咽困难, 与侵袭性甲状腺肿瘤类似,但是这些情况在手术和皮质激素干预的治疗下总是可以改善。原发性甲状腺B细胞淋巴瘤发病率小于千分之一,并且更易于影响那些自體免疫性甲状腺炎的长期患者。[35]
流行病学
[编辑]桥本氏甲状腺炎被认为是北美地区甲状腺机能减退症的主要病因; 也是非地方性甲状腺肿的主要病因之一。平均每千人中有1至1.5人发病。[36]女性的发病率可以是男性的8至15倍。虽然可以在任何年龄段发病,最常见的还是在30-60岁的女性中出现。在食谱中富碘的地区更为常见,同时基因易感人群更易发病。[35]
历史
[编辑]桥本氏甲状腺炎,也称桥本氏病,是命名自九州大学毕业的日本医师桥本策(1881-1934)[37],他在1912年通过德国的出版物第一次描述了患有淋巴性甲状腺肿的病人的甲状腺被淋巴细胞强烈浸润的症状。[38]这份报告对于那些并不存在碘缺乏证据的发达国家,和没有证据表明由饮食问题引起的甲状腺机能减退症提供了一个新的视角。
参见
[编辑]参考资料
[编辑]- ^ 1.0 1.1 1.2 1.3 1.4 1.5 1.6 Hashimoto's Disease. NIDDK. 2014-05 [2016-08-09]. (原始内容存档于2016-08-22).
- ^ Hashimoto's disease. Office on Women’s Health, U.S. Department of Health and Human Services. 2017-06-12 [2017-07-17]. (原始内容存档于2017-07-28).
 本文含有此來源中屬於公有领域的内容。
本文含有此來源中屬於公有领域的内容。
- ^ Noureldine, Salem I.; Tufano, Ralph P. Association of Hashimoto's thyroiditis and thyroid cancer. Current Opinion in Oncology. 2015-01, 27 (1). ISSN 1040-8746. PMID 25390557. doi:10.1097/CCO.0000000000000150 (英语).
- ^ 4.0 4.1 Pyzik, Aleksandra; Grywalska, Ewelina; Matyjaszek-Matuszek, Beata; Roliński, Jacek. Immune Disorders in Hashimoto’s Thyroiditis: What Do We Know So Far?. Journal of Immunology Research. 2015-04-27, 2015 [2022-10-29]. ISSN 2314-8861. PMC 4426893
 . PMID 26000316. doi:10.1155/2015/979167. (原始内容存档于2022-11-01) (英语).
. PMID 26000316. doi:10.1155/2015/979167. (原始内容存档于2022-11-01) (英语).
- ^ 5.0 5.1 5.2 Akamizu, Takashi; Amino, Nobuyuki. Hashimoto’s Thyroiditis. Feingold, Kenneth R. (编). Endotext. South Dartmouth (MA): MDText.com, Inc. 2000 [2022-10-29]. PMID 25905412. (原始内容存档于2022-10-08).
- ^ Hashimoto Thyroiditis - Endocrine and Metabolic Disorders. Merck Manuals Professional Edition. 2016-07 [2017-12-30]. (原始内容存档于2017-12-31) (加拿大英语).
- ^ Hashimoto Thyroiditis - Hormonal and Metabolic Disorders. Merck Manuals Consumer Version. [2017-12-30]. (原始内容存档于2017-12-30) (加拿大英语).
- ^ Hiromatsu, Yuji; Satoh, Hiroshi; Amino, Nobuyuki. Hashimoto’s Thyroiditis: History and Future Outlook. Hormones. 2013-01, 12 (1). ISSN 1109-3099. PMID 23624127. doi:10.1007/BF03401282 (英语).
- ^ Nakazawa, Donna. The Autoimmune Epidemic. New York: Simon & Schuster. 2008: 32–35. ISBN 978-0-7432-7775-4.
- ^ Shoenfeld, Yehuda; Cervera, Ricard; Gershwin, M. Eric. Diagnostic Criteria in Autoimmune Diseases. Springer Science & Business Media. 2010-06-08: 216. ISBN 978-1-60327-285-8 (英语).
- ^ Moore, Elaine A.; Wilkinson, Samantha. The Promise of Low Dose Naltrexone Therapy: Potential Benefits in Cancer, Autoimmune, Neurological and Infectious Disorders. McFarland. 2009-01-22: 30. ISBN 978-0-7864-5258-3 (英语).
- ^ Hashimoto's disease fact sheet. Office on Women's Health, U.S. Department of Health and Human Services, womenshealth.gov (or girlshealth.gov). 2012-07-16 [2014-11-23]. (原始内容存档于2014-12-02).
- ^ Water, Thomas R. Van de; Staecker, Hinrich. Otolaryngology: Basic Science and Clinical Review. Thieme. 2006: 56. ISBN 978-0-86577-901-3 (英语).
- ^ Slatosky, John; Shipton, Benjamin; Wahba, Haney. Thyroiditis: Differential Diagnosis and Management. American Family Physician. 2000-02-15, 61 (4) [2022-10-29]. (原始内容存档于2022-10-29) (美国英语).
- ^ Kavvoura, Fotini K.; Akamizu, Takashi; Awata, Takuya; Ban, Yoshiyuki; Chistiakov, Dimitry A.; Frydecka, Irena; Ghaderi, Abbas; Gough, Stephen C.; Hiromatsu, Yuji; Ploski, Rafal; Wang, Pei-Wen. Cytotoxic T-Lymphocyte Associated Antigen 4 Gene Polymorphisms and Autoimmune Thyroid Disease: A Meta-Analysis. The Journal of Clinical Endocrinology & Metabolism. 2007-08-01, 92 (8) [2022-10-29]. ISSN 0021-972X. PMID 17504905. doi:10.1210/jc.2007-0147. (原始内容存档于2022-10-29) (英语).
- ^ Jacobson, Eric M.; Tomer, Yaron. The CD40, CTLA-4, thyroglobulin, TSH receptor, and PTPN22 gene quintet and its contribution to thyroid autoimmunity: Back to the future. Journal of Autoimmunity. Plenary Papers on Cutting Edge Autoimmunity. 2007-03-01, 28 (2). ISSN 0896-8411. PMC 2043086
 . PMID 17369021. doi:10.1016/j.jaut.2007.02.006 (英语).
. PMID 17369021. doi:10.1016/j.jaut.2007.02.006 (英语).
- ^ Chistiakov, Dimitry A. Immunogenetics of Hashimoto's thyroiditis. Journal of Autoimmune Diseases. 2005, 2 (1) [2022-10-29]. PMC 555850
 . PMID 15762980. doi:10.1186/1740-2557-2-1. (原始内容存档于2022-10-29).
. PMID 15762980. doi:10.1186/1740-2557-2-1. (原始内容存档于2022-10-29).
- ^ Saranac, L.; Zivanovic, S.; Bjelakovic, B.; Stamenkovic, H.; Novak, M.; Kamenov, B. Why Is the Thyroid So Prone to Autoimmune Disease?. Hormone Research in Paediatrics. 2011, 75 (3) [2022-10-29]. ISSN 1663-2818. PMID 21346360. doi:10.1159/000324442. (原始内容存档于2022-10-29) (英语).
- ^ Caselli, Elisabetta; Zatelli, Maria Chiara; Rizzo, Roberta; Benedetti, Sabrina; Martorelli, Debora; Trasforini, Giorgio; Cassai, Enzo; degli Uberti, Ettore C.; Di Luca, Dario; Dolcetti, Riccardo. Moore, Patrick S. , 编. Virologic and Immunologic Evidence Supporting an Association between HHV-6 and Hashimoto's Thyroiditis. PLoS Pathogens. 2012-10-04, 8 (10). ISSN 1553-7374. PMC 3464215
 . PMID 23055929. doi:10.1371/journal.ppat.1002951 (英语).
. PMID 23055929. doi:10.1371/journal.ppat.1002951 (英语).
- ^ 20.0 20.1 Kumar, Vinay. 24: The Endocrine System. Robbins and Cotran Pathologic Mechanisms of Disease 8th. Philadelphia, PA: Elsevier. 2010: 1113.
- ^ Kumar, Vinay. 24: The Endocrine System. Robbins and Cotran Pathologic Mechanisms of Disease 8th. Philadelphia, PA: Elsevier. 2010: 1112–1113.
- ^ Giannini, AJ. The Biological Foundations of Clinical Psychiatry. New Hyde Park, NY: Medical Examination Publishing Company. 1986: 193–198. ISBN 0-87488-449-7.
- ^ Prasad's syndrome (PDF). [2014-09-25]. (原始内容存档于2011-06-09).
- ^ Does Your Doctor Know About the New TSH Lab Standards?. [2014-09-25]. (原始内容存档于2010-12-04).
- ^ Metapress | A Fast Growing Resource for Young Entrepreneurs. Metapress. [2022-10-29]. (原始内容存档于2021-03-05) (美国英语).
- ^ Nacamulli, Davide; Mian, Caterina; Petricca, Daniela; Lazzarotto, Francesca; Barollo, Susi; Pozza, Dina; Masiero, Stefano; Faggian, Diego; Plebani, Mario; Girelli, Maria E.; Mantero, Franco. Influence of physiological dietary selenium supplementation on the natural course of autoimmune thyroiditis. Clinical Endocrinology. 2010-10, 73 (4) [2022-10-29]. ISSN 1365-2265. PMID 20039895. doi:10.1111/j.1365-2265.2009.03758.x. (原始内容存档于2022-10-29).
- ^ Turker, Omer; Kumanlioglu, Kamil; Karapolat, Inanc; Dogan, Ismail. Selenium treatment in autoimmune thyroiditis: 9-month follow-up with variable doses. Journal of Endocrinology. 2006-07, 190 (1) [2022-10-29]. ISSN 0022-0795. PMID 16837619. doi:10.1677/joe.1.06661. (原始内容存档于2022-10-29).
- ^ van Zuuren, Esther J; Albusta, Amira Y; Fedorowicz, Zbys; Carter, Ben; Pijl, Hanno. Cochrane Metabolic and Endocrine Disorders Group , 编. Selenium supplementation for Hashimoto's thyroiditis. Cochrane Database of Systematic Reviews. 2013-06-06. doi:10.1002/14651858.CD010223.pub2 (英语).
- ^ Dietary Supplement Fact Sheet: Selenium. [2014-09-25]. (原始内容存档于2014-09-24).
- ^ Höfling, Danilo B.; Chavantes, Maria Cristina; Juliano, Adriana G.; Cerri, Giovanni G.; Knobel, Meyer; Yoshimura, Elisabeth M.; Chammas, Maria Cristina. Low-level laser in the treatment of patients with hypothyroidism induced by chronic autoimmune thyroiditis: a randomized, placebo-controlled clinical trial. Lasers in Medical Science. 2013-05, 28 (3). ISSN 0268-8921. PMID 22718472. doi:10.1007/s10103-012-1129-9 (英语).
- ^ Connection Found Between Celiac Disease and Hashimoto's Thyroiditis. [2014-09-25]. (原始内容存档于2014-07-22).
- ^ Wendy vs. Autoimmune Hypothyroid. [2014-09-25]. (原始内容存档于2014-07-07).[不可靠的醫學來源?]
- ^ Metso, Saara; Hyytiä-Ilmonen, Henni; Kaukinen, Katri; Huhtala, Heini; Jaatinen, Pia; Salmi, Jorma; Taurio, Jyrki; Collin, Pekka. Gluten-free diet and autoimmune thyroiditis in patients with celiac disease. A prospective controlled study. Scandinavian Journal of Gastroenterology. 2012-01, 47 (1) [2022-10-29]. ISSN 0036-5521. PMID 22126672. doi:10.3109/00365521.2011.639084. (原始内容存档于2022-10-29) (英语).
- ^ Ventura, Alessandro; Neri, Elena; Ughi, Claudio; Leopaldi, Agnese; Città, Angello; Not, Tarcisio. Gluten-dependent diabetes-related and thyroid-related autoantibodies in patients with celiac disease. The Journal of Pediatrics. 2000-08-01, 137 (2). ISSN 0022-3476. PMID 10931424. doi:10.1067/mpd.2000.107160 (英语).
- ^ 35.0 35.1 Fabrizio Monaco. Thyroid Diseases. Taylor and Francis. 2012: 78. ISBN 9781439868393.
- ^ Kumar, Vinay. 24: The Endocrine System. Robbins and Cotran Pathologic Mechanisms of Disease 8th. Philadelphia, PA: Elsevier. 2010: 1111–205.
- ^ Hakaru Hashimoto - Who Named It?
- ^ Hashimoto, H. Zur Kenntnis der lymphomatösen Veränderung der Schilddrüse (Struma lymphomatosa). Archiv für klinische Chirurgie (Berlin). 1912, 97: 219–248.
外部链接
[编辑]- Autoimmune Thyroid Disease For details about Autoimmune Thyroid Disease
- Hashimoto's disease (页面存档备份,存于互联网档案馆) at the Mayo Clinic
- Sasaki, N; Takahashi, A; Nakano, N; Saito, T. A case of 'hallucination of soliloquy' with hypothyroidism induced Hashimoto disease. Meaning of psychopathological research about symptomatic psychosis. Seishin shinkeigaku zasshi. 2001, 103 (2): 185–96. PMID 11326441.
- Hall, Richard C.W.; Popkin, Michael K.; Devaul, Richard; Hall, Anne K.; Gardner, Earl R.; Beresford, Thomas P. Psychiatric manifestations of Hashimoto's thyroiditis (PDF). Psychosomatics. 1986-04, 23 (4): 337–42 [2014-09-25]. PMID 6896238. doi:10.1016/S0033-3182(82)73397-3. (原始内容 (PDF)存档于2011-08-20).
