氯化铋
| 氯化铋 | |
|---|---|

| |

| |
| IUPAC名 Bismuth chloride | |
| 识别 | |
| CAS号 | 7787-60-2 |
| PubChem | 24591 |
| ChemSpider | 22993 |
| SMILES |
|
| InChI |
|
| InChIKey | JHXKRIRFYBPWGE-DFZHHIFOAJ |
| RTECS | EB2690000 |
| 性质 | |
| 化学式 | BiCl3 |
| 摩尔质量 | 315.34 g·mol⁻¹ |
| 外观 | 吸湿性白色至黄色晶体 |
| 密度 | 4.75 g/cm3 |
| 熔点 | 227 °C(500 K) |
| 沸点 | 447 °C(720 K) |
| 溶解性(水) | 水解生成BiOCl |
| 溶解性 | 溶于甲醇,乙醚,丙酮 |
| 热力学 | |
| ΔfHm⦵298K | -1.202 kJ/g |
| 热容 | 0.333 J/(g K) |
| 危险性 | |
| MSDS | JT Baker |
| NFPA 704 | |
| 致死量或浓度: | |
LD50(中位剂量)
|
3324 mg/kg, 口服(大鼠) |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
氯化铋化学式BiCl3,常温下是易潮解的白色晶体。与离子晶体三氟化铋不同,在气相或晶体中,氯化铋分子构型都为三角锥形,可从价层电子对互斥理论(VSEPR)解释。是常用的提供Bi3+离子的试剂。氯化铋是常用的提供Bi3+离子的试剂,以及用于制备其它铋盐,以用于颜料和化妆品。
制备[编辑]
氯化铋可从氯气与铋直接反应制得:
- 2 Bi + 3 Cl2 → 2 BiCl3
- Bi2O3 + 6 HCl → 2 BiCl3 + 3 H2O
- Bi + 6 HNO3 → Bi(NO3)3 + 3 H2O + 3 NO2
- Bi(NO3)3 + 3 NaCl → BiCl3 + 3 NaNO3
化学性质[编辑]
- Bi3+
+ Cl−
+ H
2O → BiOCl (s) + 2 H+
故配制Bi³⁺离子的溶液需要加酸抑制其水解。[3]
氯化铋是一种氧化剂,遇还原剂如氯化亚锡生成黑色的金属铋粉末,此反应可用于检验Bi³⁺。
氯配合物[编辑]
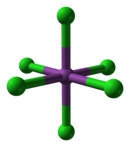
氯化铋作为一种路易斯酸,在Cl-浓度高的溶液中能形成各种氯配合物,如BiCl63−。其八面体结构与价层电子对互斥理论的判断不符, 不过BiCl52−的四方锥结构符合该理论的判断。[4]
 |
 |
 |
有机反应催化剂[编辑]
氯化铋用于有机合成的催化剂,例如麦克尔加成反应,碘的加入能提高催化效率。[5]
安全性[编辑]
氯化铋有毒,能刺激胃肠道和呼吸道,与皮肤接触可能导致灼伤。
参考资料[编辑]
- ^ Pradyot Patnaik. Handbook of Inorganic Chemicals. McGraw-Hill, 2002, ISBN 0-07-049439-8
- ^ Joel Henry Hildebrand. Principles of Chemistry. BiblioBazaar, LLC. 2008: 191. ISBN 0-559-31877-4.
- ^ Frank Welcher. Chemical Solutions. READ BOOKS. 2008: 48. ISBN 1-4437-2907-8.
- ^ Holleman, A. F.; Wiberg, E. "Inorganic Chemistry" Academic Press: San Diego, 2001. ISBN 0-12-352651-5.
- ^ Hitomi Suzuki; Yoshihiro Matano. Organobismuth chemistry. Elsevier. 2001: 403–404. ISBN 0-444-20528-4.
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|

