莽草酸途径
莽草酸途径(英语:shikimic acid pathway,又叫做分支酸途径,Chorismate pathway)是一个存在于细菌、真菌、藻类以及寄生生物和植物中的代谢途径,用于芳香族氨基酸(苯丙氨酸、酪氨酸和色氨酸)的生物合成。
这个代谢途径在动物中不存在,因此对于动物而言这些氨基酸是必需氨基酸,无法自己制造(但这三者的有些氨基酸可以另辟途径合成,如酪氨酸是在人体由苯丙氨酸合成的方法所得,虽然酪氨酸不是必需氨基酸之一,他的合成来源苯丙氨酸则是必需氨基酸之一,因此依然要先有必需氨基酸的摄取才能合成出来),要通过食物中的细菌或者植物(或者吃细菌或者植物的动物)摄取。
参与莽草酸途径的七种酶是DAHP合酶,3-脱氢奎尼酸合酶,3-脱氢奎尼酸脱水酶,莽草酸脱氢酶,莽草酸激酶,EPSP合酶,和分支酸合酶。
莽草酸的合成
[编辑]莽草酸合成的两种初始底物是糖酵解与糖异生途径中的磷酸烯醇式丙酮酸和卡尔文循环与磷酸戊糖途径中的赤藓糖-4-磷酸,它们由DAHP合酶催化合成为3-脱氧-D-阿糖基庚糖酮酸-7-磷酸(DAHP),并释放一个磷酸。DAHP再由3-脱氢奎尼酸合酶环化为3-脱氢奎尼酸(DHQ)。[1]
3-脱氢奎尼酸再由3-脱氢奎尼酸脱水酶脱水形成3-脱氢莽草酸,之后在脱氢莽草酸还原酶作用下,3-脱氢莽草酸消耗一个NADPH还原为莽草酸。
从莽草酸到芳香族氨基酸
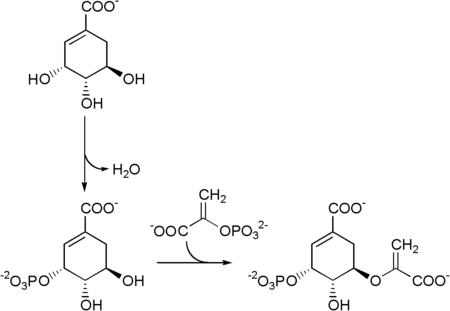
[编辑]莽草酸合成后的第一个酶是莽草酸激酶,消耗ATP催化莽草酸磷酸化为莽草酸-3-磷酸[2]。莽草酸-3-磷酸再由EPSP合酶催化与磷酸烯醇式丙酮酸结合形成5-烯醇式丙酮酸莽草酸-3-磷酸(EPSP)。
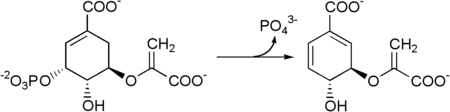
5-烯醇式丙酮酸莽草酸-3-磷酸再通过分支酸合酶转化为分支酸。
分支酸在分支酸变位酶催化下进行克莱森重排形成预苯酸[3][4]
到酪氨酸
[编辑]预苯酸在预苯酸脱氢酶催化下发生氧化脱羧(但保留羟基)形成对羟基苯丙酮酸(p-hydroxyphenylpyruvate,又叫4-羟苯丙酮酸)。再通过酪氨酸转氨酶与谷氨酸发生转氨基作用生成酪氨酸和α-酮戊二酸。
到苯丙氨酸
[编辑]预苯酸由预苯酸脱水酶催化脱羧(不保留羟基)形成苯丙酮酸,再与谷氨酸发生转氨基作用生成苯丙氨酸。[来源请求]
到色氨酸
[编辑]分支酸支路
[编辑]从分支酸开始,有多条支路合成以下多种有机化合物,分支酸也因此得名。[5]
- 泛醌和质体醌
- 生育酚(维生素E成分之一)、维生素K、叶酸(维生素B9)
- 部分铁载体
- 木质素
- 苯丙素类化合物
- 异黄酮、花色素苷、木酚素、二苯基乙烯
- 肉桂酸衍生物
- 香豆素、香草醛
- 苯甲酸衍生物(水杨酸、没食子酸、对氨基苯甲酸)
- 一些生物碱(吗啡、秋水仙素)
前酪氨酸途径
[编辑]在部分植物[6]与细菌[7]中,酪氨酸和苯丙氨酸的合成途径与以上有所不同,称为“前酪氨酸途径”(arogenate pathway),它先由预苯酸在转氨后形成L-前酪氨酸(L-arogenate),再通过前酪氨酸脱氢酶形成酪氨酸或通过前酪氨酸脱水酶形成苯丙氨酸(如图)。
参考文献
[编辑]引用
[编辑]- ^ D. E. Metzler: Biochemistry. The Chemical Reactions of Living Cells. Volume 2. Elsevier Science, 2003; S. 1420–1471 ; ISBN 0-12-492541-3.
- ^ Klaus M. Herrmann, Lisa M. Weaver. THE SHIKIMATE PATHWAY. Annual Review of Plant Physiology and Plant Molecular Biology. 1999-6, 50: 473–503 [2019-02-12]. ISSN 1040-2519. PMID 15012217. doi:10.1146/annurev.arplant.50.1.473. (原始内容存档于2019-09-30).
- ^ Helmut Goerisch. On the mechanism of the chorismate mutase reaction. Biochemistry. 1978, 17 (18): 3700. doi:10.1021/bi00611a004.
- ^ Peter Kast, Yadu B. Tewari, Olaf Wiest, Donald Hilvert, Kendall N. Houk, and Robert N. Goldberg. Thermodynamics of the Conversion of Chorismate to Prephenate: Experimental Results and Theoretical Predictions. J. Phys. Chem. B. 1997, 101 (50): 10976–10982. doi:10.1021/jp972501l.
- ^ P. M. Dewick: Medicinal Natural Products: A Biosynthetic Approach. 3. Auflage, John Wiley & Sons Ltd., 2009; S. 137–186; ISBN 978-0-470-74167-2.
- ^ Cho, Man-Ho; Corea, Oliver R. A.; Yang, Hong; Bedgar, Diana L.; Laskar, Dhrubojyoti D.; Anterola, Aldwin M.; et al. Phenylalanine biosynthesis in Arabidopsis thaliana-- identification and characterization of arogenate dehydratases. J. Biol. Chem. 2007, 282 (42): 30827–35. PMID 17726025. doi:10.1074/jbc.m702662200.
- ^ Zhao, G; Xia, T; Fischer, RS; Jensen, RA. Cyclohexadienyl dehydratase from Pseudomonas aeruginosa. Molecular cloning of the gene and characterization of the gene product. J. Biol. Chem. 1992, 267 (4): 2487–2493. PMID 1733946.
来源
[编辑]- Brown, Stewart A.; Neish, A. C. Shikimic Acid as a Precursor in Lignin Biosynthesis. Nature. 1955, 175 (4459): 688–689. ISSN 0028-0836. doi:10.1038/175688a0.
- Weinstein, L. H.; Porter, C. A.; Laurencot, H. J. Role of the Shikimic Acid Pathway in the Formation of Tryptophan in Higher Plants : Evidence for an Alternative Pathway in the Bean. Nature. 1962, 194 (4824): 205–206. ISSN 0028-0836. doi:10.1038/194205a0.
- Wilson, D J; Patton, S; Florova, G; Hale, V; Reynolds, K A. The shikimic acid pathway and polyketide biosynthesis. Journal of Industrial Microbiology and Biotechnology. 1998, 20 (5): 299–303. ISSN 1367-5435. doi:10.1038/sj.jim.2900527.