四氟肼
| 四氟肼 | |
|---|---|

| |
| |
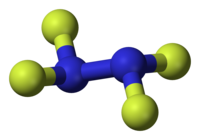
| IUPAC名 1,1,2,2-tetrafluorohydrazine | |
| 别名 | 四氟化二氮 |
| 识别 | |
| CAS号 | 10036-47-2 |
| PubChem | 24845 |
| ChemSpider | 23228 |
| SMILES |
|
| InChI |
|
| 性质 | |
| 化学式 | N2F4 |
| 摩尔质量 | 104.01 g·mol⁻¹ |
| 外观 | 无色气体[1] |
| 密度 | 4.6 kg·m−3[2] |
| 熔点 | −164.5 °C, 108.7 K[3] |
| 沸点 | −73 °C, 200 K[3] |
| 危险性 | |
| NFPA 704 | |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
四氟肼(N2F4)在常温常压下是一种无色的活泼气体。它是肼的一种含氟衍生物,有剧毒,与有机化合物接触易爆炸。
制法[编辑]
四氟肼可以由三氟化氮在铁等金属还原剂存在下制得:
三氟化氮与一氧化氮反应也可制得四氟肼,并产生亚硝酰氟[4]:
它在一些物质的化学合成中用作前体或催化剂。
结构[编辑]
四氟肼存在两种构象,能垒约为12.5kJ/mol。
性质[编辑]
四氟肼与二氟化氮自由基处于分子-自由基平衡中:
- ·
二氟化氮自由基使得四氟肼在高温下略显深蓝色。正因为自由基的存在,使得四氟肼能发生许多相关的反应[4]:
- 与一氧化氮偶联:
- 自由基取代反应:
- 由这类反应可制备含二氟氨基的高能化合物。
- 自由基加成反应,二氟氨基加在碳碳双键或三键的两端碳上。
四氟肼与水缓慢反应并产生肼和氟化氢:
四氟肼可以用作火箭燃料中的高能液体氧化剂。这项应用于1959年时提出。[5]
四氟肼也能与路易斯酸反应形成加合物,例如它与五氟化锑能形成N2F4·2SbF5和N2F4·3SbF5两种加合物。在低温下后者与二氧化硫反应能转换为前者。核磁共振表明,N2F4·2SbF5实际上是离子化合物N2F3+Sb2F11-[4]。
参考资料[编辑]
- ^ Holleman, Arnold Frederik; Wiberg, Egon, Wiberg, Nils , 编, Inorganic Chemistry, 由Eagleson, Mary; Brewer, William翻译, San Diego/Berlin: Academic Press/De Gruyter, 2001, ISBN 0-12-352651-5
- ^ Stickstoff(II)-fluorid bei webelements.com
- ^ 3.0 3.1 Greenwood, N. N.; Earnshaw, A. Chemistry of the Elements 2nd. Oxford:Butterworth-Heinemann. 1997. ISBN 0-7506-3365-4.
- ^ 4.0 4.1 4.2 张青莲. 《无机化学丛书》第四卷:氮、磷、砷分族. 北京: 科学出版社. : P397–398. ISBN 7-03-002238-6.
- ^ Tetrafluorohydrazine (页面存档备份,存于互联网档案馆) at DTIC.mil
| ||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||








