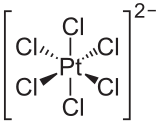铂
铂(拼音:bó,注音:ㄅㄛˊ,粤拼:bok6,音同“博”,英语:Platinum),俗称白金,是一种化学元素,其化学符号为Pt,原子序数为78,原子量为195.084 u。铂是一种密度高、延展性高、反应性低的银白色贵金属,属于过渡金属。
铂同属于铂系元素和10族元素。它共有六种自然产生的同位素。铂是地球地壳中罕见的元素[3],丰度排在第71名,平均丰度大约为5 μg/kg,地壳百万分之0.001为铂[4]。它一般出现在某些镍和铜矿石中,位于原生元素矿藏,主要分布在南非,当地的铂产量占全球的80%。铂年产量只有几百吨,应用亦十分重要,因此非常贵重,是主要的贵金属贸易商品。
铂是非常不活泼的金属[5]。即便在高温下,它也有极强的抗腐蚀性,属于抗腐蚀金属。在自然中,铂有时以纯金属状态出现,不与其他元素结合。铂自然出现在河流的冲积层中,所以前哥伦布时期的南美原住民最早用铂制作工艺品。欧洲最早在16世纪就有记载使用铂;1748年,安东尼奥·乌略亚发表报告,描述此来自哥伦比亚的新金属,这时科学家才开始研究铂元素。
铂的应用包括:催化转换器、实验室器材、电触头和电极、电阻温度计、牙科器材及首饰等。由于铂是重金属,所以它的盐会危害健康;但铂的抗腐蚀性强,所以其毒性比一些其他金属较低。[6]一些含铂化合物,特别是顺铂,可用于化学疗法以治疗某些癌症。[7]
性质
[编辑]物理性质
[编辑]纯铂为带光泽、有可延展性的银白色金属。[8]它的可延展性是所有纯金属中最高的,胜过金、银和铜,但其可锻铸性却比金低。[9][10]铂金属的抗腐蚀性极强,在高温下非常稳定,电性能亦很稳定。它在任何温度下都不会氧化,但可被各种卤素、氰化物、硫和苛性碱侵蚀。铂不可溶于氢氯酸和硝酸,但会在热王水中溶解,形成氯铂酸(H2PtCl6)。[11]
这些物理性质都使铂成为了工业上应用广泛的金属。[12]由于能够抵抗侵蚀和保留光泽,所以铂还可以用于制首饰。
化学性质
[编辑]
铂的最常见氧化态为+2和+4。铂的+1和+3较少见,双金属(或多金属)化合物中的金属键可以提高其稳定性。四配位铂(II)化合物通常具有由16个电子形成的平面四边形结构。单质铂金属的反应性很低,但它会在热王水中溶解,产生氯铂酸(H2PtCl6):[13]
- Pt + 4 HNO3 + 6 HCl → H2PtCl6 + 4 NO2 + 4 H2O
铂属于软酸,所以铂和硫有化学亲和性,例如和二甲基亚砜(DMSO);科学家已发现多种DMSO配合物。[14]
同位素
[编辑]铂有六种自然同位素:190Pt、192Pt、194Pt、195Pt、196Pt和198Pt。其中丰度最高的是195Pt,它占了所有自然铂元素的33.83%。它是唯一自旋不为零的稳定同位素;其自旋为1/2,所以在1H和31P的核磁共振波谱中(例如铂-烷基配合物及铂-膦配合物)常会出现195Pt的卫星波峰。同位素190Pt的丰度最低,仅有0.01%。190Pt是唯一不稳定的自然同位素,但其半衰期长达4.97×1011年。[2]198Pt理论上可以α衰变,但人们未观测到它的衰变(半衰期已知要大于3.2×1014年),所以可当做稳定同位素。人工合成的铂同位素共有31种,原子量在166和202之间,所以已知的铂同位素总共有37种。在人造同位素之中,稳定性最低的是166Pt,其半衰期只有300 µs;而最稳定的则是193Pt,其半衰期为50年。大部份铂同位素都会混合进行β衰变和α衰变。188Pt、191Pt和193Pt主要以电子捕获的方式衰变。190Pt和198Pt理论上都可以双β衰变。[15]
存量
[编辑]

铂非常罕见,[16]在地壳中的浓度只有百万分之0.005。[17][18]铂金属常被误认为是银。自然界中的铂常以未经化合的单质出现,或与其他铂系元素或铁形成合金。单质铂元素通常出现在冲积层次生矿床。前哥伦布时期哥伦比亚乔科省的居民曾经开采过的冲积层矿床至今仍然仍出产铂系金属。另一大冲积层矿藏位于俄罗斯乌拉尔山脉。[11]
在镍和铜矿中,铂系金属会以硫化物(如(Pt,Pd)S)、碲化物(如PtBiTe)、锑化物(PdSb)和砷化物(如PtAs2)的形态出现,并且也会与镍或铜形成合金。砷铂矿石(砷化铂PtAs2)也是此金属的主要矿源[19],它出现在镍矿当中,主要分布在加拿大安大略的索德柏立盆地。1927至1975年间,美国阿拉斯加州普拉蒂纳姆(Platinum,即“铂”之意)共产出17吨铂元素。矿场于1990年停止作业。[20]较罕见的硫砷铂矿((Pt,Pd,Ni)S)中含有铂、钯和镍元素。硫砷铂矿出现在南非豪登省布什维尔德杂岩体中的美兰斯基矿层中。[21]
1865年,人们在南非布什维尔德地区发现了铬铁矿,其后于1906年又发现了铂矿。[22]其最大原生矿床位于布什维尔德杂岩体。[23]其馀两大矿床位于俄罗斯诺里尔斯克的大型铜镍矿,以及加拿大的索德柏立盆地。索德柏立盆地的镍矿开采量巨大,因为其中的铂元素只占百万分之0.5。美国则有较小的矿藏,[23]例如蒙大拿州的阿布萨洛卡山脉。[24]2010年,南非为铂的最大产国,其占总产量的77%,其次为占13%的俄罗斯。2010年铂的全球总产量为192吨。[25]印度泰米尔纳德邦亦有铂矿藏,[26]为此印度地质调查局已与泰米尔纳德矿物有限公司(TAMIN)签署协议。[27]
月球和陨石中的铂含量更高,因此在地球上经火流星撞击后火山喷发的区域会有较高的铂丰度。这种矿藏具有商业开采价值,例如索德柏立盆地。[28]
化合物
[编辑]卤化物
[编辑]氯铂酸是十分重要的铂化合物,可以用来生产许多其他的铂化合物。氯铂酸本身的应用广泛,包括摄影、锌蚀刻、不褪色墨水、电镀、镜子、瓷器上色以及催化剂等。[29]
氯铂酸经铵盐(如氯化铵)处理后,会产生氯铂酸铵。[13]氯铂酸铵在氨溶液中的可溶性较低。在氢气中经加热后,氯铂酸铵会还原成铂金属。氯铂酸钾的可溶性同样较低;在重力测量实验中,氯铂酸可用于探测钾离子。[30]
氯铂酸在被加热时,会经过四氯化铂和二氯化铂,再分解成单质铂元素。此反应并不分步骤发生:[31]
- (H3O)2PtCl6·nH2O ⇌ PtCl4 + 2 HCl + (n + 2) H2O
- PtCl4 ⇌ PtCl2 + Cl2
- PtCl2 ⇌ Pt + Cl2
以上三项反应皆可逆。已知的铂卤化物还包括二溴化铂和四溴化铂。六氟化铂是能够对氧进行氧化的强氧化剂(见二氧基盐)。
氧化物
[编辑]二氧化铂(PtO2)亦称亚当斯催化剂,呈黑色粉末状,可溶于氢氧化钾溶液及浓酸中。[32]二氧化铂以及较为罕见的一氧化铂在加热后都会分解。[8]氧化铂(II,IV)(Pt3O4)可经以下反应生成:
- 2 Pt2+ + Pt4+ + 4 O2− → Pt3O4
其他化合物
[编辑]乙酸铂(II)像乙酸钯那样可以在市面上购买。当需要碱的时候,可以结合使用铂的卤化物和乙酸钠。[14]在合成铂的N-杂环卡宾配合物时,可用乙酰丙酮铂(II)作为初始反应物,以减少合成步骤,使反应更容易进行。[33]
在各种铂化钡化合物中,铂拥有低于零的氧化态:−1至−2。这些化合物包括BaPt、Ba
3Pt
2和Ba
2Pt。[34]铂化铯(Cs
2Pt)为深红色透明晶体,[35]含Pt2−
离子。[36]在经过电化学还原的表面上,铂也可以有低于零的氧化态。[37]负的氧化态数值对于金属元素来说十分特殊,此现象与6s电子轨域的相对论性稳定作用有关。[36]
蔡斯盐含有乙烯配位体,是较早被发现的有机金属化合物。(1,5-环辛二烯)二氯化铂(II)属于烯烃配合物,它含有能够轻易置换的1,5-环辛二烯配位体。1,5-环辛二烯配合物以及各种铂卤化物都可以作为铂化学研究的初始反应物。[14]
顺铂,又称顺式-二氯二氨合铂(II),是含铂(II)、呈平面正方形结构的化疗药物。同类药物还包括卡铂(Carboplatin)和奥沙利铂。这些化合物能够交叉链接DNA,并通过相似的反应路径产生烷化剂,杀死细胞。[38]
-
六氯铂酸离子
-
蔡斯盐阴离子
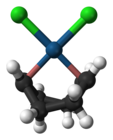
-
(1,5-环辛二烯)二氯化铂(II)
-
顺铂
历史
[编辑]主流学术观点认为,像铂这样的重元素产生于超新星爆炸。铂产生于Ib型、Ic型、II型超新星内的r-过程,被Ib型、Ic型、II型超新星喷射到宇宙各处。[39]但另有新证据显示,像铂、金这样的重元素也可能产生于两个中子星相撞。[40][41]
人类用铂史最早可追溯到古埃及。考古学家在最早公元前1200年的古埃及墓与象形文字所用的金内发现了微量铂。然而,不确定早期埃及人对此金属的了解程度,相当有可能他们未认出他们的金内有铂。[42]
前哥伦布时期,今厄瓜多尔埃斯梅拉达斯附近曾有原住民用铂以制各式各样的金铂合金制品,包括鼻环、耳环、面具。[43]1557年,意大利人文主义者朱利斯·凯撒·斯卡利杰对铂金属作出描述,称在达连和墨西哥之间所发现的未知贵金属“用火焰或任何西班牙技术都无法将其熔化”。[44]


1741年,英国冶金学家查尔斯·伍德(Charles Wood)[45]在牙买加发现了各种来自哥伦比亚的铂样本,并将样本寄往威廉·布朗里格(William Brownrigg)作进一步分析。安东尼奥·乌略亚也被认为是铂的发现者。他在法国测地线任务(French Geodesic Mission)八年后,于1746年返回了西班牙。他把铂描述为不可分离且不可煅烧的金属。乌略亚还预测铂矿将会被发现。1748年,他发表了相关报告之后,没有再继续探究此金属。[44]
1750年,布朗里格在研究过伍德所寄来的铂样本之后,向皇家学会呈交了一份有关铂的详细报告,表示在过去有关已知矿物的文献都未提及此金属。[46]布朗里格也提到了铂的熔点之高,且对硼砂有著极高的耐火度。欧洲各地化学家相继对铂进行研究,如:安德烈亚斯·西吉斯蒙德·马格拉夫、[47]托尔贝恩·奥洛夫·贝尔曼、永斯·雅各布·贝采利乌斯、威廉·李维斯(William Lewis)[48]和皮埃尔-约瑟夫·马盖(Pierre-Joseph Macquer)等。1752年,亨利克·特奥菲卢斯·谢佛尔(Henrik Teofilus Scheffer)发表了一份有关铂的详细科学描述。他将其称为“白金”,并详述了如何利用砷来熔融铂矿物。报告也指出,铂比金更易弯曲,但耐腐蚀性则相近。[44]
卡尔·冯·西金根(Carl von Sickingen)于1772年对铂进行了大量研究。他用以下步骤制成了具可塑性的铂:先将铂与金制成合金,溶于热王水之中,用氯化铵把铂沉淀出来,再将产生的氯铂酸铵点燃,最后把松散的铂敲打成块。弗朗兹·卡尔·阿哈尔德(Franz Karl Achard)于1784年制了第一个铂制坩埚。他将铂与砷结合,经过处理工序后再把砷挥发出来。[44]
由于铂是第一个被发现的铂系元素,所以谢佛尔和西金根误认为,铂的硬度(比铁稍高)会使它较难弯曲,甚至有脆性;然而事实上铂的可塑性很高,与金相近。当时他们的铂样本混杂了不少其他铂系元素,如锇和铱等,这增大了铂样本的脆性。要制成可塑的铂化合物,他们仅能掺入金。如今,人们有制高纯度铂金属的能力。由于铂的晶体结构和许多软金属相似,所以很容易制成很长的铂金属丝。[49]
1786年,西班牙国王卡洛斯三世赐给皮埃尔-弗朗索瓦·沙巴诺(Pierre-François Chabaneau)书库和实验室,以助他对铂的研究。沙巴诺成功从铂矿物中去除各种杂质,包括金、银、铅、铜和铁,这使他认为此样本是单一金属。不过,样本内有尚未被发现的铂系元素。因此沙巴诺得出了矛盾的实验结果:有时铂显得可塑,但在掺入铱后,合金却变得易碎;有时铂完全不可燃,但在掺入锇后,合金却会挥发。几个月之后,沙巴诺对白热化的海绵状含铂物质进行锤打和挤压,制备出23公斤有可塑性的纯铂金属。沙巴诺意识到铂的不熔性会赋予其制成的物品价值,所以他与华金·卡贝萨斯(Joaquín Cabezas)创业,生产铂锭与铂器皿。西班牙的“铂金时代”自此开始。[44]
一氧化碳经过催化转换器中的铂时会被氧化成二氧化碳。格哈德·埃特尔因发现该反应的具体分子机制而于2007年获得了诺贝尔化学奖。[50]
生产
[编辑]

像其馀的铂系金属一样,铂是镍和铜的商业开采加工过程的副产品。在铜的电解精炼过程中,银、金、各铂系金属、硒和碲都会下沉至槽的底部,形成“阳极泥”。铂系金属的萃取过程便是从这一泥状物质开始的。[53]
如果在飘沙沉积物或其他矿物中发现纯铂,则可以在移除杂质的过程中将铂提取。铂的密度高于大部份的杂质,所以较轻的杂质可以用浮力分离的方式轻易地提取。铂具有顺磁性,而镍和铁都具有铁磁性。混合物经过电磁铁后,镍和铁会被分离出来。铂的熔点较高,因此可以利用高温把不少杂质熔融去除。最后,铂不受氢氯酸和硫酸侵蚀,混合物在任一者中经搅拌后,杂质自然会溶解,剩馀的就是铂。[54]
原始铂中也含有金以及其他铂系元素。要纯化原始铂,可以用王水处理。钯、金和铂会溶解,而锇、铱、钌和铑则不会反应。加入二氯化铁后,金会沉淀,并可以过滤出来。加入氯化铵之后,氯铂酸铵会沉淀,经加热后可以转化为铂金属。[55]未沉淀的六氯铂酸(IV)可以经锌元素还原。在实验室中,也可用类似方法从少量残留物中萃取出铂。[56]
应用
[编辑]
2010年售出的245吨铂当中,113吨(46%)用于汽车催化转换器,76吨(31%)用于首饰,其馀35.5吨的应用包括投资、电极、抗癌药物、氧传感器、火花塞和涡轮引擎等。
当中,在医疗界铂被认为是对抗癌症肿瘤最有效的药物,用于化疗,治疗各种类型的癌症。包括肉瘤,某些癌(如小细胞肺癌,头颈癌和卵巢癌),淋巴癌,膀胱癌,子宫颈癌和生殖细胞瘤。
顺铂对睾丸癌有特效; 治愈率从原来的10%提高到85%
此外,顺铂还用于俄歇治疗。[53]
催化剂
[编辑]铂的最大用途是做化学反应的催化剂,这种催化剂通常是铂黑。19世纪早期,化学家开始用铂粉末对氢的点燃反应进行催化。铂目前最大应用于汽车的催化转换器,使废气中低浓度未燃烧的碳氢化合物能够完全燃烧,产生二氧化碳和水气。在石油业中,铂可以用来催化若干个不同的反应,特别是将石脑油催化重整为更高辛烷值的汽油。二氧化铂(或称亚当斯催化剂)是氢化反应的催化剂,特别用于生产植物油。[29]铂金属可以很好地催化过氧化氢分解为水和氧气的反应。[57]
度量衡标准
[编辑]
在1889至1960年间,米的定义以一件特制的九比一铂铱合金棒之长度为标准,这根棒称为国际米原器。在此之前的米原器是1799年用铂所制。公斤的定义也曾经用1879年的同批铂铱合金制成的圆柱体之质量为标准,[58]但这项标准在2019年被基于物理常数的定义所取代(详见2019年国际单位制基本单位重新定义)。
标准铂电阻温度计(SPRT)是定义国际实用温标(ITS-90)使用的四种温度计之一,它是国际范围内校准温度测量的标准。温度计的电阻线由纯铂制造(如NIST采用的是纯度为99.999%的铂条)。[59][60] 在实验室外,铂电阻温度计也有许多工业应用,相关标准包括ASTM E1137与IEC 60751。
贵金属
[编辑]
铂是贵金属贸易商品。铂锭的ISO货币代码为“XPT”。铂币、铂条和铂锭可以作交易或收藏。由于铂不易受侵蚀,且外表闪亮,所以也被用作首饰,通常用90%至95%合金。有关珠宝交易的出版物一般建议珠宝商在铂的表面刮出些划痕。[62][63]
在制表业中,不少公司会用铂来制限量版钟表系列。铂既不会失去光泽,又不会刮损(相比金而言),非常适宜作钟表材料。[64]

和其他工业用贸易商品一样,铂价的波动比金更高。2008年,铂价从每金衡盎司2,252美元降至774美元,[66]市值降低近三分之二。相比同时期,金价从每盎司1,000美元左右跌至700美元左右,市值降低仅三分之一。
在持续稳定增长的经济内,铂价往往是金价的双倍;而在不稳定时期,[67]由于工业需求降低,铂价一般跌至金价的水平以下。在经济滞缓时,金价更加稳定,因为其需求量并不受工业用途的推动。18世纪,法国的路易十五鉴于铂之稀有,宣告铂是唯一配得上国王的金属。[68]
其他用途
[编辑]在实验室当中,铂金属丝可用作电极。热重分析会用铂制的盘和支架,因为在高温下(约1000 °C)它必须要严格地保持化学惰性。铂是各种金属器具的合金添加剂,如金属细丝、抗腐蚀实验容器、医疗器材、假牙、电触头和热电偶等。铂钴合金、铁铂合金可以制成强力的永久磁体。[29],同时也是硬碟碟片中纪录层的主要材料。船只、管道和钢铁码头都有用到含铂的阳极。[11]
尊贵的象征
[编辑]
铂极为稀有,常被认为是尊贵的象征。信用卡、签帐卡及某些会员卡的白金卡服务水平一般比金卡更高。[69]对于唱片来说,“白金奖”是第二高的荣誉,位于钻石以下,金、银、铜之上。例如在美国,销售超过一百万张的唱片会被称为“白金唱片”,而销售超过一千万张的唱片则会被称为“钻石唱片”,但因绝大多数国家、地区没有设立钻石唱片,因此在这些国家、地区白金唱片已是当地最高荣誉。[70]其他商品如果表面呈银白色,也会被称为“白金”。伊丽莎白王后冠是为乔治六世的加冕而特制,其框架就是以铂作为材料。它是首个用到铂金属的英国皇冠。[71]
健康安全
[编辑]根据美国疾病控制与预防中心,短期暴露在铂盐中会刺激眼部和咽喉,长期暴露则有可能会导致呼吸道和皮肤的过敏反应。目前在美国的标准暴露量为每立方米空气2微克铂,数值取8小时工作时段内的平均值。[72]
铂基抗肿瘤药,例如顺铂目前用于化疗,其对付某些肿瘤的效果良好。
铂是某些矽橡胶和凝胶生产过程中的催化剂,这些物质是多种医疗植入物的成份,例如乳房植入物、关节修复体、人工腰椎间盘等等。包括美国食品药品监督管理局在内的多个机构在进行调查后,并未发现铂在体内具有毒性的证据。[73][74]
参考资料
[编辑]- ^ Prohaska, Thomas; Irrgeher, Johanna; Benefield, Jacqueline; Böhlke, John K.; Chesson, Lesley A.; Coplen, Tyler B.; Ding, Tiping; Dunn, Philip J. H.; Gröning, Manfred; Holden, Norman E.; Meijer, Harro A. J. Standard atomic weights of the elements 2021 (IUPAC Technical Report). Pure and Applied Chemistry. 2022-05-04. ISSN 1365-3075. doi:10.1515/pac-2019-0603 (英语).
- ^ 2.0 2.1 Braun, Mihály; Georgiev, Yordan M.; Schönherr, Tommy; Wilsenach, Heinrich; Zuber, Kai. A new precision measurement of the α -decay half-life of 190 Pt. Physics Letters B (Elsevier BV). 2017, 768: 317–320. ISSN 0370-2693. doi:10.1016/j.physletb.2017.02.052.
- ^ crustal abundance of elements. A Dictionary of Earth Sciences. Encyclopedia.com. [2017-05-21]. (原始内容存档于2017-09-23).
Other elements, including such desired metals as gold (Au), silver (Ag), and platinum (Pt), are rare in the crust.
- ^ Kenneth Barbalace. Periodic Table of Elements: Platinum - Pt. EnvironmentalChemistry.com. [2017-05-21].
Earth's Crust/p.p.m.: 0.001
- ^ Activity series. cod.edu. [2017-05-21]. (原始内容存档于2015-04-29).
highly unreactive
- ^ Air Quality Guidelines – Second Edition (PDF). WHO Regional Office for Europe, Copenhagen, Denmark. 2000 [2014-11-30]. (原始内容存档 (PDF)于2012-10-18).
- ^ Wheate, NJ; Walker, S; Craig, GE; Oun, R. The status of platinum anticancer drugs in the clinic and in clinical trials. Dalton transactions (Cambridge, England : 2003). 2010, 39 (35): 8113–27. PMID 20593091. doi:10.1039/C0DT00292E.
- ^ 8.0 8.1 Lagowski, J. J. (编). Chemistry Foundations and Applications 3. Thomson Gale. 2004: 267–268. ISBN 0-02-865724-1.
- ^ CRC press encyclopedia of materials and finishes, 2nd edition, Mel Schwartz , 2002
- ^ Materials handbook, fifteenth edition, McGraw-Hill, by John Vaccari, 2002
- ^ 11.0 11.1 11.2 CRC contributors. Platinum. Lide, David R. (编). CRC Handbook of Chemistry and Physics 4. New York: CRC Press. 2007–2008: 26. ISBN 978-0-8493-0488-0.
- ^ Craig, Bruce D; Anderson, David S; International, A.S.M. Platinum. Handbook of corrosion data. January 1995: 8–9 [2014-11-30]. ISBN 978-0-87170-518-1. (原始内容存档于2013-12-08).
- ^ 13.0 13.1 Kauffman, George B.; Thurner, Joseph J.; Zatko, David A. Ammonium Hexachloroplatinate(IV). Inorganic Syntheses. Inorganic Syntheses. 1967, 9: 182–185. ISBN 978-0-470-13240-1. doi:10.1002/9780470132401.ch51.
- ^ 14.0 14.1 14.2 Han, Y.; Huynh, H. V.; Tan, G. K. Mono- vs Bis(carbene) Complexes: A Detailed Study on Platinum(II)−Benzimidazolin-2-ylidenes. Organometallics. 2007, 26 (18): 4612. doi:10.1021/om700543p.
- ^ Audi, G.; Bersillon, O.; Blachot, J.; Wapstra, A.H. The NUBASE Evaluation of Nuclear and Decay Properties. Nuclear Physics A (Atomic Mass Data Center). 2003, 729: 3–128. Bibcode:2003NuPhA.729....3A. doi:10.1016/j.nuclphysa.2003.11.001.
- ^ Earth's natural wealth: an audit (页面存档备份,存于互联网档案馆). New Scientist. May 23, 2007.
- ^ Stellman, Jeanne Mager. Encyclopaedia of Occupational Health and Safety: Chemical, industries and occupations. International Labour Organization. 1998: 141 [2014-11-30]. ISBN 92-2-109816-8. (原始内容存档于2014-01-07).
- ^ Murata, K. J. in Symposium on Spectrocemical Analysis for Trace Elements. ASTM International. 1958: 71 [2014-11-30]. (原始内容存档于2014-01-07).
- ^ Properties, uses and production of platinum.. Canadian Platinum Corp. 2014-09-29 [2017-05-26]. (原始内容存档于2017-05-20).
Sperrylite (platinum arsenide, PtAs2) ore is also a major source of this metal.
- ^ The History of Platinum. Alaska Community Database Online. ExploreNorth. [2011-04-12]. (原始内容存档于2010-12-22).
Platinum is located on the Bering Sea coast, below Red Mountain on the south spit of Goodnews Bay.
- ^ Xiao, Z.; Laplante, A. R. Characterizing and recovering the platinum group minerals—a review. Minerals Engineering. 2004, 17 (9–10): 961–979. doi:10.1016/j.mineng.2004.04.001.
- ^ Dan Oancea Platinum In South Africa (页面存档备份,存于互联网档案馆). MINING.com. September 2008
- ^ 23.0 23.1 Seymour, R. J.; O'Farrelly, J. I. Platinum-group metals. Kirk Othmer Encyclopedia of Chemical Technology. Wiley. 2001. doi:10.1002/0471238961.1612012019052513.a01.pub2.
- ^ Mining Platinum in Montana. New York Times. 1998-08-13 [2008-09-09]. (原始内容存档于2008-02-03).
- ^ Loferski, P. J. Platinum–Group Metals (PDF). USGS Mineral Resources Program. July 2012 [2012-07-17]. (原始内容存档 (PDF)于2017-05-13).
- ^ Evidence of huge deposits of platinum in State. The Hindu (Chennai, India). 2010-07-02 [2014-11-30]. (原始内容存档于2011-12-06).
- ^ MOU for platinum exploration in Tamil Nadu signed (页面存档备份,存于互联网档案馆). thaindian.com. July 1, 2010
- ^ Koeberl, Christian. Identification of meteoritic components in imactites. Meteorites: flux with time and impact effects. 1998: 133–155 [2014-11-30]. ISBN 978-1-86239-017-1. (原始内容存档于2014-04-13).
- ^ 29.0 29.1 29.2 Krebs, Robert E. Platinum. The History and Use of our Earth's Chemical Elements. Greenwood Press. 1998: 124–127. ISBN 0-313-30123-9.
- ^ Smith, G. F.; Gring, J. L. The Separation and Determination of the Alkali Metals Using Perchloric Acid. V. Perchloric Acid and Chloroplatinic Acid in the Determination of Small Amounts of Potassium in the Presence of Large Amounts of Sodium. Journal of the American Chemical Society. 1933, 55 (10): 3957–3961. doi:10.1021/ja01337a007.
- ^ Schweizer, A. E.; Kerr, G. T. Thermal Decomposition of Hexachloroplatinic Acid. Inorganic Chemistry. 1978, 17 (8): 2326–2327. doi:10.1021/ic50186a067.
- ^ Perry, D. L. Handbook of Inorganic Compounds. CRC Press. 1995: 296–298. ISBN 0-8493-8671-3.
- ^ Ahrens, Sebastian; Strassner, Thomas. Detour-free synthesis of platinum-bis-NHC chloride complexes, their structure and catalytic activity in the CH activation of methane. Inorganica Chimica Acta. 2006, 359 (15): 4789. doi:10.1016/j.ica.2006.05.042.
- ^ Karpov, Andrey; Konuma, Mitsuharu; Jansen, Martin. An experimental proof for negative oxidation states of platinum: ESCA-measurements on barium platinides. Chemical Communications. 2006, (8): 838–840. PMID 16479284. doi:10.1039/b514631c.
- ^ Karpov, Andrey; Nuss, Jürgen; Wedig, Ulrich; Jansen, Martin. Cs2Pt: A Platinide(-II) Exhibiting Complete Charge Separation. Angewandte Chemie International Edition. 2003, 42 (39): 4818. doi:10.1002/anie.200352314.
- ^ 36.0 36.1 Jansen, Martin. Effects of relativistic motion of electrons on the chemistry of gold and platinum. Solid State Sciences. 2005, 7 (12): 1464. Bibcode:2005SSSci...7.1464J. doi:10.1016/j.solidstatesciences.2005.06.015.
- ^ Ghilane, J.; Lagrost, C.; Guilloux-Viry, M.; Simonet, J.; Delamar, M.; Mangeney, C.; Hapiot, P. Spectroscopic Evidence of Platinum Negative Oxidation States at Electrochemically Reduced Surfaces. Journal of Physical Chemistry C. 2007, 111 (15): 5701. doi:10.1021/jp068879d.
- ^ Richards, A.D.; Rodger, A. Synthetic metallomolecules as agents for the control of DNA structure. Chemical Society Reviews. 2007, 36 (3): 471–483 [2014-11-30]. PMID 17325786. doi:10.1039/b609495c. (原始内容存档于2007-03-03).
- ^ Ken Croswell. The Stellar Origin of Copper. KenCroswell.com. 2007-04-06 [2017-05-21]. (原始内容存档于2017-01-19).
- ^ Joel Achenbach. Origin of gold is likely in rare neutron-star collisions. The Washington Post. 2013-07-17 [2017-05-21]. (原始内容存档于2019-07-01).
- ^ Meg Urry. Gold comes from stars. CNN. 2013-07-20 [2017-05-21]. (原始内容存档于2017-07-22).
- ^ Rayner W. Hesse. Jewelrymaking Through History: An Encyclopedia. Greenwood Publishing Group. 2007: 155–156. ISBN 0-313-33507-9.
- ^ EraGem. The History of Platinum Jewelry. All Things Jewelry, Jewelry History. EraGem Post. 2013-12-02 [2017-05-21]. (原始内容存档于2024-04-02).
One group of natives (La Tolita Indians) to the platinum-rich border between Ecuador and Colombia used platinum for nose rings, earrings, and masks.
- ^ 44.0 44.1 44.2 44.3 44.4 Weeks, M. E. Discovery of the Elements 7. Journal of Chemical Education. 1968: 385–407. ISBN 0-8486-8579-2. OCLC 23991202.
- ^ Dixon, Joshua; Brownrigg, William. The literary life of William Brownrigg. To which are added an account of the coal mines near Whitehaven: And Observations on the means of preventing epidemic fevers. 1801: 52 [2014-11-30]. (原始内容存档于2014-11-12).
- ^ Watson, Wm; Brownrigg, William. Several Papers concerning a New Semi-Metal, Called Platina; Communicated to the Royal Society by Mr. Wm. Watson F. R. S (PDF). Philosophical Transactions. 1749, 46 (491–496): 584–596. doi:10.1098/rstl.1749.0110. (原始内容 (PDF)存档于2013-10-21).
- ^ Marggraf, Andreas Sigismund. Versuche mit dem neuen mineralischen Körper Platina del pinto genannt. 1760 [2014-11-30]. (原始内容存档于2015-02-24).
- ^ F. w. Gibbs. William Lewis and Platina - Bicentenary of the 'Commercium Philosophico- technicum'. The Royal Institute of Chemistry, London. [2017-05-19]. (原始内容存档于2017-02-02).
- ^ Platinum (页面存档备份,存于互联网档案馆). mysite.du.edu
- ^ Ertl, Gerhard. Reactions at Surfaces: From Atoms to Complexity (Nobel Lecture). Angewandte Chemie International Edition. 2008, 47 (19): 385–407. PMID 18357601. doi:10.1002/anie.200800480.
- ^ 21.09kg Pt. WolframAlpha. [2012-07-14]. (原始内容存档于2014-08-23).
- ^ Kelly, Thomas D. and Matos, Grecia R. (2013) Historical Statistics for Mineral and Material Commodities in the United States 互联网档案馆的存档,存档日期2013-06-04., U.S. Geological Survey
- ^ 53.0 53.1 Loferski, P. J. 2010 Minerals Yearbook; Platinum-group metals (PDF). USGS Mineral Resources Program. October 2011 [2012-07-17]. (原始内容存档 (PDF)于2012-07-08).
- ^ Heiserman, David L. Exploring Chemical Elements and their Compounds. TAB Books. 1992: 272–274. ISBN 0-8306-3018-X.
- ^ Hunt, L. B.; Lever, F. M. Platinum Metals: A Survey of Productive Resources to industrial Uses (PDF). Platinum Metals Review. 1969, 13 (4): 126–138 [2014-11-30]. (原始内容 (PDF)存档于2015-09-24).
- ^ Kauffman, George B.; Teter, Larry A. and Rhoda, Richard N. Recovery of Platinum from Laboratory Residues. Inorg. Synth. Inorganic Syntheses. 1963, 7: 232. ISBN 9780470132388. doi:10.1002/9780470132388.ch61.
- ^ Petrucci, Ralph H. General Chemistry: Principles & Modern Applications 9th. Prentice Hall. 2007: 606. ISBN 0-13-149330-2.
- ^ Gupta, S. V. Chapter 4. Metre Convention and Evolution of Base Units. Springer Series in Materials Science, Volume 122. 2010: 47. doi:10.1007/978-3-642-00738-5_4.
- ^ Guide tothe Realization of the ITS-90 - Platinum Resistance Thermometry (PDF). International Committee for Weights and Measures. [2020-10-23]. (原始内容存档 (PDF)于2021-02-24).
- ^ Standard Reference Material 1750: Standard Platinum Resistance Thermometers,13.8033 K to 429.7485 K (PDF). NIST. [2020-10-23]. (原始内容存档 (PDF)于2020-10-26).
- ^ Feltham, A. M.; Spiro, Michael. Platinized platinum electrodes. Chemical Reviews. 1971, 71 (2): 177. doi:10.1021/cr60270a002.
- ^ Professional Jeweler's Magazine Archives, issue of August 2004. [2011-06-19]. (原始内容存档于2011-09-28).
- ^ Platinum primer. Diamond Cutters International. [2011-06-18]. (原始内容存档于2011-09-27).
- ^ Unknown Facts about Platinum. watches.infoniac.com. [2008-09-09]. (原始内容存档于2017-11-10).
- ^ Fixing Statistics. The London Platinum and Palladium Market. [2010-06-13]. (原始内容存档于2010-01-25).
- ^ One Year Platinum. Kitco. [2011-06-28]. (原始内容存档于2011-09-28).
- ^ Platinum versus Gold. The Speculative Invertor. 2002-04-14. (原始内容存档于2008年10月26日).
- ^ Platinum. Minerals Zone. [2008-09-09]. (原始内容存档于2008年10月12日).
- ^ Gwin, John. Pricing Financial Institution Products. Journal of Professional Services Marketing. 1986, 1 (3): 91. doi:10.1300/J090v01n03_07.
- ^ Crouse, Richard. Big Bang Baby: The Rock Trivia Book. 2000-05-01: 126 [2014-11-30]. ISBN 978-0-88882-219-2. (原始内容存档于2013-12-08).
- ^ Gauding, Madonna. The Signs and Symbols Bible: The Definitive Guide to Mysterious Markings. 2009-10-06 [2014-11-30]. ISBN 978-1-4027-7004-3. (原始内容存档于2013-12-08).
- ^ Occupational Health Guideline for Soluble Platinum Salts (as Platinum) (PDF). Centers for Disease Control and Prevention. [2008-09-09]. (原始内容存档 (PDF)于2009-06-07).
- ^ FDA Backgrounder on Platinum in Silicone Breast Implants. U.S. Food and Drug Administration. [2008-09-09]. (原始内容存档于2008-07-24).
- ^ Brook, Michael. Platinum in silicone breast implants. Biomaterials. 2006, 27 (17): 3274–3286. PMID 16483647. doi:10.1016/j.biomaterials.2006.01.027.
外部链接
[编辑]- 元素铂在洛斯阿拉莫斯国家实验室的介绍(英文)
- EnvironmentalChemistry.com —— 铂(英文)
- 元素铂在The Periodic Table of Videos(诺丁汉大学)的介绍(英文)
- 元素铂在Peter van der Krogt elements site的介绍(英文)
- WebElements.com – 铂(英文)
- Nuclides and Isotopes (页面存档备份,存于互联网档案馆) Fourteenth Edition: Chart of the Nuclides, General Electric Company, 1989.
- NIOSH Pocket Guide to Chemical Hazards – Platinum (页面存档备份,存于互联网档案馆)(NIOSH化学危害袖珍指南:铂)美国疾病控制与预防中心
- The PGM Database. [2014-11-30]. (原始内容存档于2019-07-01).
- A balanced historical account of the sequence of discoveries of platinum; illustrated.. [2014-11-30]. (原始内容存档于2010-01-23).
- Platinum Metals Review: A free, quarterly journal of research on the science and technology of the platinum group metals and developments in their application in industry. [2014-11-30]. (原始内容存档于2015-05-29).
- Platinum-Group Metals Statistics and Information. United States Geological Survey. [2014-11-30]. (原始内容存档于2016-02-16).