汞
此条目可参照英语维基百科相应条目来扩充。 (2021年12月24日) |
此条目需要补充更多来源。 (2021年12月24日) |


汞(拼音:gǒng,注音:ㄍㄨㄥˇ,粤拼:hung3),俗称水银,是一种化学元素,其化学符号为Hg,原子序数为80,原子量为200.592 u。汞在元素周期表中位于d区,是密度大、室温下为液态的银白色过渡金属,具有轻微的挥发性,且性质与稀有气体类似。除了汞之外在常温下呈液态的稳定元素只有溴,而铯、镓和铷会在比室温稍高的温度下熔化。汞的熔点是−38.83 °C(−37.89 °F;234.32 K),沸点是356.73 °C(674.11 °F;629.88 K),是所有金属元素中液态温度范围最小的。
汞在全世界的矿产中都有产出,主要来自朱砂(硫化汞)。摄入或吸入的朱砂粉尘都是微毒的。汞中毒还能由接触可溶解于水的汞(例如氯化汞和甲基汞)引起,或是因吸入汞蒸气,食用被汞污染的海产品或吸食入汞化合物引起中毒。
汞可用于温度计、气压计、压力计、血压计、浮阀、水银开关和其他装置,但是汞的毒性导致汞温度计和血压计在医疗上正被逐步淘汰,取而代之的是使用酒精、镓铟锡合金等物质填充,或者是使用基于热电偶或压力传感器的数码温度计和血压计。汞仍被用于科学研究和补牙的汞合金材料。汞也被用于发光。荧光灯中的电流通过汞蒸气产生波长很短的紫外线,紫外线使荧光体发出荧光,从而产生可见光。
性质
[编辑]物理性质
[编辑]汞是一种银白色的液态重金属。相较于其它金属,汞导热性能差,而导电性能较佳。[3]
汞的熔点为−38.83 °C,沸点为356.73 °C,[4][5][6]都是稳定金属中最低的,不过对放射性元素鿔和𫓧的初步实验表明它们的沸点都比汞更低(鿔是元素周期表中汞之下的元素,遵循12族元素沸点降低的趋势)。[7]当汞凝固时,它的体积会降低3.59%,密度从13.69 g/cm3增加到14.184 g/cm3。固体汞具有延展性,可以用刀切割。[8]
对于这个性质的完整解释需要非常深入量子物理的领域,但是可以简述如下:汞的核外电子排布很特别,电子填满了所有1s、2s、2p、3s、3p、3d、4s、4p、4d、4f、5s、5p、5d和6s亚层。由于这样的电子排布强烈地阻止汞原子失去电子,所以汞的性质与稀有气体类似,会形成弱的分子间作用力,以至于固体非常容易熔化。
6s亚层的稳定性是源于全满的4f亚层。f亚层会微弱地屏蔽原子核的电荷,这些电荷会增加原子核对6s亚层的库仑引力。缺少填满的内层f亚层是镉和锌沸点相对较高的原因,尽管这两种金属还是很容易熔化的,而且它们的沸点也非常低。[4][5]
汞曾经作为电学测量标准。像西门子电阻单位就是在1860年订定,以汞柱电阻来计算的电阻单位[9]。1884年在巴黎的国际会议中,曾定义“法定欧姆”(legal ohm)是摄氏零度下,长度106公分,截面积为一平方公厘水银柱的电阻[10],但现今的欧姆已不用上述的定义。
汞是人类史上首先发现到的超导体,其超导临界温度为绝对温标4.2K。
商业上有关汞的交易,通常以一烧瓶的容量为单位,约重34.5公斤。
化学性质
[编辑]汞不与大多数的酸反应,例如稀盐酸、稀硫酸、氢溴酸[11];但是氧化性酸,例如浓硫酸、浓硝酸和王水可以溶解汞并形成硫酸盐、硝酸盐和氯化物。汞也可和氢碘酸反应生成氢气和H2[HgI4][11]。与银类似,汞也可以与空气中的硫化氢反应。汞还可以与粉末状的硫反应,这一点被用于处理汞泄露以后吸收汞蒸气的工具里(也有用活性炭和锌粉的)。[12]
汞具有恒定的体积膨胀系数,其金属活跃性低于锌和镉,且不能从酸溶液中置换出氢。一般汞化合物的化合价是+1或+2,+4价的汞化合物只有四氟化汞[13][14]而+3价的汞化合物不存在[15]。
汞齐
[编辑]汞容易与大部分普通金属形成合金,这些汞合金统称汞齐。能与汞形成合金的金属包括金和银,但不包括铁,所以铁粉一直以来被用于置换汞。其他一些第一行的过渡金属难于形成合金,但不包括锰、铜和锌。其他不易与汞形成合金的元素有铂[16][17]和其他一些金属。钠汞齐是有机合成中常用的还原剂,也被用于高压钠灯中。
当汞和纯金属铝接触时,它们易于形成铝汞齐,因为铝汞齐可以破坏防止金属铝的继续氧化的氧化铝层,所以即使很少量的汞也能严重腐蚀金属铝。出于这个原因,绝大多数情况下,汞不能被带上飞机,因为它很容易与飞机上暴露的铝质部件形成合金而造成危险。[18]
同位素
[编辑]汞有七种稳定的同位素,其中202Hg最丰富,占了天然汞的29.86%。汞寿命最长的放射性同位素是半衰期444年的194Hg和半衰期46.612天的203Hg,剩下的放射性同位素半衰期大多少于一天。199Hg和201Hg是最常用的核磁共振原子核,它们的自旋分别是1⁄2和3⁄2。[3]
人类对水银的认知历史
[编辑]在公元前1500年的古埃及墓中人们就找到了汞的存在。
在古代中国,汞被认为可以延长生命,治疗骨折和保持健康,尽管人们现在已经知道汞会导致严重的健康损害。据史记记载,秦始皇的陵墓中以汞为水,流动在他统治的土地的模型中[19]。秦始皇死于服用炼金术士配制的汞和玉石粉末的混合物,汞和玉粉导致了肝衰竭,汞中毒和脑损害,而它们本来是为了让秦始皇获得永生的。中国古代妇女还曾经采用口服少量汞的方式进行避孕。而在《证类本草》中记载,古代中国人用银膏(汞齐)来补牙齿脱落。
古希腊人曾将汞用于油膏中,古埃及人和古罗马人把它加入化妆品中,但有时这样的化妆品会导致脸部变形。在玛雅文明的大城市拉玛奈中,人们在一个中美洲球场里的记号下面发现了一池子的水银。在公元前500年左右,汞已用于制造与其他金属的合金。
18世纪和19世纪中汞用来将做毡帽的动物皮上的毛去掉,这在许多制帽工人中导致了脑损伤。在青霉素出现以前,水银也曾一度用于治疗梅毒。
炼金术士认为汞是形成其他所有金属的第一物质。他们认为不同的金属可由汞中包含的不同质量和含量的硫来生成。最纯的金属是金,而人们需要汞来实现不纯的金属(基础金属)到金的转变,这种转变也是很多炼金术士的目标,18世纪初,包括艾萨克·牛顿在内的许多著名科学家都相信水银可以被转化为黄金[20]。现代化学中,Hg是汞的符号,它来自人造的拉丁词hydrargyrum,其词根来自希腊语Ύδραργυρος(hydrargyros),这个词的两个词根分别表示“水”(Hydro)和“银”(argyros),由于汞与水一样是液体,又像银一样闪亮。在西方,人们用罗马神墨丘利来命名汞,墨丘利以他的速度和流动性著名。汞也与水星有关,天文学中水星的符号就是炼金术士给汞的符号“☿”;而英语中水星和汞的名称也相同。炼金术在梵文中叫Rasavātam,意思是“汞的方式”。汞是唯一一种炼金术士给的名字变成现在常用的名称的金属。
自从两千五百年前从西班牙的阿尔马登开始采汞矿以来,它和意大利的阿米塔山和现在的斯洛文尼亚的伊德里亚一直是主要的汞矿来源,直到19世纪末发现了新的汞矿。
1911年,荷兰科学家海克·卡末林·昂内斯用液氦冷却汞,当温度下降到绝对温标4.2K时水银的电阻完全消失,这种现象称为超导电性,此温度称为超导临界温度。
来源
[编辑]汞是地壳中相当稀少的一种元素,含量只有0.08ppm。因为汞的化学性质,它不易与地壳主量元素成矿,所以考虑到汞在普通岩石中的含量,汞矿中的汞是极为富集的。品位最高的汞矿有2.5%的质量是汞,即使品位最低的也有0.1%,是地壳中含量的12000倍。汞罕见于金属单质,常见于朱砂、氯硫汞矿、硫汞锑矿和其他矿物,其中以朱砂最为常见。汞矿一般形成于非常新的造山带,这里高密度的岩石被推至地壳。汞矿常见于温泉和其他火山地区。
大约世界上50%的汞来自西班牙和意大利,其他主要产地是斯洛维尼亚、俄罗斯和北美。朱砂在流动的空气中加热后其中的汞可以还原,温度降低后汞凝结,这是生产汞的最主要的方式。
1554年,人们发明了用汞从银矿中提取银的混汞法(Patio Process)。从1558年开始,汞成为了西班牙和它的美洲殖民地的重要资源。混汞法被广泛用于新西班牙和秘鲁的银矿。起初,西班牙王室在阿尔马登的矿负责提供所有殖民地所需的汞。后来人们在美洲发现了汞矿。在1953年秘鲁的万卡韦利卡地区发现汞矿之后的三个世纪中,该地区开采了超过十万吨汞。混汞法和之后发明的盘内汞化法(Pan-amalgamation)对汞有巨大需求,以便提取银矿中的银,这种情况一直持续到19世纪晚期。
意大利、美国和墨西哥的汞矿曾经供给了全世界大部分的汞需求,现在这些矿已被完全开采。在斯洛文尼亚和伊德里亚和西班牙的阿尔马登,汞矿因为汞的价格下跌而被关闭。内华达的麦克德米特是美国最后一个汞矿,于1992年关闭。汞的价格波动十分剧烈,在2006年一个76磅(34.46千克)烧瓶的汞价格是650美元。
朱砂在空气流中被加热,发生如下反应:HgS + O2 → Hg + SO2 然后凝结蒸汽以提取汞。
2005年,中国是出产汞最多的国家,占全球市场的三分之二,吉尔吉斯斯坦次之。其他国家被认为从一些未被记录的来源产出了汞,比如电解炼铜的过程和对废水的提炼。
欧盟的指令要求到2012年紧凑型荧光灯变成强制性要求。这一点促使中国重新开采朱砂矿以满足制造紧凑型荧光灯对汞的需求。于是汞对环境的影响又成为了关注的焦点,尤其是南方的佛山、广州等城市和西南的贵州省。
废弃的汞矿往往有成堆的有害的朱砂的煅烧灰。从这些地方流过的水是很大的生态破坏的来源。旧的汞矿可能可以重建以再利用。1976年,加州的圣塔克拉拉郡购买了历史上的阿尔马登汞矿,在进行了深入的安全和环保分析之后,郡政府在原来的汞矿上面建立了一座公园。
化合物
[编辑]汞有两种主要氧化态,+1价和+2价。尽管有声称发现的报告,[21]汞(III)和汞(IV)化合物仍然未知,[22][23]尽管短寿命的Hg(III)化合物可以通过电化学氧化产生。[24]
汞(I)化合物
[编辑]与同组的锌和镉不同的是,汞一般通过金属键形成简单稳定的化合物。大多数+1价汞的化合物是反磁性的,并且形成二聚离子Hg22+。稳定化合物包括盐酸盐和硝酸盐。+1价汞的络合物可以与强络合剂反应,例如硫离子和氰根离子等,发生歧化,生成Hg2+和单质汞。[25]氯化亚汞,又名甘汞,是一种无色固体,化学式为Hg2Cl2,原子的连接方式为Cl-Hg-Hg-Cl。它是电化学中的一种标准物质,也用于医学中。它可与氯气反应生成氯化汞。氢化亚汞是一种无色气体,化学式为HgH,其中没有汞-汞键。
汞易于与自身结合,形成多汞阳离子,例如Hg32+(AsF6-)2中的Hg32+。[26]
汞(II)化合物
[编辑]+2价是汞最常见的氧化态,也是自然界中非常重要的一种。汞的四种卤化物都存在。+2价汞离子与其他配合体形成正四面体的配合物,但是与卤素形成线性的配合物,与银离子类似。最常见的是氯化汞(又称氯化高汞,升汞,氯化汞(II)),一种易升华的白色固体,是腐蚀性极强的剧毒物品。氯化汞通常形成正四面体的配合物,例如HgCl42-。
氧化汞是汞的主要的氧化物,由汞与高温空气长时间接触后产生。氧化汞加热至近400 °C时会分解成汞和氧气。约瑟夫·普里斯特利早期制造纯氧时曾应用这一反应。[12]与金和银的情况类似,人们对汞的氢氧化物了解较少。
作为一种软金属,汞可以与较重的氧族元素形成稳定的化合物。其中非常突出的是硫化汞,HgS。硫化汞在自然界中以朱砂的形式出现,是一种非常好的朱红色素,常用于印泥。朱砂也是一种矿石中药材,也是道士炼丹的一种常用材料。与硫化锌一样,硫化汞也有两种同质异形体,分别是红色的立方晶体和黑色的闪锌矿结构晶体[3],后者在天然中以metacinnabar的形式存在。[27]硒化汞(HgSe)和碲化汞(HgTe)也是已知的,它们和其他一些衍生物,例如半导体碲化汞镉和碲化汞锌,都是很好的红外线探测材料。[28]
+2价汞的盐可与氨形成一系列的衍生物,包括米隆碱(Hg2N+),一维的高聚物 ((HgNH22+)n),易溶的白降汞([Hg(NH3)2]Cl2)。奈斯勒试剂,又称碘化汞钾,仍有时被用来测试氨的存在,因为氨容易于其反应形成深色的米隆碱的碘盐。
雷酸汞是一种广泛应用的烈性炸药,[3]用于早期的雷管,但目前已被更稳定的起爆药所代替。
更高价的氧化态
[编辑]高于+2价的氧化态而非离子形态的汞极为罕见。在羟汞化反应中可能会有一种中间产物是环状的有3个取代基的+4价汞离子。2007年,+4价汞的氟化物被合成出来。20世纪70年代曾有人声称合成出了+3价汞的化合物,但是现在普遍认为这是假的。
有机汞化合物
[编辑]在历史上有机汞化合物很重要,但是在西方世界几乎没有工业价值。+2价的汞盐是极少的能直接与芳香环反应的简单的金属复合物。有机汞化合物总是二价的,配位数一般是2,形成直线型化合物。与有机镉化合物和有机锌化合物不同,有机汞化合物不与水反应。有机汞化合物一般形成通式为HgR2或HgRX的化合物,前者多易挥发而后者多为固体。其中R是芳基或烷基,X一般是卤素或乙酸根。甲基汞表示一系列化学式为CH3HgX的化合物。甲基汞危害非常大,经常出现在被污染的河流或湖泊中。[29]甲基汞会导致生物甲基化作用。
其它
[编辑]实验发现在电弧中惰性气体可以与汞蒸气发生相互作用(并未真正发生化学反应)。这些包合物(HgNe、HgAr、HgKr和HgXe)以范德华力相连。
毒性
[编辑]纯汞有毒,其化合物和盐的毒性多数非常高,口服、吸入或接触后可以导致脑和肝损伤,故今天的温度计大多数使用酒精取代汞,但因其精确度高,一些医用温度计仍然使用汞。
在标准气温和气压下,纯汞最大的危险是它很容易氧化而产生氧化汞,氧化汞容易形成小颗粒从而加大它的表面积。
虽然纯汞比其化合物的毒性低,但它依然是一种很危险的污染物,因为它在生物体内会形成有机化合物。
最危险的汞有机化合物是二甲基汞[(CH3)2Hg],仅数微升接触在皮肤上就可以致死。
硫化汞是毒性较低的化合物。
汞可以在生物体内积累,很容易被皮肤以及呼吸道和消化道吸收。水俣病是汞中毒的一种。汞破坏中枢神经系统,对口、粘膜和牙齿有不良影响。长时间暴露在高汞环境中可以导致脑损伤和死亡。尽管汞沸点很高,但在室内温度下饱和的汞蒸气已经达到了中毒剂量的数倍。
因此在操作汞时要特别小心。盛汞的容器要特别防止它溢出或蒸发,加热汞或者受热易分解的汞化合物时,一定要在一个通风和过滤良好的罩子下进行。此外,有些汞的化合物即使不受热也会自动还原为纯汞,而纯汞则会蒸发,这往往会被忽视。
如果汞洒出来(例如一些温度计或者荧光灯里的汞),就需要特别的处理步骤来吸收洒出的汞和避免接触。常用的操作包括把小的液滴聚拢在坚硬的物体表面以便合成大的液滴,这样可以方便用滴管清除;也可以轻柔地把洒出的汞推进一次性的容器。吸尘器和扫帚不能使用,它们会造成汞的扩散。物理清除之后,可以在被汞污染的区域喷洒硫磺粉、锌粉或其他易与汞在室温下形成合金的粉末,然后再收集反应物并妥善处理。在清理过汞以后,再试图清理多孔的表面和衣服里残存的汞的效果就很差了,所以一般这些物品洒上汞以后应该扔掉。
汞可以导致急性和慢性的中毒。
在污染严重的地区,汞可能会随雨水落下。大气中大部分的汞来自东亚。[30]
自然界中汞的排放
[编辑]工业时代以前的大气中的汞沉降速率可能是大约4纳克每升积冰。尽管这可以看做是一般的自然界的沉降速率,这个速率会受到当地或者全球的汞的来源的极大影响。火山爆发可以使大气里的汞增加4到6倍。大气里大约一半的汞来源于自然界,例如火山。人类活动产生的另一半可以细分为以下来源:
65%来自燃料的燃烧,其中烧煤的火力发电站是最大的来源(美国1999年40%的汞排放来源于此)。这包括了发电站烧的天然气里未被清除的汞。煤的燃烧排放的汞比油排放的高一到两个数量级,各国具体情况不同。
11%来自金的生产。美国最大的三个点污染源是三个最大的金矿。在加拿大东部,水化学作用从金矿残渣中释放的汞已经是大气中汞的重要来源。
6.8%来自非铁金属的生产,常见来源为熔炉。
6.4%来自水泥的生产。
3.0%来自污物和废物的处理,包括生活垃圾和有害物的处理、火葬场以及下水道污泥的焚化。
3.0%来自氢氧化钠的生产。
1.1%来自汞的生产,主要用于电池。
2.0%来自其他所有来源。
以上的百分比来自于2000年人类活动排放的汞,不包括生物燃料燃烧的排放,而这一项在有些地区是很重要的来源。
应用
[编辑]

汞最常用的应用是造工业用化学药物以及在电子或电器产品中获得应用。汞还用于温度计,尤其是在测量高温的温度计。越来越多的气态汞仍用于制造日光灯,而很多的其他应用都因影响健康和安全的问题而被逐渐淘汰,取而代之的是毒性弱但贵很多的镓铟锡合金。除此之外汞之用途还有:
- 可将金从其矿物中分解出来,因此经常用于金矿。
- 气压计和扩散泵等仪器。
- 三相点是-38.8344 °C,它是一个温度的标准点。
- 气态汞用于汞蒸气灯。
- 用于制造液体镜面望远镜。利用旋转使液体形成抛物面形状,以此作为主镜进行天文观测的望远镜,价格为普通望远镜的三分之一。
- 1900年代至1970年代,高压交流电转换直流电的汞弧管(汞弧整流器)里面含有汞。从1970年代中期起,汞弧整流器被矽半导体整流器和大功率晶闸管电路所取代。
- 历史上曾被用于治疗梅毒等性病,但由于毒副作用过大而早已被淘汰。
- 其他用途:水银开关、杀虫剂、生产氯和氢氧化钠的过程中作为汞阴极、防腐剂、在一些电解设备中充当电极、电池和催化剂。
医药
[编辑]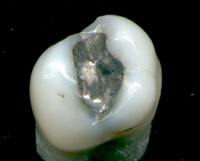
汞和它的化合物一直被用于药物,汞齐对病患是很安全的,是一种制成牙齿填补物的重要元素。尽管现在不如以前那么常见了,因为现在汞和它的化合物的毒性已经被更广泛地知晓(忧心汞齐在高温时会蒸发出汞蒸汽)。硫柳汞是一种用于疫苗中的有机物防腐剂,尽管它的使用已被禁止。另一种汞化合物,汞溴红,是一种局部外用的消毒剂,用于微小切口和表面创伤;在某些国家它仍被使用。
化妆品
[编辑]硫柳汞(Thiomersal)广泛用于制造染眉毛膏。在2008年,美国明尼苏达州成为美国第一个禁止在化妆品中加入汞的州。
法规
[编辑]2013年10月10日,由联合国环境规划署主办的“汞条约外交会议”在日本熊本市表决通过了旨在控制和减少全球汞排放的《关于汞的水俣公约》。该公约的名字是为了纪念在熊本市发现的水俣病。87个国家和地区的代表共同签署了公约。[31]
台湾
[编辑]在台湾的食用油脂食品卫生管理标准中,汞的最大容许量为0.05 ppm。[32]
美国
[编辑]美国国家环境保护局负责汞污染的控制和管理。有几个法律赋予了EPA这项权利,其中包括空气清洁法(Clean Air Act (United States)),水体清洁法(Clean Water Act),资源保护和回收法(Resource Conservation and Recovery Act)和饮水安全法(Safe Drinking Water Act)。此外,1996年通过的含汞电池和可充电电池管理法(Mercury-Containing and Rechargeable Battery Management Act)中要求逐步淘汰汞在电池的使用,并提供了多种类型的废旧电池的经济有效的处理方式。[33]1995年的统计数据中,北美地区的汞排放量约占全球的11%。[34]
欧盟
[编辑]在欧盟,限制在电气和电子设备中使用有害物质的指令(参见危害性物质限制指令)要求在某些电子电器和电子产品中禁止使用汞,而在其他产品中也有汞含量不得超过1000ppm的限制(其附表中亦针对照明光源,如萤光灯管、HID等,订定分阶段实施之更严格的汞含量限制)。[35] 包装中汞的含量有一定的限制(汞,铅,六价铬和镉的总和限制为100ppm),并且电池中这些物质的极限为5ppm(钮扣型电池<2%)。[36]2007年7月起,欧盟也禁止汞在非电测量设备的使用,如温度计和气压计。这项禁令只适用于新设备,医疗机构将获得豁免,并包含了一个给气压计制造商的两年宽限期。[37]
挪威
[编辑]2008年1月1日,挪威颁布对于汞在制造业上的使用和汞产品的进出口行为完全禁止的法令。[38]在2002年,某些挪威的湖泊被发现受到汞污染。[39]
2008年,挪威环境部部长Erik Solheim表示汞是其中一种最具危险性的环境毒素,而目前已有更好汞代替物,因此汞的使用将被禁止。[40]
瑞典
[编辑]丹麦
[编辑]丹麦从2008年起在牙科中禁止使用汞齐。[40]
中国大陆
[编辑]根据2017年8月15日环境保护部印发的《〈关于汞的水俣公约〉生效公告》,《汞公约》将自2017年8月16日生效。[43]
2020年10月,中国国家药监局在其网站发布《国家药监局综合司关于履行关于汞的水俣公约有关事项的通知》,宣布自2026年1月1日起,中国将全面禁止生产含汞体温计和含汞血压计产品[44]。
香港
[编辑]2021年12月1日起,根据香港法例第640章《汞管制条例》,任何人进口或出口条例附表1第1部化学品(第1部化学品),即汞及汞混合物;或存放或使用条例附表1第2部化学品(第2部化学品),必须领有环保署发出的许可证。[45] [46]
对生物的影响
[编辑]鱼和贝类通常会以甲基汞的形态在体内富集汞。甲基汞是一种毒性很强的有机汞。汞和甲基汞都是脂溶性的,所以它们主要富集于内脏,尽管所有的肌肉组织中也都含有汞。处于食物链顶端的鱼类,例如鲨鱼、海豚、旗鱼、国王鲭鱼、蓝鳍金枪鱼、长鳍金枪鱼和方头鱼,体内的汞含量会高于处于食物链低端的鱼类和贝类。当体内含有汞的鱼和贝类被捕食时,汞就会在捕食者内体内累积。鱼类排出甲基汞的速度低于富集的速度,所以组织中的汞含量会逐渐升高。食物链顶端的鱼类体内汞含量可达到被食用的鱼类体内汞含量的十倍。这个过程叫做生物放大作用或者生物富集作用。日本的水俣市曾经因此发生过汞中毒的事件,现在这种由汞中毒引起的严重神经疾病被称作水俣病。
参考资料
[编辑]- ^ "Magnetic susceptibility of the elements and inorganic compounds" (页面存档备份,存于互联网档案馆) in Lide, D. R. (编), CRC Handbook of Chemistry and Physics 86th, Boca Raton (FL): CRC Press, 2005, ISBN 0-8493-0486-5
- ^ Weast, Robert. CRC, Handbook of Chemistry and Physics. Boca Raton, Florida: Chemical Rubber Company Publishing. 1984: E110. ISBN 0-8493-0464-4.
- ^ 3.0 3.1 3.2 3.3 Hammond, C. R The Elements 互联网档案馆的存档,存档日期2008-06-26. in Lide, D. R. (编), CRC Handbook of Chemistry and Physics 86th, Boca Raton (FL): CRC Press, 2005, ISBN 0-8493-0486-5
- ^ 4.0 4.1 Senese, F. Why is mercury a liquid at STP?. General Chemistry Online at Frostburg State University. [2007-05-01]. (原始内容存档于2007-04-04).
- ^ 5.0 5.1 Norrby, L.J. Why is mercury liquid? Or, why do relativistic effects not get into chemistry textbooks?. Journal of Chemical Education. 1991, 68 (2): 110. Bibcode:1991JChEd..68..110N. S2CID 96003717. doi:10.1021/ed068p110.
- ^ Lide, D. R. (编), CRC Handbook of Chemistry and Physics 86th, Boca Raton (FL): CRC Press: 4.125–4.126, 2005, ISBN 0-8493-0486-5
- ^ Dynamic Periodic Table. www.ptable.com. [2016-11-22]. (原始内容存档于2016-11-20).
- ^ Simons, E. N. Guide to Uncommon Metals. Frederick Muller. 1968: 111.
- ^ Werner Siemens, Vorschlag eines reproducirbaren Widerstandsmaaßes, Annalen der Physik und Chemie. 1860, 186 (5): pp. 1–20, (德文)
- ^ Robert B. Northrop. Introduction to Instrumentation and Measurements, Third Edition. CRC Press. 2014-06-04: 20–. ISBN 978-1-4665-9679-5.
- ^ 11.0 11.1 宋天佑、徐家宁、程功臻、王莉. 無機化學 (第四版) (下冊) 2020年9月第三刷. 北京: 高等教育出版社. 2019: 744. ISBN 978-7-04-052146-7 (中文(中国大陆)).
- ^ 12.0 12.1 Greenwood, Norman Neill; Earnshaw, Alan. Chemistry of the elements. 2016. ISBN 978-0-7506-3365-9. OCLC 1040112384 (英语).
- ^ High Oxidation States: Mercury tetrafluoride synthesized. [2012-08-22]. (原始内容存档于2011-07-19).
- ^ Elusive Hg (IV) species has been synthesized under cryogenic conditions. 2007-10-12 [2012-08-22]. (原始内容存档于2012-05-08).
- ^ Riedel, Sebastian; Kaupp, Martin. The highest oxidation states of the transition metal elements. Coordination Chemistry Reviews (Elsevier BV). 2009, 253 (5-6): 606–624. ISSN 0010-8545. doi:10.1016/j.ccr.2008.07.014.
- ^ Gmelin, Leopold. Hand book of chemistry. Cavendish Society. 1852: 103 (Na), 110 (W), 122 (Zn), 128 (Fe), 247 (Au), 338 (Pt) [2012-12-30]. (原始内容存档于2013-05-09).
- ^ Soratur. Essentials of Dental Materials. Jaypee Brothers Publishers. 2002: 14. ISBN 978-81-7179-989-3. (原始内容存档于2016-06-03).
- ^ Vargel, C.; Jacques, M.; Schmidt, M. P. Corrosion of Aluminium. Elsevier. 2004: 158 [2021-12-24]. ISBN 9780080444956. (原始内容存档于2021-10-09).
- ^ 司马迁. 史记.卷6.始皇帝. [2016-11-25]. (原始内容存档于2021-03-13) (中文).
以水银为百川江河大海,机相灌输,上具天文,下具地理
- ^ 约翰·艾姆斯利. 致命元素. 三联书店. 2012-6: 1. ISBN 978-7-108-03993-4 (中文(简体)).
- ^ Wang, Xuefang; Andrews, Lester; Riedel, Sebastian; Kaupp, Martin. Mercury Is a Transition Metal: The First Experimental Evidence for HgF4. Angew. Chem. Int. Ed. 2007, 46 (44): 8371–8375. PMID 17899620. doi:10.1002/anie.200703710.
- ^ Rooms, J. F.; Wilson, A.V.; Harvey, I.; Bridgeman, A.J.; Young, N. A. Mercury-fluorine interactions: a matrix isolation investigation of Hg...F2, HgF2 and HgF4 in argon matrices. Phys Chem Chem Phys. 2008, 10 (31): 4594–605. Bibcode:2008PCCP...10.4594R. PMID 18665309. doi:10.1039/b805608k.
- ^ Riedel, S.; Kaupp, M. The Highest Oxidation States of the Transition Metal Elements. Coordination Chemistry Reviews. 2009, 253 (5–6): 606–624. doi:10.1016/j.ccr.2008.07.014.
- ^ Deming, Richard L.; et al. Tripositive mercury. Low temperature electrochemical oxidation of 1,4,8,11-tetraazacyclotetradecanemercury(II) tetrafluoroborate. Journal of the American Chemical Society. 1976, 98 (14): 4132–4137 [2021-12-25]. doi:10.1021/ja00430a020. (原始内容存档于2021-12-25).
- ^ Henderson, W. Main group chemistry. Great Britain: Royal Society of Chemistry. 2000: 162. ISBN 978-0-85404-617-1. (原始内容存档于2016-05-13).
- ^ Brown, I. D.; Gillespie, R. J.; Morgan, K. R.; Tun, Z.; Ummat, P. K. Preparation and crystal structure of mercury hexafluoroniobate (Hg
3NbF
6) and mercury hexafluorotantalate (Hg
3TaF
6): mercury layer compounds. Inorganic Chemistry. 1984, 23 (26): 4506–4508. doi:10.1021/ic00194a020. - ^ 引用错误:没有为名为
metacinnabar的参考文献提供内容 - ^ Rogalski, A. Infrared detectors. CRC Press. 2000: 507 [2021-12-25]. ISBN 978-90-5699-203-3. (原始内容存档于2021-12-25).
- ^ National Research Council (U.S.) – Board on Environmental Studies and Toxicology. Toxicological effects of methylmercury. National Academies Press. 2000 [2021-12-25]. ISBN 978-0-309-07140-6. (原始内容存档于2021-12-25).
- ^ 存档副本. [2005-12-14]. (原始内容存档于2021-02-13).
- ^ 联合国《水俣公约》在日本熊本签署. 人民网. 2013-10-10 [2013-10-11]. (原始内容存档于2020-09-14).
- ^ 食品藥物消費者知識服務網–食品法規條文查詢. Consumer.fda.gov.tw. 2013-08-20 [2014-02-07]. (原始内容存档于2019-05-02).
- ^ Mercury: Laws and regulations. 美国国家环境保护局. 2008-04-16 [2008-05-30]. (原始内容存档于2008-05-13).
- ^ Reductions in Mercury Emissons. International Joint Commission on the Great Lakes. [2012-10-10]. (原始内容存档于2008-08-28).
- ^ Directive on the Restriction of the Use of Certain Hazardous Substances in Electrical and Electronic Equipment. 2002/95/EC [2012-10-10]. (原始内容存档于2008-12-22). Article 4 Paragraph 1. e.g. "Member States shall ensure that, from July 1, 2006, new electrical and electronic equipment put on the market does not contain lead, mercury, cadmium, hexavalent chromium, polybrominated biphenyls (PBB) or polybrominated diphenyl ethers (PBDE)."
- ^ Mercury compounds in European Union:. EIA Track. 2007 [2008-05-30]. (原始内容存档于2008-04-28).
- ^ Jones H. EU bans mercury in barometers, thermometers. Reuters. 2007-07-10 [2008-05-30]. (原始内容存档于2021-03-22).
- ^ Norway to ban mercury. EU Business. 2007-12-21 [2008-05-30]. (原始内容存档于2008-01-21).
- ^ Berg, T; Fjeld, E; Steinnes, E. Atmospheric mercury in Norway: contributions from different sources. The Science of the total environment. 2006, 368 (1): 3–9. PMID 16310836. doi:10.1016/j.scitotenv.2005.09.059.
- ^ 40.0 40.1 Banning Mercury Amalgam in the United States (PDF). [2014-02-07]. (原始内容存档 (PDF)于2013-11-01).
- ^ Sweden to ban mercury - The Local. Thelocal.se. [2014-02-07]. (原始内容存档于2021-04-11).
- ^ Sweden may be forced to lift ban on mercury - The Local. Thelocal.se. [2014-02-07]. (原始内容存档于2020-11-01).
- ^ 《关于汞的水俣公约》生效公告. www.mee.gov.cn. [2019-10-25]. (原始内容存档于2020-11-01).
- ^ 2026年起全面禁止生产含汞体温计. [2020-10-20]. (原始内容存档于2020-11-01).
- ^ 存档副本. [2023-01-09]. (原始内容存档于2023-05-13).
- ^ 存档副本. [2023-01-09]. (原始内容存档于2022-07-12).
延伸阅读
[编辑][在维基数据编辑]
外部链接
[编辑]- 元素汞在洛斯阿拉莫斯国家实验室的介绍(英文)
- EnvironmentalChemistry.com —— 汞(英文)
- 元素汞在The Periodic Table of Videos(诺丁汉大学)的介绍(英文)
- 元素汞在Peter van der Krogt elements site的介绍(英文)
- WebElements.com – 汞(英文)
- 水银 Shui Yin (页面存档备份,存于互联网档案馆) 中药标本数据库 (香港浸会大学中医药学院) (繁体中文)(英文)