異染性腦白質退化症
| 異染性腦白質退化症 (Metachromatic leukodystrophy) | |
|---|---|
 | |
| 腦硫脂的結構式 | |
| 症状 | 失智症 |
| 类型 | sphingolipidosis[*]、rare hereditary metabolic disease with peripheral neuropathy[*]、rare genetic epilepsy[*]、unclassified primitive or secondary maculopathy[*]、metabolic disease with dementia[*]、hereditary retinal dystrophy[*]、rare dyslipidemia[*]、neurometabolic disease[*]、sphingolipidosis with epilepsy[*]、sulfatidosis[*]、疾病 |
| 分类和外部资源 | |
| 醫學專科 | 內分泌學、神經學 |
| ICD-11 | 5C56.02 |
| ICD-10 | E75.2 |
| ICD-9-CM | 330.0 |
| OMIM | 250100 |
| DiseasesDB | 8080 |
| MedlinePlus | 001205 |
| eMedicine | ped/2893 |
| MeSH | D007966 |
| Orphanet | 512 |
異染性腦白質退化症(Meta-chromatic leuko-dystrophy、MLD,亦稱:異染性腦白質營養不良症、芳基硫酸酯酶A缺乏症<Arylsulfatase A deficiency/ARSA deficiency>、Greenfield's disease)為一種溶酶體貯積症(lysosomal storage disease),將MLD的神經纖維切片以結晶紫染色結果不呈紫色而呈黃褐色、故名之"異染性"(meta-chromatic),一般歸於腦白質營養不良(leukodystrophies)的類別、同於鞘脂質代謝障礙(sphingolipidoses),因其影響神經鞘脂質(sphingolipids)的代謝。而腦白質營養不良影響髓磷脂的"生長"和/或"發展",而"脂質"的被覆是作為周圍神經纖維的"阻隔體"(insulator)貫穿整個中樞和外週的神经系统。MLD亦涉及脑苷脂的積累。[1][2] 異染性腦白質退化症、如同大多數的"酶缺陷"(enzyme deficiency)一樣,存有「常染色體隱性遺傳模式」。[2]
原因[编辑]
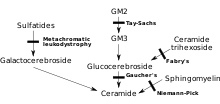
MLD是因染色體#22q13.31ARSA基因之缺失,直接導致芳基硫酸酯酶A(ARSA)的缺乏所引起,[3] 並且通常其特徵在於"酶的活性"不足人體所能控制的10%。[4] 如果沒有這種酶,腦硫脂在身體的許多組織中積聚無法分解(MLD 有較高水平的腦硫脂;相對的、阿茲海默症有較低水平的腦硫脂),最終會破壞神經系統的"髓鞘"(myelin sheath)。髓鞘是一種脂肪覆蓋體,作用是保護神經纖維。沒有髓鞘,在大腦的中樞神經(中樞神經系統-CNS)及外週神經(外週神經系統-PNS)的控制功能,其中包括肌肉的移動等活動,就"不再正常地運作"。最近的一項研究主張"腦硫脂"不完全對MLD的症狀負責,因為腦硫脂是無毒的。有人已提出"溶血腦硫脂"(溶血硫腦苷脂/lyso-sulfatide)由於其體外細胞毒性的作用而引起MLD。而"腦硫脂"已去除它的酰基、因之不完全會激起MLD病症。[5]
遺傳學[编辑]

MLD為一種「常染色體隱性遺傳模式」。在"每個出生嬰兒"的繼承概率如下:
- 如果父母雙方都是"帶原者":
- 25%(1/4)的小孩將會有此病症。
- 50%(2/4)的小孩將會成為帶原者(不過不會受到感染)。
- 25%(1/4)的小孩將不會有MLD -- 未感染的小孩不會成為帶原者。
- 如果父母只有一方"感染",而另一方"沒有感染MLD":
- 0%(0)的小孩將會有此症狀 -- 父母只有一方受到感染,另一方總是遺傳正常基因。
- 100%(4/4)小孩將會成為帶原者(不過不會受到感染)。
- 如果父母只有一方為帶原者,而另一方沒有感染MLD:
- 50%(2/4)的小孩將會成為帶原者(不過不會受到感染)。
- 50%(2/4)的小孩將不會有MLD -- 未感染的小孩不會成為帶原者。
除了這些遺傳模式出現繼承概率外、還存有一種「偽-ARSA缺乏症(pseudo-(Arylsulfatase A) deficiency)」,影響到7%-15%的人口。[6][7] 有"偽-缺乏症"的人沒有任何MLD的問題,除非他們也受到感染。以目前的診斷測試分析、"偽-缺乏症"呈現出"低酶"的水平,但"腦硫脂"的運作正常、因此MLD症狀不存在。這種"偽-現象"造成"傳統的檢查法"至"新生兒篩查法"(Newborn Screening)嚴重的誤判,因此"更新的篩選法"也正在研發。
欲了解更多信息,請參見隱性基因和顯性關係等條目。此外,也可諮詢<MLD基金會>的MLD遺傳學網頁。
發病率[编辑]
估計"異染性腦白質退化症"在全世界人口中的发病率分佈在<1比40,000>至<1比160,000>之間。[8] 有更高的發病率發生在"特定的遺傳隔離群體"(certain genetically isolated populations)裡、如<1比75>的以色列哈巴尼猶太人(Habbani Jews、從阿拉伯南部移民到以色列的一小群猶太人)、<1比2,500>在美國纳瓦霍族保留地的西部地區,以及<1比8000>在以色列的阿拉伯群體裡。[8]
症狀和MLD形式[编辑]
如同其他許多會影響"脂質代謝"(lipid metabolism)的遺傳性疾病一樣,MLD也有多種病發期的MLD形式,如嬰幼兒後期、青少年儿童期,及成人期。
- 在"嬰幼兒後期"的MLD形式,這是MLD的最常見的病發期(佔病症人口的50-60%之間),受感染的嬰幼兒在出生第一年後行走困難,病發期通常分佈在出生後15-24個月之間。[9] 發病症狀包括肌肉萎縮及無力、肌肉強直、發育遲緩、視力逐漸喪失、導致失明、抽搐、吞嚥障礙、瘫痪和癡呆。孩子可能會轉為昏迷。未及時治療,多數患有這種形式MLD的孩子會死於5歲左右,通常會更快。
- 青少年兒童期的MLD形式(發病於3至10歲之間),通常開始於學校的表現落後、智力減退、癡呆、或一些精神症狀出現,病發的症狀相似於"嬰幼兒後期",但病情發展較慢。死亡年齡為"變量"(variable),但通常介於症狀發作期的10歲至15歲之間,然而有些青少年可以繼續存活至發病後數十年或更長的時間。
安寧療法、或者針灸療法可以對MLD症狀有許多幫助,[11]通常可以改善生活品質和延長壽命。
帶原者和他們的家人相比之下呈現"低酶水平"("正常的酶水平"因家庭而異),不過即使是低酶水平仍足以處理身體的"腦硫脂積累"現象。
治療方法[编辑]
由於神經系統髓鞘的缺損在時下的醫學治療上屬於不可逆性,故而目前還沒有確切的治療或治愈MLD的方法,僅能針對MLD病狀做改善、或安寧性治療。"較長的青少年"或"成人"開始發病及"嬰幼兒後期"的患者在症狀顯示後接受治療,會拘限於疼痛和病症處理等之問題;有少數患者可用Vighafvine(抗抽筋藥)來緩解痙攣的疼痛。[12]在症狀前期之"嬰幼兒後期"的MLD患者,以及那些青少年或成年MLD患者,要麼出現"症狀前期病徵"或者顯示"輕度至中度的症狀";而對於可選擇骨髓移植(包括幹細胞移植)的患者,目前正在研究,看它是否可能讓MLD的症狀進展放緩、或停止MLD在中樞神經系統中的症狀進展。然而,結果顯示MLD的症狀進展在周圍神經系統一直沒有顯著的放緩,而這些長期治療的效果好壞參半。
幾個未來的治療方案,目前正在進行研究。這些措施包括基因治療、酶替代療法(Enzyme replacement therapy/ERT)、底物減少療法(Substrate reduction therapy/SRT),及"潛在性酶增強療法"(potentially enzyme enhancement therapy/EET)等。
一組國際研究人員及基金會在2008年組成國際MLD註冊單位 (页面存档备份,存于互联网档案馆)創建和管理知識共享資源庫,包括MLD的自然史(NHS)基礎。該組織包括科學,學術和工業資源。然而、之後註冊單位從來沒有開始運作。[13]
臨床試驗[编辑]
骨髓和幹細胞移植療法[编辑]
基因治療[编辑]
目前正在研究兩種不同的基因療法、以之來治療MLD病症。
- 基因治療與自體(Autotransplantation)幹細胞移植 -- 意大利的研究人員在"聖拉斐爾特勒松"研究院 (页面存档备份,存于互联网档案馆)(San Raffaele Telethon Institute)測試"結合基因治療幹細胞移植"的新方法。[14] 計劃為招募MLD患者進行"第I/II期"的臨床試驗、時程自意大利當局2010年3月24日批准後正式啟動。最初招募的試驗組為8名MLD患者,計劃完成於2013年三月中旬。該試驗是測試"自體"(Autologous blood donation、利用患者自身的細胞)的造血幹細胞移植(HSCT)機制、在經由"血細胞路徑"(route of the blood cells)將"基因修飾"(genetic modification)過再傳送<"超治療"(強調性質)的"芳基硫酸酯酶A"(ARSA enzyme)>到達"神經系統"後之有效性和安全性的評測。即利用患者自身的"幹細胞"(stem cell)與基因來修正,應該可以減少或消除"嫁接"(graft)對於"宿主"(host)的併發症。並且能夠對於出現在MLD病患身體裡的ARSA提供長期的解決方案。在"標準試驗"(bench)及動物試驗下均顯示出正向成果。研究人員在2013年7月公佈二年來第一批3名患者的療程成效。結果被認為有研發潛力。[15]
- 亞洲自體幹細胞基因移植 -- 亞洲首宗由香港大學李嘉誠醫學院、大陸深圳市第二人民醫院,及台灣的臺大醫院。於2014年9月為成人期MLD形式的後期患者俞潤潤,於深圳市第二人民醫院進行亞洲首宗自體幹細胞基因移植。[17] 至今患者恢復情況良好。[18]
- 腦基因治療 -- 在2013年的三月下旬於巴黎開始招募"第I/II期"臨床試驗病患、進行"腦基因"(Intracerebral Gene Therapy)治療的臨床試驗,其中特殊的"向量體"(vector)載送"基因修飾過的材料"直接注射到大腦中的十幾個地點。希望"修正過的細胞"來製造"酶"然後擴散到大腦的周邊地區。在實驗室的延伸工作及一些令人鼓舞的ALD研究 (页面存档备份,存于互联网档案馆),提供了這項試驗的依據。
- 招募5個年紀較大的小孩、年齡介於4歲及6歲之間、進行為期兩年的研究。
- 必須在過去的12個月裡第一次出現過症狀。
- 附加的試驗入選標準和資訊可以在這兒找到
酶替代療法(ERT)[编辑]
- 希雷修曼(Shire Human)基因療法 (页面存档备份,存于互联网档案馆)(希雷HGT)為英國希雷PLC (页面存档备份,存于互联网档案馆)的一個部門,2012年1月開始為它們的鞘内注射(脊髓腔內注射/IT)"HGT-1110ERT產品"之臨床試驗[19]招募病患。[20]
- 入選標準
- 第一次症狀出現在2歲半之前、而目前為7歲或年齡更小的幼兒。
- 在門診走廊 -- 只用一隻手扶著能夠走10步。
- 額外的臨床試驗資訊和入選標準,可以在MLD基金會網站這兒,及在臨床Trials.gov (页面存档备份,存于互联网档案馆)網站上找到。
- 這次臨床試驗為期38週、18個兒童以三種不同的劑量分組,且分散在多個地點進行。"不治療"(no treatment)安慰劑組從2012年6月的試驗裡刪除。[21]
- 患者必須到五個試驗地點之一進行每間隔一周的酶注射:丹麥哥本哈根,法國巴黎,德國蒂宾根,澳大利亞悉尼,或巴西阿雷格里港。而阿根廷的"德爾基"(Derqui)正等待批复。
- 2013年12月被批准開始從一個新的供應商獲得一個新的"鞘内注射埠口"(intrathecal port)。更詳細資訊請參見MLD基金會網頁。
- HGT-1110ERT在歐洲[22]和美國[23]均是"孤兒產品"(orphan product)狀態。
- 歷史: 希雷在2010年暫停"元酶靜脈ERT"(Metazyme intravenous ERT)產品的開發。在2008年從賽門艾克(Zymenex)(由"希雷"收購後更名為HGT-1111)收購時它只是一個臨床試驗,在歐洲的"第I/II期"臨床試驗之後它被證明不具有足夠的功效。最初的研究2008年9月完成,而且伴隨著"停止供應產品給試驗參與者"的擴展研究於2010年10月完成。[24][25]
- 入選標準
底物減少療法(SRT)[编辑]
- "白莫林南方公司"(Biomarin South、於2013年1月被"白莫林"收購之前屬於拉凱隆(Zacharon)公司)在美國聖地亞哥已經啟動了"溶酶體貯積症"(Lysosomal storage disorders/LSDS)的藥物研發計劃。這個計劃是基於使用檢測來量測"腦硫脂積累"(sulfatide accumulation)程度,也是為藉由"培養過的纖維細胞"(cultured fibroblast)來作為研究和開發MLD"小分子藥物"(small molecule drug)的方法。(此方法不同於其他的方法像是由所測得的酶活性來研發有效性藥物) 至2011年7月、拉凱隆(Zacharon)公司已先開始進行化驗分析工作,主要是為了"溶酶體貯積症"而進行藥品研發,如此他們可以被聘僱來研究和開發MLD的藥物。(2013年3月)
- "庫珀健康系統"(Cooper Health System、新澤西州)在2009年贊助治療MLD之臨床試驗,以確定"維生素K拮抗劑"(华法林)的安全性和有效性。眾所周知所發表的報告顯示SRT是沒有什麼成果。[26] (2013年3月)
自然史研究[编辑]
按此了解更多資料(目前為2014年2月)
由MLD基金會提供研究和臨床試驗的更新資訊
参考文献[编辑]
引用[编辑]
- ^ 道兰氏医学词典中的metachromatic leukodystrophy
- ^ 2.0 2.1 Le, Tao; Bhushan, Vikas; Hofmann, Jeffrey. First Aid for the USMLE Step 1. McGraw-Hill. 2012: 117.
- ^ Poeppel P, Habetha M, Marcão A, Büssow H, Berna L, Gieselmann V. Missense mutations as a cause of metachromatic leukodystrophy, Degradation of arylsulfatase A in the endoplasmic reticulum. FEBS J. March 2005, 272 (5): 1179–88. PMID 15720392. doi:10.1111/j.1742-4658.2005.04553.x.
- ^ Fluharty, Arvan. "Arylsulfatase A Deficiency: Metachromatic Leukodystrophy, ARSA Deficiency". GeneReviews, 2006
- ^ Maria Blomqvist, Volkmar Gieselmann, Jan-Eric Månsson. Accumulation of lysosulfatide in the brain of arylsulfatase A-deficient mice. Lipids in Health and Disease. 2011-02-07, 10: 28 [2018-04-02]. ISSN 1476-511X. doi:10.1186/1476-511x-10-28.
- ^ Hohenschutz, C; Eich P, Friedl W, Waheed A, Conzelmann E, Propping P. Pseudodeficiency of arylsulfatase A. Human Genetics. April 1989, 45–8 [2012-09-30]. PMID 2565866. (原始内容存档于2014-03-01).
- ^ Herz, Barbara; Bach, G. Arylsulfatase A in pseudodeficiency. HUMAN GENETICS. 1984, 66: 147–150 [2012-09-30]. [永久失效連結]
- ^ 8.0 8.1 Metachromatic leukodystrophy (页面存档备份,存于互联网档案馆) at Genetics Home Reference. Reviewed September 2007
- ^ 地方中心/綜合報導,"潤潤翻版!台中2歲女童罹患MLD絕症"[1] (页面存档备份,存于互联网档案馆),ETtoday 東森新聞雲,2014年02月9日 16:47. (中文)
- ^ 地方中心/綜合報導,"募款最後一哩路,點亮MLD孩子的希望曙光還差500萬"[2] (页面存档备份,存于互联网档案馆),ETtoday 東森新聞雲,2014年02月27日 16:34. (中文)
- ^ 生活中心/綜合報導,"罕病少女潤潤好轉 忍皮肉痛周針灸5次維持體力"[3] (页面存档备份,存于互联网档案馆),ETtoday 新聞雲,2014年03月16日/16:06.
- ^ 黃正宏醫師審稿/蕭雅慧編譯,"MLD症候群(Metachromatic Leukodystrophy)"[4] (页面存档备份,存于互联网档案馆),財團法人罕見疾病基金會,2016年3月14日查閱.
- ^ MLD Registry http://www.MLDregistry.org. [2020-09-15]. (原始内容存档于2018-03-22). 外部链接存在于
|title=(帮助) - ^ Biffi A, Lucchini G, Rovelli A, Sessa M. Metachromatic leukodystrophy: an overview of current and prospective treatments. Bone Marrow Transplant. October 2008,. 42 Suppl 2: S2–6. PMID 18978739. doi:10.1038/bmt.2008.275.
- ^ Alessandra Biffi, Eugenio Montini, Laura Lorioli, Martina Cesani, Francesca Fumagalli, Tiziana Plati, Cristina Baldoli, Sabata Martino, Andrea Calabria, Sabrina Canale, Fabrizio Benedicenti, Giuliana Vallanti, Luca Biasco, Simone Leo, Nabil Kabbara, Gianluigi Zanetti, William B. Rizzo, Nalini A. L. Mehta, Maria Pia Cicalese, Miriam Casiraghi, Jaap J. Boelens, Ubaldo Del Carro, David J. Dow, Manfred Schmidt, Andrea Assanelli, Victor Neduva, Clelia Di Serio, Elia Stupka, Jason Gardner, Christof von Kalle, Claudio Bordignon, Fabio Ciceri, Attilio Rovelli, Maria Grazia Roncarolo, Alessandro Aiuti, Maria Sessa, Luigi Naldini. Lentiviral Hematopoietic Stem Cell Gene Therapy Benefits Metachromatic Leukodystrophy. Science. 2013-08-23, 341 (6148): 1233158 [2018-04-02]. ISSN 0036-8075. doi:10.1126/science.1233158. (原始内容存档于2018-03-17) (英语).
- ^ Inclusion criteria, Therapy Description & Contact information 互联网档案馆的存檔,存档日期2012-04-04.
- ^ 生活中心/綜合報導,"世界第一例!潤潤堅強挺過毒針治療 期待再創奇蹟"[5] (页面存档备份,存于互联网档案馆),ETtoday 東森新聞雲,2014年09月30日 15:40. (中文)
- ^ 記者曾雅玲/綜合報導,"世界首例!港大醫療團隊正式向國際宣告 成功救回潤潤"[6] (页面存档备份,存于互联网档案馆),ETtoday 東森新聞雲,2015年05月20日 19:43. (中文)
- ^ http://clinicaltrials.gov/ct2/show/NCT01510028. [2014-02-21]. (原始内容存档于2012-03-05). 外部链接存在于
|title=(帮助) - ^ [7]
- ^ 存档副本. [2014-02-21]. (原始内容存档于2013-04-09).
- ^ EU/3/10/813 European Commission orphan designation EU/3/10/813 issued 26-November-2010. [2020-09-15]. (原始内容存档于2016-03-05).
- ^ FDA/OOPD issued 27-February-2008. [2014-02-21]. (原始内容存档于2014-01-04).
- ^ http://clinicaltrials.gov/ct2/show/NCT00633139. [2014-02-21]. (原始内容存档于2011-12-30). 外部链接存在于
|title=(帮助) - ^ http://clinicaltrials.gov/ct2/show/NCT00681811. [2014-02-21]. (原始内容存档于2012-03-08). 外部链接存在于
|title=(帮助) - ^ http://clinicaltrials.gov/ct2/show/NCT00683189. [2014-02-21]. (原始内容存档于2011-12-30). 外部链接存在于
|title=(帮助)
来源[编辑]
- 本文的某些部分出自美國神經學疾病與中風研究所(National Institute of Neurological Disorders and Stroke)的公共領域文章:
- NINDS Metachromatic Leukodystrophy Information Page. [2009-06-07]. (原始内容存档于2009-06-03).
參見[编辑]
- 髓鞘再生研究計劃(The Myelin Project)
- 羅倫佐的油
- 髓磷脂修復基金會 (页面存档备份,存于互联网档案馆)
- 嚴重免疫缺陷綜合症(Severe combined immunodeficiency/SCID)
- 氯苯甲嗪(Meclizine/HCL/Meclizine 25mg Tab/美克洛嗪、美克旅鎮片、敏可靜、美克利靜、保暈錠/暈眩止吐用藥/白色圓扁形/錠劑)
- 鞘内注射泵(Intrathecal pump)
- 多硫酸酯酶缺乏症(Multiple sulfatase deficiency)
- 曲吡那敏(Tripelennamine)
- 硫酸酯酶(Sulfatase)
- 22q13缺失綜合症(22q13 deletion syndrome)
- 腦苷−硫酸酯酶(cerebroside-sulfatase)
- PNPLA3(PNPLA3)
- 鞘磷脂磷酸二酯酶1(Sphingomyelin phosphodiesterase 1)
- 腎上腺腦白質失養症(ALD)
- 臺灣腦組織資源聯盟建置策略(臺灣腦庫)
外部链接[编辑]
- 全球性MLD专门組織
- 異染性腦白質營養不良及溶酶體病組織
- Australian Leukodystrophy Support Group (Australia)
- Bethany's Hope (Canada) (页面存档备份,存于互联网档案馆)
- ELA, The European Leukodystrophy Association (页面存档备份,存于互联网档案馆)
- The Evanosky Foundation (页面存档备份,存于互联网档案馆)
- Hide & Seek Foundation for Lysosomal Disease Research (页面存档备份,存于互联网档案馆)
- New Zealand Organisation for Rare Disorders (页面存档备份,存于互联网档案馆)
- The Stennis Foundation
- 有關MLD的進一步信息、治療、遺傳學,和當前的研究項目
- Lentiviral Hematopoietic Stem Cell Gene Therapy Benefits Metachromatic Leukodystrophy (页面存档备份,存于互联网档案馆)
- The Evanosky Foundation
- MLD Foundation
- The Stennis Foundation (页面存档备份,存于互联网档案馆)
- 其它參考鏈接
- 財團法人罕見疾病基金會(Taiwan Foundation for Rare Disorders/TFRD) (页面存档备份,存于互联网档案馆)
- Biomarin (页面存档备份,存于互联网档案馆)
- Shire HGT (页面存档备份,存于互联网档案馆) drug development pipeline
- 2008 eMedicine article (页面存档备份,存于互联网档案馆) about MLD by Ikeda & Moore of UCLA and Steiner of OHSU
- NIH/GeneReviews overview of MLD written by Arvan Fluharty of UCLA (updated August 2011)
- 台灣神經罕見疾病學會(Society for Neurological Rare Disorders-Taiwan - About TBTRC) (页面存档备份,存于互联网档案馆)
- 臺灣腦組織資源聯盟建置策略(臺灣腦庫) – 國家衛生研究院論壇 (页面存档备份,存于互联网档案馆)
| ||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||
