氯化鋅
| 氯化鋅 | |
|---|---|

| |
| IUPAC名 Zinc chloride | |
| 別名 | 氯化鋅(II)、二氯化鋅 |
| 識別 | |
| CAS號 | 7646-85-7(無水) 21351-92-8(一水) 19417-15-3(二水) 74182-35-7(三水) 29426-92-4(四水) |
| PubChem | 3007855 |
| ChemSpider | 5525 |
| SMILES |
|
| InChI |
|
| InChIKey | JIAARYAFYJHUJI-NUQVWONBAB |
| UN編號 | 2331 |
| EINECS | 231-592-0 |
| ChEBI | 49976 |
| RTECS | ZH1400000 |
| 性質 | |
| 化學式 | ZnCl2 |
| 莫耳質量 | 136.315 g·mol⁻¹ |
| 外觀 | 白色晶體 |
| 密度 | 2.907 g/cm³ |
| 熔點 | 290 °C(563 K)([1]) |
| 沸點 | 732 °C(1005 K)([1]) |
| 溶解性(水) | 432 g/100 mL (25 °C) |
| 結構 | |
| 晶體結構 | 有四種已知的結構,六方密堆積是無水狀態下唯一穩定的結構 |
| 配位幾何 | 四面體,氣態時為直線型 |
| 危險性 | |
| 歐盟危險性符號 | |
| 警示術語 | R:R34-R50-R53 |
| 安全術語 | S:S7/8-S28-S45-S60-S61 |
| MSDS | 英文MSDS |
| NFPA 704 | |
| 致死量或濃度: | |
LD50(中位劑量)
|
350 mg/kg, 大鼠 (口服) |
| 相關物質 | |
| 其他陰離子 | 氟化鋅、溴化鋅、碘化鋅 |
| 其他陽離子 | 氯化銅、氯化鎘 |
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |
氯化鋅是氯和鋅的化合物,化學式為ZnCl2。它是無色或白色固體,有極強的水溶性和吸濕性,甚至會潮解,應在乾燥處密封儲存,避免與空氣中的水蒸氣接觸。
在紡織加工、焊接、化學合成等方面,氯化鋅有著廣泛應用。
結構和物性[編輯]
氯化鋅是一種離子化合物,有多晶型性,目前已發現四種晶體結構。但純氯化鋅只能形成δ型(六方密堆積),即在晶體中,每個鋅離子被4個氯離子成正四面體狀包圍。[2] 將它熔融後再冷卻可以得到玻璃狀的物質。
氯化鋅還顯示出共價化合物的特性,如熔點低(275 °C)、易溶於乙醚等溶劑形成形如ZnCl2L2(其中L代表溶劑分子)的加合物。氯化鋅的濃水溶液(質量分數高於64%)有能夠溶解澱粉、絲和纖維素的特殊性質,所以不能使用普通的濾紙來進行過濾。它屬於路易斯酸,強度中等,稀水溶液的pH值在4左右,6 mol/L的濃水溶液pH=1。[3] 當含水的氯化鋅被加熱時,會水解成氯氧化物。
氯化鋅已知4種結晶水合物,以及至少一種鹼式鹽如ZnOHCl。[2] 從氯化鋅水溶液中可以析出它的結晶水合物ZnCl2(H2O)n,以n=4為最主要的成分,其他的形態n值分別為1、1.5、2.5、3。[3] 水合的氯化鋅加熱後可得到ZnOHCl。
在水溶液中,無水、水合等各種晶體形態的氯化鋅均完全解離出Zn2+,以便製備其他鋅鹽。比如製備碳酸鋅:
由於各種氯化鋅及其他鹵化鋅、硫酸鋅在水中一樣能完全解離,因而這些物質在製備其他鋅鹽中與ZnCl2是等效的。
製備與提純[編輯]
水合的氯化鋅也能通過濃鹽酸與鋅反應得到,又可以使用氧化鋅或硫化鋅。
平時所能購買到的氯化鋅通常含有水和主要的水解產物。一般通過以下步驟來提純:將100g的氯化鋅加入800mL的二惡烷中加熱,進行分餾。趁熱進行過濾,除去鋅粉,冷卻後氯化鋅變為白色沉澱。而無水的氯化鋅則可以先在氯化氫氣流中加熱升華,然後在乾燥的氮氣流中加熱到400°C。也可以將樣品通過二氯亞碸處理。[4]
用途[編輯]
紡織加工方面[編輯]
由於氯化鋅與絲綢、纖維素等材料的親和性,它可用作衣料的防火物質,也可用在織物氣味潔淨劑中。
焊接方面[編輯]
氯化鋅可以攻擊金屬氧化物(MO)生成MZnOCl2,這就是它作為金屬焊劑的原理。ZnCl2溶解掉金屬表面的緻密氧化層,使金屬裸露出來。[3] 將鋅箔片溶解在稀鹽酸中,直至不再產生氫氣,即得此種焊劑,因此它得名焊酸。由於其腐蝕性,如果工作後的殘餘物不能清理乾淨,就不能用焊酸作為焊劑,如焊電子元件時。
利用這一原理,ZnCl2還可以用於製造牙充填所用的氧化鎂水泥,某些品牌的漱口水也用它作活性成分。
化學合成方面[編輯]
在化學合成中,氯化鋅作為一種中強路易斯酸,用途廣泛。它可以做費舍爾吲哚環合反應(A)的催化劑,[5] 也可以催化活化芳香環上的傅-克醯基化反應(B)。[6][7]
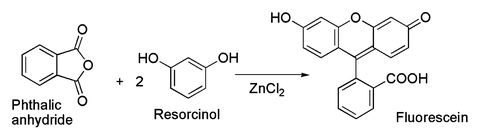
製備染料螢光黃的經典方法,就是用氯化鋅催化的傅-克醯基化反應,原料是鄰苯二甲酸酐和雷索辛。[8] 其中無水和水合的氯化鋅皆能催化。
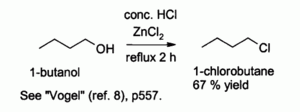
ZnCl2和鹽酸組成的試劑叫盧卡斯試劑(Lucas reagent),用於伯醇和仲醇醇羥基的氯代,反應溫度130 °C。試劑中ZnCl2的加入提高了氯化氫的反應效率。對伯醇的反應一般通過SN2機理,而對仲醇則是SN1。
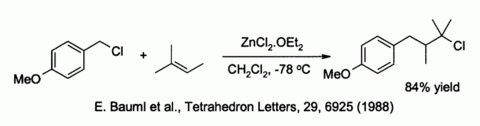
ZnCl2可以活化一些鹵原子的取代。如烯烴等弱親核試劑對苯甲基鹵、烯丙基鹵上的取代(見下圖)[9]、NaBH3CN對苯甲基鹵、烯丙基鹵、叔鹵原子的選擇性還原。
ZnCl2是合成許多有機鋅試劑的起始物。這些有機鋅試劑,一般通過有機鋰試劑或格林尼亞試劑的金屬交換反應製備,用於偶聯等反應,如與芳基鹵、乙烯基鹵進行的根岸偶聯。[10]
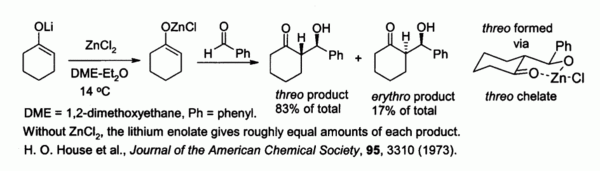
ZnCl2與鹼金屬烯醇鹽生成的鋅烯醇鹽可以在羥醛縮合時控制手性。如下圖[11],由於鋅的存在,形成了螯合環,體積較大的苯環傾向於占據「平伏」的位置,即「反式」構型,產物中「反式」(threo)與「順式」(erythro)比例為5:1。相比之下,反應機理中沒有螯合環時,「順式」「反式」產物的比例為1:1。
安全事項[編輯]
有腐蝕性和刺激性。操作時戴好防護眼鏡、手套,注意避免與無水氯化鋅接觸,這一類無水金屬鹵化物水解時都會放熱。細節參見表中MSDS連結。
參考[編輯]
- ^ 1.0 1.1 O'Neil, M. J.; et al. The Merck index : an encyclopedia of chemicals, drugs, and biologicals
 . N. J.: Whitehouse Station. 2001. ISBN 978-0911910131.
. N. J.: Whitehouse Station. 2001. ISBN 978-0911910131.
- ^ 2.0 2.1 Wells, A.F. (1984) Structural Inorganic Chemistry, Oxford: Clarendon Press. ISBN 0-19-855370-6.
- ^ 3.0 3.1 3.2 Holleman, A. F.; Wiberg, E. "Inorganic Chemistry" Academic Press: San Diego, 2001. ISBN 0-12-352651-5.
- ^ Pray, A. P. 「Anhydrous Metal Chlorides」 "Inorganic Syntheses," vol. XXVIII, 321-2, 1990ISBN 0-471-52619-3. Describes the formation of anhydrous LiCl, CuCl2, ZnCl2, CdCl2, ThCl4, CrCl3, FeCl3, CoCl2, and NiCl2 from the corresponding hydrates.
- ^ R. L. Shriner, W. C. Ashley, E. Welch, in Organic Syntheses Collective Volume 3, p 725, Wiley, New York, 1955.
- ^ S. R. Cooper, in Organic Syntheses Collective Volume 3, p 761, Wiley, New York, 1955.
- ^ S. Y. Dike, J. R. Merchant, N. Y. Sapre, Tetrahedron, 47, 4775 (1991)
- ^ B. S. Furnell et al., Vogel's Textbook of Practical Organic Chemistry, 5th edition, Longman/Wiley, New York, 1989.
- ^ E. Bauml, K. Tschemschlok, R. Pock, H. Mayr, Tetrahedron Letters, 29, 6925 (1988)
- ^ S. Kim, Y. J. Kim, K. H. Ahn, Tetrahedron Letters, 24, 3369 (1983).
- ^ H. O. House, D. S. Crumrine, A. Y. Teranishi, H. D. Olmstead, Journal of the American Chemical Society, 95, 3310 (1973)
- N. N. Greenwood, A. Earnshaw, Chemistry of the Elements, 2nd ed., Butterworth-Heinemann, Oxford, UK, 1997.
- Handbook of Chemistry and Physics, 71st edition, CRC Press, Ann Arbor, Michigan, 1990.
- The Merck Index, 7th edition, Merck & Co, Rahway, New Jersey, USA, 1960.
- D. Nicholls, Complexes and First-Row Transition Elements, Macmillan Press, London, 1973.
- A. F. Wells, 'Structural Inorganic Chemistry, 5th ed., Oxford University Press, Oxford, UK, 1984.
- J. March, Advanced Organic Chemistry, 4th ed., p. 723, Wiley, New York, 1992.
- G. J. McGarvey, in Handbook of Reagents for Organic Synthesis, Volume 1: Reagents, Auxiliaries and Catalysts for C-C Bond Formation, (R. M. Coates, S. E. Denmark, eds.), pp. 220–3, Wiley, New York, 1999.
外部連結[編輯]
- 氯化鋅的分級和應用 (頁面存檔備份,存於網際網路檔案館)
- PubChem ZnCl2 摘要 (頁面存檔備份,存於網際網路檔案館).
- 英文 MSDS 數據表 (頁面存檔備份,存於網際網路檔案館).
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||