ROC曲線
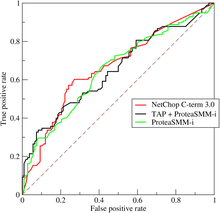
在訊號檢測理論中,接收者操作特徵曲線,或者叫ROC曲線(英語:Receiver operating characteristic curve),是一種坐標圖式的分析工具,用於選擇最佳的訊號偵測模型、捨棄次佳的模型或者在同一模型中設置最佳閾值。
在做決策時,ROC分析能不受成本/效益的影響,給出客觀中立的建議。
ROC曲線首先是由二戰中的電子工程師和雷達工程師發明的,用來偵測戰場上的敵軍載具(飛機、船艦),也就是訊號檢測理論。之後很快就被引入了心理學來進行訊號的知覺檢測。數十年來,ROC分析被用於醫學、無線電、生物學、犯罪心理學領域中,而且最近在機器學習(machine learning)和數據探勘(data mining)領域也得到了很好的發展。
基本概念
[編輯]
|
| Source: Fawcett (2006). |
分類模型(又稱分類器,或診斷)是將一個實例對映到一個特定類的過程。ROC分析的是二元分類模型,也就是輸出結果只有兩種類別的模型,例如:(陽性/陰性)(有病/沒病)(垃圾郵件/非垃圾郵件)(敵軍/非敵軍)。
當訊號偵測(或變量測量)的結果是一個連續值時,類與類的邊界必須用一個閾值(英語:threshold)來界定。舉例來說,用血壓值來檢測一個人是否有高血壓,測出的血壓值是連續的實數(從0~200都有可能),以收縮壓140/舒張壓90為閾值,閾值以上便診斷為有高血壓,閾值未滿者診斷為無高血壓。二元分類模型的個案預測有四種結局:
- 真陽性(TP):診斷為有,實際上也有高血壓。
- 偽陽性(FP):診斷為有,實際卻沒有高血壓。
- 真陰性(TN):診斷為沒有,實際上也沒有高血壓。
- 偽陰性(FN):診斷為沒有,實際卻有高血壓。
這四種結局可以畫成2 × 2的混淆矩陣:
| 真實值 | 總 數 | |||
|---|---|---|---|---|
| p | n | |||
| 預 測 輸 出 |
p' | 真陽性 (TP) |
偽陽性 (FP) |
P' |
| n' | 偽陰性 (FN) |
真陰性 (TN) |
N' | |
| 總數 | P | N | ||
ROC空間
[編輯]ROC空間將偽陽性率(FPR)定義為 X 軸,真陽性率(TPR)定義為 Y 軸。
- TPR:在所有實際為陽性的樣本中,被正確地判斷為陽性之比率。
- FPR:在所有實際為陰性的樣本中,被錯誤地判斷為陽性之比率。
給定一個二元分類模型和它的閾值,就能從所有樣本的(陽性/陰性)真實值和預測值計算出一個 (X=FPR, Y=TPR) 座標點。 在這條線的以上的點代表了一個好的分類結果(勝過隨機分類),而在這條線以下的點代表了差的分類結果(劣於隨機分類)。
完美的預測是一個在左上角的點,在ROC空間座標 (0,1)點,X=0 代表着沒有偽陽性,Y=1 代表着沒有偽陰性(所有的陽性都是真陽性);也就是說,不管分類器輸出結果是陽性或陰性,都是100%正確。一個隨機的預測會得到位於從 (0, 0) 到 (1, 1) 對角線(也叫無辨識率線)上的一個點;最直觀的隨機預測的例子就是拋硬幣。
讓我們來看在實際有100個陽性和100個陰性的案例時,四種預測方法(可能是四種分類器,或是同一分類器的四種閾值設置)的結果差異:
| A | B | C | C' | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
|
|
|
| ||||||||||||||||||||||||||||||||||||
| TPR = 0.63 | TPR = 0.77 | TPR = 0.24 | TPR = 0.76 | ||||||||||||||||||||||||||||||||||||
| FPR = 0.28 | FPR = 0.77 | FPR = 0.88 | FPR = 0.12 | ||||||||||||||||||||||||||||||||||||
| ACC = 0.675 | ACC = 0.500 | ACC = 0.180 | ACC = 0.820 |
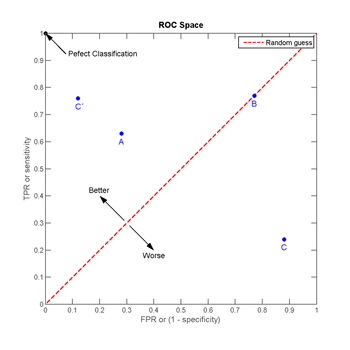
將這4種結果畫在ROC空間裏:
- 點與隨機猜測線的距離,是預測力的指標:離左上角越近的點預測(診斷)準確率越高。離右下角越近的點,預測越不準。
- 在A、B、C三者當中,最好的結果是A方法。
- B方法的結果位於隨機猜測線(對角線)上,在例子中我們可以看到B的準確度(ACC,定義見前面表格)是50%。
- C雖然預測準確度最差,甚至劣於隨機分類,也就是低於0.5(低於對角線)。然而,當將C以 (0.5, 0.5) 為中點作一個鏡像後,C'的結果甚至要比A還要好。這個作鏡像的方法,簡單說,不管C(或任何ROC點低於對角線的情況)預測了什麼,就做相反的結論。
ROC曲線
[編輯]
上述ROC空間裏的單點,是給定分類模型且給定閾值後得出的。但同一個二元分類模型的閾值可能設置為高或低,每種閾值的設置會得出不同的FPR和TPR。
- 將同一模型每個閾值 的 (FPR, TPR) 座標都畫在ROC空間裏,就成為特定模型的ROC曲線。
例如右圖,人體的血液蛋白濃度是呈正態分佈的連續變量,病人的分佈是紅色,平均值為A g/dL,健康人的分佈是藍色,平均值是C g/dL。健康檢查會測量血液樣本中的某種蛋白質濃度,達到某個值(閾值,threshold)以上診斷為有疾病徵兆。研究者可以調整閾值的高低(將左上圖的B垂直線往左或右移動),便會得出不同的偽陽性率與真陽性率,總之即得出不同的預測準確率。
1. 由於每個不同的分類器(診斷工具、偵測工具)有各自的測量標準和測量值的單位(標示為:「健康人-病人分佈圖」的橫軸),所以不同分類器的「健康人-病人分佈圖」都長得不一樣。
2. 比較不同分類器時,ROC曲線的實際形狀,便視兩個實際分佈的重疊範圍而定,沒有規律可循。
3. 但在同一個分類器之內,閾值的不同設置對ROC曲線的影響,仍有一些規律可循:
- 當閾值設置為最高時,亦即所有樣本都被預測為陰性,沒有樣本被預測為陽性,此時在偽陽性率 FPR = FP / ( FP + TN ) 算式中的 FP = 0,所以 FPR = 0%。同時在真陽性率(TPR)算式中, TPR = TP / ( TP + FN ) 算式中的 TP = 0,所以 TPR = 0%
- → 當閾值設置為最高時,必得出ROC座標系左下角的點 (0, 0)。
- 當閾值設置為最低時,亦即所有樣本都被預測為陽性,沒有樣本被預測為陰性,此時在偽陽性率FPR = FP / ( FP + TN ) 算式中的 TN = 0,所以 FPR = 100%。同時在真陽性率 TPR = TP / ( TP + FN ) 算式中的 FN = 0,所以 TPR=100%
- → 當閾值設置為最低時,必得出ROC座標系右上角的點 (1, 1)。
- 因為TP、FP、TN、FN都是累積次數,TN和FN隨着閾值調低而減少(或持平),TP和FP隨着閾值調低而增加(或持平),所以FPR和TPR皆必隨着閾值調低而增加(或持平)。
- → 隨着閾值調低,ROC點 往右上(或右/或上)移動,或不動;但絕不會往左下(或左/或下)移動。
曲線下面積(AUC)
[編輯]
在比較不同的分類模型時,可以將每個模型的ROC曲線都畫出來,比較曲線下面積做為模型優劣的指標。
意義
[編輯]ROC曲線下方的面積(英語:Area under the Curve of ROC (AUC ROC)),其意義是:
- 因為是在1x1的方格裏求面積,AUC必在0~1之間。
- 假設閾值以上是陽性,以下是陰性;
- 若隨機抽取一個陽性樣本和一個陰性樣本,分類器正確判斷陽性樣本的值高於陰性樣本之概率 [1]。
- 簡單說:AUC值越大的分類器,正確率越高。
從AUC判斷分類器(預測模型)優劣的標準:
- AUC = 1,是完美分類器,採用這個預測模型時,存在至少一個閾值能得出完美預測。絕大多數預測的場合,不存在完美分類器。
- 0.5 < AUC < 1,優於隨機猜測。這個分類器(模型)妥善設置閾值的話,能有預測價值。
- AUC = 0.5,跟隨機猜測一樣(例:丟銅板),模型沒有預測價值。
- AUC < 0.5,比隨機猜測還差;但只要總是反預測而行,就優於隨機猜測。
計算
[編輯]AUC的計算有兩種方式,都是以逼近法求近似值。
梯形法
[編輯]梯形法(英語:trapezoid method):簡單地將每個相鄰的點以直線連接,計算連線下方的總面積。因為每一線段下方都是一個梯形,所以叫梯形法。
- 優點:簡單,所以常用。
- 缺點:傾向於低估AUC。
ROC AUCH法
[編輯]潛在問題
[編輯]AUC of ROC是機器學習的社群最常使用來比較不同模型優劣的方法[2] 。然而近來這個做法開始受到質疑,因為有些機器學習的研究指出,AUC的雜訊太多,並且很常求不出可信又有效的AUC值(此時便不能保證AUC傳達本節開頭所述之意義),使得AUC在模型比較時產生的問題比解釋的問題更多[3][4][5] 。
分析軟件
[編輯]所有常用於統計分析的軟件(例:SPSS、SAS、SYSTAT、S-Plus、ROCKIT、RscorePlus)都有依據不同閾值自動計算真陽性和偽陽性比率、並依此繪製ROC曲線的功能。
離散分類器(英語:discrete,或稱「間斷分類器」),如決策樹,產生的是離散的數值或者一個二元標籤。應用到實例中,這樣的分類器最後只會在ROC空間產生單一的點。而一些其他的分類器,如樸素貝葉斯分類器,邏輯斯諦迴歸或者類神經網絡,產生的是實例屬於某一類的可能性,對於這些方法,一個閾值就決定了ROC空間中點的位置。舉例來說,如果可能值低於或者等於0.8這個閾值就將其認為是陽性的類,而其他的值被認為是陰性類。這樣就可以通過畫每一個閾值的ROC點來生成一個生成一條曲線。MedCalc是較好的ROC曲線分析軟件。
參考文獻
[編輯]參照
[編輯]- ^ Fawcett, Tom (2006); An introduction to ROC analysis, Pattern Recognition Letters, 27, 861–874.
- ^ Hanley, James A.; McNeil, Barbara J. A method of comparing the areas under receiver operating characteristic curves derived from the same cases. Radiology. 1983-09-01, 148 (3): 839–843 [2008-12-03]. PMID 6878708. (原始內容存檔於2008-09-05).
- ^ Hanczar, Blaise; Hua, Jianping; Sima, Chao; Weinstein, John; Bittner, Michael; and Dougherty, Edward R. (2010); Small-sample precision of ROC-related estimates, Bioinformatics 26 (6): 822–830
- ^ Lobo, Jorge M.; Jiménez-Valverde, Alberto; and Real, Raimundo (2008), AUC: a misleading measure of the performance of predictive distribution models, Global Ecology and Biogeography, 17: 145–151
- ^ Hand, David J. (2009); Measuring classifier performance: A coherent alternative to the area under the ROC curve, Machine Learning, 77: 103–123
來源
[編輯]- Zou, K.H., O'Malley, A.J., Mauri, L. (2007). Receiver-operating characteristic analysis for evaluating diagnostic tests and predictive models. Circulation, 6;115(5):654–7.
- X. H., Zhou. Statistical Methods in Diagnostic Medicine. Wiley & Sons. 2002. ISBN 9780471347729.
- Lasko, T.A., J.G. Bhagwat, K.H. Zou and Ohno-Machado, L. (2005). The use of receiver operating characteristic curves in biomedical informatics. Journal of Biomedical Informatics, 38(5):404–415.
- Balakrishnan, N., (1991) Handbook of the Logistic Distribution, Marcel Dekker, Inc., ISBN 978-0824785871.
- Gonen M., (2007) Analyzing Receiver Operating Characteristic Curves Using SAS, SAS Press, ISBN 978-1-59994-298-1.
- Green, W.H., (2003) Econometric Analysis, fifth edition, Prentice Hall, ISBN 0-13-066189-9.
- Heagerty, P.J., Lumley, T., Pepe, M. S. (2000) Time-dependent ROC Curves for Censored Survival Data and a Diagnostic Marker Biometrics, 56:337–344
- Hosmer, D.W. and Lemeshow, S., (2000) Applied Logistic Regression, 2nd ed., New York; Chichester, Wiley, ISBN 0-471-35632-8.
- Brown, C.D., and Davis, H.T. (2006) Receiver operating characteristic curves and related decision measures: a tutorial, Chemometrics and Intelligent Laboratory Systems, 80:24–38
- Mason, S.J. and Graham, N.E. (2002) Areas beneath the relative operating characteristics (ROC) and relative operating levels (ROL) curves: Statistical significance and interpretation. Q.J.R. Meteorol. Soc., 128:2145–2166.
- Pepe, M.S. (2003). The statistical evaluation of medical tests for classification and prediction. Oxford. ISBN 0198565828.
- Carsten, S. Wesseling, S., Schink, T., and Jung, K. (2003) Comparison of Eight Computer Programs for Receiver-Operating Characteristic Analysis. Clinical Chemistry, 49:433–439
- Swets, J.A. (1995). Signal detection theory and ROC analysis in psychology and diagnostics: Collected papers. Lawrence Erlbaum Associates.
- Swets, J.A., Dawes, R., and Monahan, J. (2000) Better Decisions through Science. Scientific American, October, pages 82–87.
外部連結
[編輯]- An introduction to ROC analysis
- A more thorough treatment of ROC curves and signal detection theory
- Tom Fawcett's ROC Convex Hull: tutorial, program and papers(頁面存檔備份,存於互聯網檔案館)
- Peter Flach's tutorial on ROC analysis in machine learning
- The magnificent ROC(頁面存檔備份,存於互聯網檔案館) — An explanation and interactive demonstration of the connection of ROCs to archetypal bi-normal test result plots





