鋁
鋁因其低密度以及耐腐蝕(由於鈍化現象)而受到重視。其合金根據工藝的不同性質差異很大,利用鋁及其合金製造的結構件不僅在航空航天工業中非常關鍵,在交通和結構材料領域也非常重要。最有用的鋁化合物是它的氧化物和硫酸鹽。
儘管鋁在環境中廣泛存在,但沒有一種已知生命形式需要鋁元素。
物理性質[編輯]
鋁是輕金屬,密度為2.70 g/cm3,僅是鋼的三分之一左右。使鋁製零件通過它們的輕盈易於識別。[7]與大多數金屬相比,鋁的密度低是因為它的原子核要輕得多,而晶胞大小的差異並不能彌補這種差異。比鋁的密度低的金屬只有反應性太高,不能用作結構的鹼金屬和鹼土金屬(鈹和鎂除外,但鈹有劇毒)。[8]鋁不像鋼那樣堅固和堅硬,但在航空航天工業等應用中,低密度彌補了這一點。[9]純鋁較軟,在300℃左右失去抗張強度,熔點660.4度。經處理過的鋁合金較堅韌、易延展。有著金屬光澤,光滑時表面銀白而發亮,粗糙時呈暗灰色。無磁性且不易點燃。反射可見光能力強(約92%),反射中遠紅外線可達98%。純鋁相當軟,缺乏強度。在大多數應用中,都會使用各種鋁合金,因為它們具有更高的強度和硬度。[10]純鋁的屈服為7~11MPa,而鋁合金可達200~600MPa。[11]鋁是有延展性的,伸長率為50-70%,[12]容易拉拔和擠型。[13]它也很容易被機械加工和鑄造。[13]
鋁有良好的導電導熱性(都為銅的59%),而遠輕於銅。[14]鋁可以在低於1.2K 的溫度和磁通量大於100高斯下超導。[15]它是順磁性的,因此基本上不受靜磁場的影響。[16]然而,高導電性意味著它通過渦電流的感應,受到交變磁場的強烈影響。[17]
電子層[編輯]
鋁原子有13個電子,電子組態為 [Ne] 3s2 3p1,[18]比穩定的惰性氣體氖多出三個電子。因此,鋁的第一、第二和第三電離能的總和遠低於第四電離能。[19]這種電子組態和其它硼族元素類似。在許多化學反應中,鋁可以相對容易地釋放其最外層的三個電子(見下)。鋁的電負性為1.61(鮑林標度)。[20]
一個自由鋁原子的原子半徑為143 pm。[21]當三個價電子被移除時,Al3+的離子半徑縮小到 39 pm(四配位)或 53.5 pm(六配位)。[21]在標準情況下,鋁原子以面心立方晶系排列,由原子最外層電子提供的金屬鍵結合,因此鋁是一種金屬。[22]許多金屬都有這種晶系,例如鉛和銅。鋁的晶胞大小與其他金屬相當。[22]然而,其它硼族元素都不是這種晶系的。硼的電離能太高而無法金屬化,鉈具有六方最密堆積結構,而鎵和銦具有不是最密堆積的不尋常結構。鋁原子可用於形成金屬鍵的少量電子可能是它柔軟、熔點低和電阻率低的原因。[23]
同位素[編輯]
在所有鋁同位素中,只有27
Al
是穩定的。這在原子序是奇數的元素中很常見。[a]它是唯一一種原生鋁同位素,也就是從地球形成到現在一直存在的同位素。地球上幾乎所有的鋁都是這種同位素,使得鋁是一種單一天然同位素元素。鋁的標準原子量幾乎和鋁-27的質量一樣。這使得鋁在核磁共振(NMR)中非常有用,因為鋁-27有很高的 NMR靈敏度。[25]鋁的標準原子量相較於其它金屬很低,[b]這對元素的屬性有影響。
剩下的鋁同位素都有放射性。其中最穩定的是26Al:雖然它與穩定的27Al一起存在於形成太陽系的星際介質中,也是可以通過恆星核合成產生的,但它的半衰期只有717000年,因此自行星形成以來,鋁-26就全部衰變了。[27]然而,由於宇宙射線質子轟擊大氣層中的氬氣引起散裂,會產生微量的26Al。26Al 和10Be的比例可用於放射性定年法,適用於105至106年的尺度(運輸、沉積、沉積物儲存、埋藏時間和侵蝕)。[28]大多數隕石學家認為,26Al衰變釋放的能量是一些小行星在45.5億年前形成後熔化和分異的原因。[29]
剩下的鋁同位素的質量數介於22到43之間,半衰期都小於一小時。鋁還有三個已知的同核異構物,半衰期都小於一分鐘。[24]
化學性質[編輯]
鋁結合了過渡金屬和後過渡金屬的特性。由於它幾乎沒有可用於金屬鍵的電子,就像其較重的硼族元素一樣,它具有後過渡金屬的物理性質,原子間的距離長於預期。[23]此外,由於 Al3+是一種小而高度帶電的陽離子,它具有很強的極化性。這使得鋁化合物的化學鍵趨向於共價鍵。[30]這種性質和鈹(Be2+)類似,它們存在對角線關係。[31]
鋁的原子實的電子結構是惰性氣體核心,而較重的同族元素鎵、銦、鉈和鉨已經有充滿的d殼層,有些還有f殼層。因此,鋁的內部電子幾乎完全屏蔽了價電子,這與較重的同族元素不同。鋁是整個硼族元素中電正性最高的元素,它的氫氧化物也比氫氧化鎵的鹼性更強。[30][c]鋁與同族的類金屬硼也有細微的相似之處:AlX3和 BX3是等電子體(它們具有相同的價電子結構),並且兩者都表現為路易斯酸,且很容易形成加合物。[32]
鋁容易與氧反應,暴露於空氣中會在其表面生成緻密的氧化鋁 Al2O3(此過程為鈍化)薄層(室溫下厚度為5奈米)[33],有效的防止其繼續氧化,或是與水和稀酸反應。[30][34]由於鋁具有一般的耐腐蝕性,因此它是為數不多的以細粉形式保留銀色的金屬之一,使其成為銀色顏料的重要組成部分。[35]在常溫下,鋁在強氧化性酸中被鈍化,不與它們反應,所以濃硝酸、濃硫酸和一些有機酸是用鋁罐存放的。[36]
在熱濃鹽酸中,鋁與水反應放出氫氣,並在氫氧化鈉或氫氧化鉀水溶液中形成鋁酸鹽——在這些條件下保護性鈍化可以忽略不計。[37]王水也會溶解鋁。[36]鋁會被溶解的氯化物腐蝕,例如常見的氯化鈉,這就是為什麼家用管道從不由鋁製成的原因。[37]鋁的氧化層會因為汞的汞齊化,或是接觸電正性元素的鹽而被破壞。[30]因此,由於伽凡尼電池與合金化銅的反應,最強的鋁合金的耐腐蝕性較差,[11]鋁的耐腐蝕性也會因含水鹽的存在而大大降低,尤其是在有不同金屬存在的情況下。[23]
鋁和大部分非金屬加熱時反應,形成像是氮化鋁(AlN)、硫化鋁(Al2S3)和鹵化鋁(AlX3)的化合物。鋁也可以和幾乎整個周期表的元素混合,形成金屬間化合物。[30]
無機化合物[編輯]
大部分的鋁化合物中,鋁的氧化態為 +3。Al3+的配位數通常是4或6。幾乎所有的鋁(III)化合物都是無色的。[30]
在水溶液中,Al3+以六水合物[Al(H2O)6]3+的形式存在,Ka約為10−5。[25]這種溶液是酸性的,因為這種陽離子可以作為質子供體並逐漸水解,直到形成氫氧化鋁(Al(OH)3)沉澱。
氫氧化鋁可溶於酸和鹼,分別形成鋁鹽和鋁酸鹽,也與酸性和鹼性氧化物融合。[30]因此,Al(OH)3是兩性的,為弱鹼性陽離子的特徵。弱鹼性陽離子會形成不溶性氫氧化物,其水合物也可以提供質子。這樣的一個影響是鋁的弱酸鹽在水中會水解成水合氫氧化物和相應的非金屬氫化物。舉個例子,硫化鋁水解形成硫化氫。對於鋁的強酸鹽,如鹵化鋁、硝酸鋁和硫酸鋁,只會發生不完全水解。由於類似的原因,無水鋁化合物不能由加熱它們的「水合物」而成。水合氯化鋁的結構不是 AlCl3·6H2O ,而是[Al(H2O)6]Cl3,且 Al–O 鍵是如此的強,以至於加熱不足以破壞它們並形成 Al-Cl 鍵:[30]
- 2[Al(H2O)6]Cl3 Al2O3 + 6 HCl + 9 H2O
鋁的四種三鹵化物都是已知的。不像更重的三種鹵化物,氟化鋁(AlF3)具有六配位鋁,這解釋了它的不揮發性、不溶性以及高生成熱。每個鋁原子都被六個氟原子包圍,形成扭曲八面體結構,每個氟原子則橋接在兩個八面體的角之間。這些{AlF6}單元也存在於三元氟化物中,例如冰晶石Na3AlF6。AlF3的熔點是1,290 °C(2,354 °F),可以由氧化鋁和氟化氫在700 °C(1,300 °F)下反應而成。[38]
鋁在重鹵化物中的配位數較少。這些鹵化物是二聚體或多聚體,含有四配位鋁中心。氯化鋁(AlCl3)在熔點192.4 °C(378 °F)以下時為層狀聚合物結構,在液態為 Al2Cl6二聚體。在高溫下,它會分解成AlCl3單體,結構類似於BCl3。溴化鋁和碘化鋁在固態、液態和氣態都是Al2X6二聚體,因此在改變相態時沒有顯著的變化。[38]它們都可以由鋁和鹵素直接反應而成。三鹵化鋁可以形成許多加合物或配合物。它們是路易斯酸,使它們可用作傅-克反應的催化劑。三氯化鋁具有涉及該反應的主要工業用途,例如製造蒽醌和苯乙烯。它也經常用作其它鋁化合物的前體和將非金屬氟化物轉化為相應氯化物的試劑(轉移鹵化反應)。[38]
鋁形成一種穩定的氧化物——氧化鋁,化學式Al2O3。[39]它在自然界中以剛玉(α-氧化鋁)的形式存在。[40]γ-氧化鋁也是存在的。[25]氧化鋁的結晶——剛玉是非常硬的(莫氏硬度9),有著高熔點2,045 °C(3,713 °F),極低的揮發性,化學惰性,也是良好的電絕緣體。它常用於磨料(如牙膏)、耐火材料和陶瓷器,以及作為電解生產鋁金屬的起始材料。藍寶石和紅寶石是不純的剛玉,裡面有其它金屬。[25]兩種鹼式氧化鋁,化學式 AlO(OH)的晶體分別為勃姆石和硬水鋁石。氫氧化鋁有三種主要的礦物:三羥鋁石、三水鋁石和斜三水鋁石,它們的晶體結構不同。[25]
鋁有三種標準情況下穩定的硫屬化物,分別為硫化鋁(Al2S3)、硒化鋁(Al2Se3)和碲化鋁(Al2Te3)。它們三個都可以由鋁的硫屬元素在1,000 °C(1,800 °F)下反應而成。它們會迅速水解,形成氫氧化鋁和對應的氧族元素氫化物。[41]
鋁有四種氮族元素化物——氮化鋁(AlN)、磷化鋁(AlP)、砷化鋁(AlAs)和銻化鋁(AlSb)。它們都是三五半導體,和矽和鍺是等電子體,除了 AlN 外,所有這些都具有閃鋅礦結構。它們都可以由在高溫(可能需要高壓)下組成元素直接反應而成。[41]
鋁和其它金屬(大多數鹼金屬和硼族元素除外)形成的合金和150種金屬互化物都是已知的。製備這些合金和金屬互化物的方法包括按一定比例將金屬混合加熱,然後逐漸冷卻和退火。它們中的鍵主要是金屬鍵,晶體結構主要取決於堆積效率。[42]
鋁也有一些低氧化態的化合物。一些鋁(I)化合物是已知的:AlF、AlCl、AlBr和 AlI 存在於氣相。它們可以由三鹵化鋁和金屬鋁加熱或在低溫下反應而成。[38]一種穩定的一碘化鋁衍生物是它和三乙胺形成的加合物,化學式Al4I4(NEt3)4。Al2O 和Al2S 也存在,不過非常不穩定。[43]在鋁金屬與氧化劑的反應中會觀察到非常簡單的鋁(II)化合物。例如,一氧化鋁,化學式 AlO,已經在爆炸中[44]和恆星吸收光譜中檢測到。[45]研究較徹底的鋁(II)化合物的通式為 R4Al2,含有一根 Al–Al鍵,其中 R 是一個大的有機基團。[46]
有機鋁化合物和相關的氫化物[編輯]
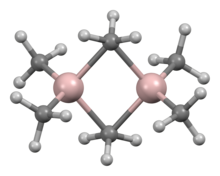
一系列實驗式 AlR3和AlR1.5Cl1.5的化合物都是已知的。[47]三烷基/芳基鋁都有高反應性,揮發性,外觀為無色液體或低熔點固體。它們在空氣中自燃並與水發生反應,因此在處理它們時需要採取預防措施。不像對應的硼化合物,有機鋁化合物是二聚體。不過,如果 R基團是有支鏈的(例如Pri、Bui和 Me3CCH2),它就可能以單體存在。舉個例子,三異丁基鋁以單體和二聚體的混合物的形式存在。[48][49]這些二聚體,像是三甲基鋁(Al2Me6),含有四面體型的鋁中心,在兩個鋁原子之間有兩個橋接烷基。它們硬酸,會和配體反應,形成加合物。在工業上,它們主要用於烯烴插入反應。一些雜環和簇合的有機鋁化合物也是已知的,其中含有Al–N鍵。[48]
工業上最重要的鋁氫化物是氫化鋁鋰(LiAlH4),在有機化學中用作還原劑。它可以由氫化鋰和氯化鋁反應而成。[50]最簡單的鋁氫化物是氫化鋁,又稱鋁烷,比較不重要。它是一種聚合物,化學式 (AlH3)n。作為對比,最簡單的硼烷是乙硼烷 (BH3)2。[50]
分布[編輯]
太空[編輯]
鋁在太陽系的豐度是3.15 ppm。[51][d]它是宇宙中第12多的元素,也是奇原子序的元素中第三多的,僅次於氫和氮。[51]鋁唯一的穩定同位素27Al,是宇宙中第18多的核素。它幾乎是在大質量恆星中的碳融合之後產生的,這些恆星後來將成為II型超新星。碳融合會產生26Mg,然後這種同位素吸收一個質子或中子,形成鋁-27。較少的27Al則是在氫燃燒中,26Mg捕獲一個質子而成的。[52]幾乎所有的鋁都是27Al,而當時存在於太陽系的26Al 的豐度為27Al的 0.005%。不過,728,000年的半衰期無法使鋁-26在今天仍然存在,因此26Al滅絕了。[52]不像27Al,氫燃燒是26Al的主要來源,由25Mg 和自由質子聚合而成。不過,今天仍然存在的微量的26Al是星際物質中最常見的伽馬射線發射體。[52]如果那時的26Al仍然存在,銀河系的伽馬射線圖將會更亮。[52]
地球[編輯]

整個地球由1.59%的鋁組成(質量計,排在第七位)[53]地殼中的鋁則更加豐富,因為它易於形成氧化物,並被束縛在岩石而留在地殼中,而活性較低的金屬沉入地核。[52]在地殼中,鋁是豐度最高的金屬,占了 8.23%(質量計),[12],也是僅次於氧和矽,第三多的元素。[54]地殼中的大量矽酸鹽含有鋁。[55]相較之下,地球地函只含2.38%的鋁(質量計)。[56]鋁也存在於海水中,濃度2μg/kg。[12]
由於鋁對氧的高親和性,它幾乎不以游離態存在。鋁通常以氧化物和矽酸鹽的形式出現。長石,地殼中最常見的一類礦物,是由鋁矽酸鹽組成的。鋁也存在於綠柱石、冰晶石、石榴石、尖晶石和綠松石中。[57]Al2O3中的雜質鉻和鐵會分別形成紅寶石和藍寶石。[58]游離鋁金屬極度稀有,並且只能在低氧逸度環境中作為次要相態被發現,例如某些火山的內部。[59]在南海東北部大陸坡的冷泉中,已經發現了游離鋁。這些游離鋁可能是細菌還原Al(OH)4−的產物。[60]
儘管鋁是一種常見且廣泛使用的元素,但並非所有鋁礦都是經濟上可行的金屬鋁的來源。幾乎所有的金屬鋁都是從鋁礬土(AlOx(OH)3–2x)生產的。鋁礬土是熱帶氣候條件下低鐵和二氧化矽基岩的風化產物。[61]2017 年,大部分鋁礬土在澳洲、中國、幾內亞和印度開採。[62]
歷史[編輯]

鋁的歷史是從明礬的使用開始塑造的。古希臘歷史學家希羅多德對明礬的第一個書面記錄可以追溯到公元前5世紀。[63]古人曾將明礬用作媒染劑和用於城市防禦。[63]十字軍東征後,明礬是歐洲織物工業中不可或缺的商品,[64]也成為國際貿易的對象。[65]直到15 世紀中葉,礬才從地中海東部進口到歐洲。[66]
當時明礬的性質仍然未知。大約在1530年,瑞士醫生帕拉塞爾蘇斯認為明礬是礬土的鹽。[67]1595年,德國醫生和化學家安德烈亞斯·利巴菲烏斯用實驗證實了這一點。[68]1722年,德國化學家Friedrich Hoffmann宣布了他的意見,即明礬的基礎是一種獨特的土。[69]1754年,德國化學家馬格拉夫通過在硫酸中煮沸粘土,然後加入鉀鹽合成了鋁土(氧化鋁)。[69]
相對於其他金屬,鋁的發現比較晚。生產金屬鋁的嘗試可以追溯到1760年。[70]1808年,漢弗里·戴維爵士首次使用了「aluminum」這個詞,[71]並開始嘗試生產鋁。1825年丹麥化學家漢斯·奧斯特成功用鉀汞齊從氯化鋁中還原出一塊看起來像錫的金屬塊,也就是鋁[72][73][74]:

他在1825年展示了他的結果並展示了新金屬的樣品。[75][76]1827年,弗里德里希·維勒重複了奧斯特的實驗,不過沒有得到任何鋁。[77](這種不一致的原因直到1921年才被發現。)[78]同年,他用金屬鉀還原熔融的無水氯化鋁得到較純的金屬鋁單質。[74]1845年,他能夠生產出小塊的金屬鋁,並描述了這種金屬的一些物理特性。[78]多年後,維勒被認為是鋁的發現者。[79]
由於取之不易,當時鋁的價格高於黃金。[77]1856 年,法國化學家德維爾(Henri Etienne Sainte-Claire Deville)及其同伴建立了鋁的第一個工業生產。[80]他發現到比鉀更方便也更便宜的鈉也可以還原氯化鋁。[81]即便如此,鋁的純度仍然不高,而且所生產的鋁的特性因樣品而異。[82]
1886年,查爾斯·馬丁·霍爾(Charles Martin Hall)和保羅·埃魯(Paul Héroult)各自獨立發現了電解制鋁法,後來這種方法被稱為霍爾-埃魯法[83]。這種方法把氧化鋁轉化成金屬鋁。在1889年,卡爾·約瑟夫·拜耳繼續最佳化了從鋁礬土中提取氧化鋁的過程,使得生產鋁的原料氧化鋁更加經濟易得。[84]迄今以拜耳法與霍爾-埃魯法聯用生產鋁的方法為大規模工業制鋁的主要手段。[85]
鋁的價格下降,之後在1890年代和20世紀初被廣泛用於珠寶、日常用品、眼鏡架、光學儀器、餐具和鋁箔中。鋁與其他金屬形成堅硬而輕的合金的能力為當時的其它金屬提供了多種用途。[86]在一戰期間,主要政府要求將大量的鋁用于堅硬而輕的機身;[87]到了二戰,主要政府對於鋁的這些需求更高。[88][89][90]
到了20世紀中葉,鋁已成為日常生活的一部分和家庭用品的重要組成部分。[91]1954年,鋁的產量超過了銅,[e]歷史上的總產量僅次於鐵,[94]成為產量最高的有色金屬。在這期間,鋁作為一種土木工程材料出現,在基礎建築和室內裝修中都有應用,[95]且越來越多地用於軍事工程,用於飛機和陸地裝甲車輛發動機。[96]第一個人造衛星於1957年發射,由兩個單獨的鋁半球連接在一起組成,隨後所有的太空飛行器都在某種程度上使用了鋁。[85]鋁罐於1956年發明,1958年用作飲料的容器。[97]

在20世紀期間,鋁的產量迅速上升:1900年世界鋁產量為6800公噸,1916年的年產量首次突破10萬噸,1941年突破100萬噸,1971年則突破1000萬噸。[92]1970年代,對鋁的需求增加使其成為交易商品。它於1978年進入倫敦金屬交易所,這是世界上最古老的工業金屬交易所。[85]之後鋁的產量持續增長:2013年,鋁的年產量突破5000萬噸。[92]
鋁的實際價格從1900年的每公噸14000美元下降到1948年的每公噸2340美元(以1998年美元計)。[92]技術進步和經濟規模降低了鋁的提取和加工成本。然而,開發低品位、質量較差的礦床的需求以及快速增加的投入成本(主要是能源)的使用增加了鋁的淨成本,[98]鋁的實際價格開始了1970年代隨著能源成本的上升而增長。[99]鋁的生產從工業化國家轉移到生產成本較低的國家。[100]由於技術進步、能源價格下降、美元匯率和氧化鋁的價格,20世紀後期鋁的生產成本發生了變化。[101]金磚國家在初級生產和初級消費中的總份額在2000年代大幅增長。[102]得益於豐富的資源、廉價的能源和政府的刺激,中國占了世界產量特別大的份額。[103]中國的消費份額也從1972年的2%增加到2010年的40%。[104]在美國、西歐和日本,大部分的鋁用於運輸、工程、建築和包裝。[105]
生產和細化[編輯]
鋁的生產從地下提取的鋁礬土開始。鋁礬土使用拜耳法加工並轉化為氧化鋁,然後使用霍爾-埃魯法加工,從而形成金屬鋁。
生產鋁是高度耗能的,因此鋁的生產商傾向於將冶煉廠設在電力充足且價格低廉的地方。[106]截至 2019 年,全球最大的鋁冶煉廠位於中國、印度、俄羅斯、加拿大和阿拉伯聯合大公國,[107]而中國是迄今為止最大的鋁生產國,占世界份額的 55%。
根據國際資源委員會的社會金屬庫存報告,全球平均每人在社會中使用的鋁(即汽車、建築、電子產品等)為80公斤(180磅)。[108]
拜耳法[編輯]
鋁礬土通過拜耳法轉化成氧化鋁。將鋁礬土混合均勻,然後研磨。將得到的泥漿與熱氫氧化鈉溶液混合,然後在遠高於大氣壓的壓力下的反應釜中處理混合物。將氫氧化鋁溶解在鋁礬土中,同時將雜質轉化為相對不溶的化合物:[109]
在該反應之後,這些泥漿處於高於其常壓沸點的溫度。隨著壓力的降低,它通過去除蒸汽來冷卻。鋁礬土的殘留物將從溶液中分離並丟棄。這時,溶液中不含固體,之後以小的氫氧化鋁晶體為晶種,使[Al(OH)4]−離子分解成氫氧化鋁。在大約一半的鋁沉澱後,混合物被送到分級器。之後,收集小的氫氧化鋁晶體作為晶種,而粗的氫氧化鋁顆粒通過加熱轉化為氧化鋁。多餘的溶液將通過蒸發去除,純化(如果需要),並循環使用。[109]
霍爾-埃魯法[編輯]

在把鋁礬土轉化成氧化鋁之後,可以通過霍爾-埃魯法變成金屬鋁。氧化鋁、冰晶石(Na3AlF6)和氟化鈣在950和980 °C(1,740和1,800 °F)的熔融混合物中電解,形成金屬鋁。液態鋁金屬會沉到溶液底部並被取出,通常澆鑄成稱為鋁坯的大塊進一步加工。[36]
電解槽的陽極由碳——最耐氟化物腐蝕的材料製成,並在過程中或過程前烘烤。前者(過程中烘烤)也稱為 Söderberg 陽極,功率效率較低,並且在烘烤過程中釋放的煙霧收集起來成本很高,這就是為什麼它們被後者取代的原因,儘管它們節省了預前烘烤陰極的電力、能源和勞動力。用於陽極的碳最好是純的,這樣鋁和電解質都不會被灰污染。儘管碳具有抗腐蝕能力,但每生產一千克鋁仍以 0.4-0.5 千克的速度消耗碳。電解槽的陰極則是由無煙煤製成。它們不需要高純度,因為雜質的浸出非常緩慢。陰極的消耗率為每千克鋁 0.02-0.04 千克。電解槽的電池通常在陰極失效後 2-6 年後終止。[36]
霍爾-埃魯法可以生產純度超過 99%的鋁。繼續純化可以通過Hoopes法實現。該過程涉及使用鈉、鋇和鋁的氟化物電解液電解熔融的鋁。在這個過程之後,鋁的純度達到 99.99%。[36][110]
電力約占鋁的生產成本的20%至40%,具體取決於冶煉廠的位置。鋁的生產消耗了美國大約5%的電力。[111]因此,人們研究了霍爾-埃魯法的替代方案,但沒有一個在經濟上可行。[36]
低溫電解法[編輯]
通過在電解槽內加入氯化鋁(AlCl3)和助熔劑氯酸鉀、氯化鈣、氯 化鈉及少量的氯化鋰,可以使之形成熔岩體系,讓在熔融態下本不導電的氯化鋁發生電解,實現較低溫度下的電解法冶煉鋁。該法也被視為替代電解氧化鋁潛在替代,因該法「耗電省,成本低,無環境污染。」
陽極反應式[編輯]
4AlCl4--2e-=2Al2Cl7-+Cl2↑
陰極反應式[編輯]
4Al2Cl7-+3e-=Al+7AlCl4-
資源回收[編輯]

資源回收金屬已成為鋁工業的一項重要任務。直到1960年代後期,回收利用一直是一項低調的活動。當時,鋁製飲料罐的使用量不斷增加,使公眾意識到了這一點。[112]回收涉及熔化廢料,這一過程僅需要用於從礦石中生產鋁的5%的能量,儘管很大一部分(高達15%的輸入材料)會作為灰狀氧化物浪費掉。[113]鋁堆熔爐產生的熔渣顯著減少,報告值低於 1%。[114]
來自原鋁生產和二次回收操作的浮渣仍然含有可工業提取的鋁。這個過程生產鋁坯以及高度複雜的廢料,並且浪費很難管理。它與水反應,釋放出混合氣體(包括氫氣、乙炔和氨),與空氣接觸時會自燃,[115]與潮濕空氣接觸會釋放大量氨氣。儘管存在這些問題,這些廢物仍被用作瀝青和混凝土的填充材料。[116]
應用[編輯]
金屬鋁[編輯]
鋁在 2016年的全球產量為 5880萬噸,僅次於鐵(12.31億噸)。[117][118]
鋁幾乎總是以合金的形式出現,這顯著改善了其機械性能,尤其是回火時。例如,常見的鋁箔和飲料罐都是含有92%~99%鋁的合金。[119]鋁主要和銅、鋅、鎂、錳和矽形成合金。[120]

鋁金屬的主要用途是:[121]
等)。
- 因為無毒(見下)、不易吸附和不易產生碎片,鋁也用於包裝(鋁罐、箔、框架等)。
- 當需要重量輕、耐腐蝕性或工程特性很重要的情況下,鋁也用於建築和施工(窗戶、門、建築電線、護套、屋頂等)。
- 鋁可用於與電力相關的用途(導體合金、電動機和發電機、變壓器、電容器等),因為它相對便宜、導電性高、具有足夠的機械強度和低密度、並且耐腐蝕。
- 從炊具到家具,很多家庭物品都是用鋁製成的。低密度、美觀、易於製造和耐用是鋁製物品使用的關鍵因素。
- 機械設備(加工設備、管道、工具)中也會使用鋁,因為它具有耐腐蝕性、不會自燃和足夠的機械強度。
- 鋁也用於製造可攜式電腦機箱。2018年,蘋果公司公開了使用使用過的飲料罐(UBC)材料來包裹其MacBook Air產品的電子元件。鋁可以回收利用,清潔的鋁具有剩餘的市場價值。[122]
鋁化合物[編輯]
大部分(約 90%)的氧化鋁會被轉化成金屬鋁。[109]作為一種非常硬的材料(莫氏硬度9),[123]氧化鋁被廣泛用作磨料,[124]且因為極度的化學惰性,被用於高反應性環境中,像是高壓鈉燈中。[125]氧化鋁也用作工業過程的催化劑,[109]例如催化克勞斯法(煉油廠中將硫化氫轉化為硫的反應)。[126][127]許多工業催化劑是由氧化鋁負擔的,這意味著昂貴的催化劑材料會分散在惰性氧化鋁的表面上。[128]氧化鋁的另一個主要用途是作為乾燥劑或吸收劑。[109][129]

鋁的各種硫酸鹽具有工業和商業應用。硫酸鋁的水合物的年生產規模達到了數百萬噸。[130]其中,約三分之二的硫酸鋁用於水處理。[130]硫酸鋁的另一個主要應用是造紙。[130]它還用作媒染劑,用於染色、酸洗種子、為礦物油除臭、鞣製皮革,以及生產其他鋁化合物。[130]兩種礬,銨明礬和明礬, 以前用於媒染和皮革鞣製,但隨著高純度硫酸鋁的出現,它們的使用量顯著下降。[130]無水的氯化鋁在化學和石化工業、染色工業以及合成各種無機和有機化合物中用作催化劑。[130]鋁酸鈉可用於水處理和水泥凝固的促進劑。[130]
許多鋁化合物都有應用,例如:
- 乙酸鋁的溶液是一類收斂劑。[131]
- 磷酸鋁可用於製造玻璃、陶瓷、木漿和紙製品、化妝品、油漆、油光漆和牙科水泥。[132]
- 氫氧化鋁是一種抗酸藥和媒染劑。它也用於水淨化、玻璃和陶瓷的製造以及織物的防水。[133][134]
- 氫化鋁鋰是一種強還原劑,用於有機化學。[135][136]
- 有機鋁化合物是一類路易斯酸和助催化劑。[137]
- 聚甲基鋁氧烷可用於生產乙烯基聚合物,例如聚乙烯。[138]
- 水合鋁離子(如水合硫酸鋁)用於對付魚類寄生蟲,如Gyrodactylus salaris。[139]
- 在許多疫苗中,某些鋁鹽作為免疫佐劑(免疫反應增強劑),使疫苗中的蛋白質發揮足夠的免疫刺激作用。[140]
對人體的影響[編輯]

儘管鋁廣泛存在於地殼,它沒有已知的生物作用。[36]在pH值 6-9(大多數天然水的pH值)時,鋁會以氫氧化物的形式從水中沉澱出來,因此無法使用。大多數具有這種行為的元素沒有生物作用,或是有毒。[142]硫酸鋁的LD50為6207 mg/kg(小鼠,口服),相當於一個70公斤(150磅)的人的半數致死量為435克,[36]儘管致死性和神經毒性的含義不同。[143]Andrási 等人發現,阿爾茨海默病症患者的屍檢與沒有阿爾茨海默症的受試者比較時,某些大腦區域的鋁含量「顯著更高」。[144]鋁會和草甘膦寫成螯合物。[145]
毒性[編輯]
美國衛生與公共服務部將鋁歸類為非致癌物質。[146][f]1988年發表的一篇評論說,幾乎沒有證據表明正常接觸鋁會對健康成人構成風險,[149]2014年的多元素毒理學審查則未能發現每公斤體重消耗量不超過40毫克/天的鋁的有害影響。[146]大多數消耗的鋁會留在糞便中,進入血液的小部分鋁大部分將通過尿液排出。[150]儘管如此,一些鋁確實可以通過血腦屏障,並優先留在阿爾茨海默病患者的大腦中。[151][152]1989年發表的證據似乎表明,對於阿爾茨海默病患者,鋁可能通過靜電與蛋白質交叉連結,從而調降顳上回中的基因。[153]
效果[編輯]
雖然很少見,但鋁會導致維生素D抗性的骨質軟化,促紅血球生成素抗性的小細胞性貧血和中樞神經系統改變。腎功能不全的人尤其處於危險之中。[146]長期攝入水合矽酸鋁(用於控制胃酸過多)可能會導致鋁與腸內容物結合,並增加其他金屬的排除,例如鐵或鋅。足夠高的鋁(>50克/天)會導致貧血。[146]
在1988年卡姆爾福德水污染事件期間,卡姆爾福德的人們的飲用水被硫酸鋁污染了幾個星期。2013年對該事件的最終報告得出結論,這不太可能導致長期的健康問題。[154]
鋁被懷疑是阿爾茨海默病的可能原因,[155]但四十多年來對此的研究發現,截至2018年[update],沒有很好的因果關係證據。[156][157]
在實驗室培養的人類乳腺癌細胞中,鋁會增加與雌激素相關的基因表達。[158]在非常高的劑量下,鋁與血腦屏障的功能改變有關。[159]一小部分的人[160]接觸鋁會過敏,並在接觸含鋁產品後出現發癢的紅疹、頭痛、肌肉疼痛、關節痛、記憶力差、失眠、抑鬱、哮喘、腸易激症候群或其他症狀。[161]
接觸鋁粉或鋁焊接的煙霧會導致肺纖維化。[162]細鋁粉會燃燒或爆炸,構成另一種工作場所的危險。[163][164]
接觸途徑[編輯]
食物是鋁的主要來源。飲用水比固體食物含有更多的鋁。[146]然而,食物中的鋁可能比從水中吸收的鋁更多。[165]人類口服鋁的主要來源包括食物(由於其用於食品添加劑、食品和飲料包裝以及炊具)、飲用水(由於其用於市政水處理)和含鋁藥物(特別是抗酸藥、抗潰瘍和緩衝阿司匹林製劑)。[166]歐洲人鋁的膳食暴露平均為 0.2–1.5 毫克/公斤/周,但可能高達 2.3 毫克/公斤/周。[146]較高的鋁暴露水平主要限於礦工、鋁生產工人和透析患者。[167]
抗酸藥、止汗劑、疫苗和化妝品的消費提供了可能的鋁接觸途徑。[168]食用含鋁的酸性食物或液體可增強鋁的吸收[169],而麥芽酚已被證明可以增加鋁在神經和骨組織中的積累。[170]
治療[編輯]
如果懷疑突然攝入大量鋁,唯一的治療方法是甲磺酸去鐵胺,可以通過螯合從體內清除鋁。[171][172]但是應謹慎使用,因為這不僅會降低鋁體含量,還會降低其他金屬(例如銅或鐵)的含量。[171]
對環境的影響[編輯]

礦區附近的鋁含量很高,少量的鋁則在燃煤發電廠或焚化爐中釋放到環境中。[173]空氣中的鋁通常會沉澱下來,或被雨水沖走,但小顆粒的鋁會長時間留在空氣中。[173]
酸性沉澱是從天然來源中調動鋁的主要自然因素[146],也是鋁對環境產生影響的主要原因。[174]然而,鹽水和淡水中鋁存在的主要因素是工業過程將鋁釋放到空氣中。[146]
當水呈酸性時,鋁會成為用鰓呼吸的動物(如魚)的毒劑,其中鋁可能會沉澱在鰓上,[175]這會導致血漿和血淋巴離子的損失,從而導致滲透調節失敗。[174]鋁的有機配合物可能很容易被吸收,並干擾哺乳動物和鳥類的新陳代謝,儘管這實際上很少發生。[174]
雖然鋁在pH值中性土壤中難溶並且對植物一般是無害的,但它在酸性土壤中是減緩植物生長的首要因素。在酸性土壤中,Al3+陽離子濃度會升高,並影響植物的根部生長和功能。[176][177][178][179]絕大多數酸性土壤中鋁(而不是氫)是飽和的。因此,土壤的酸度來源於鋁化合物的水解。[180]「修正石灰位」的概念[181]是用來定義土壤中鹼飽和的程度。在土壤測試實驗室中,這個概念成為了確定土壤的「石灰需求」[182]的測試程序的基礎。[183]小麥對鋁具有適應耐受性,會釋放有機化合物,與有害的鋁陽離子結合。高粱被認為具有相同的耐受機制。[184]
鋁在生產過程的每一步都對環境是挑戰。它的主要挑戰是溫室氣體排放。[167]這些氣體來自冶煉廠的電力消耗和加工副產品。其中,最持久的是來自冶煉過程的碳氟化合物。[167]它產生的二氧化硫是酸雨的主要前體之一。[167]
一份來自2001年的西班牙科學報告聲稱真菌白地黴會消耗光碟中的鋁。[185][186]其他報告都參考了該報告,並且沒有支持原始研究。更好的記錄表明,細菌銅綠假單胞菌和真菌枝孢菌通常在使用煤油燃料(不是航空汽油)的飛機油箱中檢測到。實驗室的培養物可以降解鋁。[187]然而,這些生命形式不會直接攻擊或消耗鋁;相反,金屬鋁會被微生物的廢物腐蝕。[188]
參見[編輯]
注釋[編輯]
- ^ 只有少數原子序是奇數的元素有超過兩個穩定同位素,而原子序為偶數的元素具有多種穩定同位素,錫(元素50)在所有元素中的穩定同位素數量最多,有十個。唯一的例外是鈹,它的原子序是偶數但只有一種穩定同位素。[24]參見奇數和偶數原子核來獲得更多詳情。
- ^ 大多數其它金屬具有更大的標準原子量:例如,鐵的原子量是55.8、銅63.5、鉛207.2。 [26]
- ^ 事實上,鋁的電正性、對氧的高親和力和高負值的標準電極電勢都與鈧、釔、鑭和錒相似,它們像鋁一樣在惰性氣體核心外具有三個價電子,顯示出連續的趨勢。然而,硼族元素的趨勢被鎵添加的 d殼層和由此產生的d區塊收縮和鉈添加的 f殼層以及由此產生的鑭系收縮打破。[30]
- ^ 來源中的豐度是相對於矽而不是按粒子表示法列出的。在定義矽為106時,所有元素的總和為 2.6682×1010,其中鋁就是其中的 8.410×104。
- ^ 比較USGS給出的鋁[92]和銅[93]的年產量
- ^ 雖然鋁本身不致癌,但國際癌症研究機構特別指出Söderberg鋁生產,[147]可能是由於暴露於多環芳香烴。[148]
參考資料[編輯]
- ^ Prohaska, Thomas; Irrgeher, Johanna; Benefield, Jacqueline; Böhlke, John K.; Chesson, Lesley A.; Coplen, Tyler B.; Ding, Tiping; Dunn, Philip J. H.; Gröning, Manfred; Holden, Norman E.; Meijer, Harro A. J. Standard atomic weights of the elements 2021 (IUPAC Technical Report). Pure and Applied Chemistry. 2022-05-04. ISSN 1365-3075. doi:10.1515/pac-2019-0603 (英語).
- ^ 2.0 2.1 2.2 2.3 Aluminium. Los Alamos National Laboratory. [2013-03-03]. (原始內容存檔於2012-08-04).
- ^ Dohmeier, C.; Loos, D.; Schnöckel, H. Aluminum(I) and Gallium(I) Compounds: Syntheses, Structures, and Reactions. Angewandte Chemie International Edition. 1996, 35 (2): 129–149. doi:10.1002/anie.199601291.
- ^ D. C. Tyte. Red (B2Π–A2σ) Band System of Aluminium Monoxide. Nature. 1964, 202 (4930): 383. Bibcode:1964Natur.202..383T. S2CID 4163250. doi:10.1038/202383a0.
- ^ Lide, D. R. Magnetic susceptibility of the elements and inorganic compounds. CRC Handbook of Chemistry and Physics (PDF) 81st. CRC Press. 2000. ISBN 0849304814. (原始內容 (PDF)存檔於2011-03-03).
- ^ Shakhashiri, B. Z. Chemical of the Week: Aluminum (PDF). SciFun.org. University of Wisconsin. 2008-03-17 [2012-03-04]. (原始內容 (PDF)存檔於2012年5月9日).
- ^ Lide 2004,第4-3頁.
- ^ Puchta, Ralph. A brighter beryllium. Nature Chemistry. 2011, 3 (5): 416. Bibcode:2011NatCh...3..416P. PMID 21505503. doi:10.1038/nchem.1033.
- ^ Davis 1999,第1–3頁.
- ^ Davis 1999,第2頁.
- ^ 11.0 11.1 Polmear, I.J. Light Alloys: Metallurgy of the Light Metals 3. Butterworth-Heinemann. 1995. ISBN 978-0-340-63207-9.
- ^ 12.0 12.1 12.2 Cardarelli, François. Materials handbook : a concise desktop reference 2nd. London: Springer. 2008: 158–163. ISBN 978-1-84628-669-8. OCLC 261324602.
- ^ 13.0 13.1 Davis 1999,第4頁.
- ^ Davis 1999,第2–3頁.
- ^ Cochran, J.F.; Mapother, D.E. Superconducting Transition in Aluminum. Physical Review. 1958, 111 (1): 132–142. Bibcode:1958PhRv..111..132C. doi:10.1103/PhysRev.111.132.
- ^ Schmitz 2006,第6頁.
- ^ Schmitz 2006,第161頁.
- ^ Dean 1999,第4.2頁.
- ^ Dean 1999,第4.6頁.
- ^ Dean 1999,第4.29頁.
- ^ 21.0 21.1 Dean 1999,第4.30頁.
- ^ 22.0 22.1 Enghag, Per. Encyclopedia of the Elements: Technical Data – History – Processing – Applications. John Wiley & Sons. 2008: 139, 819, 949 [2017-12-07]. ISBN 978-3-527-61234-5. (原始內容存檔於2019-12-25).
- ^ 23.0 23.1 23.2 Greenwood & Earnshaw 1997,第222–4頁.
- ^ 24.0 24.1 IAEA – Nuclear Data Section. Livechart – Table of Nuclides – Nuclear structure and decay data. www-nds.iaea.org. International Atomic Energy Agency. 2017 [2017-03-31]. (原始內容存檔於2019-03-23).
- ^ 25.0 25.1 25.2 25.3 25.4 Greenwood & Earnshaw 1997,第242–252頁.
- ^ Meija, Juris; et al. Atomic weights of the elements 2013 (IUPAC Technical Report). Pure and Applied Chemistry. 2016, 88 (3): 265–91. doi:10.1515/pac-2015-0305.
- ^ Aluminium. The Commission on Isotopic Abundances and Atomic Weights. [2020-10-20]. (原始內容存檔於2020-09-23).
- ^ Dickin, A.P. In situ Cosmogenic Isotopes. Radiogenic Isotope Geology. Cambridge University Press. 2005 [2008-07-16]. ISBN 978-0-521-53017-0. (原始內容存檔於2008-12-06).
- ^ Dodd, R.T. Thunderstones and Shooting Stars. Harvard University Press. 1986: 89–90. ISBN 978-0-674-89137-1.
- ^ 30.0 30.1 30.2 30.3 30.4 30.5 30.6 30.7 30.8 Greenwood & Earnshaw 1997,第224–227頁.
- ^ Greenwood & Earnshaw 1997,第112–113頁.
- ^ King 1995,第241頁.
- ^ Hatch, John E. Aluminum : properties and physical metallurgy. Aluminum Association., American Society for Metals. Metals Park, Ohio: American Society for Metals. 1984: 242. ISBN 978-1-61503-169-6. OCLC 759213422.
- ^ Vargel, Christian. Corrosion of Aluminium. Elsevier. 2004 [French edition published 1999]. ISBN 978-0-08-044495-6. (原始內容存檔於2016-05-21).
- ^ Macleod, H.A. Thin-film optical filters. CRC Press. 2001: 158159. ISBN 978-0-7503-0688-1.
- ^ 36.0 36.1 36.2 36.3 36.4 36.5 36.6 36.7 Frank, W.B. Aluminum. Ullmann's Encyclopedia of Industrial Chemistry. Wiley-VCH. 2009. ISBN 978-3-527-30673-2. doi:10.1002/14356007.a01_459.pub2.
- ^ 37.0 37.1 Beal, Roy E. Engine Coolant Testing : Fourth Volume. ASTM International. 1999: 90. ISBN 978-0-8031-2610-7. (原始內容存檔於24 April 2016).
- ^ 38.0 38.1 38.2 38.3 Greenwood & Earnshaw 1997,第233–237頁.
- ^ Eastaugh, Nicholas; Walsh, Valentine; Chaplin, Tracey; Siddall, Ruth. Pigment Compendium. Routledge. 2008 [2020-10-01]. ISBN 978-1-136-37393-0. (原始內容存檔於2021-04-15) (英語).
- ^ Roscoe, Henry Enfield; Schorlemmer, Carl. A treatise on chemistry. Macmillan. 1913 [2020-10-01]. (原始內容存檔於2021-04-15) (英語).
- ^ 41.0 41.1 Greenwood & Earnshaw 1997,第252–257頁.
- ^ Downs, A. J. Chemistry of Aluminium, Gallium, Indium and Thallium. Springer Science & Business Media. 1993: 218 [2020-10-01]. ISBN 978-0-7514-0103-5. (原始內容存檔於2021-04-15) (英語).
- ^ Dohmeier, C.; Loos, D.; Schnöckel, H. Aluminum(I) and Gallium(I) Compounds: Syntheses, Structures, and Reactions. Angewandte Chemie International Edition. 1996, 35 (2): 129–149. doi:10.1002/anie.199601291.
- ^ Tyte, D.C. Red (B2Π–A2σ) Band System of Aluminium Monoxide. Nature. 1964, 202 (4930): 383–384. Bibcode:1964Natur.202..383T. S2CID 4163250. doi:10.1038/202383a0.
- ^ Merrill, P.W.; Deutsch, A.J.; Keenan, P.C. Absorption Spectra of M-Type Mira Variables. The Astrophysical Journal. 1962, 136: 21. Bibcode:1962ApJ...136...21M. doi:10.1086/147348.
- ^ Uhl, W. Organoelement Compounds Possessing Al–Al, Ga–Ga, In–In, and Tl–Tl Single Bonds. Organoelement Compounds Possessing Al–Al, Ga–Ga, In–In, and Tl–Tl Single Bonds. Advances in Organometallic Chemistry 51. 2004: 53–108. ISBN 978-0-12-031151-4. doi:10.1016/S0065-3055(03)51002-4.
- ^ Elschenbroich, C. Organometallics. Wiley-VCH. 2006. ISBN 978-3-527-29390-2.
- ^ 48.0 48.1 Greenwood & Earnshaw 1997,第257–67頁.
- ^ Smith, Martin B. The monomer-dimer equilibria of liquid aluminum alkyls. Journal of Organometallic Chemistry. 1970, 22 (2): 273–281. doi:10.1016/S0022-328X(00)86043-X.
- ^ 50.0 50.1 Greenwood & Earnshaw 1997,第227–232頁.
- ^ 51.0 51.1 Lodders, K. Solar System abundances and condensation temperatures of the elements (PDF). The Astrophysical Journal. 2003, 591 (2): 1220–1247 [2018-06-15]. Bibcode:2003ApJ...591.1220L. ISSN 0004-637X. doi:10.1086/375492. (原始內容存檔 (PDF)於2019-04-12).
- ^ 52.0 52.1 52.2 52.3 52.4 Clayton, D. Handbook of Isotopes in the Cosmos : Hydrogen to Gallium.. Leiden: Cambridge University Press. 2003: 129–137 [2020-09-13]. ISBN 978-0-511-67305-4. OCLC 609856530. (原始內容存檔於2021-06-11).
- ^ William F McDonough The composition of the Earth. quake.mit.edu, archived by the Internet Archive Wayback Machine.
- ^ Greenwood & Earnshaw 1997,第217–9頁.
- ^ Wade, K.; Banister, A.J. The Chemistry of Aluminium, Gallium, Indium and Thallium: Comprehensive Inorganic Chemistry. Elsevier. 2016: 1049 [2018-06-17]. ISBN 978-1-4831-5322-3. (原始內容存檔於2019-11-30).
- ^ Palme, H.; O'Neill, Hugh St. C. Cosmochemical Estimates of Mantle Composition (PDF). Carlson, Richard W. (編). The Mantle and Core. Elseiver. 2005: 14 [2021-06-11]. (原始內容存檔 (PDF)於2021-04-03).
- ^ Downs, A.J. Chemistry of Aluminium, Gallium, Indium and Thallium. Springer Science & Business Media. 1993 [2017-06-14]. ISBN 978-0-7514-0103-5. (原始內容存檔於2020-07-25) (英語).
- ^ Kotz, John C.; Treichel, Paul M.; Townsend, John. Chemistry and Chemical Reactivity. Cengage Learning. 2012: 300 [2018-06-17]. ISBN 978-1-133-42007-1. (原始內容存檔於2019-12-22).
- ^ Barthelmy, D. Aluminum Mineral Data. Mineralogy Database. [2008-07-09]. (原始內容存檔於2008-07-04).
- ^ Chen, Z.; Huang, Chi-Yue; Zhao, Meixun; Yan, Wen; Chien, Chih-Wei; Chen, Muhong; Yang, Huaping; Machiyama, Hideaki; Lin, Saulwood. Characteristics and possible origin of native aluminum in cold seep sediments from the northeastern South China Sea. Journal of Asian Earth Sciences. 2011, 40 (1): 363–370. Bibcode:2011JAESc..40..363C. doi:10.1016/j.jseaes.2010.06.006.
- ^ Guilbert, J.F.; Park, C.F. The Geology of Ore Deposits. W.H. Freeman. 1986: 774–795. ISBN 978-0-7167-1456-9.
- ^ United States Geological Survey. Bauxite and alumina (PDF). Mineral Commodities Summaries. 2018 [2018-06-17]. (原始內容存檔 (PDF)於2018-03-11).
- ^ 63.0 63.1 Drozdov 2007,第12頁.
- ^ Clapham, John Harold; Power, Eileen Edna. The Cambridge Economic History of Europe: From the Decline of the Roman Empire. CUP Archive. 1941: 207. ISBN 978-0-521-08710-0.
- ^ Drozdov 2007,第16頁.
- ^ Setton, Kenneth M. The papacy and the Levant: 1204-1571. 1 The thirteenth and fourteenth centuries. American Philosophical Society. 1976. ISBN 978-0-87169-127-9. OCLC 165383496.
- ^ Drozdov 2007,第25頁.
- ^ Weeks, Mary Elvira. Discovery of the elements 1 7. Journal of chemical education. 1968: 187. ISBN 9780608300177.
- ^ 69.0 69.1 Richards 1896,第2頁.
- ^ Richards 1896,第3頁.
- ^ Davy, Humphry. Electro Chemical Researches, on the Decomposition of the Earths; with Observations on the Metals obtained from the alkaline Earths, and on the Amalgam procured from Ammonia. Philosophical Transactions of the Royal Society. 1808, 98: 353 [2009-12-10]. Bibcode:1808RSPT...98..333D. doi:10.1098/rstl.1808.0023
 . (原始內容存檔於2021-04-15).
. (原始內容存檔於2021-04-15).
- ^ Örsted, H. C. Oversigt over det Kongelige Danske Videnskabernes Selskabs Forhanlingar og dets Medlemmerz Arbeider, fra 31 Mai 1824 til 31 Mai 1825 [Overview of the Royal Danish Science Society's Proceedings and the Work of its Members, from 31 May 1824 to 31 May 1825]: 15–16. 1825 [2020-02-27]. (原始內容存檔於2020-03-16) (丹麥語).
- ^ Royal Danish Academy of Sciences and Letters. Det Kongelige Danske Videnskabernes Selskabs philosophiske og historiske afhandlinger [The philosophical and historical dissertations of the Royal Danish Science Society]. Popp. 1827: xxv–xxvi [2016-03-11]. (原始內容存檔於2017-03-24) (丹麥語).
- ^ 74.0 74.1 Wöhler, Friedrich. Ueber das Aluminium. Annalen der Physik und Chemie. 2. 1827, 11 (9): 146–161 [2016-03-11]. Bibcode:1828AnP....87..146W. doi:10.1002/andp.18270870912. (原始內容存檔於2021-06-11).
- ^ Drozdov 2007,第36頁.
- ^ Fontani, Marco; Costa, Mariagrazia; Orna, Mary Virginia. The Lost Elements: The Periodic Table's Shadow Side. Oxford University Press. 2014: 30. ISBN 978-0-19-938334-4.
- ^ 77.0 77.1 Venetski, S. 'Silver' from clay. Metallurgist. 1969, 13 (7): 451–453. S2CID 137541986. doi:10.1007/BF00741130.
- ^ 78.0 78.1 Drozdov 2007,第38頁.
- ^ Holmes, Harry N. Fifty Years of Industrial Aluminum. The Scientific Monthly. 1936, 42 (3): 236–239. Bibcode:1936SciMo..42..236H. JSTOR 15938.
- ^ Drozdov 2007,第39頁.
- ^ Sainte-Claire Deville, H.E. De l'aluminium, ses propriétés, sa fabrication. Paris: Mallet-Bachelier. 1859. (原始內容存檔於2016-04-30).
- ^ Drozdov 2007,第46頁.
- ^ Drozdov 2007,第55–61頁.
- ^ Drozdov 2007,第74頁.
- ^ 85.0 85.1 85.2 Aluminium history. All about aluminium. [2017-11-07]. (原始內容存檔於2017-11-07).
- ^ Drozdov 2007,第64–69頁.
- ^ Ingulstad, Mats. 'We Want Aluminum, No Excuses': Business-Government Relations in the American Aluminum Industry, 1917–1957. Ingulstad, Mats; Frøland, Hans Otto (編). From Warfare to Welfare: Business-Government Relations in the Aluminium Industry. Tapir Academic Press. 2012: 33–68 [2020-05-07]. ISBN 978-82-321-0049-1. (原始內容存檔於2020-07-25).
- ^ Seldes, George. Facts and Fascism 5. In Fact, Inc. 1943: 261.
- ^ Thorsheim, Peter. Waste into Weapons. Cambridge University Press. 2015: 66–69 [2021-01-07]. ISBN 978-1-107-09935-7. (原始內容存檔於2020-04-06).
- ^ Weeks, Albert Loren. Russia's Life-saver: Lend-lease Aid to the U.S.S.R. in World War II. Lexington Books. 2004: 135 [2021-01-07]. ISBN 978-0-7391-0736-2. (原始內容存檔於2020-04-06).
- ^ Drozdov 2007,第69–70頁.
- ^ 92.0 92.1 92.2 92.3 Aluminum. Historical Statistics for Mineral Commodities in the United States (報告). United States Geological Survey. 2017 [9 November 2017]. (原始內容存檔於8 March 2018) (英語).
- ^ Copper. Supply-Demand Statistics. Historical Statistics for Mineral Commodities in the United States (報告). United States Geological Survey. 2017 [2019-06-04]. (原始內容存檔於2018-03-08) (英語).
- ^ Gregersen, Erik. Copper. Encyclopedia Britannica. [2019-06-04]. (原始內容存檔於2019-06-22) (英語).
- ^ Drozdov 2007,第165–166頁.
- ^ Drozdov 2007,第85頁.
- ^ Drozdov 2007,第135頁.
- ^ Nappi 2013,第9頁.
- ^ Nappi 2013,第9–10頁.
- ^ Nappi 2013,第10頁.
- ^ Nappi 2013,第14–15頁.
- ^ Nappi 2013,第17頁.
- ^ Nappi 2013,第20頁.
- ^ Nappi 2013,第22頁.
- ^ Nappi 2013,第23頁.
- ^ Brown, T.J. World Mineral Production 2003–2007. British Geological Survey. 2009 [2014-12-01]. (原始內容存檔於2019-07-13).
- ^ USGS Minerals Information: Mineral Commodity Summaries (PDF). minerals.usgs.gov. [2020-12-17]. doi:10.3133/70194932. (原始內容存檔 (PDF)於2021-01-22) (英語).
- ^ Graedel, T.E.; et al. Metal stocks in Society – Scientific Synthesis (PDF) (報告). International Resource Panel: 17. 2010 [18 April 2017]. ISBN 978-92-807-3082-1. (原始內容存檔 (PDF)於26 April 2018).
- ^ 109.0 109.1 109.2 109.3 109.4 Hudson, L. Keith; Misra, Chanakya; Perrotta, Anthony J.; et al. Aluminum Oxide. Ullmann's Encyclopedia of Industrial Chemistry. Wiley-VCH. 2005.
- ^ Totten, G.E.; Mackenzie, D.S. Handbook of Aluminum. Marcel Dekker. 2003: 40. ISBN 978-0-8247-4843-2. (原始內容存檔於2016-06-15).
- ^ Emsley, John. Nature's Building Blocks: An A–Z Guide to the Elements. OUP Oxford. 2011: 24–30 [2017-11-16]. ISBN 978-0-19-960563-7. (原始內容存檔於2019-12-22).
- ^ Schlesinger, Mark. Aluminum Recycling. CRC Press. 2006: 248 [2018-06-25]. ISBN 978-0-8493-9662-5. (原始內容存檔於2017-02-15).
- ^ Benefits of Recycling. Ohio Department of Natural Resources. (原始內容存檔於2003-06-24).
- ^ Theoretical/Best Practice Energy Use in Metalcasting Operations (PDF). [2013-10-28]. (原始內容 (PDF)存檔於2013-10-31).
- ^ Why are dross & saltcake a concern?. www.experts123.com. (原始內容存檔於2012-11-14).
- ^ Dunster, A.M.; et al. Added value of using new industrial waste streams as secondary aggregates in both concrete and asphalt (PDF). Waste & Resources Action Programme. 2005. (原始內容存檔於2010-04-02).
- ^ Brown, T.J.; Idoine, N.E.; Raycraft, E.R.; et al. World Mineral Production: 2012–2016. British Geological Survey. 2018 [2018-07-10]. ISBN 978-0-85272-882-6. (原始內容存檔於2020-05-16).
- ^ Aluminum. Encyclopædia Britannica. [6 March 2012]. (原始內容存檔於12 March 2012).
- ^ Millberg, L.S. Aluminum Foil. How Products are Made. [2007-08-11]. (原始內容存檔於2007-07-13).
|volume=被忽略 (幫助) - ^ Lyle, J.P.; Granger, D.A.; Sanders, R.E. Aluminum Alloys. Ullmann's Encyclopedia of Industrial Chemistry. Wiley-VCH. 2005. ISBN 978-3-527-30673-2. doi:10.1002/14356007.a01_481.
- ^ Davis 1999,第17–24頁.
- ^ Apple Patents reveal how the Aluminum Unibody MacBook Enclosure is made from Recycled Pop and Beer Cans & more. Patenly Apple. March 2021 [2021-05-24]. (原始內容存檔於2021-05-24).
- ^ Lumley, Roger. Fundamentals of Aluminium Metallurgy: Production, Processing and Applications. Elsevier Science. 2010: 42 [2018-07-13]. ISBN 978-0-85709-025-6. (原始內容存檔於2019-12-22).
- ^ Mortensen, Andreas. Concise Encyclopedia of Composite Materials. Elsevier. 2006: 281 [2018-07-13]. ISBN 978-0-08-052462-7. (原始內容存檔於2019-12-20).
- ^ The Ceramic Society of Japan. Advanced Ceramic Technologies & Products. Springer Science & Business Media. 2012: 541 [2018-07-13]. ISBN 978-4-431-54108-0. (原始內容存檔於2019-11-29).
- ^ Slesser, Malcolm. Dictionary of Energy. Palgrave Macmillan UK. 1988: 138 [2018-07-13]. ISBN 978-1-349-19476-6. (原始內容存檔於2021-06-11).
- ^ Supp, Emil. How to Produce Methanol from Coal. Springer Science & Business Media. 2013: 164–165 [2018-07-13]. ISBN 978-3-662-00895-9. (原始內容存檔於2019-12-26).
- ^ Ertl, Gerhard; Knözinger, Helmut; Weitkamp, Jens. Preparation of Solid Catalysts. John Wiley & Sons. 2008: 80 [2018-07-13]. ISBN 978-3-527-62068-5. (原始內容存檔於2019-12-24).
- ^ Armarego, W.L.F.; Chai, Christina. Purification of Laboratory Chemicals. Butterworth-Heinemann. 2009: 73, 109, 116, 155 [2018-07-13]. ISBN 978-0-08-087824-9. (原始內容存檔於2019-12-22).
- ^ 130.0 130.1 130.2 130.3 130.4 130.5 130.6 Helmboldt, O. Aluminum Compounds, Inorganic. Ullmann's Encyclopedia of Industrial Chemistry. Wiley-VCH. 2007. ISBN 978-3-527-30673-2. doi:10.1002/14356007.a01_527.pub2.
- ^ World Health Organization. Stuart MC, Kouimtzi M, Hill SR , 編. WHO Model Formulary 2008. World Health Organization. 2009. ISBN 9789241547659. hdl:10665/44053
 .
.
- ^ Occupational Skin Disease. Grune & Stratton. 1983 [2017-06-14]. ISBN 978-0-8089-1494-5. (原始內容存檔於2021-04-15) (英語).
- ^ Galbraith, A; Bullock, S; Manias, E; Hunt, B; Richards, A. Fundamentals of pharmacology: a text for nurses and health professionals. Harlow: Pearson. 1999: 482.
- ^ Papich, Mark G. Aluminum Hydroxide and Aluminum Carbonate. Saunders Handbook of Veterinary Drugs 2nd. St. Louis, Mo: Saunders/Elsevier. 2007: 15–16. ISBN 978-1-4160-2888-8.
- ^ Brown, Weldon G., John Wiley & Sons, Inc. , 編, Reductions by Lithium Aluminum Hydride, Organic Reactions (Hoboken, NJ, USA: John Wiley & Sons, Inc.), 2011-03-15: 469–510 [2021-05-22], ISBN 978-0-471-26418-7, doi:10.1002/0471264180.or006.10, (原始內容存檔於2021-06-11) (英語)
- ^ Gerrans, G.C.; Hartmann-Petersen, P. Lithium Aluminium Hydride. SASOL Encyclopaedia of Science and Technology. New Africa Books: 143. 2007 [6 September 2017]. ISBN 978-1-86928-384-1. (原始內容存檔於23 August 2017).
- ^ M. Witt; H.W. Roesky. Organoaluminum chemistry at the forefront of research and development (PDF). Curr. Sci. 2000, 78 (4): 410. (原始內容 (PDF)存檔於2014-10-06).
- ^ A. Andresen; H.G. Cordes; J. Herwig; W. Kaminsky; A. Merck; R. Mottweiler; J. Pein; H. Sinn; H.J. Vollmer. Halogen-free Soluble Ziegler-Catalysts for the Polymerization of Ethylene. Angew. Chem. Int. Ed. 1976, 15 (10): 630–632. doi:10.1002/anie.197606301.
- ^ Aas, Øystein; Klemetsen, Anders; Einum, Sigurd; et al. Atlantic Salmon Ecology. John Wiley & Sons. 2011: 240 [2018-07-14]. ISBN 978-1-4443-4819-4. (原始內容存檔於2019-12-21).
- ^ Singh, Manmohan. Vaccine Adjuvants and Delivery Systems. John Wiley & Sons. 2007: 81–109 [2018-07-14]. ISBN 978-0-470-13492-4. (原始內容存檔於2019-12-20).
- ^ 141.0 141.1 Exley, C. Human exposure to aluminium. Environmental Science: Processes & Impacts. 2013, 15 (10): 1807–1816. PMID 23982047. doi:10.1039/C3EM00374D
 .
.
- ^ Environmental Applications. Part I. Common Forms of the Elements in Water. Western Oregon University. Western Oregon University. [30 September 2019]. (原始內容存檔於11 December 2018).
- ^ Shaw, Christopher A.; Seneff, Stephanie; Kette, Stephen D.; Tomljenovic, Lucija; Oller, John W.; Davidson, Robert M. Aluminum-Induced Entropy in Biological Systems: Implications for Neurological Disease. Journal of Toxicology. 2014, 2014: 1–27. PMC 4202242
 . PMID 25349607. doi:10.1155/2014/491316
. PMID 25349607. doi:10.1155/2014/491316  .
.
- ^ Andrási, Erzsébet; Páli, Noémi; Molnár, Zsuzsa; Kösel, Siegfried. Brain aluminum, magnesium and phosphorus contents of control and Alzheimer-diseased patients. Journal of Alzheimer's Disease. 2005, 7 (4): 273–284. PMID 16131728. doi:10.3233/jad-2005-7402.
- ^ Purgel, Mihály; Takács, Zoltán; Jonsson, Caroline M.; Nagy, Lajos; Andersson, Ingegärd; Bányai, István; Pápai, Imre; Persson, Per; Sjöberg, Staffan; Tóth, Imre. Glyphosate complexation to aluminium(III). An equilibrium and structural study in solution using potentiometry, multinuclear NMR, ATR–FTIR, ESI-MS and DFT calculations. 10.1016/J.jinorgbio.2009.06.011. 2009, 103 (11): 1426–1438. PMID 19766319. doi:10.1016/j.jinorgbio.2009.06.011.
- ^ 146.0 146.1 146.2 146.3 146.4 146.5 146.6 146.7 Dolara, Piero. Occurrence, exposure, effects, recommended intake and possible dietary use of selected trace compounds (aluminium, bismuth, cobalt, gold, lithium, nickel, silver). International Journal of Food Sciences and Nutrition. 21 July 2014, 65 (8): 911–924. ISSN 1465-3478. PMID 25045935. S2CID 43779869. doi:10.3109/09637486.2014.937801.
- ^ Polynuclear aromatic compounds. part 3, Industrial exposures in aluminium production, coal gasification, coke production, and iron and steel founding.. International Agency for Research on Cancer. International Agency for Research on Cancer. 1984: 51–59 [7 January 2021]. ISBN 92-832-1534-6. OCLC 11527472. (原始內容存檔於11 June 2021).
- ^ Wesdock, J. C.; Arnold, I. M. F. Occupational and Environmental Health in the Aluminum Industry. Journal of Occupational and Environmental Medicine. 2014, 56 (5 Suppl): S5–S11. ISSN 1076-2752. PMC 4131940
 . PMID 24806726. doi:10.1097/JOM.0000000000000071 (美國英語).
. PMID 24806726. doi:10.1097/JOM.0000000000000071 (美國英語).
- ^ Physiology of Aluminum in Man. Aluminum and Health (CRC Press). 1988: 90. ISBN 0-8247-8026-4. (原始內容存檔於19 May 2016).
- ^ ATSDR – Public Health Statement: Aluminum. www.atsdr.cdc.gov. [2018-07-18]. (原始內容存檔於12 December 2016) (英語).
- ^ Xu, N.; Majidi, V.; Markesbery, W. R.; Ehmann, W. D. Brain aluminum in Alzheimer's disease using an improved GFAAS method. Neurotoxicology. 1992, 13 (4): 735–743. PMID 1302300.
- ^ Yumoto, Sakae; Kakimi, Shigeo; Ohsaki, Akihiro; Ishikawa, Akira. Demonstration of aluminum in amyloid fibers in the cores of senile plaques in the brains of patients with Alzheimer's disease. Journal of Inorganic Biochemistry. 2009, 103 (11): 1579–1584. PMID 19744735. doi:10.1016/j.jinorgbio.2009.07.023.
- ^ Crapper Mclachlan, D.R.; Lukiw, W.J.; Kruck, T.P.A. New Evidence for an Active Role of Aluminum in Alzheimer's Disease. Canadian Journal of Neurological Sciences. 1989, 16 (4 Suppl): 490–497. PMID 2680008. doi:10.1017/S0317167100029826.
- ^ Lowermoor Water Pollution incident 'unlikely' to have caused long term health effects (PDF). Committee on Toxicity of Chemicals in Food, Consumer Products and the Environment. 18 April 2013 [21 December 2019]. (原始內容存檔 (PDF)於21 December 2019).
- ^ Tomljenovic, Lucija. Aluminum and Alzheimer's Disease: After a Century of Controversy, Is there a Plausible Link?. Journal of Alzheimer's Disease. 2011-03-21, 23 (4): 567–598 [11 June 2021]. PMID 21157018. doi:10.3233/JAD-2010-101494. (原始內容存檔於11 June 2021).
- ^ Aluminum and dementia: Is there a link?. Alzheimer Society Canada. 24 August 2018 [21 December 2019]. (原始內容存檔於21 December 2019).
- ^ Santibáñez, Miguel; Bolumar, Francisco; García, Ana M. Occupational risk factors in Alzheimer's disease: a review assessing the quality of published epidemiological studies. Occupational and Environmental Medicine. 2007, 64 (11): 723–732. ISSN 1351-0711. PMC 2078415
 . PMID 17525096. doi:10.1136/oem.2006.028209.
. PMID 17525096. doi:10.1136/oem.2006.028209.
- ^ Darbre, P.D. Metalloestrogens: an emerging class of inorganic xenoestrogens with potential to add to the oestrogenic burden of the human breast. Journal of Applied Toxicology. 2006, 26 (3): 191–197. PMID 16489580. S2CID 26291680. doi:10.1002/jat.1135.
- ^ Banks, W.A.; Kastin, A.J. Aluminum-induced neurotoxicity: alterations in membrane function at the blood–brain barrier. Neurosci Biobehav Rev. 1989, 13 (1): 47–53. PMID 2671833. S2CID 46507895. doi:10.1016/S0149-7634(89)80051-X.
- ^ Bingham, Eula; Cohrssen, Barbara. Patty's Toxicology, 6 Volume Set. John Wiley & Sons. 2012: 244 [23 July 2018]. ISBN 978-0-470-41081-3. (原始內容存檔於20 December 2019).
- ^ Aluminum Allergy Symptoms and Diagnosis. Allergy-symptoms.org. 2016-09-20 [2018-07-23]. (原始內容存檔於23 July 2018) (美國英語).
- ^ al-Masalkhi, A.; Walton, S.P. Pulmonary fibrosis and occupational exposure to aluminum. The Journal of the Kentucky Medical Association. 1994, 92 (2): 59–61. ISSN 0023-0294. PMID 8163901.
- ^ CDC – NIOSH Pocket Guide to Chemical Hazards – Aluminum. www.cdc.gov. [11 June 2015]. (原始內容存檔於30 May 2015).
- ^ CDC – NIOSH Pocket Guide to Chemical Hazards – Aluminum (pyro powders and welding fumes, as Al). www.cdc.gov. [11 June 2015]. (原始內容存檔於30 May 2015).
- ^ Yokel R.A.; Hicks C.L.; Florence R.L. Aluminum bioavailability from basic sodium aluminum phosphate, an approved food additive emulsifying agent, incorporated in cheese. Food and Chemical Toxicology. 2008, 46 (6): 2261–2266. PMC 2449821
 . PMID 18436363. doi:10.1016/j.fct.2008.03.004.
. PMID 18436363. doi:10.1016/j.fct.2008.03.004.
- ^ United States Department of Health and Human Services. Toxicological profile for aluminum (PDF) (報告). 1999 [2018-08-03]. (原始內容存檔 (PDF)於9 May 2020).
- ^ 167.0 167.1 167.2 167.3 Aluminum. The Environmental Literacy Council. [2018-07-29]. (原始內容存檔於27 October 2020) (美國英語).
- ^ Chen, Jennifer K.; Thyssen, Jacob P. Metal Allergy: From Dermatitis to Implant and Device Failure. Springer. 2018: 333 [23 July 2018]. ISBN 978-3-319-58503-1. (原始內容存檔於26 December 2019).
- ^ Slanina, P.; French, W.; Ekström, L.G.; Lööf, L.; Slorach, S.; Cedergren, A. Dietary citric acid enhances absorption of aluminum in antacids. Clinical Chemistry. 1986, 32 (3): 539–541. PMID 3948402. doi:10.1093/clinchem/32.3.539.
- ^ Van Ginkel, M.F.; Van Der Voet, G.B.; D'haese, P.C.; De Broe, M.E.; De Wolff, F.A. Effect of citric acid and maltol on the accumulation of aluminum in rat brain and bone. The Journal of Laboratory and Clinical Medicine. 1993, 121 (3): 453–460. PMID 8445293.
- ^ 171.0 171.1 ARL: Aluminum Toxicity. www.arltma.com. [2018-07-24]. (原始內容存檔於31 August 2019).
- ^ Aluminum Toxicity 網際網路檔案館的存檔,存檔日期3 February 2014. from NYU Langone Medical Center. Last reviewed November 2012 by Igor Puzanov, MD
- ^ 173.0 173.1 ATSDR – Public Health Statement: Aluminum. www.atsdr.cdc.gov. [2018-07-28]. (原始內容存檔於12 December 2016) (英語).
- ^ 174.0 174.1 174.2 Rosseland, B.O.; Eldhuset, T.D.; Staurnes, M. Environmental effects of aluminium. Environmental Geochemistry and Health. 1990, 12 (1–2): 17–27. ISSN 0269-4042. PMID 24202562. S2CID 23714684. doi:10.1007/BF01734045.
- ^ Baker, Joan P.; Schofield, Carl L. Aluminum toxicity to fish in acidic waters. Water, Air, and Soil Pollution. 1982, 18 (1–3): 289–309 [27 December 2020]. Bibcode:1982WASP...18..289B. ISSN 0049-6979. S2CID 98363768. doi:10.1007/BF02419419. (原始內容存檔於11 June 2021) (英語).
- ^ Belmonte Pereira, Luciane; Aimed Tabaldi, Luciane; Fabbrin Gonçalves, Jamile; Jucoski, Gladis Oliveira; Pauletto, Mareni Maria; Nardin Weis, Simone; Texeira Nicoloso, Fernando; Brother, Denise; Batista Teixeira Rocha, João; Chitolina Schetinger, Maria Rosa Chitolina. Effect of aluminum on δ-aminolevulinic acid dehydratase (ALA-D) and the development of cucumber (Cucumis sativus). Environmental and experimental botany. 2006, 57 (1–2): 106–115. doi:10.1016/j.envexpbot.2005.05.004.
- ^ Andersson, Maud. Toxicity and tolerance of aluminum in vascular plants. Water, Air, & Soil Pollution. 1988, 39 (3–4): 439–462. doi:10.1007/BF00279487.
- ^ Horst, Walter J. The role of the apoplast in aluminum toxicity and resistance of higher plants: A review. Zeitschrift für Pflanzenernährung und Bodenkunde. 1995, 158 (5): 419–428. doi:10.1002/jpln.19951580503.
- ^ Ma, Jian Feng; Ryan, PR; Delhaize, E. Aluminum tolerance in plants and the complexing role of organic acids. Trends in Plant Science. 2001, 6 (6): 273–278. PMID 11378470. doi:10.1016/S1360-1385(01)01961-6.
- ^ Turner, R.C. and Clark J.S. Lime potential in acid clay and soil suspensions. Trans. Comm. II & IV Int. Soc. Soil Science. 1966: 208–215.
- ^ corrected lime potential (formula). Sis.agr.gc.ca. 2008-11-27 [2010-05-03]. (原始內容存檔於2012-02-04).
- ^ Turner, R.C. A Study of the Lime Potential. Research Branch, Department Of Agriculture. 1965 [2013-09-30]. (原始內容存檔於2012-07-09).
- ^ 應用石灰來降低鋁對植物的毒性。One Hundred Harvests Research Branch Agriculture Canada 1886–1986. Historical series / Agriculture Canada – Série historique / Agriculture Canada. Government of Canada. [2008-12-22]. (原始內容存檔於2009-07-28).
- ^ Magalhaes, J.V.; Garvin, D.F.; Wang, Y.; Sorrells, M.E.; Klein, P.E.; Schaffert, R.E.; Li, L.; Kochian, L.V. Comparative Mapping of a Major Aluminum Tolerance Gene in Sorghum and Other Species in the Poaceae. Genetics. 2004, 167 (4): 1905–1914. PMC 1471010
 . PMID 15342528. doi:10.1534/genetics.103.023580.
. PMID 15342528. doi:10.1534/genetics.103.023580.
- ^ Fungus 'eats' CDs. BBC. 22 June 2001. (原始內容存檔於12 December 2013).
- ^ Bosch, Xavier. Fungus eats CD. Nature. 27 June 2001: news010628–11. doi:10.1038/news010628-11. (原始內容存檔於31 December 2010).
- ^ Sheridan, J.E.; Nelson, Jan; Tan, Y.L. Studies on the 'Kerosene Fungus' Cladosporium resinae (Lindau) De Vries: Part I. The Problem of Microbial Contamination of Aviation Fuels. Tuatara: 29. (原始內容存檔於13 December 2013).
- ^ Fuel System Contamination & Starvation. Duncan Aviation. 2011. (原始內容存檔於25 February 2015).
延伸閱讀[編輯]
- Davis, J. R. Corrosion of Aluminum and Aluminum Alloys. ASM International. 1999. ISBN 978-1-61503-238-9 (英語).
- Dean, J. A. Lange's handbook of chemistry 15. McGraw-Hill. 1999. ISBN 978-0-07-016384-3. OCLC 40213725.
- Drozdov, A. Aluminium: The Thirteenth Element. RUSAL Library. 2007. ISBN 978-5-91523-002-5.
- Greenwood, N. N.; Earnshaw, A. Chemistry of the Elements 2nd. Butterworth-Heinemann. 1997. ISBN 978-0-08-037941-8.
- King, R. B. Inorganic Chemistry of Main Group Elements. Wiley-VCH. 1995. ISBN 978-0-471-18602-1.
- Lide, D. R. (編). Handbook of Chemistry and Physics
 84. CRC Press. 2004. ISBN 978-0-8493-0566-5.
84. CRC Press. 2004. ISBN 978-0-8493-0566-5. - Nappi, C. The global aluminium industry 40 years from 1972 (PDF) (報告). International Aluminium Institute. 2013. (原始內容存檔 (PDF)於2022-10-09).
- Richards, J. W. Aluminium: Its history, occurrence, properties, metallurgy and applications, including its alloys 3. Henry Carey Baird & Co. 1896.
- Schmitz, C. Handbook of Aluminium Recycling. Vulkan-Verlag GmbH. 2006. ISBN 978-3-8027-2936-2 (英語).
外部連結[編輯]
- 元素鋁在洛斯阿拉莫斯國家實驗室的介紹(英文)
- EnvironmentalChemistry.com —— 鋁(英文)
- 元素鋁在The Periodic Table of Videos(諾丁罕大學)的介紹(英文)
- 元素鋁在Peter van der Krogt elements site的介紹(英文)
- WebElements.com – 鋁(英文)
| 維基共享資源上的相關多媒體資源:鋁 |
- Aluminum (頁面存檔備份,存於網際網路檔案館) at The Periodic Table of Videos (University of Nottingham)
- CDC - NIOSH Pocket Guide to Chemical Hazards - Aluminum (頁面存檔備份,存於網際網路檔案館)
- Electrolytic production
- World production of primary aluminum, by country (頁面存檔備份,存於網際網路檔案館)
- Price history of aluminum, according to the IMF (頁面存檔備份,存於網際網路檔案館)
- History of Aluminum (頁面存檔備份,存於網際網路檔案館) – from the website of the International Aluminum Institute
- Emedicine – Aluminum (頁面存檔備份,存於網際網路檔案館)
- 短片 ALUMINUM (1941) 可在網際網路檔案館自由下載
| 元素週期表(主族金屬) | |||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| IA 1 |
IIA 2 |
IIIB 3 |
IVB 4 |
VB 5 |
VIB 6 |
VIIB 7 |
VIIIB 8 |
VIIIB 9 |
VIIIB 10 |
IB 11 |
IIB 12 |
IIIA 13 |
IVA 14 |
VA 15 |
VIA 16 |
VIIA 17 |
VIIIA 18 | ||||||||||||||||||||
| 1 | H | He | |||||||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | |||||||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |||||
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |||||
| |||||||||||||||||||||||||||||||||||||
| |||||||||||||||||



