苯酚
此條目需要精通或熟悉化學的編者參與及協助編輯。 (2020年6月26日) |
| 苯酚 | |||
|---|---|---|---|
| |||
| |||

| |||
| IUPAC名 Hydroxybenzene 羥基苯 | |||
| 別名 | 石炭酸 | ||
| 識別 | |||
| CAS號 | 108-95-2 | ||
| PubChem | 996 | ||
| ChemSpider | 971 | ||
| SMILES |
| ||
| InChI |
| ||
| ChEBI | 15882 | ||
| RTECS | SJ3325000 | ||
| DrugBank | DB03255 | ||
| KEGG | D06536 | ||
| 性質 | |||
| 化學式 | C6H5OH | ||
| 摩爾質量 | 94.11 g·mol⁻¹ | ||
| 外觀 | 無色結晶狀固體 | ||
| 密度 | 1.07 g/cm³ | ||
| 熔點 | 40.5 °C | ||
| 沸點 | 181.7 °C | ||
| 溶解性(水) | 8.3 g/100 ml (20 °C) | ||
| pKa | 9.95 | ||
| 偶極矩 | 1.7 D | ||
| 危險性 | |||
| 歐盟分類 | 有毒 (T) 突變原 腐蝕性 (C) | ||
| NFPA 704 | |||
| 閃點 | 79 °C | ||
| 相關物質 | |||
| 相關化學品 | 苯硫酚、苯硒酚、苯碲酚 | ||
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |||
苯酚(phenol)又名石炭酸(carbolic acid)、羥基苯(hydroxybenzene)、苯醇(benzenol)、酚酸(phenolic acid)等,是最簡單的酚類有機物,化學式 C
6H
5OH(PhOH),常溫下為一種無色針狀晶體。具毒性、弱酸性,易潮解。
苯酚是一種常見的化學品,是生產某些樹脂、殺菌劑、防腐劑以及藥物(如阿司匹林)的重要原料。
發現
[編輯]苯酚是由德國化學家榮格(Runge F)於1834年在煤焦油中發現的,故又稱石炭酸(Carbolic acid)。
結構
[編輯]苯酚分子由一個羥基直接連在苯環上構成。根據苯的凱庫勒式,這個羥基是連在雙鍵上的,為烯醇式結構。但由於苯環的穩定性,這樣的結構幾乎不會轉化為酮式結構。
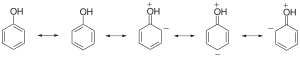
苯酚具有以下共振結構:
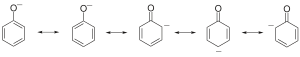
苯酚鹽負離子則有以下共振結構:
酚羥基的氧原子採用sp2雜化,提供1對孤電子與苯環的6個碳原子共同形成離域 鍵。大Π鍵加強了烯醇的酸性,羥基的推電子效應又加強了O-H鍵的極性,因此苯酚中羥基的氫可以電離出來。
物理性質
[編輯]苯酚熔點為40.5℃,沸點為181.7℃,常溫下為一種無色或白色的晶體,有特殊氣味。苯酚密度比水大,微溶於冷水,可在水中形成白色混濁;但易溶於65℃以上的熱水。易溶於醇、醚等有機溶劑。常溫時苯酚含水27%可成為均勻液體。
化學性質
[編輯]- 酸鹼反應
苯酚具有弱酸性,能與鹼反應:
苯酚pKa=10,酸性介於碳酸兩級電離之間,因此苯酚不能與碳酸氫鈉等弱鹼反應:
此反應現象:二氧化碳通入後,溶液中出現白色混濁。
- 顯色反應
苯酚遇三氯化鐵溶液顯紫色,原因是苯酚根離子與Fe3+形成了有顏色的配合物。
- (紫色)
- 取代反應

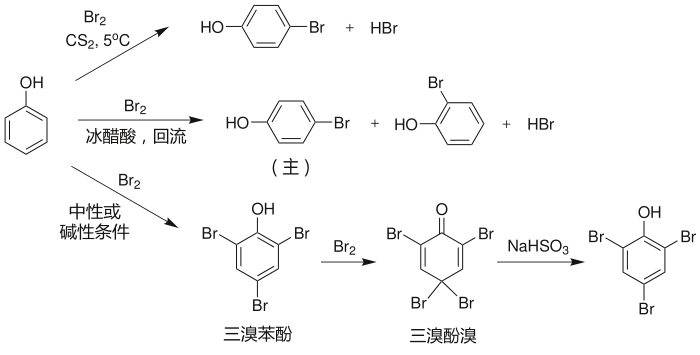
對比苯的相應反應可以發現,苯酚環上的取代比苯容易得多。這是因為羥基有給電子效應,使苯環電子雲密度增加。
值得注意的是,苯酚的親電取代總是發生在羥基的鄰位和對位。這是羥基等給電子基團的共性。
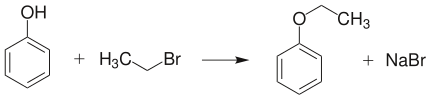
- 氧化還原反應
苯酚在空氣中久置會變為粉紅色,是因為生成了苯醌:
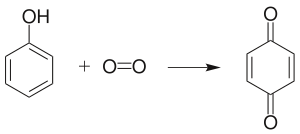
- 縮合反應
苯酚與甲醛在酸或鹼的催化下發生縮合,生成酚醛樹脂。
製備
[編輯]- 熔融苯磺酸法

用酸處理即得苯酚。此法是最早用來製取苯酚的方法,萘酚也用類似的方法製取。
此法初始原料為苯,通過傅-克反應與丙烯加成為異丙苯,再由異丙苯氧化為苯酚。此法同時生成丙酮。
第二步反應是一個自由基反應。
- 氯苯水解
通過氯苯在氫氧化鈉水溶液中的水解,也可以製得苯酚。由於氯苯的氯原子參與苯環的共軛,這個水解過程十分困難,需要在高壓(28MPa)、高溫(300℃)、以銅作催化劑的條件下進行。
- 其他方法

2007年吉林大學化學學院的馮守華等人在有機化學通訊期刊上發表文章稱,他們用碳酸氫鈉和鐵粉在仿早期地球環境的條件下進行水熱合成(水,200℃,1.9GPa),在產物中得到了產率為0.8%的苯酚。[1]

他們認為反應機理如下:[2]

安全
[編輯]苯酚有毒。苯酚及其濃溶液對皮膚有強烈的刺激作用,若不慎將苯酚沾到皮膚上,應用酒精或聚乙二醇清洗;若量較大或者混有氯仿,則需要進行急救。沾到衣服上也需用大量水沖洗。
工業及醫學用途
[編輯]苯酚可作殺菌劑、麻醉劑、防腐劑。英國外科醫生約瑟夫·李斯特(Lister J)於1865年將其用於外科手術消毒,為最早以藥劑進行術前消毒的醫生;但由於苯酚的毒性,這一技術最終被取代。現在苯酚可用於製備消毒劑,如TCP;或用其稀溶液直接進行消毒。
苯酚是多種化工產品的原料,用來合成阿司匹林等藥品,以及一些農藥、香料、染料。亦用來合成樹脂,最主要的一種是和甲醛縮合而成的酚醛樹脂。
儘管苯酚的濃溶液毒性很強,它仍在整形外科手術中充當脫皮劑。
衍生物
[編輯]參見
[編輯]註釋
[編輯]- ^ Tian, Ge; Yuan, Hongming; Mu, Ying; He, Chao; Feng, Shouhua. Hydrothermal Reactions from Sodium Hydrogen Carbonate to Phenol. Organic Letters. 2007-05, 9 (10): 2019–2021 [2020-11-05]. ISSN 1523-7060. doi:10.1021/ol070597o. (原始內容存檔於2019-12-02) (英語).
- ^ Shouhua Feng, Ge Tian, Hongming Yuan, Ying Mu & Chao He. Supporting Information for Hydrothermal Reactions from Sodium Hydrogen Carbonate to Phenol (PDF). [2009-08-15]. (原始內容 (PDF)存檔於2007-12-15).
參考文獻
[編輯]- 邢其毅. 第十七章. 基础有机化学. 北京: 高等教育出版社. 1993 [2020-11-05]. ISBN 978-7-04-004276-4. OCLC 768503522. (原始內容存檔於2020-12-18) (中文).









![{\displaystyle {\rm {\ 6PhOH+FeCl_{3}\rightarrow H_{3}[Fe(OPh)_{6}]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/046c2cd1dfbf511b14ae46217344394c8b98d953)



