氟
在所有元素中,氟在宇宙中的豐度排名為24,在地殼中豐度排名13。螢石是氟的主要礦物來源,1529年該礦物的性質首次被描述。由於在冶煉中將螢石加入金屬礦石可以降低礦石的熔點,螢石和氟包含有拉丁語中表示流動的詞根fluo。儘管在1810年就已經認為存在氟這種元素,由於氟非常難以從其化合物中分離出來,並且分離過程也非常危險,直到1886年,法國化學家亨利·莫瓦桑才採用低溫電解的方法分離出氟單質。許多早期實驗者都因為嘗試分離氟單質而受傷甚至去世。莫瓦桑的分離方法在現代生產中仍在使用。自第二次世界大戰的曼哈頓工程以來,單質氟的最大應用就是合成鈾濃縮所需的六氟化鈾。
由於提純氟單質的費用甚高,大多數的氟的商業應用都是使用其化合物,開採出的螢石中幾乎一半都用於煉鋼。其餘的螢石轉化為具有腐蝕性的氟化氫並用於合成有機氟化物,或者轉化為在鋁冶煉中起到關鍵作用的冰晶石。有機氟化物具有很高的化學穩定性,其主要用途是製冷劑、絕緣材料以及廚具(特氟龍)。諸如阿托伐他汀和氟西汀等藥物也含有氟。由於氟離子能夠抑制齲齒,氟化水和牙膏中也含有氟。全球與氟相關的化工業年銷售額超過150億美元。
碳氟化合物氣體是溫室氣體,其溫室效應是二氧化碳的100到20000倍。由於碳氟鍵強度極高,有機氟化合物在環境中難以降解,能夠長期存在。在哺乳動物中,氟沒有已知的代謝作用,而一些植物和海綿能夠合成能夠阻止食草動物的有機氟毒素,通常為氟乙酸鹽。[13]
性質[編輯]
電子組態[編輯]

氟原子有9個電子,比氖原子少一個。其電子組態為1s22s22p5:內層填滿了兩個電子,外層離滿殼層僅差一個電子。氟原子中外層電子不產生遮蔽效應,並且受到很高有效核電荷(9-2=7)的作用。這影響了氟原子的物理性質[2]。
氟擁有所有元素中第三高的第一游離能,僅次於氦和氖[14] ,這使得將電子從氟原子中剝離非常困難。氟的電子親和能很高,僅次於氯[15],具有捕捉一個電子以變成惰性氣體氖的等電子體的趨勢[2]。氟的電負度是所有元素中最高的[16]。氟原子的共價半徑也比較小,大約60 pm,與其在第二週期中相鄰的元素氧和氖相似[17][18][note 1]。
反應[編輯]
氟是自然界電負度最強的元素(3.98鮑林標度),也是氧化性最強的非金屬單質。在常溫下,氟能同絕大多數元素單質發生化合反應,並劇烈放熱。和氫氣即使在-250攝氏度的黑暗中混合也能發生爆炸,故液氟和液氫理論上適合用作高能液體火箭推進劑。氟分子中氟-氟鍵的鍵能和過氧化物中非常容易切斷的過氧鍵類似,比與都低得多。這一性質和氟原子的高電負度使得氟容易分解、高度活躍,與其它非氟原子形成的化學鍵非常強[19][20]。諸如粉末鋼、玻璃碎片、石棉纖維等不活躍物質都可以與氟氣在低溫下快速反應,木頭和水在氟射流中可以自燃[3][21]。
| 外部影片連結 | |
|---|---|
氟和不同的金屬的反應所需要條件不同。常溫下,鹼金屬可以直接與氟反應並引起爆炸,鹼土金屬也可以直接與氟發生劇烈的反應。但是鋁、鐵這樣的金屬在常溫下與氟作用,金屬表面會形成一層氟化物而阻止反應進一步發生。換言之,它們會被氟鈍化。如果要用這些金屬和氟直接反應製備氟化物,需要將它們磨成粉末。[19]貴金屬需要在300–450 °C 的溫度下才能與純氟發生反應[22]。
一些固體非金屬元素如硫、磷等可以與液化氟在低溫下反應[23]。硫化氫[23]與二氧化硫[24]容易與氟發生反應,後者有時甚至會發生爆炸。硫酸的活性較低,需要在較高的溫度下才能與氟反應[25]。氫和一些鹼金屬類似,可以與氟發生爆炸性的反應[26]。碳以炭黑的形式可以在室溫下與氟反應,生成四氟化碳。石墨與氟在高於400 °C發生反應產生非整比化合物氟化石墨,溫度更高時產生氣體的四氟化碳,有時還會發生爆炸[27]。二氧化碳和一氧化碳可以在室溫或者略高於室溫的條件下反應[28]。有機化合物,如甲烷、石蠟,會與氟劇烈反應[29],即使通常不可燃的有機物,如四氯化碳等完全取代的鹵烷也可能發生爆炸[30]。儘管三氟化氮非常穩定,由於氮分子的三鍵鍵能較高,氮氣需要在較高溫度下才能與氟反應[31]。氨與氟能夠發生爆炸性的反應[32][33]。氧與氟在常溫常壓下不發生反應,但是在低溫和低壓時通過放電可以使氟和氧化合,產物在加熱時又會分解為其構成元素[34][35][36]。較重的鹵素和惰性氣體氡容易與氟發生反應,其它惰性氣體中只有氙和氪在特殊條件下才能與氟發生反應。[37]
相態[編輯]
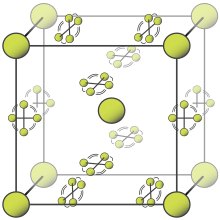
2分子,其它分子被限制在平面中。
在室溫下,氟是一種由雙原子分子構成的氣體[3]。純氟呈淺黃色,有時也被描述為黃綠色[38]。氟有一種特殊的刺激性氣味,濃度在20ppb即可聞到[39]。在−188°C時,氟可以凝結為亮黃色液體,其沸點與氧氣和氮氣類似[40]。
氟有兩種晶相,分別為α相和β相。β相在−220°C結晶,是一種軟且透明的晶體,晶體結構不是其它鹵素所形成的正交晶系結構[41][42],而是與剛結晶的固體氧相同的失序立方晶系結構[40][note 2]。進一步冷卻至−228°C將使處於β相的氟轉化為堅硬不透明的α相氟。α相氟屬於單斜晶系,具有密集的成角度的分子層。β相氟轉化為α相氟要比氟的凝固過程放出更多熱量,相變過程比較劇烈。[41][42][note 3]。
同位素[編輯]
氟只有一種穩定的天然同位素,即包含有10個中子的19
F[46]。該原子具有較高的磁旋比[note 4],原子核能階受磁場的影響比較明顯。又由於氟僅有一種穩定同位素,它經常用於核磁共振。[48]目前一共合成了質量數從13到31的18種氟的放射性同位素,其中半衰期為109.77分鐘的18
F最為穩定。其它同位素的半衰期都小於70秒,大多數都小於半秒鐘。[46]同位素17
F與18
F的衰變方式為正電子發射和電子俘獲,更輕的同位素的衰變方式為質子發射,而更重的同位素的衰變方式為β衰變(最重的同位素還會在β衰變之後發射中子)。[46]目前已知氟有兩種同核異構物,分別是半衰期為162奈秒的18m
F和半衰期為2.2毫秒的26m
F。[46]
存量[編輯]
宇宙存量[編輯]
| 原子序數 | 元素名 | 相對數量 |
|---|---|---|
| 6 | 碳 | 4,800 |
| 7 | 氮 | 1,500 |
| 8 | 氧 | 8,800 |
| 9 | 氟 | 1 |
| 10 | 氖 | 1,400 |
| 11 | 鈉 | 24 |
| 12 | 鎂 | 430 |
作為較輕的元素,氟在宇宙中的豐度相當低,約為400ppb,在各種元素中排名第24。其它的從碳至鎂的輕元素豐度是氟的20倍甚至更多[50]。這是由於恆星核合成的反應過程跳過了氟,而其它反應中生成的氟原子具有較高的核截面,使得氟原子可以與氫原子或氦原子聚變生成氧原子或者氖原子[50][51]。
基於氟只能短暫存在,對氟的留存提出了三種解釋[50][52]:
地球存量[編輯]
氟是地殼中豐度排名第13的元素,其質量豐度為600-700ppm[53]。在地球大氣層中,氟單質可以輕易的和大氣中的水蒸氣發生反應,因此無法在大氣中自然出現[54][55]。氟僅以礦物質的形式出現,工業上主要的含氟礦物質為螢石、氟磷灰石以及冰晶石[53][56]。螢石的化學式為(),有各種顏色,在世界各地都大量分布。它是氟的主要來源,中國和墨西哥是螢石的主要生產國。20世紀早期,美國的螢石開採量在世界領先,但是1995年停止開採[56][57][58][59][60]。儘管氟磷灰石()含有的世界上最多的氟,其中氟的質量分數僅為3.5%,這意味它的大部分都是磷灰石。在美國,少量的氟化合物是通過氟矽酸得到的,這是一種磷酸鹽工業的副產品[56]。曾經直接用於生產鋁的冰晶石()是三種氟礦石中最稀少的也是氟含量最高的一種。格陵蘭島西海岸的商業冰晶石礦於1987年關閉,目前大多數的冰晶石都是人工合成的[56]。
| 主要的含氟礦石 | ||

|

|

|
| 螢石 | 氟磷灰石 | 冰晶石 |
諸如黃玉等其它的礦物質也含有氟。氟化物與其它鹵化物不同,不溶於水且不能以具有商業利益的濃度出現在鹽水中[56]。曾經在火山噴發和地熱噴泉中檢測到了來源不明的痕量氟化物。[61]粉碎的嘔吐石所發出的氣味表明氣體氟可能存在於晶體中[62][63] 。一項2012年的研究報告了嘔吐石中含有質量分數約0.04%的,而這些氟可能來自於礦物質中存在的微量的鈾[63]。
歷史[編輯]
早期發現[編輯]

1529年,格奧爾格·阿格里科拉將螢石描述為在冶煉中用於降低金屬熔點的添加劑[64][65][note 5]。他用拉丁詞fluorés來表示螢石。該名字後來演化為fluorspar,直至fluorite[57][69][70]。螢石的成分後來被確定為氟化鈣[71]。
早在1720年人們就已經開始使用螢石蝕刻玻璃[note 6]。馬格拉夫於1764年從螢石和硫酸的混合物中分離出了一種新物質氫氟酸,他發現該物質腐蝕了玻璃容器[73][74]。瑞典化學家卡爾·威廉·舍勒於1771年重複了該實驗,並將得到的酸性產物命名為fluss-spats-syran(螢石酸)[74][75]。1810年,法國物理學家安德烈-馬里·安培提出氫和一種與氯類似的元素構成了氫氟酸[76]。漢弗里·戴維將這種當時未知的元素命名為氟fluorine,這一名字來自氟酸與其它鹵素的後綴-ine。這個詞經過變形在大多數歐洲語言中使用。希臘語、俄語、以及其他一些語言使用來自希臘語φθόριος 的ftor或其衍生詞[77][78]。氟的元素符號來自於其拉丁文名稱fluorum,在早期論文中也使用Fl作為其符號[79][note 7]。
日文音譯德文Fluor的第一個發音而稱之為「弗素」。19世紀70年代化學家徐壽將、、、、譯為輕氣、養氣、淡氣、弗氣、綠氣,直至1933年,化學家鄭貞文在其主持編寫出版的《化學命名原則》一書中改成氫、氧、氮、氟、氯,一直沿用至今。[80]
分離[編輯]
對氟的研究最初相當危險,有數名19世紀的實驗人員在不幸地接觸到氫氟酸以後失去了生命,他們被稱為氟烈士[note 8]。由於氟和氫氟酸具有極大的腐蝕性,並且當時缺少簡單適用的電解質,分離氟單質的工作被嚴重阻礙了[71][81]。埃德蒙·弗雷米假定可以通過電解純的氫氟酸來產生氟單質,並且設計了一種方法來通過酸化氟化氫鉀來生產無水樣本。然而他發現得到(乾燥)的氟化氫無法導電[71][81][82]。弗雷米以前的學生亨利·莫瓦桑堅持研究,在經過多次的試錯過程後發現氟化氫鉀與無水氟化氫的混合物是一種導體,這樣就可以應用電解法了。為了防止他的電化電池中的鉑被快速腐蝕,莫瓦桑通過特殊的方式將其實驗設備冷卻至極低的溫度,採用更耐腐蝕的鉑銥合金作為電極,並且使用了螢石瓶塞[81][83]。1876年,在經過了74年和多位化學家的努力後,莫瓦桑終於製備出了氟單質[82][84]。
1906年,莫瓦桑在他去世的兩個月前獲得了諾貝爾化學獎[85],評獎委員會對其評價如下:[81]
表彰他對氟元素的研究和分離工作……全世界對您所研究的用於馴服最兇猛的元素的偉大實驗技術表示尊敬。[note 9]
-
莫瓦桑的設備畫像(1887)
-
莫瓦桑的諾貝爾獎照片
用途[編輯]

通用汽車公司的北極品牌(Frigidaire)部門在20世紀20年代末期實驗採用氯氟烴作為製冷劑。1930年,通用汽車與杜邦公司聯合成立了動力化學公司以將氟利昂-12 (CCl
2F
2)推向市場。氟利昂取代了更早的毒性更強的製冷劑,增加了廚房電冰箱的需求,從而變得有經濟利益。到1949年,杜邦公司已經買下了動力化學公司並銷售了若干種其它氟利昂化合物[74][86][87][88]。1938年,在動力化學公司工作的羅伊·J·賓吉在研究製冷劑的事後偶然發現了聚四氟乙烯(特氟龍),該物質高超的化學穩定性與熱穩定性使其快速商業化,在1941年開始了大規模生產[74][86][87]。
氟元素的大規模人工製備開始於二戰期間。德國使用高溫電解的方法生產了成噸的三氟化氯,計劃用於燃燒彈[89];而曼哈頓工程使用大量氟生產六氟化鈾以進行鈾濃縮。由於UF
6一樣具有腐蝕性,氣體擴散工廠使用特殊的材料:薄膜以鎳製造,密封件使用氟聚合物製造,並且使用碳氟化合物作為製冷劑與潤滑劑。新興的核工業驅動了戰後氟化工的發展[90]。
化合物[編輯]
氟可以產生豐富的無機和有機化學反應。它可以與金屬、非金屬以及類金屬發生反應,甚至大多數惰性氣體也都能和氟發生化學反應[91]。通常情況下氟的氧化數為-1[note 10]。氟的高電子親和力導致其容易產生離子鍵;即使產生共價鍵,也容易產生極性,並且幾乎總是單鍵[94][95][note 11]。
金屬[編輯]
鹼金屬離子可以與氟結合,形成易溶的單氟化物,這些化合物具有和氯化物類似的立方體結構[96][97]。除了二氟化鈹鹼土金屬與氟形成的二氟化物也有很強的離子鍵,但是難溶[79]。二氟化鈹表現出一些共價鍵的特徵,並且具有類似石英的結構[98]。稀土元素以及許多其它的金屬多與氟反應生成三氟化物[99][100][101]。
與氟形成的四氟化物開始表現出顯著的共價鍵特徵[102][103]。諸如鋯、鉿等以及若干錒系元素[104]與氟反應得到的產物為離子晶體,熔點較高[105][note 12],而鈦[108]、釩[109]以及鈮與氟得到的產物為聚合體[110],不超過350 °C就會熔解或者分解[111]。五氟化物以及它們的線性聚合物和低聚體錯合物繼續保持了這個趨勢[112][113][114]。目前已知有13種金屬六氟化物[note 13] ,都具有八面體結構,除了液體的MoF
6和ReF
6與氣體的WF
6以外多為易揮發的固體[115][116][117]。七氟化錸是唯一的金屬七氟化物,它使一種低熔點分子固體,具有雙五角錐形分子構型[118]。有很多氟原子的金屬氟化物特別活潑[119]。
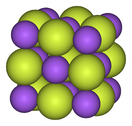
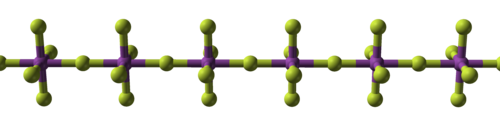
| 金屬氟化物結構演化 | ||
|
|

|
| 氟化鈉,離子晶體 | 五氟化鉍,聚合物 | 七氟化錸, 分子晶體 |
氫[編輯]
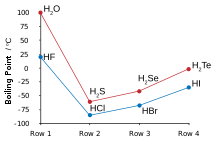
氫與氟相結合生成氟化氫,其中離散的分子通過氫鍵聚成團,從而與氯化氫相比,氟化氫的性質更接近水[120][121][122]。氟化氫的沸點比其它鹵化氫高得多,而且可以與水以任意比例互溶,這一點也和其它鹵化氫不同[123]。氟化氫接觸水以後可以與水結合,生成水合氟化氫,亦稱氫氟酸。與其它為強酸的氫鹵酸不同,氫氟酸在低濃度時為弱酸[124][note 14]。然而,氫氟酸可以腐蝕玻璃,這一點其它氫鹵酸無法做到[126]。
其它活潑的非金屬元素[編輯]

類金屬與非金屬的二氟化物通常是共價化合物,易揮發,具有不同的活潑程度。第三週期以及更重的非金屬可以與氟形成高價氟化物[128]。
三氟化硼具有平面結構,為缺電子分子。作為一種路易斯酸,它可以與諸如氨等路易斯鹼反應形成加合物[129]。四氟化碳為四面體結構,具有惰性[note 15],其它碳族元素與之類似,四氟化矽與四氟化鍺都是四面體結構[130],但是表現為路易斯酸[131][132]。氮族元素與氟反應生成三氟化物,活躍度和鹼性都隨著分子量增加而增加,除了三氟化氮無法水解,不表現出鹼性[133]。磷,砷和銻的五氟化物比其三氟化物更加活潑,五氟化銻是已知最強的中性路易斯酸[112][134][135]。
氧族元素具有不同的氟化物:有報告稱氧、硫和硒可以和氟生成不穩定的二氟化物(二氟化氧是已知的氧具有正氧化數+的罕見化合物之一);硫、硒和碲可以與氟生成四氟化物與六氟化物。氟原子越多、中心原子越輕,氟化物就越穩定,因此六氟化硫相當穩定[136][137]。氯、溴和碘可以和氟反應生成一氟化物、三氟化物以及五氟化物,但是僅有碘可以和氟反應生成七氟化碘[138]。這些氟化物中許多種都可作為強氟原子源,並且三氟化氯在工業應用中需要與和使用氟一樣小心謹慎。[139][140]
惰性氣體[編輯]

惰性氣體具有滿電子殼層,在1962年化學家尼爾·巴特利特報告了六氟合鉑酸氙的合成以前,人們認為它們不與其他元素反應[142] 。從那以後,二氟化氙、四氟化氙、六氟化氙以及多種氧氟化物陸續被合成出來[143]。在其它惰性氣體中,氪可以與氟形成二氟化氪[144],而氡可以與氟形成一種固體,據推測為二氟化氡[145][146]。氟與更輕的惰性氣體形成的二元氟化物極不穩定。在極端條件下,氬可以與氟化氫結合產生氟氬化氫,氦與氖則無法形成穩定的氟化物[147],並且從未觀察到氟化氖的存在[148]。高壓低溫下,曾經檢測到壽命為若干毫秒的氟化氦[147]。
有機化合物[編輯]

碳氟鍵是有機化學中最強的化學鍵[150],這是有機氟化物較為穩定的原因[151][note 16]。自然界中幾乎不存在碳氟鍵,但是該化學鍵在人工化合物得到了應用。該領域的研究通常都具有商業目的[152],涉及到的化合物多種多樣,這也反映出了有機化學的複雜性。
離散分子[編輯]
將烷烴中的氫原子逐漸由更多的氟原子取代將會逐漸產生如下的性質的改變:熔點和沸點降低、密度增加、在烴中的溶解度下降,而整體的穩定性上升。全氟化碳中所有的氫原子都被氟取代了,它在大多數有機溶劑中都無法溶解,通常的條件下只能在液氨中與鈉發生反應[153]。
全氟化合物指的是除了官能基以外所有的氫原子都被氟原子取代的有機化合物[154][note 17],通常是羧酸。這些化合物與全氟化碳有許多共同的特徵,例如穩定性、疏水性等等[156],而官能基則增加了他們的活躍度,使得他們可以附著於表面或者作為表面活性劑[157]。特別的,氟表面活性劑可以降低水的表面張力,效果比烴基活性劑更好。氟調聚物的官能基附近有一些未氟化的碳原子,它們也常被認為是全氟化物[156]。
聚合物[編輯]
由於氟取代了單體中的氫原子,對應的聚合物的穩定性也相應的增加了,通常情況下其熔點也會增加[158]。聚四氟乙烯是最簡單的氟聚合物,它是與聚乙烯對應的全氟化合物,結構單元為–CF
2–。該物質具有所預期的因氟取代氫所造成的變化,但是其非常高的熔點使得它難以造型。只有氟單質、三氟化氯、五氟化氯和熔融鹼金屬可以在高溫下腐蝕聚四氟乙烯。氟化乙丙烯以三氟甲基取代了一些氟原子,全氟烷氧基烷烴以三氟甲氧基官能基取代一些氟原子[159],而全氟磺酸則包含有含有磺酸官能基的全氟醚側鏈[160][161]。其它氟聚合物保留了一些氫原子,聚偏氟乙烯中一半的氫原子為氟原子所取代,聚氟乙烯則有四分之一的氫原子被取代,而二者具有和聚四氟乙烯相似的性質[162]。
生產[編輯]
工業生產[編輯]

莫瓦桑所提出的通過電解氟化氫與氟化鉀混合物製備氟的方法可以用於工業生產,其中的氫離子在鋼製成的陰極容器中還原生成氫氣,而氟離子在碳制陽極被氧化生成氟氣。陰極陽極之間的電壓大約為8-12伏[58][163]。電解的溫度有所提高,KF·2HF 在70 °C(158 °F)熔化,而電解溫度為70—130 °C(158—266 °F)。氟可以使用具有鈍化內層的鋼罐在200 °C(392 °F)以下儲存,否則將使用鎳[74][164]。調節閥與管道使用鎳製造,而管道也可以使用蒙乃爾銅鎳合金製造[165]。使用氟必須對設備經常鈍化,並且嚴格禁止接觸水和油脂。在實驗室中,在低溫和無水的條件下可以使用玻璃器皿裝氟氣[165],某些文獻推薦使用鎳-蒙乃爾-聚四氟乙烯系統[166]。
純化學方法[編輯]
在準備莫瓦桑成功分離氟100周年的紀念會議的時候,卡爾·O·克里斯特認為通過化學方法應當可以製備氟。這是因為一些金屬氟陰離子對應的中性物質 不穩定,這樣他們的酸化反應很有可能引起氧化反應。因此他設計了一種方法能夠在大氣壓力下以較高產率獲得氟[167]:
克里斯特後來認為該反應「已經為人所知超過100年,即使莫瓦桑也可能會想到這一方法」[168]。直至2008年,某些文獻仍然認為氟過於活躍,無法通過任何化學方法分離[169]。
工業應用[編輯]
螢石礦的開採是全球氟的最大來源,1989年達到了560萬噸的礦石開採量頂點。限制使用氯氟烴導致螢石產量下降,1994年下降到了360萬噸。隨後產量開始上升,2003達到了產量450萬噸、產值55億美元的規模。後續報告估計2011年全球氟化工的銷售額達到了150億美元,並且預測2016年將開採350萬至590萬噸礦石,產值將至少200億美元[74][170][171][172][173]。泡沫浮選將開採出的螢石以相同比例分為兩個主要的冶金等級:純度為60-85%的冶金級螢石和純度超過97%的酸級螢石。冶金螢石几乎全部用於鋼鐵冶煉,而酸級螢石主要被轉化為關鍵的工業中間體氟化氫[58][74][174]。


6變壓器
每年全世界至少生產17000噸氟。氟的成本與六氟化鈾或六氟化硫類似,每千克大約5-8美元,但是處理它的難度使其價格翻倍,而且大多數使用六氟化鈾或者六氟化硫的工藝在垂直整合下都採用原地生產的方式[175]。
全世界對氟的最大的應用是在核燃料循環中生產,每年消耗近7000噸氟。首先二氧化鈾與氫氟酸反應生成四氟化鈾,然後四氟化鈾被氟氣氟化生成[175]。由於氟只有一種穩定的同位素,六氟化鈾分子的任何質量區別都是由或者造成的。這使得可以通過氣體擴散法或者氣體離心法對鈾進行濃縮[3][58]。每年大約有6000噸氟用於生產惰性電介質六氟化硫,該物質可以用於高壓變壓器與斷路器,這樣就不必在充油設備中使用危險的多氯聯苯了[176]。電子產品中會使用一些氟化合物:在化學氣相沉積中會使用六氟化鎢或者六氟化錸,在電漿蝕刻中會使用聚四氟乙烯[177][178][179]和三氟化氮[58]。氟也被用於有機氟化物合成,但是由於其特別活潑,通常有必要先將其轉化為更溫和的、或以進行更精確的氟化。含氟醫藥通常使用四氟化硫代替氟[58]。
無機氟[編輯]

每煉一噸鋼或其它鐵合金大約需要3.5千克冶金級螢石,氟離子降低了鋼鐵的熔點與粘性[58][180]。除了用於作為搪瓷和焊條塗層的添加劑以外,大多數酸級螢石與硫酸反應生成氫氟酸,而氫氟酸將會用於酸洗、玻璃蝕刻以及烷烴裂化[58]。氫氟酸產量的三分之一都用於合成冰晶石與三氟化鋁,這是提煉鋁的霍爾-埃魯法中的重要助熔劑。由於它們偶爾會與熔煉設備發生反應,需要及時補充它們。每生產一噸鋁大約需要23千克助熔劑[58][181]。氟矽酸鹽消耗了第二多的氟。氟矽酸鈉用於氟化飲用水和洗衣廢水處理,並且是合成冰晶石與四氟化矽的過程中的中間體[182]。其它重要的無機氟化物包括氟化鈷、氟化鎳以及氟化銨[58][97][183]。
有機氟[編輯]
有機氟消耗了螢石開採量的20%以及氫氟酸產量的40%,其中氣體製冷劑占主要部分,而氟聚合物的市場份額在不斷增長[58][184]。表面活性劑的應用較少,但是年產值超過10億美元[185]。由於直接讓烴與氟在高於−150 °C的條件下反應相當危險,工業上的氟碳化合物都是間接生產的,多通過鹵素交換反應來完成,例如史瓦茨氟化反應在催化劑的作用下使氯烴與氟化氫反應,將氯原子替換為氟原子。電化學氟化將烴在氟化氫中電解,而福勒工藝使用諸如三氟化鈷等的固體氟化物處理烴類[86][186]。
氣體製冷劑[編輯]
鹵化製冷劑在非正式語境中常被稱為氟利昂,由R-數標示,該數字標示了氟、氯、碳、氫的數量[58][187]。R-11、R-12、R-114等氟氯烴曾經占據了有機氟產量的主要部分,在20世紀80年代產量達到了頂峰。這些氟化物用於空調系統、推進劑或者用作溶劑。在國際上禁止使用以後,21世紀開始的產量已經下降至了峰值的十分之一[58]。為了取代氟利昂而設計出的氫氯氟烴(HCFC)和氫氟烴(HFC)的合成消耗了有機行業中超過90%的氟。重要的氫氯氟烴包括R22與R-141b。主要的氫氟碳化合物包括R-134a[58],而HFO-1234yf漸漸成為主流,這主要是因為HFO-1234yf的全球暖化潛勢僅為R-134a的1%[188]。
氟聚合物[編輯]

2006年與2007年大約生產了18萬噸氟聚合物,產值達到每年35億美元[189]。預計全球市場在2011年略少於60億美元,到2016年將以每年6.5%的速度增長[190]。氟聚合物僅能通過自由基聚合形成[158]。
聚四氟乙烯(PTFE)通常被稱作特氟龍,這是杜邦公司給它起的名字[191]。它占據了全世界氟聚合物產量的60-80%[189]。由於聚四氟乙烯是優秀的電介質,其最大應用就是電氣絕緣。它在化學工業中也用於管道、油管以及墊片的塗料以防止腐蝕。聚四氟乙烯的另一重要應用是用於體育館房頂的玻纖布塗層。聚四氟乙烯的主要消費應用是不粘廚具[191]。膨體聚四氟乙烯(ePTFE)是一種有細孔的薄膜,有時也被稱為戈爾特斯(為其商標名),它常被用於製造雨衣、防護服以及過濾器。膨體聚四氟乙烯纖維可以製成機械密封裝置和灰塵過濾器[191]。其它氟聚合物,包括氟化乙烯丙烯與聚四氟乙烯的性質類似,並且可以作為其替代品。這些氟聚合物更加容易成型,但是成本更高,熱穩定性更低。兩種氟聚合物製成的薄膜可以取代太陽能電池中的玻璃[191][192]。
成本較高但耐化學腐蝕的氟化離子交聯聚合物可以用作電化學電池中的薄膜,其中最早也是最重要的物質為全氟磺酸。全氟磺酸是在20世紀60年代發展出來的,首先用於宇宙飛船的燃料電池材料,隨後取代了汞基氯鹼工藝電池。進來,燃料電池的應用隨著將質子交換薄膜燃料電池安裝在汽車上的努力重新獲得了重視[193][194][195]。氟橡膠為交聯的氟聚合物的混合物,主要用於O形環[191]。全氟丁烷 C
4F
10被用作滅火劑[196]。
表面活性劑[編輯]
含氟表面活性劑為小分子含氟有機物,用於防水和防鏽。儘管其價格昂貴,其年產值在2006年已達10億美元;思高潔在2000年就已達到3億美元的銷售額[185][197][198]。含氟表面活性劑在整個表面活性劑市場中占據份額較少,市場中的大部分為以便宜得多的烴為基礎的產品。由於配置成本高昂,2006年對含氟表面活性劑在塗料中的應用估值僅為1億美元[185]。
農藥[編輯]
大約30%的農藥都含有氟[199],大多數是除草劑與殺菌劑,還有一些是植物激素。與含氟醫藥相似,氟原子經常取代一個單獨的原子或者最多一個三氟甲基官能基,這種改變可以增加在生物體內停留時間,增強細胞膜穿透能力,並且可以改變分子識別[200]。氟樂靈是一個突出的例子,該農藥在美國大規模用作除草劑[200][201],但是懷疑它具有致癌作用,在許多歐洲國家都被禁止使用[202]。氟乙酸鈉是一種哺乳動物毒劑,其中乙酸上的兩個氫原子分別由氟和鈉取代。在三羧酸循環過程中,該物質會取代乙酸從而干擾細胞新陳代謝。該物質首先與19世紀晚期合成,在20世紀早期發現了其殺蟲劑的作用,隨後開始使用。紐西蘭是該物質的最大消費者,用它來殺死來自澳大利亞的入侵物種刷尾負鼠以保護鷸鴕[203]。歐洲和美國都禁止使用氟乙酸鈉[204][205][note 18]。
醫療應用[編輯]
牙齒護理[編輯]
20世紀中葉以來的研究表明,外用氟化物可以減少齲齒。最初研究認為這是由於牙釉質羥基磷灰石轉變為了更耐磨的氟磷灰石,但是對預先氟化的牙齒的研究否定了這一假設。目前解釋這一現象的理論是在齲齒較小時,氟化物能夠促進牙釉質的生長[206]。在研究了生活在飲用水中存在天然氟化物的地區的兒童以後,1940年開始通過在公共供水中添加氟化物並控制其含量來防止齲齒[207]。目前全球人口的6%接受了氟化飲用水,而在美國這一比例更是達到了三分之二[208][209]。發表於2000年和2007年的學術文獻綜述認為,飲水氟化明顯的降低了兒童中齲齒發生的概率[note 19]。儘管飲水氟化得到了學術研究的支持,除了良性的氟牙症外,並無顯著副作用[212],在倫理和安全層面仍存在著針對飲水氟化的反對意見[209][213]。由於目前生活中存在著其它氟化物來源,飲水氟化的效果有所降低,但在低收入群體中仍存在可觀測到的作用[214]。單氟磷酸鈉以及氟化鈉、氟化亞錫常常作為氟化牙膏的成分。1995年,美國首先使用這些物質,而目前在已開發國家,氟化物在漱口水、凝膠、泡沫等,都有廣泛應用[214][215]。
製藥[編輯]
20%的現代藥物中都含有氟[216]。含氟藥物阿托伐他汀在2011年成為通用名藥物以前在所有藥物中銷售額居於榜首[217]。治療哮喘的組合處方藥物舒利迭,在2000年代中期銷售額也排在前10,其中的兩種活性成分之一氟替卡松也是一種氟化物[218]。由於碳氟鍵非常穩定,許多藥物氟化是為了降低活躍度以延長給藥週期[219]。由於碳氟鍵較碳氫鍵疏水性更強,氟化還能增加親油性,這可以幫助藥物穿過細胞膜,提高生物利用度[218]。
三環類抗抑鬱藥以及其他20世紀80年代早期的抗抑鬱藥因其無選擇性的干擾除了羥色胺以外的神經遞質而具有許多副作用。而氟化藥物氟西汀則因其選擇性而成為第一類能夠避免這些問題的藥物之一。目前許多抗抑鬱藥物都經過類似的氟化處理,包括選擇性血清素再攝取抑制劑:酞普蘭、其異構物依他普侖、以及氟伏沙明和帕羅西汀[220][221]。人造廣譜抗生素喹諾酮類藥物通常也會通過氟化來提高療效。這些藥物包括環丙沙星和左氧氟沙星[222][223][224][225]。在類固醇藥物中也會使用氟[226]:氟氫可的松是可以使血壓升高的鹽皮質激素;去炎松與地塞米松是很強的糖皮質激素[227]。大多數吸入型麻醉劑都是重度氟化的。其原型氟烷在同時代藥物中更為穩定與有效。後來諸如七氟醚、地氟醚等氟化醚化合物比氟烷更好,它們基本不溶於血液,可以使人更快清醒[228][229]。
PET掃描[編輯]

F PET掃描
18
F常作為正電子發射計算機斷層掃描中的放射性示蹤劑,其約兩個小時的半衰期足夠將其從生產設備運輸至成像中心了[230]。氟代脫氧葡萄糖是最常用的示蹤劑[230],在經過靜脈注射後,會由諸如大腦和大多數惡性腫瘤等最消耗葡萄糖的器官組織吸收[231]。隨後,計算機輔助斷層掃描可以用來對細節成像[232]。
攜帶氧氣[編輯]
液體氟化碳可以攜帶比血液更多的氧氣或者二氧化碳,因而在人工血和液體呼吸方面引起了很大的關注[233]。由於氟化碳正常情況下無法與水混合,必須將它們混合成為乳狀液(全氟化碳小液滴懸浮於水中)以用作血液[234][235]。Oxycyte就是一種已經通過初步臨床試驗的人工血液產品[236]。這些物質可以提高運動員的耐力,因此在運動中禁止使用。1998年,一位瀕臨死亡的自行車運動員引起了對濫用人工血液的調查[237][238]。純的全氟化碳液體呼吸的應用(使用的是純全氟化碳液體,而不是與水混合的乳狀液)包括輔助燒傷患者以及肺功能發育不全的早產兒。考慮的液體呼吸方案包括將肺部分填滿或者全部填滿,但是僅前者經過了人體測試[239]。製藥聯盟的努力使得該方案達到了臨床測試的水平,但是由於實驗結果並不比正常的治療方案好,最終放棄了該方案[240]。
生物作用[編輯]

氟並非人或者其它哺乳動物必須的元素。少量的氟可能對增加骨強度有益,但是該理論尚未確立。由於日常環境中有很多微量氟的來源,氟缺乏的可能性僅能通過人工飲食來實現[241][242]。在微生物和植物體內曾經發現過有機氟[61],但是在動物體內尚未發現[243]。最常見的天然有機氟產物是氟乙酸,可以幫助植物抵禦食草動物。至少有40種植物含有該物質,這些植物分布在非洲、澳大利亞以及巴西[204]。其它的天然有機氟產物包括末端氟化脂肪酸、氟丙酮以及2-氟代檸檬酸[243]。2002年在細菌中發現了建立氟碳鍵的酶(腺苷甲硫胺酸氟化物合酶)[244]。
毒性[編輯]
氟元素對生物活體有劇毒。氰化氫在濃度為50ppm時就會對人體產生影響,而氟所需要的濃度更低[246],影響與氯相似[247]:在濃度超過25ppm時對眼睛與呼吸系統有強烈刺激,對肝臟與腎臟可以造成損傷,這一濃度也是氟的即刻性損傷或致死濃度[248][249]。氟的濃度達到100ppm時,眼睛與鼻子將會受到嚴重損傷[248],若濃度達到1000ppm,數分鐘的呼吸即可致命[250]。氰化氫的濃度達到270ppm即可使人在數分鐘內死亡[251]。
氫氟酸[編輯]

儘管氫氟酸是一種弱酸,它可以通過接觸產生比諸如硫酸等強酸更嚴重的傷害。這一部分原因是因為它在水溶液是電中性的,故無論是通過呼吸道、消化道還是皮膚吸收的氟化氫都能迅速穿透組織。1984-1994年間,至少有9名美國工人死於與氫氟酸接觸的事故中。氫氟酸可以與血液里的鈣和鎂發生反應,導致低鈣血症,並且可能因心律失常導致死亡[253]。與氟化氫接觸生成的不易溶解的氟化鈣可以觸發強烈的疼痛[254],若燒傷面積超過160平方厘米將導致嚴重的全身中毒[255]。
氫氟酸燒傷的症狀可能在一開始時不明顯,對於50%的溶液,需要8小時才有明顯症狀,對於更稀的溶液則或許需要24小時。因為氟化氫影響了神經功能,所以氫氟酸的燒傷病患可能在一開始時並無痛感。 當皮膚接觸到氫氟酸時,及時用流水沖洗10-15分鐘並移除被污染的衣物可以有效減少傷害。[256]通常,在進一步的處理中,會使用葡萄糖酸鈣。其提供鈣離子與氟離子形成不可溶的氟化鈣。皮膚燒傷可以施用2.5%葡萄糖酸鈣凝膠或者特製清洗溶液。[257][258][259]氫氟酸吸入需要進一步的治療,可能需要靜脈注射葡萄糖酸鈣。但不可使用氯化鈣,因為它可能造成更複雜的情況。可能需要切除或截除受侵染的部位。[255][260]
氟離子[編輯]
可溶氟化物具有中等毒性,對於成人來說,氟化鈉的致死劑量為5-10克,也就是說氟離子的致死劑量為32-64毫克每千克體重[261]。五分之一的致死劑量會對健康產生不利影響,而慢性的過量食用會導致氟骨症,這是一種影響了亞洲和非洲數百萬人的疾病[262][263]。通過消化系統攝入氟化物會在胃內形成氫氟酸,而氫氟酸很容易被小腸吸收。在通過尿排出之前,它將穿過細胞膜,與鈣結合併干擾多種酶的作用。接觸極限值將通過檢測人體排出氟離子的能力的尿檢來確定[262][264]。
大多數氟中毒都是由於偶然攝入了含有無機氟化物的殺蟲劑造成的[265]。而目前與氟中毒有關的打給毒藥控制中心的電話多是由於攝入了含氟牙膏[262]。飲水加氟設備的故障是另一個氟中毒的原因,一次發生於阿拉斯加的事故導致近300人中毒,並且一人死亡[266]。牙膏帶來的風險對幼年兒童尤其嚴重,因此疾病控制預防中心建議監督六歲以下的兒童刷牙以防止吞咽牙膏[267]。一個區域性調查研究調查了一年內發生的一共87件低於十歲的兒童氟中毒事件,其中包括了一起因攝入殺蟲劑導致死亡的案例,除了30%的人胃痛,大多數都沒有症狀[265]。一項更大的覆蓋全美的調查結論相似,80%的氟中毒案例都包含有低於6歲的兒童,幾乎沒有嚴重的案例[268]。
環境問題[編輯]
大氣層[編輯]
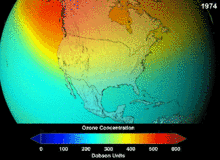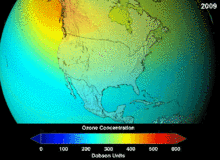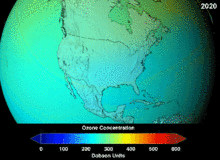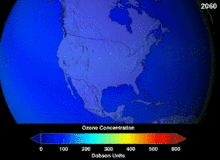
由於氯氟烴與溴氟烴的臭氧層破壞潛能,簽署於1987年的蒙特婁議定書對這兩種物質的使用做出了嚴格規定。由於碳氟鍵的穩定性,這兩種物質在到達海拔較高的平流層之前無法分解,而在平流層他們釋放出來的氯原子與溴原子將攻擊臭氧分子[270]。有預測警告說,儘管有了禁令,臭氧層全面恢復仍需要數代人的時間[271][272]。目前氫氯氟烴成為氯氟烴的替代品,其臭氧層破壞潛能僅為氯氟烴的10%[273],並且計劃到2030-2040年,將以不含氯、不會破壞臭氧層的氫氟烴替換氫氯氟烴[274]。2007年要求已開發國家將該替換日期提前至2020年[275]。美國國家環境保護局已經在2003年禁止了氫氯氟烴的生產[274]。氣體氟碳化合物通常是溫室氣體,其全球暖化潛能約為100至10000。六氟化硫的全球暖化潛能約為20000[276]。HFO-1234yf的全球暖化潛能為4,遠遠小於潛能為1340的標準製冷劑HFC-134a,因而吸引了全球的需求[188]。
生物持久性[編輯]
由於碳氟鍵很強,有機氟化物具有較長的生物持久性。由於其酸性官能基而不易溶於水的全氟烷磺酸就是持久性有機污染物[278]。全氟辛烷磺酸與全氟辛酸是最常研究的物質[279][280][281]。全氟烷磺酸在全世界的生物體內都能發現其蹤跡,從北極熊到人類,而已知全氟辛烷磺酸與全氟辛酸存在於母乳和新生兒的血液中。一項2013年的調查表明,地下水與土壤中的全氟烷磺酸與人類活動有一些相關性,但是並沒有明確的結果表明哪一種化學物質會占主導地位;較高的全氟辛烷磺酸和較高全氟辛酸呈現相關性[279][280][282]。在人體內,全氟烷磺酸會與諸如血清白蛋白等的蛋白質相結合,並且具有在通過腎臟排出之前在人體內的肝臟和血液中聚集的趨勢[279][280][283]。大劑量的全氟辛烷磺酸和全氟辛酸可以導致癌症,並且導致新生幼鼠的死亡,但是還沒有關於在當前的暴露水平下其對人影響的人體研究。[279][280][283]
注釋[編輯]
- ^ 來源對氧、氟和氖的共價半徑有爭議,因此不能精確比較。
- ^ α相的氟的分子具有規則排列,是一種晶體,但是其分子沒有特定的取向。β相的氟分子具有固定位置和最小的旋轉不確定度。參見[43]以了解α相氟晶體結構的一些細節。[44][45]
- ^ 相變過程會產生巨響,並使樣本和容器破裂。
- ^ 磁矩與角動量之比稱為磁旋比。原子核經常可以不嚴格的想像為繞著一個軸自轉的帶電陀螺,通常這種自旋會帶給原子核角動量和磁矩。角動量來自於原子核的質量,而磁矩則來自於旋轉的全部或者部分電荷。[47]
- ^ 巴希爾·瓦倫丁可能在15世紀末就描述了螢石,但由於這篇文章直到200年後才被發現而存疑。[66][67][68]
- ^ 另說1670年,Partington[72]和Weeks[71]給出不同的說法。
- ^ Fl從2012年起表示第114號元素鈇。
- ^ 漢弗里·戴維、約瑟夫·路易·給呂薩克、路易斯·賈奎斯·瑟納德和愛爾蘭化學家aThomas和George Knox都因此受傷,而比利時化學家Paulin Louyet和法國化學家Jérôme Nicklès則死於氟。莫瓦桑也經歷過嚴重的氫氟酸中毒。[71][81]
- ^ 同時他也因他發明的電弧爐而獲獎。
- ^ F
2中的氟被定義為具有氧化數0。不穩定的F−
2 和 F−
3具有中間氧化態,它們在40 K即分解[92]。F+
4以及其它一些類似的物質據預測為穩定的[93]。 - ^ 亞穩態的一氟化硼和一氟化氮具有更高階的共價鍵,一些金屬錯合物使用其作為橋接配位基。氫鍵是另一個可能性。
- ^ ZrF
4的熔點為932 °C(1,710 °F)[106],HfF
4在968 °C(1,774 °F)下升華[103],UF
4的熔點為1,036 °C(1,897 °F)。[107] - ^ 這13種金屬元素為鉬、鎝、釕、銠、鎢、錸、鋨、銥、鉑、釙、鈾、錼和鈽。
- ^ 參見這個參考資料。[125]
- ^ 四氟化碳形式上是有機化合物,但為了與SiF
4和GeF
4比較而被包括到這個章節中,而不是我們討論更複雜的化合物的有機化合物章節。 - ^ 有機全氟化物十分穩定,但單氟化物的反應性相對活潑
- ^ 該術語並不精確,全氟化物質也是常用的術語。[155]
- ^ 美國的羊和牛可能還會使用氟乙酸鈉來對付郊狼等掠食者。
- ^ [210],另見總結[211]
參考文獻[編輯]
- ^ Prohaska, Thomas; Irrgeher, Johanna; Benefield, Jacqueline; Böhlke, John K.; Chesson, Lesley A.; Coplen, Tyler B.; Ding, Tiping; Dunn, Philip J. H.; Gröning, Manfred; Holden, Norman E.; Meijer, Harro A. J. Standard atomic weights of the elements 2021 (IUPAC Technical Report). Pure and Applied Chemistry. 2022-05-04. ISSN 1365-3075. doi:10.1515/pac-2019-0603 (英語).
- ^ 2.0 2.1 2.2 2.3 2.4 2.5 Jaccaud 2000,第381頁.
- ^ 3.0 3.1 3.2 3.3 Jaccaud 2000,第382頁.
- ^ 4.0 4.1 4.2 4.3 Compressed Gas Association. Handbook of compressed gases. Springer. 1999: 365. ISBN 9780412782305.
- ^ 5.0 5.1 Dean 1999,第3.29頁.
- ^ Haynes, William M. (編). Handbook of Chemistry and Physics 92nd. Boca Raton: CRC Press. 2011: 4.121. ISBN 978-1-4398-5511-9.
- ^ Himmel, D.; Riedel, S. After 20 Years, Theoretical Evidence That 'AuF7' Is Actually AuF5·F2. Inorganic Chemistry. 2007, 46 (13). 5338–5342. doi:10.1021/ic700431s.
- ^ 8.0 8.1 8.2 Dean 1999,第4.6頁.
- ^ Dean 1999,第4.35頁.
- ^ Kim, Sung-Hoon. Functional dyes. Elsevier. 2006: 257. ISBN 9780444521767.
- ^ Mackay, Mackay & Henderson 2002,第72頁.
- ^ Yaws, Carl L.; Braker, William. Fluorine. Matheson Gas Data Book 7th. Parsippany: Matheson Tri-Gas. 2001: 385. ISBN 978-0-07-135854-5.
- ^ Lee, Stephen; et al. Monofluoroacetate-Containing Plants That Are Potentially Toxic to Livestock. Journal of Agricultural and Food Chemistry (ACS Publications). 2014, 62 (30): 7345–7354. PMID 24724702. doi:10.1021/jf500563h.
- ^ Dean 1999,第564頁.
- ^ Lide 2004,第10.137–10.138頁.
- ^ Moore, John W.; Stanitski, Conrad L.; Jurs, Peter C. Principles of Chemistry: The Molecular Science. Belmont: Brooks/Cole. 2010: 156. ISBN 978-0-495-39079-4.
- ^ Cordero, B.; Gómez, V.; Platero-Prats, A. E.; Revés, M.; Echeverría, J.; Cremades, E.; Barragán, F.; Alvarez, S. Covalent Radii Revisited. Dalton Transactions. 2008, (21): 2832–2838. PMID 18478144. doi:10.1039/b801115j.
- ^ Pyykkö, Pekka; Atsumi, Michiko. Molecular Double-Bond Covalent Radii for Elements Li–E112. Chemistry: A European Journal. 2009, 15 (46): 12770–9. PMID 19856342. doi:10.1002/chem.200901472.
- ^ 19.0 19.1 Greenwood & Earnshaw 1998,第804頁.
- ^ Macomber, Roger. Organic chemistry 1. Sausalito: University Science Books. 1996: 230. ISBN 978-0-935702-90-3.
- ^ Nelson, Eugene W. 'Bad Man' of The Elements. Popular Mechanics. 1947, 88 (2): 106–108, 260 [2022-10-21]. (原始內容存檔於2023-07-22).
- ^ Lidin, Molochko & Andreeva 2000,第442–455頁.
- ^ 23.0 23.1 Wiberg, Wiberg & Holleman 2001,第404頁.
- ^ Patnaik 2007,第472頁.
- ^ Aigueperse 2000,第400頁.
- ^ Greenwood & Earnshaw 1998,第76, 804頁.
- ^ Kuriakose, A. K.; Margrave, J. L. Kinetics of the Reactions of Elemental Fluorine. IV. Fluorination of Graphite. Journal of Physical Chemistry. 1965, 69 (8): 2772–2775. doi:10.1021/j100892a049.
- ^ Hasegawa, Y.; Otani, R.; Yonezawa, S.; Takashima, M. Reaction Between Carbon Dioxide and Elementary Fluorine. Journal of Fluorine Chemistry. 2007, 128 (1): 17–28. S2CID 95754841. doi:10.1016/j.jfluchem.2006.09.002. hdl:10098/1665
 .
.
- ^ Lagow, R. J. The Reactions of Elemental Fluorine; A New Approach to Fluorine Chemistry (PDF) (學位論文). Ann Arbor: UMI: 64–78. 1970 [2022-10-21]. (原始內容存檔 (PDF)於2020-07-26).
- ^ Lidin, Molochko & Andreeva 2000,第252頁.
- ^ Tanner Industries. Anhydrous Ammonia: (MSDS) Material Safety Data Sheet. tannerind.com. January 2011 [2013-10-24]. (原始內容存檔於2020-08-06).
- ^ Morrow, S. I.; Perry, D. D.; Cohen, M. S. The Formation of Dinitrogen Tetrafluoride in the Reaction of Fluorine and Ammonia. Journal of the American Chemical Society. 1959, 81 (23): 6338–6339. doi:10.1021/ja01532a066.
- ^ Emeléus, H. J.; Sharpe, A. G. Advances in Inorganic Chemistry and Radiochemistry 16. New York: Academic Press. 1974: 111. ISBN 978-0-08-057865-1.
- ^ Wiberg, Wiberg & Holleman 2001,第457頁.
- ^ Brantley, L. R. Squires, Roy; Clarke, Arthur C. , 編. Fluorine. Pacific Rockets: Journal of the Pacific Rocket Society (South Pasadena: Sawyer Publishing/Pacific Rocket Society Historical Library). 1949, 3 (1): 26. ISBN 978-0-9794418-5-1.
- ^ Khriachtchev, L.; Pettersson, M.; Runeberg, N.; Lundell, J.; Räsänen, M. A Stable Argon Compound. Nature. 2000, 406 (6798): 874–876 [2022-10-21]. Bibcode:2000Natur.406..874K. PMID 10972285. S2CID 4382128. doi:10.1038/35022551. (原始內容存檔於2016-04-13).
- ^ Burdon, J.; Emson, B.; Edwards, A. J. Is Fluorine Gas Really Yellow?. Journal of Fluorine Chemistry. 1987, 34 (3–4): 471–474. doi:10.1016/S0022-1139(00)85188-X.
- ^ Lide 2004,第4.12頁.
- ^ 40.0 40.1 Dean 1999,第523頁.
- ^ 41.0 41.1 Young, David A. Phase Diagrams of the Elements (PDF) (報告). Lawrence Livermore Laboratory. 1975 [2011-06-10]. (原始內容存檔於2020-08-13).
- ^ 42.0 42.1 Barrett, C. S.; Meyer, L.; Wasserman, J. Argon—Fluorine Phase Diagram. The Journal of Chemical Physics. 1967, 47 (2): 740–743. Bibcode:1967JChPh..47..740B. doi:10.1063/1.1711946.
- ^ Pauling, L.; Keaveny, I.; Robinson, A. B. The Crystal Structure of α-Fluorine. Journal of Solid State Chemistry. 1970, 2 (2): 225–227. Bibcode:1970JSSCh...2..225P. doi:10.1016/0022-4596(70)90074-5.
- ^ Bürgi, H. B. Motion and Disorder in Crystal Structure Analysis: Measuring and Distinguishing them. Annual Review of Physical Chemistry. 2000, 51: 275–296. Bibcode:2000ARPC...51..275B. PMID 11031283. doi:10.1146/annurev.physchem.51.1.275.
- ^ Müller, Peter. 5.067 Crystal Structure Refinement (PDF). Cambridge: MIT OpenCourseWare. 2009 [2013-10-13]. (原始內容存檔 (PDF)於2020-08-06).
- ^ 46.0 46.1 46.2 46.3 Kondev, F. G.; Wang, M.; Huang, W. J.; Naimi, S.; Audi, G. The NUBASE2020 evaluation of nuclear properties (PDF). Chinese Physics C. 2021, 45 (3): 030001. doi:10.1088/1674-1137/abddae.
- ^ Vigoureux, P. The Gyromagnetic Ratio of the Proton. Contemporary Physics. 1961, 2 (5): 360–366. Bibcode:1961ConPh...2..360V. S2CID 5092147. doi:10.1080/00107516108205282.
- ^ Meusinger, Reinhard; Chippendale, A. Margaret; Fairhurst, Shirley A. Nuclear Magnetic Resonance and Electron Spin Resonance Spectroscopy. Weinheim: Wiley-VCH: 752, 754. 2012. doi:10.1002/14356007.b05_471.
- ^ Cameron, A. G. W. Abundance of the Elements in the Solar System (PDF). Space Science Reviews. 1973, 15 (1): 121–146. Bibcode:1973SSRv...15..121C. S2CID 120201972. doi:10.1007/BF00172440. (原始內容 (PDF)存檔於2011-10-21).
- ^ 50.0 50.1 50.2 Croswell, Ken. Fluorine: An element–ary Mystery. Sky and Telescope. September 2003 [2013-10-17]. (原始內容存檔於2016-03-04).
- ^ Clayton, Donald. Handbook of Isotopes in the Cosmos: Hydrogen to Gallium. New York: Cambridge University Press. 2003: 101-104. ISBN 978-0-521-82381-4.
- ^ Renda, Agostino; Fenner, Yeshe; Gibson, Brad K.; Karakas, Amanda I.; Lattanzio, John C.; Campbell, Simon; Chieffi, Alessandro; Cunha, Katia; Smith, Verne V. On the origin of fluorine in the Milky Way. Monthly Notices of the Royal Astronomical Society. 2004, 354 (2): 575–580. Bibcode:2004MNRAS.354..575R. S2CID 12330666. arXiv:astro-ph/0410580
 . doi:10.1111/j.1365-2966.2004.08215.x.
. doi:10.1111/j.1365-2966.2004.08215.x.
- ^ 53.0 53.1 Jaccaud 2000,第384頁.
- ^ Schulze-Makuch, D.; Irwin, L. N. Life in the Universe: Expectations and Constraints 2nd. Berlin: Springer-Verlag. 2008: 121. ISBN 978-3-540-76816-6.
- ^ Haxel, G. B.; Hedrick, J. B.; Orris, G. J. Stauffer, P. H.; Hendley II, J. W. , 編. Rare Earth Elements—Critical Resources for High Technology, Fact Sheet 087-02 (報告). U.S. Geological Survey. 2005 [2014-01-31]. (原始內容存檔於2020-07-19).
- ^ 56.0 56.1 56.2 56.3 56.4 Greenwood & Earnshaw 1998,第795頁.
- ^ 57.0 57.1 Norwood, Charles J.; Fohs, F. Julius. Kentucky Geological Survey, Bulletin No. 9: Fluorspar Deposits of Kentucky. Kentucky Geological Survey. 1907: 52.
- ^ 58.00 58.01 58.02 58.03 58.04 58.05 58.06 58.07 58.08 58.09 58.10 58.11 58.12 58.13 Villalba, Gara; Ayres, Robert U.; Schroder, Hans. Accounting for Fluorine: Production, Use, and Loss. Journal of Industrial Ecology. 2008, 11: 85–101. S2CID 153740615. doi:10.1162/jiec.2007.1075.
- ^ Kelly, T. D.; Miller, M. M. Historical Fluorspar Statistics. U.S. Geological Service. 2005 [2014-02-10]. (原始內容存檔於2013-05-22).
- ^ Lusty, P. A. J.; Brown, T. J.; Ward, J.; Bloomfield, S. The Need for Indigenous Fluorspar Production in England. British Geological Survey. 2008 [2013-10-13]. (原始內容存檔於2016-08-07).
- ^ 61.0 61.1 Gribble, G. W. Naturally Occurring Organofluorines. Neison, A. H. (編). Organofluorines. The Handbook of Environmental Chemistry 3N. Berlin: Springer. 2002: 121–136. ISBN 3-540-42064-9. doi:10.1007/10721878_5.
- ^ Richter, M.; Hahn, O.; Fuchs, R. Purple Fluorite: A Little Known Artists' Pigment and Its Use in Late Gothic and Early Renaissance Painting in Northern Europe. Studies in Conservation. 2001, 46 (1): 3. JSTOR 1506878. S2CID 191611885. doi:10.1179/sic.2001.46.1.1.
- ^ 63.0 63.1 Schmedt Auf Der Günne, Jörn; Mangstl, Martin; Kraus, Florian. Occurrence of Difluorine F2 in Nature-In Situ Proof and Quantification by NMR Spectroscopy. Angewandte Chemie International Edition. 2012, 51 (31): 7847–7849. ISSN 1521-3773. PMID 22763992. doi:10.1002/anie.201203515.
- ^ Greenwood & Earnshaw 1998,第790頁.
- ^ Senning, A. Elsevier's Dictionary of Chemoetymology: The Whies and Whences of Chemical Nomenclature and Terminology. Amsterdam and Oxford: Elsevier. 2007: 149. ISBN 978-0-444-52239-9.
- ^ Stillman, John Maxson. Basil Valentine, A Seventeenth Century Hoax. Popular Science Monthly. December 1912, 81 [2013-10-14]. (原始內容存檔於2023-07-22).
- ^ Principe, Lawrence M. The Secrets of Alchemy. Chicago: University of Chicago Press. 2012: 140, 145. ISBN 978-0-226-68295-2.
- ^ Agricola, Hoover & Hoover 1912,footnotes and commentary, pp. xxx, 38, 409, 430, 461, 608.
- ^ Greenwood & Earnshaw 1998,第109頁.
- ^ Agricola, Hoover & Hoover 1912,preface, pp. 380–381.
- ^ 71.0 71.1 71.2 71.3 71.4 Weeks, M. E. The Discovery of the Elements. XVII. The Halogen Family. Journal of Chemical Education. 1932, 9 (11): 1915–1939. Bibcode:1932JChEd...9.1915W. doi:10.1021/ed009p1915.
- ^ Partington, J. R. The early history of hydrofluoric acid. Memoirs and Proceedings of the Manchester Literary and Philosophical Society. 1923, 67 (6): 73–87.
- ^ Marggraf, Andreas Sigismun. Observation concernant une volatilisation remarquable d'une partie de l'espece de pierre, à laquelle on donne les noms de flosse, flüsse, flus-spaht, et aussi celui d'hesperos; laquelle volatilisation a été effectuée au moyen des acides [Observation of a remarkable volatilization of part of a type of stone to which one gives the name flosse, flüsse, flus-spaht, as well as that of hesperos; which volatilization was effected by means of acids]. Mémoires de l'Académie royale des sciences et belles-lettres. 1770, XXIV: 3–11 (法語).
- ^ 74.0 74.1 74.2 74.3 74.4 74.5 74.6 Kirsch 2004,第3–10頁.
- ^ Scheele, Carl Wilhelm. Undersŏkning om fluss-spat och dess syra [Investigation of Fluorite and Its Acid]. Kungliga Svenska Vetenskapsademiens Handlingar [Proceedings of the Royal Swedish Academy of Science]. 1771, 32: 129–138 (瑞典語).
- ^ Ampère, André-Marie. Suite d'une classification naturelle pour les corps simples. Annales de chimie et de physique. 1816, 2: 1–5 (法語).
- ^ Davy, Humphry. Some experiments and observations on the substances produced in different chemical processes on fluor spar. Philosophical Transactions of the Royal Society. 1813, 103: 278. doi:10.1098/rstl.1813.0034
 .
.
- ^ Banks, R. E. Isolation of fluorine by Moissan: Setting the scene. Journal of Fluorine Chemistry. 1986, 33 (1–4): 3–26. doi:10.1016/S0022-1139(00)85269-0.
- ^ 79.0 79.1 Storer, Frank H. First Outlines of a Dictionary of Solubilities of Chemical Substances. Cambridge: Sever and Francis. 1864: 278–280.
- ^ 劉懷樂. 化學鑑源與略考. 化學教育. 1994, (04) [2013-02-25]. (原始內容存檔於2013-10-04).
- ^ 81.0 81.1 81.2 81.3 81.4 Toon, Richard. The discovery of fluorine. Education in Chemistry. Vol. 48 no. 5 (Royal Society of Chemistry). 2011-09-01: 148–151 [2022-10-23]. ISSN 0013-1350. (原始內容存檔於2019-03-29).
- ^ 82.0 82.1 Asimov, Isaac. The Noble Gases. New York: Basic Books. 1966: 162. ISBN 978-0-465-05129-8.
- ^ Greenwood & Earnshaw 1998,第789–791頁.
- ^ Moissan, Henri. Action d'un courant électrique sur l'acide fluorhydrique anhydre. Comptes rendus hebdomadaires des séances de l'Académie des sciences. 1886, 102: 1543–1544 [2013-10-09]. (原始內容存檔於2020-08-06) (法語).
- ^ Viel, Claude; Goldwhite, Harold. 1906 Nobel Laureate: Henri Moissan, 1852–1907. Laylin, K. James (編). Nobel Laureates in Chemistry, 1901–1992. Washington: American Chemical Society; Chemical Heritage Foundation. 1993: 35. ISBN 978-0-8412-2690-6.
- ^ 86.0 86.1 86.2 Okazoe, T. Overview on the History of Organofluorine Chemistry from the Viewpoint of Material Industry. Proceedings of the Japan Academy, Series B. 2009, 85 (8): 276–289 [2022-10-23]. Bibcode:2009PJAB...85..276O. PMC 3621566
 . PMID 19838009. doi:10.2183/pjab.85.276. (原始內容存檔於2020-08-06).
. PMID 19838009. doi:10.2183/pjab.85.276. (原始內容存檔於2020-08-06).
- ^ 87.0 87.1 Hounshell, David A.; Smith, John Kelly. Science and Corporate Strategy: DuPont R & D, 1902–1980. Cambridge: Cambridge University Press. 1988: 156–157. ISBN 0-521-32767-9.
- ^ DuPont. Freon. 2013a [2013-10-17]. (原始內容存檔於2015-02-21).
- ^ Meyer, Eugene. Chemistry of Hazardous Materials. Englewood Cliffs: Prentice Hall. 1977: 111. ISBN 978-0-13-129239-0.
- ^ Kirsch 2004,第60–66頁.
- ^ Riedel, Sebastian; Kaupp, Martin. The highest oxidation states of the transition metal elements. Coordination Chemistry Reviews. 2009, 253 (5–6): 606–624. doi:10.1016/j.ccr.2008.07.014.
- ^ Wiberg, Wiberg & Holleman 2001,第422頁.
- ^ Schlöder, T.; Riedel, S. Investigation of Heterodimeric and Homodimeric Radical Cations of the Series: [F2O2]+, [F2Cl2]+, [Cl2O2]+, [F4]+, and [Cl4]+. RSC Advances (Royal Society of Chemistry). 2012, 2 (3): 876–881. Bibcode:2012RSCAd...2..876S. doi:10.1039/C1RA00804H.
- ^ Harbison, G. S. The Electric Dipole Polarity of the Ground and Low-lying Metastable Excited States of NF. Journal of the American Chemical Society. 2002, 124 (3): 366–367. PMID 11792193. doi:10.1021/ja0159261.
- ^ Edwards, Philip Neil. Use of Fluorine in Chemotherapy. Banks, R. E.; Smart, B. E.; Tatlow, J. C. (編). Organofluorine Chemistry: Principles and Commercial Applications. New York: Plenum Press. 1994: 515. ISBN 978-0-306-44610-8.
- ^ Katakuse, Itsuo; Ichihara, Toshio; Ito, Hiroyuki; Sakurai, Tohru; Matsuo, Takekiyo. SIMS Experiment. Arai, T.; Mihama, K.; Yamamoto, K.; Sugano, S. (編). Mesoscopic Materials and Clusters: Their Physical and Chemical Properties. Tokyo: Kodansha. 1999: 267. ISBN 4-06-208635-2.
- ^ 97.0 97.1 Aigueperse 2000,第420–422頁.
- ^ Walsh, Kenneth A. Beryllium Chemistry and Processing. Materials Park: ASM International. 2009. ISBN 978-0-87170-721-5.
- ^ Emeléus & Sharpe 1983,第89–97頁.
- ^ Babel, Dietrich; Tressaud, Alain. Crystal Chemistry of Fluorides. Hagenmuller, Paul (編). Inorganic Solid Fluorides: Chemistry And Physics. Orlando: Academic Press. 1985: 91–96. ISBN 978-0-12-412490-5.
- ^ Einstein, F. W. B.; Rao, P. R.; Trotter, J.; Bartlett, N. The Crystal Structure of Gold Trifluoride. Journal of the Chemical Society A: Inorganic, Physical, Theoretical. 1967, 4: 478–482. doi:10.1039/J19670000478.
- ^ Brown, Paul L.; Mompean, Federico J.; Perrone, Jane; Illemassène, Myriam. Chemical Thermodynamics of Zirconium. Amsterdam: Elsevier B. V. 2005: 144. ISBN 978-0-444-51803-3.
- ^ 103.0 103.1 Perry, Dale L. Handbook of Inorganic Compounds 2nd. Boca Raton: CRC Press. 2011: 193. ISBN 978-1-4398-1461-1.
- ^ Kern, S.; Hayward, J.; Roberts, S.; Richardson, J. W.; Rotella, F. J.; Soderholm, L.; Cort, B.; Tinkle, M.; West, M.; Hoisington, D.; Lander, G. A. Temperature Variation of the Structural Parameters in Actinide Tetrafluorides. The Journal of Chemical Physics. 1994, 101 (11): 9333–9337 [2022-11-04]. Bibcode:1994JChPh.101.9333K. doi:10.1063/1.467963. (原始內容存檔於2021-04-14).
- ^ Lide 2004,第4.60, 4.76, 4.92, 4.96頁.
- ^ Lide 2004,第4.96頁.
- ^ Lide 2004,第4.92頁.
- ^ Greenwood & Earnshaw 1998,第964頁.
- ^ Becker, S.; Müller, B. G. Vanadium Tetrafluoride. Angewandte Chemie International Edition in English. 1990, 29 (4): 406–407. doi:10.1002/anie.199004061.
- ^ Greenwood & Earnshaw 1998,第990頁.
- ^ Lide 2004,第4.72, 4.91, 4.93頁.
- ^ 112.0 112.1 Greenwood & Earnshaw 1998,第561–563頁.
- ^ Emeléus & Sharpe 1983,第256–277頁.
- ^ Mackay, Mackay & Henderson 2002,第355–356頁.
- ^ Greenwood & Earnshaw 1998,看對應金屬的頁面.
- ^ Lide 2004,第4.71, 4.78, 4.92頁.
- ^ Drews, T.; Supeł, J.; Hagenbach, A.; Seppelt, K. Solid State Molecular Structures of Transition Metal Hexafluorides. Inorganic Chemistry. 2006, 45 (9): 3782–3788. PMID 16634614. doi:10.1021/ic052029f.
- ^ Greenwood & Earnshaw 1998,第819頁.
- ^ Einstein, F. W. B.; Rao, P. R.; Trotter, J.; Bartlett, N. The Crystal Structure of Gold Trifluoride. Journal of the Chemical Society A: Inorganic, Physical, Theoretical. 1967, 4: 478–482. doi:10.1039/J19670000478.
- ^ Pauling, Linus. The Nature of the Chemical Bond
 3rd. Ithaca: Cornell University Press. 1960: 454–464. ISBN 978-0-8014-0333-0.
3rd. Ithaca: Cornell University Press. 1960: 454–464. ISBN 978-0-8014-0333-0.
- ^ Atkins, Peter; Jones, Loretta. Chemical Principles: The Quest for Insight
 4th. New York: W. H. Freeman. 2007: 184–185. ISBN 978-1-4292-0965-6.
4th. New York: W. H. Freeman. 2007: 184–185. ISBN 978-1-4292-0965-6.
- ^ Emsley, John. The Hidden Strength of Hydrogen. New Scientist. 1981, 91 (1264): 291–292 [2024-01-18]. (原始內容存檔於2023-07-22).
- ^ Greenwood & Earnshaw 1998,第812–816頁.
- ^ Wiberg, Wiberg & Holleman 2001,第425頁.
- ^ Clark, Jim. The Acidity of the Hydrogen Halides. chemguide.co.uk. 2002 [2013-10-15]. (原始內容存檔於2012-05-31).
- ^ Chambers, C.; Holliday, A. K. Modern Inorganic Chemistry: An Intermediate Text (PDF). London: Butterworth & Co. 1975: 328–329. ISBN 978-0-408-70663-6. (原始內容 (PDF)存檔於2013-03-23).
- ^ Air Products and Chemicals. Safetygram #39 Chlorine Trifluoride (PDF). Air Products and Chemicals: 1. 2004 [2014-02-16]. (原始內容 (PDF)存檔於2006-03-18).
- ^ Noury, S.; Silvi, B.; Gillespie, R. J. Chemical Bonding in Hypervalent Molecules: Is the Octet Rule Relevant? (PDF). Inorganic Chemistry. 2002, 41 (8): 2164–2172 [2012-05-23]. PMID 11952370. doi:10.1021/ic011003v. (原始內容存檔於2020-05-11).
- ^ Chang, Raymond; Goldsby, Kenneth A. Chemistry 11th. New York: McGraw-Hill. 2013: 706. ISBN 978-0-07-131787-0.
- ^ Ellis, Brian. Scientific Essentialism. Cambridge: Cambridge University Press. 2001: 69. ISBN 978-0-521-80094-5.
- ^ Aigueperse 2000,第423頁.
- ^ Wiberg, Wiberg & Holleman 2001,第897頁.
- ^ Raghavan, P. S. Concepts and Problems in Inorganic Chemistry. Delhi: Discovery Publishing House. 1998: 164–165. ISBN 978-81-7141-418-5.
- ^ Godfrey, S. M.; McAuliffe, C. A.; Mackie, A. G.; Pritchard, R. G. Inorganic Derivatives of the Elements. Norman, Nicholas C. (編). Chemistry of Arsenic, Antimony and Bismuth. London: Blackie Academic & Professional. 1998: 98. ISBN 978-0-7514-0389-3.
- ^ Aigueperse 2000,第432頁.
- ^ Murthy, C. Parameshwara; Mehdi Ali, S. F.; Ashok, D. University Chemistry I. New Delhi: New Age International. 1995: 180–182, 206–208. ISBN 978-81-224-0742-6.
- ^ Greenwood & Earnshaw 1998,第638–640, 683–689, 767–778頁.
- ^ Wiberg, Wiberg & Holleman 2001,第435–436頁.
- ^ Greenwood & Earnshaw 1998,第828–830頁.
- ^ Patnaik 2007,第478–479頁.
- ^ Moeller, T.; Bailar, J. C.; Kleinberg. Chemistry, with Inorganic Qualitative Analysis 3rd. New York: Academic Press. 1980: 236. ISBN 0-12-503350-8.
- ^ Wiberg, Wiberg & Holleman 2001,第392–393頁.
- ^ Wiberg, Wiberg & Holleman 2001,第395–397, 400頁.
- ^ Lewars 2008,第68頁.
- ^ Pitzer, Kenneth S. (編). Molecular Structure and Statistical Thermodynamics: Selected Papers of Kenneth S. Pitzer. Singapore: World Scientific Publishing. 1993: 111. ISBN 978-981-02-1439-5.
- ^ Lewars 2008,第67頁.
- ^ 147.0 147.1 Bihary, Z.; Chaban, G. M.; Gerber, R. B. Stability of a Chemically Bound Helium Compound in High-pressure Solid Helium. The Journal of Chemical Physics. 2002, 117 (11): 5105–5108. Bibcode:2002JChPh.117.5105B. doi:10.1063/1.1506150.
- ^ Lewars 2008,第71頁.
- ^ Hoogers, G. Fuel Cell Components and Their Impact on Performance. Hoogers, G. (編). Fuel Cell Technology Handbook. Boca Raton: CRC Press. 2002: 4-12. ISBN 0-8493-0877-1.
- ^ O'Hagan, D. Understanding Organofluorine Chemistry. An Introduction to the C–F Bond. Chemical Society Reviews. 2008, 37 (2): 308–319. PMID 18197347. doi:10.1039/b711844a.
- ^ Siegemund 2005,第444頁.
- ^ Sandford, Graham. Organofluorine Chemistry. Philosophical Transactions. 2000, 358 (1766): 455. Bibcode:2000RSPTA.358..455S. S2CID 202574641. doi:10.1098/rsta.2000.0541.
- ^ Siegemund 2005,第451–452頁.
- ^ Barbee, K.; McCormack, K.; Vartanian, V. EHS Concerns with Ozonated Water Spray Processing. Mendicino, L. (編). Environmental Issues in the Electronics and Semiconductor Industries. Pennington, NJ: The Electrochemical Society. 2000: 116. ISBN 978-1-56677-230-3.
- ^ Posner, Stefan; et al. Per- and Polyfluorinated Substances in the Nordic Countries: Use Occurrence and Toxicology (PDF). Copenhagen: Nordic Council of Ministers. 2013: 187–190 [2024-01-18]. ISBN 978-92-893-2562-2. doi:10.6027/TN2013-542. (原始內容存檔 (PDF)於2023-07-09).
- ^ 156.0 156.1 Posner, Stefan. Perfluorinated Compounds: Occurrence and Uses in Products. Knepper, Thomas P.; Large, Frank T. (編). Polyfluorinated Chemicals and Transformation Products. Heidelberg: Springer Science+Business Media. 2011: 27. ISBN 978-3-642-21871-2.
- ^ Salager, Jean-Louis. Surfactants: Types and Uses (PDF). FIRP Booklet # 300-A. Laboratory of Formulation, Interfaces, Rheology, and Processes, Universidad de los Andes. 2002: 45 [2013-10-13]. (原始內容 (PDF)存檔於2020-07-31).
- ^ 158.0 158.1 Carlson & Schmiegel 2000,第3頁.
- ^ Carlson & Schmiegel 2000,第3–4頁.
- ^ Rhoades, David Walter. Broadband Dielectric Spectroscopy Studies of Nafion (PhD dissertation, University of Southern Mississippi, MS). Ann Arbor. 2008: 2. ISBN 978-0-549-78540-8.
- ^ Okada, T.; Xie, G.; Gorseth, O.; Kjelstrup, S.; Nakamura, N.; Arimura, T. Ion and Water Transport Characteristics of Nafion Membranes as Electrolytes. Electrochimica Acta. 1998, 43 (24): 3741–3747. doi:10.1016/S0013-4686(98)00132-7.
- ^ Carlson & Schmiegel 2000,第4頁.
- ^ Jaccaud 2000,第386頁.
- ^ Jaccaud 2000,第384–385頁.
- ^ 165.0 165.1 Jaccaud 2000,第390–391頁.
- ^ Shriver, Duward; Atkins, Peter. Solutions Manual for Inorganic Chemistry. New York: W. H. Freeman. 2010: 427. ISBN 978-1-4292-5255-3.
- ^ Christe, Karl O. Chemical Synthesis of Elemental Fluorine. Inorganic Chemistry. 1986, 25 (21): 3721–3722. doi:10.1021/ic00241a001.
- ^ Christe Research Group. Chemical Synthesis of Elemental Fluorine. n.d. [2013-01-12]. (原始內容存檔於2016-03-04).
- ^ Carey, Charles W. African Americans in Science. Santa Barbara: ABC-CLIO. 2008: 173. ISBN 978-1-85109-998-6.
- ^ Miller, M. Michael. Mineral Resource of the Month, Fluorspar (PDF). U.S. Geological Survey. 2003 [2013-10-24]. (原始內容存檔 (PDF)於2017-02-17).
- ^ PRWeb. Global Fluorspar Market to Reach 5.94 Million Metric Tons by 2017, According to New Report by Global Industry Analysts, Inc.. prweb.com. 2012-02-23 [2013-10-24]. (原始內容存檔於2020-07-31).
- ^ Bombourg, Nicolas. World Fluorochemicals Market, Freedonia. Reporterlinker. 2012-07-04 [2013-10-20]. (原始內容存檔於2020-04-23).
- ^ Transparency Market Research. Fluorochemicals Market is Expected to Reach USD 21.5 Billion Globally by 2018: Transparency Market Research. Transparency Market Research Blog. 2013-05-17 [2013-10-15]. (原始內容存檔於2014-02-22).
- ^ Fulton, Robert B.; Miller, M. Michael. Fluorspar. Kogel, Jessica Elzea; Trivedi, Nikhil C.; Barker, James M.; Krukowski, Stanley T. (編). Industrial Minerals & Rocks: Commodities, Markets, and Uses. Littleton: Society for Mining, Metallurgy, and Exploration (U.S.). 2006: 471. ISBN 978-0-87335-233-8.
- ^ 175.0 175.1 Jaccaud 2000,第392頁.
- ^ Aigueperse 2000,第430頁.
- ^ Jaccaud 2000,第391–392頁.
- ^ El-Kareh, Badih. Fundamentals of Semiconductor Processing Technology. Norwell and Dordrecht: Kluwer Academic Publishers. 1994: 317. ISBN 978-0-7923-9534-8.
- ^ Arana, L. R.; Mas, N.; Schmidt, R.; Franz, A. J.; Schmidt, M. A.; Jensen, K. F. Isotropic Etching of Silicon in Fluorine Gas for MEMS Micromachining. Journal of Micromechanics and Microengineering. 2007, 17 (2): 384–392. Bibcode:2007JMiMi..17..384A. S2CID 135708022. doi:10.1088/0960-1317/17/2/026.
- ^ Miller, M. Michael. Fluorspar (PDF). U.S. Geological Survey Minerals Yearbook. U.S. Geological Survey. 2003: 27.1–27.12 [2023-11-19]. (原始內容存檔 (PDF)於2004-11-01).
- ^ Energetics, Inc. Energy and Environmental Profile of the U.S. Aluminum Industry (PDF) (報告): 41, 50. 1997 [2013-10-15].
- ^ Aigueperse 2000,第428頁.
- ^ Willey, Ronald R. Practical Equipment, Materials, and Processes for Optical Thin Films. Charlevoix: Willey Optical. 2007: 113. ISBN 978-0-615-14397-2.
- ^ PRWeb. Global Fluorochemicals Market to Exceed 2.6 Million Tons by 2015, According to a New Report by Global Industry Analysts, Inc.. prweb.com. 2010-10-28 [2013-10-24]. (原始內容存檔於2020-07-31).
- ^ 185.0 185.1 185.2 Renner, R. The Long and the Short of Perfluorinated Replacements. Environmental Science & Technology. 2006, 40 (1): 12–13. Bibcode:2006EnST...40...12R. PMID 16433328. doi:10.1021/es062612a
 .
.
- ^ Green, S. W.; Slinn, D. S. L.; Simpson, R. N. F.; Woytek, A. J. Perfluorocarbon Fluids. Banks, R. E.; Smart, B. E.; Tatlow, J. C. (編). Organofluorine Chemistry: Principles and Applications. New York: Plenum Press. 1994: 91–93. ISBN 978-0-306-44610-8.
- ^ DuPont. Understanding the Refrigerant 'R' Nomenclature. 2013b [2013-10-17]. (原始內容存檔於2014-10-03).
- ^ 188.0 188.1 Walter, P. Honeywell Invests $300m in Green Refrigerant. Chemistry World. 2013 [2024-01-18]. (原始內容存檔於2016-03-04).
- ^ 189.0 189.1 Buznik, V. M. Fluoropolymer Chemistry in Russia: Current Situation and Prospects. Russian Journal of General Chemistry. 2009, 79 (3): 520–526. S2CID 97518401. doi:10.1134/S1070363209030335.
- ^ PRWeb. Fluoropolymers Market is Poised to Grow at a CAGR of 6.5% & to Reach $9,446.0 Million by 2016 – New report by MarketsandMarkets. prweb.com. 2013-04-07 [2013-10-24]. (原始內容存檔於2020-07-31).
- ^ 191.0 191.1 191.2 191.3 191.4 Martin, John W. (編). Concise Encyclopedia of the Structure of Materials. Oxford and Amsterdam: Elsevier. 2007: 187–194. ISBN 978-0-08-045127-5.
- ^ DeBergalis, Michael. Fluoropolymer films in the photovoltaic industry. Journal of Fluorine Chemistry. 2004, 125 (8): 1255–1257. doi:10.1016/j.jfluchem.2004.05.013.
- ^ Grot, Walter. Fluorinated Ionomers 2nd. Oxford and Waltham: Elsevier. 2011: 1–10. ISBN 978-1-4377-4457-6.
- ^ Ramkumar, Jayshree. Nafion Perfluorosulphonate Membrane: Unique Properties and Various Applications. Banerjee, S.; Tyagi, A. K. (編). Functional Materials: Preparation, Processing and Applications. London and Waltham: Elsevier. 2012: 567. ISBN 978-0-12-385142-0.
- ^ Burney, H. Past, Present and Future of the Chlor-Alkali Industry. Burney, H. S.; Furuya, N.; Hine, F.; Ota, K.-I. (編). Chlor-Alkali and Chlorate Technology: R. B. MacMullin Memorial Symposium. Pennington: The Electrochemical Society. 1999: 111. ISBN 1-56677-244-3.
- ^ Slye, Orville M. Fire Extinguishing Agents. Ullmann, Franz (編). Ullmann's Encyclopedia of Industrial Chemistry 15. Weinheim: Wiley-VCH. 2012: 10. ISBN 978-3527306732. doi:10.1002/14356007.a11_113.pub2.
- ^ Kissa, Erik. Fluorinated Surfactants and Repellents 2nd. New York: Marcel Dekker. 2001: 516–551. ISBN 978-0-8247-0472-8.
- ^ Ullmann, Fritz. Ullmann's Fibers (2 volumes). Weinheim: Wiley-VCH. 2008: 538, 543–547. ISBN 978-3-527-31772-1.
- ^ ICIS. Fluorine's Treasure Trove. Reed Business Information. 2006-10-02 [2013-10-24]. (原始內容存檔於2009-02-26).
- ^ 200.0 200.1 Theodoridis, George. Fluorine-Containing Agrochemicals: An Overview of Recent Developments. Tressaud, Alain (編). Fluorine and the Environment: Agrochemicals, Archaeology, Green Chemistry & Water. Amsterdam and Oxford: Elsevier. 2006: 121–176. ISBN 978-0-444-52672-4.
- ^ United States Environmental Protection Agency. R.E.D. Facts: Trifluralin (PDF). 1996 [2013-10-17]. (原始內容 (PDF)存檔於2013-10-18).
- ^ Directorate-General for the Environment (European Commission). Trifluralin (PDF) (報告). European Commission. 2007 [2013-10-14]. (原始內容存檔於2020-07-28).
- ^ Beasley, Michael. Guidelines for the safe use of sodium fluoroacetate (1080) (PDF). Wellington: Occupational Safety & Health Service, Department of Labour (New Zealand). August 2002 [2013-11-11]. ISBN 0-477-03664-3. (原始內容 (PDF)存檔於2013-11-11).
- ^ 204.0 204.1 Proudfoot, A. T.; Bradberry, S. M.; Vale, J. A. Sodium Fluoroacetate Poisoning. Toxicological Reviews. 2006, 25 (4): 213–219. PMID 17288493. S2CID 29189551. doi:10.2165/00139709-200625040-00002.
- ^ Eisler, Ronald. Sodium Monofluoroacetate (1080) Hazards to Fish, Wildlife and Invertebrates: A Synoptic Review (PDF) (報告). Patuxent Environmental Science Center (U.S. National Biological Service). 1995 [2011-06-05]. (原始內容存檔 (PDF)於2020-03-07).
- ^ Pizzo, G.; Piscopo, M. R.; Pizzo, I.; Giuliana, G. Community Water Fluoridation and Caries Prevention: A Critical Review (PDF). Clinical Oral Investigations. 2007, 11 (3): 189–193 [2023-02-23]. PMID 17333303. S2CID 13189520. doi:10.1007/s00784-007-0111-6. (原始內容存檔 (PDF)於2020-07-24).
- ^ Centers for Disease Control and Prevention. Recommendations for Using Fluoride to Prevent and Control Dental Caries in the United States. MMWR Recommendations and Reports. 2001, 50 (RR–14): 1–42 [2013-10-14]. PMID 11521913. (原始內容存檔於2007-02-08).
- ^ Ripa, L. W. A Half-century of Community Water Fluoridation in the United States: Review and Commentary (PDF). Journal of Public Health Dentistry. 1993, 53 (1): 17–44. PMID 8474047. doi:10.1111/j.1752-7325.1993.tb02666.x. (原始內容 (PDF)存檔於2009-03-04).
- ^ 209.0 209.1 Cheng, K. K.; Chalmers, I.; Sheldon, T. A. Adding Fluoride to Water Supplies (PDF). BMJ. 2007, 335 (7622): 699–702 [2012-03-26]. PMC 2001050
 . PMID 17916854. doi:10.1136/bmj.39318.562951.BE. (原始內容 (PDF)存檔於2016-03-03).
. PMID 17916854. doi:10.1136/bmj.39318.562951.BE. (原始內容 (PDF)存檔於2016-03-03).
- ^ National Health and Medical Research Council. A Systematic Review of the Efficacy and Safety of Fluoridation, Part A: Review of Methodology and Results (PDF). Canberra: Australian Government. 2007 [2013-10-08]. ISBN 978-1-86496-421-9. (原始內容 (PDF)存檔於2012-01-13).
- ^ Yeung, C. A. A Systematic Review of the Efficacy and Safety of Fluoridation. Evidence-Based Dentistry. 2008, 9 (2): 39–43. PMID 18584000. doi:10.1038/sj.ebd.6400578
 .
.
- ^ Marya, C. M. A Textbook of Public Health Dentistry. New Delhi: Jaypee Brothers Medical Publishers. 2011: 343. ISBN 978-93-5025-216-1.
- ^ Armfield, J. M. When Public Action Undermines Public Health: A Critical Examination of Antifluoridationist Literature. Australia and New Zealand Health Policy. 2007, 4: 25 [2023-02-28]. PMC 2222595
 . PMID 18067684. doi:10.1186/1743-8462-4-25. (原始內容存檔於2016-01-27).
. PMID 18067684. doi:10.1186/1743-8462-4-25. (原始內容存檔於2016-01-27).
- ^ 214.0 214.1 Baelum, Vibeke; Sheiham, Aubrey; Burt, Brian. Caries Control for Populations. Fejerskov, Ole; Kidd, Edwina (編). Dental Caries: The Disease and Its Clinical Management 2nd. Oxford: Blackwell Munksgaard. 2008: 518. ISBN 978-1-4051-3889-5.
- ^ Cracher, Connie M. Current Concepts in Preventive Dentistry (PDF). dentalcare.com: 12. 2012 [2013-10-14]. (原始內容 (PDF)存檔於2013-10-14).
- ^ Emsley 2011,第178頁.
- ^ Johnson, Linda A. Against Odds, Lipitor Became World's Top Seller. The Boston Globe. 2011-12-28 [2013-10-24].
- ^ 218.0 218.1 Swinson, Joel. Fluorine – A Vital Element in the Medicine Chest (PDF). PharmaChem (Pharmaceutical Chemistry). June 2005: 26–27 [2013-10-09]. (原始內容 (PDF)存檔於2012-02-08).
- ^ Hagmann, W. K. The Many Roles for Fluorine in Medicinal Chemistry. Journal of Medicinal Chemistry. 2008, 51 (15): 4359–4369. PMID 18570365. doi:10.1021/jm800219f.
- ^ Mitchell, E. Siobhan. Antidepressants
 . New York: Chelsea House Publishers. 2004: 37–39. ISBN 978-1-4381-0192-7.
. New York: Chelsea House Publishers. 2004: 37–39. ISBN 978-1-4381-0192-7.
- ^ Preskorn, Sheldon H. Clinical Pharmacology of Selective Serotonin Reuptake Inhibitors. Caddo: Professional Communications. 1996. ISBN 978-1-884735-08-0.
- ^ Werner, N. L.; Hecker, M. T.; Sethi, A. K.; Donskey, C. J. Unnecessary use of Fluoroquinolone Antibiotics in Hospitalized Patients. BMC Infectious Diseases. 2011, 11: 187–193. PMC 3145580
 . PMID 21729289. doi:10.1186/1471-2334-11-187.
. PMID 21729289. doi:10.1186/1471-2334-11-187.
- ^ Brody, Jane E. Popular Antibiotics May Carry Serious Side Effects. The New York Times Well Blog. 2012-09-10 [2013-10-18].
- ^ Nelson, J. M.; Chiller, T. M.; Powers, J. H.; Angulo, F. J. Food Safety: Fluoroquinolone‐ResistantCampylobacterSpecies and the Withdrawal of Fluoroquinolones from Use in Poultry: A Public Health Success Story (PDF). Clinical Infectious Diseases. 2007, 44 (7): 977–980 [2023-12-08]. PMID 17342653. doi:10.1086/512369
 . (原始內容存檔 (PDF)於2022-09-01).
. (原始內容存檔 (PDF)於2022-09-01).
- ^ King, D. E.; Malone, R.; Lilley, S. H. New Classification and Update on the Quinolone Antibiotics. American Family Physician. 2000, 61 (9): 2741–2748 [2013-10-08]. PMID 10821154.
- ^ Parente, Luca. The Development of Synthetic Glucocorticoids. Goulding, Nicolas J.; Flower, Rod J. (編). Glucocorticoids. Basel: Birkhäuser. 2001: 40. ISBN 978-3-7643-6059-7.
- ^ Raj, P. Prithvi; Erdine, Serdar. Pain-Relieving Procedures: The Illustrated Guide. Chichester: John Wiley & Sons. 2012: 58. ISBN 978-0-470-67038-5.
- ^ Filler, R.; Saha, R. Fluorine in Medicinal Chemistry: A Century of Progress and a 60-year Retrospective of Selected Highlights (PDF). Future Medicinal Chemistry. 2009, 1 (5): 777–791. PMID 21426080. doi:10.4155/fmc.09.65. (原始內容 (PDF)存檔於2013-10-22).
- ^ Bégué, Jean-Pierre; Bonnet-Delpon, Danièle. Bioorganic and Medicinal Chemistry of Fluorine. Hoboken: John Wiley & Sons. 2008: 335–336. ISBN 978-0-470-27830-7..
- ^ 230.0 230.1 Schmitz, A.; Kälicke, T.; Willkomm, P.; Grünwald, F.; Kandyba, J.; Schmitt, O. Use of Fluorine-18 Fluoro-2-deoxy-D-glucose Positron Emission Tomography in Assessing the Process of Tuberculous Spondylitis (PDF). Journal of Spinal Disorders. 2000, 13 (6): 541–544 [2013-10-08]. PMID 11132989. doi:10.1097/00002517-200012000-00016. (原始內容存檔 (PDF)於2020-05-08).
- ^ Bustamante, E.; Pedersen, P. L. High Aerobic Glycolysis of Rat Hepatoma Cells in Culture: Role of Mitochondrial Hexokinase. Proceedings of the National Academy of Sciences. 1977, 74 (9): 3735–3739. Bibcode:1977PNAS...74.3735B. PMC 431708
 . PMID 198801. doi:10.1073/pnas.74.9.3735
. PMID 198801. doi:10.1073/pnas.74.9.3735  .
.
- ^ Alavi, Abbas; Huang, Steve S. Positron Emission Tomography in Medicine: An Overview. Hayat, M. A. (編). Cancer Imaging, Volume 1: Lung and Breast Carcinomas. Burlington: Academic Press. 2007: 41. ISBN 978-0-12-370468-9.
- ^ Gabriel, J. L.; Miller, T. F. Jr.; Wolfson, M. R.; Shaffer, T. H. Quantitative Structure-Activity Relationships of Perfluorinated Hetero-Hydrocarbons as Potential Respiratory Media. ASAIO Journal. 1996, 42 (6): 968–973. PMID 8959271. S2CID 31161098. doi:10.1097/00002480-199642060-00009.
- ^ Sarkar, S. Artificial Blood. Indian Journal of Critical Care Medicine. 2008, 12 (3): 140–144. PMC 2738310
 . PMID 19742251. doi:10.4103/0972-5229.43685.
. PMID 19742251. doi:10.4103/0972-5229.43685.
- ^ Schimmeyer, S. The Search for a Blood Substitute. Illumin (Columbia: University of Southern Carolina). 2002, 15 (1) [2013-10-15]. (原始內容存檔於2011-10-02).
- ^ Davis, Nicole. Better than blood. Popular Science. November 2006 [2013-10-20]. (原始內容存檔於2011-06-04).
- ^ Gains, Paul. A New Threat in Blood Doping. The New York Times. 1998-10-18 [2013-10-18]. (原始內容存檔於2023-04-07).
- ^ Taber, Andrew. Dying to ride. Salon. 1999-04-22 [2013-10-18]. (原始內容存檔於2018-11-06).
- ^ Shaffer, T. H.; Wolfson, M. R.; Clark, L. C. Jr. Liquid Ventilation. Pediatric Pulmonology. 1992, 14 (2): 102. PMID 1437347. S2CID 222167378. doi:10.1002/ppul.1950140208.
- ^ Kacmarek, Robert M.; Wiedemann, Herbert P.; Lavin, Philip T.; Wedel, Mark K.; Tütüncü, Ahmet S.; Slutsky, Arthur S. Partial Liquid Ventilation in Adult Patients with Acute Respiratory Distress Syndrome. American Journal of Respiratory and Critical Care Medicine. 2006, 173 (8): 882–9. PMID 16254269. doi:10.1164/rccm.200508-1196OC.
- ^ Nielsen, Forrest H. Micronutrients in Parenteral Nutrition: Boron, Silicon, and Fluoride. Gastroenterology. 2009, 137 (5): S55–60 [2018-04-29]. PMID 19874950. doi:10.1053/j.gastro.2009.07.072
 . (原始內容存檔於2020-07-30).
. (原始內容存檔於2020-07-30).
- ^ Olivares, M.; Uauy, R. Essential Nutrients in Drinking Water (Draft) (PDF) (報告). World Health Organization (WHO). 2004 [2013-10-14]. (原始內容 (PDF)存檔於2012-10-19).
- ^ 243.0 243.1 Murphy, C. D.; Schaffrath, C.; O'Hagan, D. Fluorinated Natural Products: The Biosynthesis of Fluoroacetate and 4-Fluorothreonine in Streptomyces cattleya. Chemosphere. 2003, 52 (2): 455–461. Bibcode:2003Chmsp..52..455M. PMID 12738270. doi:10.1016/S0045-6535(03)00191-7.
- ^ O'Hagan, D.; Schaffrath, C.; Cobb, S. L.; Hamilton, J. T. G.; Murphy, C. D. Biochemistry: Biosynthesis of an Organofluorine Molecule. Nature. 2002, 416 (6878): 279. Bibcode:2002Natur.416..279O. PMID 11907567. S2CID 4415511. doi:10.1038/416279a
 .
.
- ^ National Oceanic and Atmospheric Administration.
- ^ The National Institute for Occupational Safety and Health. Fluorine. Documentation for Immediately Dangerous To Life or Health Concentrations (IDLHs). 1994 [2014-01-15]. (原始內容存檔於2022-12-08).
- ^ The National Institute for Occupational Safety and Health. Chlorine. Documentation for Immediately Dangerous To Life or Health Concentrations (IDLHs). 1994 [2014-07-13]. (原始內容存檔於2023-02-05).
- ^ 248.0 248.1 Keplinger, M. L.; Suissa, L. W. Toxicity of Fluorine Short-Term Inhalation. American Industrial Hygiene Association Journal. 1968, 29 (1): 10–18. PMID 5667185. doi:10.1080/00028896809342975.
- ^ CDC - NIOSH Pocket Guide to Chemical Hazards -Fluorine. www.cdc.gov. [2015-11-03]. (原始內容存檔於2015-11-17).
- ^ Emsley 2011,第179頁.
- ^ Biller, José. Interface of Neurology and Internal Medicine illustrated. Philadelphia: Lippincott Williams & Wilkins. 2007: 939 [2023-02-19]. ISBN 978-0-7817-7906-7. (原始內容存檔於2023-07-22).
- ^ Eaton, Charles. Figure hfl. E-Hand.com: The Electronic Textbook of Hand Surgery. The Hand Center (former practice of Dr. Eaton). 1997 [2013-09-28].
- ^ Blodgett, D. W.; Suruda, A. J.; Crouch, B. I. Fatal Unintentional Occupational Poisonings by Hydrofluoric Acid in the U.S (PDF). American Journal of Industrial Medicine. 2001, 40 (2): 215–220. PMID 11494350. doi:10.1002/ajim.1090. (原始內容 (PDF)存檔於2012-07-17).
- ^ Hoffman, Robert; Nelson, Lewis; Howland, Mary; Lewin, Neal; Flomenbaum, Neal; Goldfrank, Lewis. Goldfrank's Manual of Toxicologic Emergencies. New York: McGraw-Hill Professional. 2007: 1333. ISBN 978-0-07-144310-4.
- ^ 255.0 255.1 Honeywell. Recommended medical treatment for hydrofluoric acid exposure (PDF). Morristown: Honeywell International. 2006 [2014-01-09]. (原始內容 (PDF)存檔於2013-10-08).
- ^ Fischman, Michael L. Semiconductor Manufacturing Hazards. Sullivan, John B.; Krieger, Gary R. (編). Clinical Environmental Health and Toxic Exposures 2nd. Philadelphia: Lippincott Williams & Wilkins. 2001: 458–459. ISBN 978-0-683-08027-8.
- ^ El Saadi, M. S.; Hall, A. H.; Hall, P. K.; Riggs, B. S.; Augenstein, W. L.; Rumack, B. H. Hydrofluoric Acid Dermal Exposure. Veterinary and Human Toxicology. 1989, 31 (3): 243–247. PMID 2741315.
- ^ Roblin, I.; Urban, M.; Flicoteau, D.; Martin, C.; Pradeau, D. Topical Treatment of Experimental Hydrofluoric Acid Skin Burns by 2.5% Calcium Gluconate. Journal of Burn Care & Research. 2006, 27 (6): 889–894. PMID 17091088. S2CID 3691306. doi:10.1097/01.BCR.0000245767.54278.09.
- ^ Hultén, P.; Höjer, J.; Ludwigs, U.; Janson, A. Hexafluorine vs. Standard Decontamination to Reduce Systemic Toxicity After Dermal Exposure to Hydrofluoric Acid. Clinical Toxicology. 2004, 42 (4): 355–361. PMID 15461243. S2CID 27090208. doi:10.1081/CLT-120039541.
- ^ Zorich, Robert. Handbook of Quality Integrated Circuit Manufacturing. San Diego: Academic Press. 1991: 182-183. ISBN 978-0-323-14055-3.
- ^ Liteplo, R.; Gomes, R.; Howe, P.; Malcolm, H. Environmental Health Criteria 227 (Fluoride). Geneva: United Nations Environment Programme; International Labour Organization; World Health Organization. 2002: 100 [2013-10-14]. ISBN 92-4-157227-2. (原始內容存檔於2020-01-12).
- ^ 262.0 262.1 262.2 Shin, Richard D.; Silverberg, Mark A. Fluoride Toxicity. Medscape. 2013 [2013-10-15]. (原始內容存檔於2020-08-06).
- ^ Reddy, D. Neurology of Endemic Skeletal Fluorosis. Neurology India. 2009, 57 (1): 7–12 [2023-02-23]. PMID 19305069. doi:10.4103/0028-3886.48793. (原始內容存檔於2021-11-05).
- ^ Baez, Ramon J.; Baez, Martha X.; Marthaler, Thomas M. Urinary Fluoride Excretion by Children 4–6 Years Old in a South Texas Community. Revista Panamericana de Salud Pública. 2000, 7 (4): 242–248. PMID 10846927. doi:10.1590/S1020-49892000000400005
 .
.
- ^ 265.0 265.1 Augenstein, W. L.; et al. Fluoride Ingestion in Children: A Review of 87 cases. Pediatrics. 1991, 88 (5): 907–912 [2023-02-19]. PMID 1945630. S2CID 22106466. doi:10.1542/peds.88.5.907. (原始內容存檔於2010-10-02).
- ^ Gessner, B. D.; Beller, M.; Middaugh, J. P.; Whitford, G. M. Acute Fluoride Poisoning from a Public Water System. New England Journal of Medicine. 1994, 330 (2): 95–99. PMID 8259189. doi:10.1056/NEJM199401133300203
 .
.
- ^ Centers for Disease for Control and Prevention. Community Water Fluoridation. 2013-07-10 [2013-10-25]. (原始內容存檔於2017-07-05).
- ^ Shulman, J. D.; Wells, L. M. Acute Fluoride Toxicity from Ingesting Home-use Dental Products in Children, Birth to 6 Years of Age. Journal of Public Health Dentistry. 1997, 57 (3): 150–158. PMID 9383753. doi:10.1111/j.1752-7325.1997.tb02966.x.
- ^ Beck, Jefferson; Newman, Paul; Schindler, Trent L.; Perkins, Lori. What Would have Happened to the Ozone Layer if Chlorofluorocarbons (CFCs) had not been Regulated?. National Aeronautics and Space Administration. 2011 [2013-10-15].
- ^ Aucamp, Pieter J.; Björn, Lars Olof. Questions and Answers about the Environmental Effects of the Ozone Layer Depletion and Climate Change: 2010 Update (PDF). United Nations Environmental Programme. 2010 [2013-10-14]. (原始內容 (PDF)存檔於2013-09-03).
- ^ Mitchell Crow, James. First signs of ozone-hole recovery spotted. Nature. 2011. doi:10.1038/news.2011.293.
- ^ Barry, Patrick L.; Phillips, Tony. Good News and a Puzzle. National Aeronautics and Space Administration. 2006-05-26 [2012-01-06]. (原始內容存檔於2010-05-27).
- ^ United States Environmental Protection Agency. Class I Ozone-depleting Substances. 2013a [2013-10-15]. (原始內容存檔於2010-12-10).
- ^ 274.0 274.1 United States Environmental Protection Agency. Phaseout of HCFCs (Class II Ozone-Depleting Substances). 2013b [2013-10-15]. (原始內容存檔於2015-09-24).
- ^ McCoy, M. SURVEY Market Challenges Dim the Confidence of the World's Chemical CEOs. Chemical & Engineering News. 2007, 85 (23): 11. doi:10.1021/cen-v085n023.p011a.
- ^ Forster, P.; Ramaswamy, V.; Artaxo, P.; Berntsen, T.; Betts, R.; Fahey, D. W.; Haywood, J.; Lean, J.; Lowe, D. C.; Myhr e, G.; Nganga, J.; Prinn, R.; Raga, G.; Schulz, M.; Van Dorland, R. Changes in Atmospheric Constituents and in Radiative Forcing. Solomon, S.; Manning, M.; Chen, Z.; Marquis, M.; Averyt, K. B.; Tignor, M.; Miller, H. L. (編). Climate Change 2007: The Physical Science Basis. Contribution of Working Group I to the Fourth Assessment Report of the Intergovernmental Panel on Climate Change. Cambridge: Cambridge University. 2007: 212–213. ISBN 978-0-521-70596-7.
- ^ Schwarcz, Joseph A. The Fly in the Ointment: 70 Fascinating Commentaries on the Science of Everyday Life
 . Toronto: ECW Press. 2004. ISBN 1-55022-621-5.
. Toronto: ECW Press. 2004. ISBN 1-55022-621-5.
- ^ Giesy, J. P.; Kannan, K. Perfluorochemical Surfactants in the Environment. Environmental Science & Technology. 2002, 36 (7): 146A–152A. Bibcode:2002EnST...36..146G. PMID 11999053. doi:10.1021/es022253t
 .
.
- ^ 279.0 279.1 279.2 279.3 Steenland, K.; Fletcher, T.; Savitz, D. A. Epidemiologic Evidence on the Health Effects of Perfluorooctanoic Acid (PFOA). Environmental Health Perspectives. 2010, 118 (8): 1100–1108. PMC 2920088
 . PMID 20423814. doi:10.1289/ehp.0901827.
. PMID 20423814. doi:10.1289/ehp.0901827.
- ^ 280.0 280.1 280.2 280.3 Betts, K. S. Perfluoroalkyl Acids: What is the Evidence Telling Us?. Environmental Health Perspectives. 2007, 115 (5): A250–A256. PMC 1867999
 . PMID 17520044. doi:10.1289/ehp.115-a250.
. PMID 17520044. doi:10.1289/ehp.115-a250.
- ^ United States Environmental Protection Agency. Emerging Contaminants – Perfluorooctane Sulfonate (PFOS) and Perfluorooctanoic Acid (PFOA) (PDF). 2012 [2013-11-04]. (原始內容 (PDF)存檔於2013-10-29).
- ^ Zareitalabad, P.; Siemens, J.; Hamer, M.; Amelung, W. Perfluorooctanoic acid (PFOA) and perfluorooctanesulfonic acid (PFOS) in surface waters, sediments, soils and wastewater – A review on concentrations and distribution coefficients. Chemosphere. 2013, 91 (6): 725–32. Bibcode:2013Chmsp..91..725Z. PMID 23498059. doi:10.1016/j.chemosphere.2013.02.024.
- ^ 283.0 283.1 Lau, C.; Anitole, K.; Hodes, C.; Lai, D.; Pfahles-Hutchens, A.; Seed, J. Perfluoroalkyl Acids: A Review of Monitoring and Toxicological Findings. Toxicological Sciences. 2007, 99 (2): 366–394. PMID 17519394. doi:10.1093/toxsci/kfm128
 .
.
參考書目[編輯]
- Agricola, Georgius; Hoover, Herbert Clark; Hoover, Lou Henry. De Re Metallica. London: The Mining Magazine. 1912.
- Aigueperse, J.; Mollard, P.; Devilliers, D.; Chemla, M.; Faron, R.; Romano, R. E.; Cue, J. P. Fluorine Compounds, Inorganic. Weinheim: Wiley-VCH: 397–441. 2000. ISBN 3527306730. doi:10.1002/14356007.
- Carlson, D. P.; Schmiegel, W., Fluoropolymers, Organic: 495–533, 2000, ISBN 3527306730, doi:10.1002/14356007.a11_393
- Dean, John A. Lange's Handbook of Chemistry 15th. New York: McGraw-Hill. 1999. ISBN 0-07-016190-9.
- Emeléus, H. J.; Sharpe, A. G. Advances in Inorganic Chemistry and Radiochemistry 27. Academic Press. 1983. ISBN 0-12-023627-3.
- Emsley, John. Nature's Building Blocks: An A–Z Guide to the Elements 2nd. Oxford: Oxford University Press. 2011. ISBN 978-0-19-960563-7.
- Greenwood, N. N.; Earnshaw, A. Chemistry of the Elements 2nd. Oxford: Butterworth Heinemann. 1998. ISBN 0-7506-3365-4.
- Jaccaud, M.; Faron, R.; Devilliers, D.; Romano, R. Fluorine. Weinheim: Wiley-VCH: 381–395. 2000. ISBN 3527306730. doi:10.1002/14356007.a11_293.
- Kirsch, Peer. Modern Fluoroorganic Chemistry: Synthesis, Reactivity, Applications. Weinheim: Wiley-VCH. 2004. ISBN 978-3-527-30691-6.
- Lewars, Errol G. Modeling Marvels: Computational Anticipation of Novel Molecules. Dordrecht: Springer. 2008 [2023-11-19]. ISBN 978-1-4020-6972-7. (原始內容存檔於2023-07-22).
- Lide, David R. Handbook of Chemistry and Physics
 84th. Boca Raton: CRC Press. 2004. ISBN 0-8493-0566-7.
84th. Boca Raton: CRC Press. 2004. ISBN 0-8493-0566-7. - Lidin, R.; Molochko, V. A.; Andreeva, L. L. Химические свойства неорганических веществ [Chemical Properties of Inorganic Substances]. Moscow: Khimiya. 2000. ISBN 5-7245-1163-0 (俄語).
- Mackay, Kenneth Malcolm; Mackay, Rosemary Ann; Henderson, W. Introduction to Modern Inorganic Chemistry 6th. Cheltenham: Nelson Thornes. 2002. ISBN 0-7487-6420-8.
- Patnaik, Pradyot. A Comprehensive Guide to the Hazardous Properties of Chemical Substances 3rd. Hoboken: John Wiley & Sons. 2007. ISBN 978-0-471-71458-3.
- Siegemund, Günter; Schwertfeger, Werner; Feiring, Andrew; Smart, Bruce; Behr, Fred; Vogel, Herward; McKusick, Blaine, Fluorine Compounds, Organic, Wiley, 2000-06-15, ISBN 978-3-527-30385-4, doi:10.1002/14356007.a11_349
- Wiberg, Egon; Wiberg, Nils; Holleman, Arnold Frederick. Inorganic Chemistry. San Diego: Academic Press. 2001. ISBN 978-0-12-352651-9.
外部連結[編輯]
- 元素氟在洛斯阿拉莫斯國家實驗室的介紹(英文)
- EnvironmentalChemistry.com —— 氟(英文)
- 元素氟在The Periodic Table of Videos(諾丁漢大學)的介紹(英文)
- 元素氟在Peter van der Krogt elements site的介紹(英文)
- WebElements.com – 氟(英文)
| 元素週期表(鹵素) | |||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| IA 1 |
IIA 2 |
IIIB 3 |
IVB 4 |
VB 5 |
VIB 6 |
VIIB 7 |
VIIIB 8 |
VIIIB 9 |
VIIIB 10 |
IB 11 |
IIB 12 |
IIIA 13 |
IVA 14 |
VA 15 |
VIA 16 |
VIIA 17 |
VIIIA 18 | ||||||||||||||||||||
| 1 | H | He | |||||||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | |||||||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |||||
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |||||
| |||||||||||||||||||||||||||||||||||||
| |||||||||||||||||




























