维生素D
| 維生素D | |
|---|---|
| 药物种类 | |
 膽鈣化醇 (D3) | |
| 生物靶标 | 維生素D受體 |
| ATC代码 | A11CC |
| 外部链接 | |
| MeSH | D014807 |
| AHFS/Drugs.com | MedFacts天然产品 |
維生素D(英語:Vitamin D)是一種親脂性類固醇衍生物,為一種激素的前體,屬於脂溶性維生素,負責促進腸道對鈣、鎂和磷酸鹽的吸收,另外還有其他多種生物效應[1]。對人類而言,維生素D中最重要的化合物是維生素D2(麥角鈣化醇)和維生素D3(又稱為膽鈣化醇)[2]。維生素D對鈣元素在人體內的平衡和代謝中具有重要作用,可用以預防佝僂病和「成人骨軟化症」,與鈣質合用可以預防出現常見於老年人群的骨質疏鬆症。此外,維生素D對於神經肌肉功能、炎症都有功效,同時還影響許多基因的表達和轉譯,調節細胞的增殖、分化和凋亡[3]。
維生素D的主要天然來源是通過日光照射后在皮膚表皮的下層的化學反應生成膽鈣化固醇(特別是UVB輻射)[4][5],而维生素D3需由紫外線照射后,由7-脫氫膽固醇經光照進行光化學反應轉變而成,動物皮膚細胞中含有7-脫氫膽固醇,因此多曬太陽是獲取维生素D的簡易方法。人類一天只需暴露在陽光下10分鐘,自身即可合成足夠的维生素D3[6]。由於每個人對陽光耐受有差異,而且考慮到罹患皮膚癌的風險,因此關於安全的日照量的建議尚不確定,參考膳食攝入量通常會假設一個人的所有維生素D都是通過口腔攝取[7]。
膽鈣化醇和麥角鈣化醇可以從飲食和補充劑中攝取[2][8][9]。只有少數食物,例如富含脂肪的魚類,天然含有顯著大量的維生素D[7][10]。在美國和其他國家或地區,牛奶和植物奶的替代品都富含維生素D,而許多早餐穀物也是如此。暴露於紫外線下的蘑菇也能提供有用的維生素D[7]。
飲食中或皮膚合成中的維他命D於生物學上缺乏活性,它需要透過兩種蛋白質酶羥基化的步驟激活,首先在肝臟中進行,其後在腎臟中進行。由於大多數哺乳類動物暴露於充足的陽光下即可合成足夠分量的維生素D,因此維生素D並非必需的。所以,從技術上講它並不是一種維他命[9]。相反,它可以被認為是一種激素,其中激活維他命D激素原,形成骨化三醇的活性形式,然後透過核受體在多個位置產生作用[9]。膽鈣化固醇在肝臟中轉化為骨化二醇(25-羥基膽鈣化固醇);麥角鈣化醇被轉化為25-羥基麥角鈣化固醇,然後這些物質作為一種激素重新進入循環系統,調節鈣和磷的吸收,促進骨骼的生長和重構。骨化二醇活性不高,必須經肝臟及腎臟的酶促反應,最終生成骨化三醇,這才是其活性最高的形式,可以調節小腸、腎臟和骨骼對鈣的吸收與代謝。
維生素D會進一步被腎臟羥化形成維他命D的生物活性形式──骨化三醇(也稱為1,25-二羥基膽鈣化固醇)[11]。骨化三醇在血液中作為激素循環,主要作用是調節鈣和磷酸鹽的濃度,並促進骨骼的健康生長和重塑。骨化三醇還具有其他作用,包括對細胞生長、神經肌肉和免疫功能以及減輕炎症的作用[7]。
在血清中測量兩種維他命D代謝物(稱為25-羥基維生素D或25(OH)D)的含量,可以以此確定一個人的維他命D狀況[12][13]。檢測血漿中的維他命D3可以反映UVB照射皮膚合成與食物攝入的維他命D的總水平,現在主要認為人體內獲取維他命D的主要途徑是由人體自身合成。維他命D對人體有益的最佳證據是對骨骼有益處並減少老年女性的死亡率,然而在一般人口統計中並沒有一致的證據顯示維他命D對健康有影響的效果。
維他命D的發現是由於努力尋找佝僂病兒童(兒童時期的軟骨症)所缺乏的飲食物質(維他命D3)[14],此病症較常見於寒帶地區,由於當地居民須穿著厚重衣物以防寒,隔絕了陽光對皮膚的照射,因此無法自行生成維他命D3,只能經由飲食攝取來改善。維他命D補充劑可治療或預防軟骨症和佝僂病,然而在普遍人群中對補充維他命D的其他健康影響的證據不一致[15][16]。補充維他命D對死亡率的影響尚不清楚,一項綜合分析發現,老年人的死亡率略有下降[17],另一個建議服用補充劑以預防多種疾病的建議則沒有明確理由的結論,因此在這些領域中無需進行類似設計的進一步研究[18]。攝取過量的維他命D會導致中毒,因爲這會使軟組織出現鈣化現象。
種類
[编辑]| 名稱 | 化學名稱 | 化學結構 |
|---|---|---|
| 维生素D1 | 麥角鈣化醇和光甾醇的比例為1:1的分子化合物 | |
| 维生素D2 | 麥角鈣化醇(由麥角固醇形成) | 
|
| 维生素D3 | 膽鈣化醇(7-脫氫膽固醇於皮膚上形成) 骨化三醇(维生素D3的在體內的活性形式 — 1,25-二羥膽鈣化醇) |

|
| 维生素D4 | 22-二氫麥角鈣化醇 | 
|
| 维生素D5 | 谷鈣化醇 (7-脫氫谷固醇形成) | 
|
維生素D有很多種不同的形式存在。兩種最主要的維生素D種類分別是維生素D2(麥角鈣化醇)和維生素D3(膽鈣化醇),它們統稱為鈣化醇。1932年,研究人員闡明了維生素D2的結構,而人們於1936年發現了維生素D3,並發現它可以由7-脫氫膽固醇經紫外線照射轉化而成[19]。沒有下標的是涵蓋所有維生素D,指D2或D3或是兩者,這些統稱為鈣化醇[20]。維生素D2的化學特徵是在1931年獲證明,維生素D3的化學結構於1935年建立,並證明是紫外線照射7-脫氫膽固醇而產生的[21]。從化學結構上來說,維他命D都屬於開環甾體化合物,也就是甾體激素的一個環狀結構打開了[21],維生素D2與維生素D3結構的不同之處在於其側鏈,維生素D2的22和23位碳之間是雙鍵,而且在24位碳上多了一個甲基;維生素D3(膽鈣化醇)可以由其前體7-脫氫膽固醇經過紫外線照射變構形成,只要讓皮膚暴露於充足的紫外光下即可以自然產生足夠維生素D3的分量,奶製品廠家通常把牛奶置於紫外線光下,以強化其中的維生素D3。
化學上,各種形式的維他命D都是開環甾體,即類固醇,類固醇環的其中之一個鍵被破壞[21]。維他命D2和維他命D3之間的結構差異在於D2在碳22和23之間包含著一個側鏈,以及在碳24上有一個甲基。
維他命D2是麥角固醇的衍生物,麥角固醇之所以以「麥角」命名,因為它是從一種名為麥角菌的真菌細胞膜上找到的固醇。麥角固醇同時也可以由浮游生物、無脊椎動物以及其他真菌合成。麥角固醇一經合成,在紫外線照射下就可以轉化為麥角鈣化醇,陸地動物和脊椎動物中的維他命D2,由於牠們體內不能合成麥角固醇,但能夠合成維他命D3[22],但關於人類只服用維他命D2能否代替維他命D3攝入的討論,當中的爭論還是很激烈[23][24]。
生物學
[编辑]活性維他命D代謝物骨化三醇透過跟主要位於靶細胞的細胞核中的維他命D受體(VDR)結合來介導其生物學作用[21]。骨化三醇與VDR的結合使VDR可以作為轉錄因子來調節轉運蛋白的基因表達(如TRPV6和鈣合蛋白),它們參與腸道中鈣質的吸收[25]。維他命D受體屬於類固醇/甲狀腺激素受體的核受體超級家族,以及VDR表現於大多數器官的細胞中,包括腦、心臟、皮膚、生殖腺、前列腺和乳房。
在小腸、骨骼、腎臟及甲狀旁腺細胞的VDR激活導致血液中鈣和磷的水平得以維持(在甲狀旁腺激素和降鈣素的輔助下),並維持了骨骼含量[1]。
維他命D的最重要作用之一是透過促進腸道內的鈣代謝以維持骨骼中鈣質的平衡,並通過增加破骨細胞的數量和保持成骨作用中鈣和磷酸鹽水平以促進骨吸收,並讓甲狀旁腺激素的正常運作以維持血清中鈣的水平。維他命D缺乏症會導致骨骼礦物質密度降低,並由於缺乏維他命D會改變人體中的礦物質代謝,導致骨密度降低(骨質疏鬆症)或骨折風險的增加[26]。因此,維他命D通過作為骨吸收中有效刺激物的作用,這對骨骼重塑也至關重要[26]。
VDR調節細胞增殖和細胞分化。維他命D也影響免疫系統,而VDR在幾種白血球中表達,包括單核白血球和活化的T細胞和B細胞[27]。在體外,維他命D增加腎上腺髓質細胞中酪氨酸羥化酶基因的表達,並影響了神經營養因子、一氧化氮合酶及穀胱甘肽的合成[28]。
維他命D受體的表達會隨年齡增長而降低,研究結果表明維他命D與肌肉力量、質量和功能直接相關,而所有這些都是影響運動員表現的重要因素[29]。
膳食攝入
[编辑]建議攝入量
[编辑]| 美國 | ||
| 年齡組別 | RDA (IU/日) | (μg/日)[30] |
|---|---|---|
| 0–6個月嬰兒 | 400* | 10 |
| 6–12個月嬰兒 | 400* | 10 |
| 1–70歲 | 600 | 15 |
| 71+歲以上 | 800 | 20 |
| 懷孕/哺乳 | 600 | 15 |
| 年齡組別 | 容許攝入量上限(IU/日) | (μg/日) |
| 0–6個月嬰兒 | 1,000 | 25 |
| 6–12個月嬰兒 | 1,500 | 37.5 |
| 1–3歲兒童 | 2,500 | 62.5 |
| 4–8歲兒童 | 3,000 | 75 |
| 9+歲 | 4,000 | 100 |
| 懷孕/哺乳 | 4,000 | 100 [30] |
| 加拿大 | ||
| 年齡組別 | RDA (IU) | 容許攝入量上限(IU)[31] |
| 0–6個月嬰兒 | 400* | 1,000 |
| 6–12個月嬰兒 | 400* | 1,500 |
| 1–3歲兒童 | 600 | 2,500 |
| 4–8歲兒童 | 600 | 3,000 |
| 9–70歲兒童及成人 | 600 | 4,000 |
| 70歲以上成人 | 800 | 4,000 |
| 懷孕/哺乳 | 600 | 4,000 |
| 澳洲及紐西蘭 | ||
| 年齡組別 | 充足攝入量(μg) | 最高攝入量(μg)[32] |
| 0–12個月嬰兒 | 5* | 25 |
| 1–18歲兒童 | 5* | 80 |
| 19–50歲成人 | 5* | 80 |
| 51–70歲成人 | 10* | 80 |
| 70歲以上成人 | 15* | 80 |
| 歐洲食品安全局 | ||
| 年齡組別 | 充足攝入量(μg)[33] | 可容忍上限(μg)[34] |
| 0–12個月嬰兒 | 10 | 25 |
| 1–10歲兒童 | 15 | 50 |
| 11–17歲兒童 | 15 | 100 |
| 成年人 | 15 | 100 |
| 懷孕/哺乳 | 15 | 100 |
| * 充足攝入量,尚未建立RDA/RDI | ||
轉換:1μg = 40 IU。
各種機構對維他命D的每日攝入量都提出了不同的建議。這些數據都根據精確的定義,因應不同的年齡、懷孕或哺乳期而有所不同,關於維他命D對皮膚的合成作出了程度的假設[30][31][32][33]。
美國
[编辑]由美國醫學研究所(IoM,2015年更名為美國國家醫學研究院)於2010年發布的維他命D膳食參考攝入量,取代了先前的建議,這些建議是根據攝入量表示的。提出建議的前提是,假設由於暴露在陽光下不足,個別人士皮膚不能合成維他命D。維他命D的參考攝入量指的是食物、飲料和補品中的總攝入量,並假設已滿足鈣的需求[30]。參考膳食攝取量(UL)被定義為「幾乎對所有普通人來說的幾乎沒有健康不利影響風險的每天平均營養素的最高攝入量[30]。」儘管人們認為參考膳食攝取量十分安全,但有關長期影響的信息並不完整,因此不建議長期攝入這些分量[30]。
為了美國食品和膳食補充劑標籤的目的,每份的含量表示為每日數值的百分比(%DV)。維他命D標籤的目的,每日數值的100%為400 IU(10 μg),然而在2016年5月27日,該標準修訂為800 IU(20 μg),以使其與RDA達成一致[35][36]。對於每年食品銷售額超過1,000萬美元的食品製造商,必須在2020年1月1日之前遵守最新的標籤規定,而每年食品銷售額不足1,000萬美元的食品製造商,則必須於2021年1月1日之前達到更新的標籤法規[37][38][39]。在2020年1月1日合規日期之後的前六個月中,FDA計劃與製造商合作以達到新的營養成分標籤要求,並且在此期間將不著重於針對這些要求的執法行動[37]。參考每日攝入量的新與舊表中列出了每日成人數值量。
加拿大
[编辑]根據美國醫學研究所的報告[30],加拿大衛生部於2012年發布了建議膳食攝入量(RDA)及維他命D的攝入量上限[31]。
澳洲及紐西蘭
[编辑]澳洲及紐西蘭在2005年發布了營養參考值,當中包括了飲食中維他命D的攝入量指南[32]。大約有三分之一的澳洲人缺乏維他命D[40]。
歐盟
[编辑]歐洲食品安全局(EFSA)於2016年審視了目前的證據[33],發現血清25(OH)D濃度與與肌肉骨骼健康的結果有很大的差異。他們認為無法得出維他命D的平均需求量與人口參考維他命D的攝入量值,血清25(OH)D濃度為50 nmol / L是合適的目標值。對於所有1歲以上的人們,包括孕婦或哺乳期的婦女,他們設定的每日攝入量為每天15μg(600 IU)[33]。
EFSA審查了2012年的安全攝入量[34],成年人的容許上限為每天100μg(4,000 IU),這與IOM有類似的結論。
英國國民保健署建議6個月至5歲的嬰幼兒、懷孕或哺乳婦女,以及缺乏陽光的老年人應每天服用維他命補充劑,以確保攝入足夠的維他命D[41]。2016年7月,英國公共衛生部建議每人都考慮在秋季和冬季每天服用10µg的維他命補充劑,因為該時期的日光不足以合成維他命D[42]。
瑞典國家食品管理局建議,對於75歲以下的成人和兒童,每天應攝入10μg(400 IU)的維他命D3,而75歲及以上的成年人應服用20μg(800 IU)的分量[43]。
歐洲的非政府組織提出了其建議:德國營養學會推薦20μg[44];歐洲更年期協會建議更年期婦女於70歲之前服用15μg(600 IU),以及從71歲開始服用20μg(800 IU)。對於某些維他命D含量很低或合併症的患者,該劑量應增加至100μg(4,000 IU)[45]。
其他
[编辑]- 隨着近幾十年對維他命D的認識不斷加深,其重要性和需求量也在不斷調整,例如:
- 妊娠期和哺乳期女性應適當增加攝入量,以維持正常的血液濃度,特別是在高緯度地區和預產期在春冬季節的孕婦。但需注意的是維他命D的攝入量不是越高越好。
- 在陽光下曬15分鐘,而且維持每星期幾天,能夠在一定程度上防止缺乏維他命D[48]。
- 過量表現:長期臨床實踐表明,一次性地注射30萬個單位能夠保證其安全性,但60萬單位則有過量中毒的風險;而口服中毒風險有個體差異存在,目前現有的實驗數據表明持續補充維生素D每日4,000-10,000國際單位不超過2個月未觀察到中毒現象。但由於維生素D為脂溶性,還是應該避免長期過量服用。建議在新的理論支持出現以前,預備終身服用者,每天的預防保健補充量不超過2,000國際單位(治療劑量除外)。維生素D中毒的症狀是異常口渴,眼睛發炎,皮膚瘙癢,厭食、嗜睡、嘔吐、腹瀉、尿頻以及鈣於血管壁、肝臟、肺部、腎臟、胃中的異常沉澱,關節疼痛和瀰漫性骨質脫礦化。
來源
[编辑]因維他命D在大多數食物中都不是天然存在的[2][9],故其通常作為食品強化劑被添加到加工食物中。在某些國家/地區,主食都以維他命D來人工強化[49]。
天然來源
[编辑]通常,維他命D2都是發現於真菌中,而維他命D3都在動物中發現[50][51]。維他命D2是由許多真菌中發現的麥角固醇在紫外線照射下產生的。蘑菇和地衣會隨著紫外線的照射而增加維他命D2的含量[52][53]。這個過程於工業紫外線燈的模擬下,維他命D2有更高的濃度[51]。
美國農業部報告維他命D2和D3含量合計為一個值:
| 來源 | 每克(μg) | 每克(IU) | |
|---|---|---|---|
| C. 地衣, 葉狀體, 乾的[52] | 維他命D3 | 0.67 – 2.04 | 27 – 82 |
| 維他命D2 | 0.22 – 0.55 | 8.8 – 22 | |
| 雙孢蘑菇(一般蘑菇):D2 + D3 | |||
| 波多貝羅(Portobello) | 原始的 | 0.003 | 0.1 |
| 暴露於紫外線下 | 0.112 | 4.46 | |
| 克里米尼(Crimini) | 原始的 | 0.001 | 0.03 |
| 暴露於紫外線下 | 0.319 | 12.76 | |
| 來源 | 每克(IU) | 不規則狀況 |
|---|---|---|
| 煮熟的蛋黃 | 0.7 | 61克的蛋含有44 IU |
| 已煮熟的紅燒牛肝 | 0.5 | |
| 魚肝油 | 100 | 每茶匙含450 IU(4.5 克) |
| 脂肪魚類 | ||
| 已乾熱煮熟粉紅色的鮭魚 | 5.2 | |
| 已乾熱煮熟的混合品種鯖魚 | 4.6 | |
| 油浸罐裝吞拿魚 | 2.7 | |
| 油浸沙丁魚罐頭 | 1.9 | |
食品強化
[编辑]含有維他命D的加工食品強化包括了一些果汁和果汁飲品,代餐能量棒、大豆蛋白的飲料、某些奶酪和奶酪產品、麵粉製品、嬰兒配方奶粉、許多早餐穀物和乳製品[55][56]。
2016年,美國食品藥品監督管理局(FDA)修改了牛奶強化食品添加劑的法規[57],規定每100克乳製品中的維他命D3含量不得超過42 IU(美國每夸脫的400 IU);每100克的植物奶有84 IU的維他命D2(每夸脫800 IU);而基於植物的乳酪或在大豆飲料產品中,每100克含有89 IU(每夸脫800 IU)[58][59][60]。植物奶被定義為由大豆、杏仁、米以及其他可替代為乳汁的植物來源而製成的飲料[61][62]。
雖然一些研究發現維他命D3可以更快地提高血液中25(OH)D的水平,並在體內保持更長的活躍時間[63][64],然而其他研究則認為維他命D2的來源具有相同的生物利用度,以及如維他命D3般有效用於提高和維持25(OH)D[51][65][66]。
食物準備
[编辑]典型的食物中的維他命D含量會因烹飪而減少。煮沸、油炸和烘烤食品可保留原始維他命D的69–89%[67]。
維他命D缺乏症
[编辑]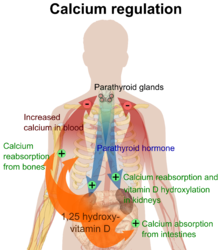
全世界估計有十億人處於維他命D不足或缺乏[29]。維他命D不足的飲食加上日照不足會導致缺乏維他命D。兒童嚴重缺乏維他命D會導致患上佝僂病,這是一種骨骼的軟化和弱化的疾病,是一種發達國家中罕見的疾病[69]。維生素D缺乏症發現於世界各地的老年人中,在兒童及成年人中仍然很常見[70][71][72]。缺乏症會導致骨骼礦化受損和骨骼損傷,從而導致出現骨骼軟化疾病[73],包括兒童的佝僂病和成人的軟骨病。避免日曬會導致血液中的骨化二醇(25-羥基維他命D)含量低[74]。維他命D缺乏會導致飲食中腸道對鈣的吸收下降至15%[1]。當不缺乏時,一個人通常吸收60-80%[1]。
皮膚色素沉著
[编辑]生活在溫帶氣候中的深色皮膚的人被指出具低維他命D水平,但這個含義並不明確[75][76][77]。深色皮膚的人產生維他命D的效率較低,因為其皮膚裡的黑色素會阻礙維他命D的合成[78]。維生素D缺乏症常見於美國的西班牙裔和非裔美國人,其維他命D水平會於冬季中顯著下降[22]。這是由於他們皮膚裡的黑色素所導致,黑色素是天然的防曬霜[22]。
骨骼健康
[编辑]佝僂病
[编辑]一種兒童時期的疾病 — 佝僂病,好發於3—18個月大之間[79],其特點是其骨骼生長受到阻礙,變得柔軟和虛弱,隨著幼童開始學步時,變形的長骨會因其體重的作用下而變得彎曲。北美和其他西方國家相繼有病例指出,首見於母乳餵養的初生嬰兒,以及膚色較深的人[79]。佝僂症的特徵是弓腿[73]——可能是因缺乏鈣或磷及缺乏維他命D引起的;如今,該病主要在非洲,亞洲或中東等低收入國家中發現[80]許多患有遺傳疾病的人(如偽維他命D缺乏性佝僂病)[81]。
孕婦維他命D缺乏症可能會導致嬰兒於出生前就出現明顯的骨骼疾病以及出生後骨骼質量受損[82][83]。營養性佝僂病(Nutritional rickets)存在於一年四季都有陽光的國家,例如尼日利亞,並且可在不缺乏維他命D症的情況下發生[84][85]。
儘管現在英國很少發生佝僂病和骨質疏鬆症,但卻大量發生在某些移民社區,其中骨質疏鬆症的患者包括了穿著西式服裝、在看似在充足的日光下進行戶外活動的婦女[86]。除非飲食偏離以高攝入量的肉類、魚類和蛋以及低攝入量的高提取物穀物為特徵的西方雜食動物習慣,膚色較黝黑和減少陽光照射不會產生此病[87][88][89]。佝僂病的飲食風險因素包括禁止食用動物食品[86][90]。
在大多數國家中,維他命D缺乏症仍然是嬰兒的主要病因,因為母乳中的維他命D含量不足,且社會風氣和氣候條件使人們避免獲得足購的日曬。在陽光充足的國家,例如尼日利亞,南非和孟加拉國,發病於較年長學步的幼會和兒童中,它被歸因於飲食中鈣攝入量低,這是只能有限地使用乳製品並佐以穀物為基礎的飲食[89]。
佝僂病曾是美國的主要公衛問題。在丹佛,同一緯度的紫外線強度比海平面強20%[91],在1920年代後期,近500名兒童中有近三分之二患有輕度的佝僂病[92]。20世紀美國飲食中的動物性蛋白比例增加[90][93]加上牛奶的消耗量增加[94][95],強化相對維他命D含量較少的情況下,佝僂病病例的數字急劇下降[1]。同樣,在美國和加拿大,維他命D強化牛奶、嬰兒補充劑和維他命補充劑已消除大多數佝僂病兒童所患有的脂肪吸收不良[73]。
骨質疏鬆症和骨軟化病
[编辑]骨質疏鬆症是成年人的維他命D缺乏引起的疾病。該疾病的特徵是使骨骼軟化,導致脊柱彎曲、腿部彎曲、近端肌肉無力、骨骼脆弱,增加骨折風險[96]。骨質疏鬆症減少了鈣質的吸收並增加了骨骼中鈣質的流失,那增加了骨折的風險。骨質疏鬆症通常出現於25-羥基維他命D水平低於約10ng/mL時[2]。儘管人們認為軟骨病的影響可導致慢性肌肉骨骼系統疼痛[97],這裡沒有具說服力的證據指出慢性疼痛患者出現較低的維他命D水平[98],或該補充劑可減輕慢性非特異性肌肉骨骼疼痛[99]。
補充劑的使用
[编辑]維他命D補充劑是預防或治療佝僂病的一個可靠方法,然而它對非骨骼健康的影響尚未確定[16][100]。2013年的一項評論發現,除了可以降低老年人的死亡率外,並沒有發現補充劑對非骨骼疾病發生率有任何影響[101]。維他命D補充劑不會改變心肌梗塞、中風或腦血管疾病、癌症、膝蓋骨關節炎的結果[18][102]。維他命D水平可能是疾病引起,而非引致疾病的發生[101]。美國醫學研究院(IOM)的一份報告指出:「跟癌症、心血管疾病及高血壓,以及糖尿病與代謝綜合症相關的結果,跌倒和身體機能、免疫功能和自體免疫性疾病、感染、神經心理機能及子癇前症都不能與鈣質或維他命D攝入可靠地聯繫在一起,並且經常出現相互矛盾[30]。」一些研究人員聲稱,IOM的建議過於明確,在計算與骨骼健康相關的維他命D水平時犯了數學上的錯誤[103]。IOM小組成員堅持認為他們使用了「飲食建議的標準程序」,並且該報告是完全基於這些數據。維他命D補充劑的研究,包括了大規模的臨床試驗,繼續正在進行中[103]。
骨骼健康
[编辑]在一般情況下,人們普遍認為維他命D補充劑有助預防骨質疏鬆症的觀點並沒有很好的證據支持[18]。它通常用於預防這種疾病,因此那些沒有維他命D缺乏症的人可能沒有需要[104]。對於患有骨質疏鬆症的老年人,把維他命D跟鈣質一同服用可能有助於預防髖部骨折,但它也會輕微增加了患上胃部及腎臟疾病的風險[105]。在65歲以上的人裡,調高劑量的維他命D補充劑可以降低骨折風險[106]。對於獨立生活的人而言,其影響是很小甚至是沒有的[107][108]。低血清維他命D水平跟跌倒與低骨質密度有關[109]。然而,服用額外的維他命D似乎並沒有改變風險[110]。維他命D缺乏症的運動員,特別是那些從事接觸運動的人,他們會增加患上疲勞性骨折及/或嚴重骨折的風險。補充劑最大的好處可見於25(OH)D血清水平不足(<30 ng/mL),或25(OH)D血清水平嚴重不足(<25 ng/mL)的人身上。血清25(OH)D濃度升高穩定在50 ng/mL時,可觀察到風險增加,而在超過這一點的水平上,沒有其他可見的額外好處[111]。
由於發現了越來越多的有益於骨骼健康的證據,儘管它沒有找到其他益處的充分證據,美國食品藥品監督管理局(FDA)自2016年5月起要求製造商於營養標籤上聲明維他命D的含量,以作為「具有公共衛生意義的營養素」。每年食品銷售額少於$1,000萬美元的小型製造商透過提議的截止日期延長,將必須在2021年1月1日之前遵守法規,而較大的則必須在2020年1月1日之前遵守[38]。單一成分糖(例如蜜糖和楓糖漿)及某些蔓越莓產品的製造商必須在2021年7月1日之前作出更改[38]。
癌症
[编辑]維他命D補充劑因其聲稱的抗癌特性而被廣泛銷售[112]。在觀察性研究中,維他命D水平低與某些癌症的發生風險之間存在著關聯[113]。然而,尚未清楚在飲食中或作為維他命D補充劑是否會影響癌症的風險。評論把證據描述為「因果關係不一致,不確定,並且不足以告知營養需求」[30],和「不足以得出結論」[107]。2014年的一篇評論發現補充劑對癌症風險沒有顯著影響[18]。
2014年的另一篇評論得出結論,維他命D3可以降低癌症的死亡風險(在5年內接受治療的150人中,死亡人數減少了1人),但注意到對數據質量的擔憂[17]。儘管有證據表明維他命D缺乏症對某些癌症結果更糟[114],在診斷時有較高的25-羥基維他命D水平與更好的結果有關[115]。
心血管疾病
[编辑]服用維他命D補充劑並不能有效降低中風、腦血管疾病、心肌梗塞或冠狀動脈疾病的風險[18][116]。補充劑可能對血壓並沒有影響[117]。
免疫系統
[编辑]自身免疫性疾病
[编辑]儘管有初步數據表明哮喘跟維他命D水平低有關,但支持補充劑對哮喘患者具有益作用的證據則沒有證據支持[118]。一項評論發現,維他命D補充劑可以減少用於抑制輕度至中度哮喘發作頻率類固醇的需要,並且這種補充對日常哮喘症狀沒有影響[119]。在一般情況下,維他命D補充劑是並不建議用於治療或預防哮喘[120]。
發炎性腸病
[编辑]維他命D含量低與兩種人類炎症性腸病(IBD)的主要形式有關:克隆氏症及潰瘍性結腸炎[121]。對於患有維他命D缺乏症的IBD患者進行維他命D治療的綜合分析顯示,補充劑可有效糾正維他命D水平,並與臨床疾病活動及生化標誌物指標的改進有關[122]。
傳染病與COVID-19
[编辑]通常,維他命D的功能是激活先天免疫系統和抑制後天免疫系統[123]。缺乏症跟病毒性疾病的風險或嚴重性增加有關,包括HIV[124][125]。維他命D的含量過低似乎是結核病的風險因素[126],在歷史上一直被用作治療用途[127]。補充劑可稍微降低急性呼吸道感染的風險和嚴重程度,也可減輕哮喘的惡化[128][129]。這裡沒有證據表明維他命D影響5歲以下兒童的呼吸道感染[130]。
2019冠状病毒病疫情引起人們對維他命D缺乏症可能是呼吸道感染的危險因素的關注[129][131][132][133],但只有初步證據證明維他命D缺乏症和COVID-19感染之間存在直接關聯[134]。一項英國的研究發現,當對族群等潛在的混雜因素進行調整時,先前所測量得到的維他命D水平跟COVID-19感染的發生率之間並沒有關聯[135]。維他命D缺乏症在許多COVID-19病例和死亡人數最多的國家中很普遍,例如美國,西班牙,英國,意大利和伊朗[131][133]。一份由UK NICE發表的證據摘要得出結論,這裡沒有任何證據支持以維他命D補充劑用作預防或治療COVID‑19[136]。根據ClinicalTrials.gov,一些第二至四期臨床試驗正在進行以評估使用維他命D預防或治療COVID‑19感染的用途。截至2020年5月,大多數研究都處於初步階段,尚未完成[137]。大多數試驗的設計都是用以研究維他命D缺乏症的COVID-19感染者[137][138] 。
其他狀況
[编辑]- 糖尿病 — 2014年的系統評價的結論是,現有的研究顯示,沒有證據表明維他命D3補充劑對葡萄糖穩態或糖尿病的預防有效[139]。2016年的一篇評論文章報告指,儘管越來越多的證據表明維他命D缺乏可能是糖尿病的風險因素,關於維他命D水平跟糖尿病的全面證據是互相矛盾的,這方面需要進一步研究[140]。
- 抑鬱症 — 維他命D補充劑對於抑鬱症狀的臨床試驗普遍是低質量並沒有顯示整體效果,儘管小群分析顯示,對於具有臨床上明顯的抑鬱症狀或抑鬱障礙的參與者俱有中度療效[141]。
- 認知與癡呆 — 一份臨床研究的系統性評價維他命D水平低與認知障礙之間存在著關聯,以及患上阿茲海默症有更高的風險。然而,較低的維他命D濃度也跟營養不良和戶外活動時間減少有關。因此無法確定對於增加存在認知障礙的替代解釋,以及由此而來的維他命D水平與認知之間的直接因果關係[142]。
- 體重減少 — 儘管假設維他命D補充劑在除了卡路里限制以外對肥胖症來說可能是一種有效的治療方法,一項系統性評價發現補充劑與體重或脂肪量沒有關聯[143]。2016年的一份元分析發現減輕體重可改善循環維他命D的狀態,這表明脂肪量可能跟血液中維他命D的水平成反比[144]。
- 懷孕 — 懷孕期間的維他命D含量低跟妊娠糖尿病、妊娠毒血症和細小嬰兒(胎齡)有關[145]。儘管孕婦在懷孕期間服用維他命D原則上會增加足月母親的維他命D的血液水平[146],但對於懷孕母親或嬰兒的全部益處尚未清楚[145][146][147]。孕婦在妊娠期間攝取足夠的維他命D可能會降低子癇前症[148]及積極免疫效果[149]的風險。維他命D補充劑還可能降低妊娠糖尿病、體型過小的嬰兒[148]以及其生長速度不良的風險[150]。孕婦通常不會服用維他命D的建議用量[149]。
允許的健康聲明
[编辑]政府監管機構針對食物和膳食補充劑行業規定了於包裝上聲明某些允許範圍的健康聲明:
- 美國食品藥品監督管理局(FDA)—
- 「充足的鈣和維他命D作為均衡飲食的一部分,加上體育鍛鍊,可以降低患上骨質疏鬆症的風險[153]。」
死亡率的所有成因
[编辑]初步發現維他命D3補充劑可降低老年人的死亡風險[17][101],但效果尚未得到足夠明顯和足夠肯定使補充劑值得推薦[18]。其他形式(維他命D2、阿法骨化醇和骨化三醇)似乎對死亡風險沒有任何有益的作用[17]。血液中較高的水平似乎跟較低的死亡風險有關,但尚未清楚補充劑是否可以帶來這種益處[157]。過量及缺乏維他命D都會導致身體功能異常和過早衰老[158][159][160]。血清降鈣素水平與死亡率的所有成因之間的關係是呈拋物線的[30]。在黑色人口中出現維他命D含量較低的維他命D危害似乎較低於白色人口[30]。
維他命D過量
[编辑]維他命D毒性很少[72],這是由於高劑量的維他命D補充劑而非陽光引致的。維他命D毒性的下限尚未確定;然而根據一些研究,對於9-71歲的年齡組別的最高容許攝入量(UL)為每天4,000 IU(每天100 µg)[161],而其他研究得出的結論是,在健康的成年人中,持續攝入超過每天1,250μg(50,000 IU)可在幾個月後產生明顯的毒性,並可以增加血清25-羥基維他命D水平增加至150 ng/mL或更高[72][162]。那些患有某些疾病,例如原發性副甲狀腺功能亢進症[163]對維他命D更加敏感,並為了應對維他命D營養增加時會產生高血鈣症,而孕婦在懷孕期間的高鈣血症可能會增加對維他命D作用的胎兒敏感性,及智力低下綜合症和臉部畸形[163][164]。
突發性嬰兒高鈣血症(Idiopathic infantile hypercalcemia)是由於CYP24A1的基因突變引致的,導致這種基因突變的嬰兒減少對維他命D的降解。患有這種基因突變的嬰兒對維他命D的敏感性增加,如果額外攝入的話會有發生高鈣血症的風險[165][166]。這種紊亂可以持續到成年[167]。
2015年發表的一篇評論指出,僅在25(OH)D血清濃度高於200 nmol/L時才報告有不良反應[168]。已知的涉及高鈣血症的已公佈毒性病例(其中已知的維他命D劑量和25-羥基維他命D水平為已知所有每天攝入≥40,000 IU(1,000 μg)[163]。
孕婦或哺乳期婦女在服用維他命D補充劑之前應諮詢醫生。FDA建議維他命D液體補充劑的製造商應清晰準確地將這些產品隨附的滴管標記為400 IU(1 IU為25 ng膽鈣化固醇/麥角鈣化固醇的生物等效物)。此外,對於用於嬰兒的產品,FDA建議滴管的容量不能超過400 IU[169]。對於嬰兒(由出生起至12個月),其允許的上限(無傷害的最大可以忍受量)設定為每天25 μg(1,000 IU)。對嬰兒來說,每天1,000mg的話,在一個月內會產生毒性[162]。受加拿大和美國政府委託,國家醫學科學院(IoM)截至2010年11月30日[update]已將1至3歲年齡段的容許上限(UL)增加至每天2,500 IU,4至8歲的兒童每天3,000 IU,而9-71歲以上則是每天4,000 IU(包括了孕婦或哺乳期婦女)[161]。
骨化三醇本身以負反饋周期自動調節,並且受到副甲狀腺激素、成纖維細胞生長因子23、細胞因子、鈣質和磷酸鹽的影響[170]。
過量的影響
[编辑]維他命D過量會引致高鈣血症,這是維他命D毒性的強烈顯示 — 透過排尿和口渴的增加可以注意到這一點。若高鈣血症不獲處理,其結果會引致鈣質於軟組織和器官(如腎臟,肝臟和心臟)有過量的沉積,最後導致疼痛和器官損傷[72][73][96]。
維他命D過量的主要症狀都是高鈣血症的症狀,包括食欲不振、噁心和嘔吐。這些可能隨後是多尿症、劇渴、虛弱、失眠、緊張、痕癢,最後是腎衰竭。此外,它有可能發展為蛋白尿、管型尿液、氮質血症及轉移性鈣化(尤其出現於腎臟)[162]。維他命D毒性的其他症狀包括幼兒智力低下、骨骼異常生長和形成、腹瀉、易怒、體重減輕和嚴重抑鬱[72][96]。
維他命D毒性可透過停止維他命D補充劑並限制鈣的攝入來處理。腎臟損害可能是不可逆轉的。長時間暴露於陽光下通常不會引起維他命D毒性。在皮膚中產生的維他命D前體的濃度達到化學平衡,並且產生的任何進一步的維他命D都會被降解[163]。
生物合成
[编辑]自然界中維他命D的合成取決於紫外線輻射的存在,以及隨後在肝臟和腎臟中的活化。許多動物從7-脫氫膽固醇合成維他命D3,許多真菌從麥角固醇合成維生素D2[50][51]。
光化學
[编辑]

把7-脫氫膽固醇轉化為維他命D3的轉化過程涉及兩個步驟[171][172]:首先,7-脫氫膽固醇在6-電子順旋/對旋開環電環化反應中被紫外線以光分解作用光解;其產物為前維生素D3。其次,維他命原D3自發地同分異構至維生素D3(膽鈣化醇),在σ遷移反應中的異面與同面。在室溫下,維生素原D3在有機溶劑中向維生素D3的轉化大約需要12天才能完成。皮膚中維他命原D3向維他命D3的轉化比有機溶劑中快約10倍[173]。
麥角固醇向維他命D2的轉化遵循相似的過程,透過光解形成維生素原D2,因而會異構化成維生素D2[174]。維他命原D2在甲醇中向維他命D2的轉化速率與維他命原D3相約。此過程於白色蘑菇中會更快[51](fig. 3)。
皮膚合成
[编辑]
在大多數脊椎動物的皮膚中(包括人類)[175],而裸鼴鼠似乎生來缺乏膽骨化醇[176],因為其血液中檢測不到25(OH)D,對某些動物來說,其厚厚的毛皮阻擋了紫外線,而這些鳥獸也有自己的辦法,牠們把7-脫氫膽固醇分泌到毛皮表面,合成維他命D3後再自己舔回肚子裡[177]。
維他命D3是由7-脫氫膽固醇以光化學方式產生的[178]。維他命D3的前體,7-脫氫膽固醇的產量相對較高。7-脫氫膽固醇在290-315 nm的波長下跟UVB光產生反應[179]。這些波長不僅存在於太陽光中,而且存在於室內曬黑中的紫外線燈發出的光(那是主要在UVA的光譜中產生紫外線,但通常會產生UVB總量的4%至10%)。透過窗戶暴露的陽光不足,因為玻璃幾乎會完全阻擋了UVB的光線[180][181]。
面部、手臂和腿部的皮膚適量地暴露於陽光下,可以產生足夠分量的維他命D,而每星期兩次,每次平均5–30分鐘,又或大約25%的時間,可將曬傷程度降至最低。皮膚顏色越深,日光越微弱,則需要暴露的時間越長。暴露在紫外線下不可能引致維他命D過量:皮膚達到平衡時,該維他命降解的速度與其產生的速度一樣快[72][182][183]。
防曬油把紫外線吸收或反射,並防止大部分紫外線到達皮膚[184]。根據UVB光譜得出的防曬係數(SPF)為8的防曬霜可使維他命D的合成能力降低95%,而SPF 15則使其降低98%[30]。
皮膚由兩個主要層級組成:主要由結締組織組成,稱為真皮的內層,以及外面比較薄的表皮[185]。厚表皮包括了手掌和腳底的五個層級組成,從外到內,它們是:角質層、透明層、顆粒層、棘層和基底層;維他命D於兩個最內層中產生角質形成細胞[186],分別是基底層和棘層[184]。
7-脫氫膽固醇在波長在270-300納米(峰值295-297納米)之間的紫外線照射下可以變構轉化為維他命D3[187],在陽光中的紫外線指數(夜間的紫外線指數為0,熱帶、高原地區、晴天時的紫外線指數為15),>3的時候或在日光浴燈下才會有這種能發揮作用的紫外線。日光浴燈產生的紫外線大多數是長波的UVA,而產生維他命D3所需要的是中波紫外線(UVB)佔其中的4-10%,從地域上說,熱帶地區的人每天都可以產生維他命D3,溫帶地區的人在春夏季節時也可以,而極地地區的人們,該處的紫外線強度幾乎不可能使其產生維他命D3[188]。血清25(OH)D的平均濃度的差異似乎應該隨緯度升高而降低,然而實際上並不跟預期的一致,例如在夏天,加拿大北部地區的日照強度與時間加起來比赤道地區的還要強,而且高緯度地區的生物於春夏季或秋季都有可能形成並儲存足夠的維他命D,UVB產生的維他命D功能(無法控制非酶促反應的異構作用)非常強大,以至於皮膚形成多餘的維他命D3必須及時降解掉,以免其產生毒性,最終使維他命D的合成和降解達到了平衡的狀態[189]。
身體合成
[编辑]維他命D透過血流輸送到肝臟,在那裏轉化為激素前體骨化二醇,循環中的骨化二醇在腎臟和單核巨噬細胞系統中轉化為骨化三醇,從而成為具有生物活性的維他命D,而在免疫系統中,骨化三醇(1,25(OH)D)發揮着細胞因子的作用,保護機體抵抗微生物入侵[190]。腎臟將骨化二醇轉化為骨化三醇釋放到血液中,跟維他命的結合蛋白結合,轉送到靶器官[21]。骨化三醇透過激活維他命D受體發揮生物學效應,VDR存在於靶細胞表面[21]的活化VDR可以作為轉錄因子,調節運載蛋白(如TRPV6和鈣結合蛋白)的表達,從而參與小腸內鈣的吸收[25]。VDR屬於核受體中類固醇/甲狀腺素受體超級家族,可以在大多數器官中表達,包括腦部、心臟、皮膚、前列腺和乳腺等,VDR在小腸、骨骼、腎臟和甲狀旁腺的表達能夠保證血鈣血磷代謝正常(這與甲狀旁腺激素和降鈣素協同作用),並可以維持正常骨的質量[191]。維他命D提高了腎上腺髓質細胞酪氨酸羥化酶的表達,也參與了神經營養因子、一氧化氮等物質的合成,並能提高機體穀胱甘肽的水平[28]。現在有意見認為VDR也干預了細胞增殖和分化,而且對免疫系統也起了很強的免疫促進作用,很多種白血球細胞包括單核細胞、T細胞、B細胞都能夠表達VDR[27]。VDR除了可以激活某些基因外,還有其他一些作用機理已經闡明,其中一個非常重要效果是,它可以抑制刺蝟激素(一種參與器官形成的激素)的信號轉導[192][193]。
維他命D最重要的功能就是保持骨骼中鈣質的平衡,它可以增強小腸對鈣質的吸收、提高破骨細胞的數量和增強骨吸收、維持血鈣及血磷濃度以維持正常骨量,並調整甲狀旁腺激素來維持血鈣平衡。缺乏維他命D會引致鈣磷代謝異常,導致骨質密度降低、骨質流失(骨質疏鬆症),甚至是骨折。
演化
[编辑]維他命D只能透過光化學過程合成。海洋中的浮游植物(例如鈣板金藻和赫氏圓石藻)已經超過5億年以來都是一直利用紫外線進行光合作用來合成維他命D。海洋中的原始脊椎動物可以把海洋中的鈣質吸收到其骨骼中,並食用富含維他命D的浮游生物來吸收該種維他命。
陸地上的脊椎動物已經超過3.5億年來以光合作用合成維他命D[194]。 牠們的鈣化骨骼需要植物以外的另一種維他命D來源。牠們必須攝取它,或暴露於陽光下才能在皮膚中進行光合作用[50][173]。對於硬骨類脊椎動物來說,離開富含鈣質的海水來到陸地上,維他命D對保證其骨骼中的鈣質來說非常重要,由於維他命D的合成必須要有紫外線參與,所以早期登陸岸上的脊椎動物必須把身體暴露於陽光下或者補充富含維他命D的食物來滿足其身體對維他命D的需求[173]。
在鳥類和帶有皮毛的哺乳類動物中,皮毛或羽毛會阻擋紫外線到達皮膚。相反,維他命D是由沉積於其羽毛或皮毛上皮膚的油性分泌物產生的,在修飾過程中通過口服獲得該種維他命[195]。然而,由於無法檢測到血清中25-OH維他命D水平,因此某些動物(如裸鼴鼠),是天然膽鈣化醇缺乏症的動物[196]。
工業合成
[编辑]維他命D3(膽鈣化固醇)的生產是通過將7-脫氫膽固醇暴露於UVB光下,然後進行純化來生產的[197]。7-脫氫膽固醇是魚類器官特別是肝臟中的天然物質[198],或廣泛存在於綿羊的羊毛脂(綿羊油)以及其他動物毛髮中的天然物質。
維他命D2(麥角鈣化醇)的生產方法也類似,利用酵母或蘑菇中的麥角甾醇作為起始原材料[197][51]。
合成機制
[编辑]| 皮膚中的7-脫氫膽固醇經紫外線照射後6號電子發生順旋電環化反應,形成前維他命D3。 | 
|
| 同時前維他命D3透過異側氫原子σ移位重排,變構產生維他命D3。在室溫的條件下,由前維他命D3轉化至維他命D3需時12天完成。 | 
|
| 不論是自身合成的還是食物中攝取到的維他命D3,都要在肝臟中處理,在25位碳上加上一個羥基,從而形成25-羥基膽骨化醇(骨化二醇/25(OH)D)[199]。這個過程是由肝臟微粒體酶——25羥化酶催化的,25(OH)D一經合成,便釋放到血液中,與α-球蛋白結合,就成為所謂的維他命D結合蛋白α-球蛋白結合體[200]。 | 
|
| 25(OH)D輸送到腎臟近段的腎小管,在那裏發生1-α(分子下角右邊的那個碳原子)位羥化而形成骨化三醇(1,25(OH)2D),可以有效的激活維他命D受體(VDR),活化的VDR介導維他命D所需要發揮的主要功能。25(OH)D向1,25(OH)2D的轉換需要25D31-α羥化酶,血液中甲狀旁腺激素水平升高可以提高這種酶的合成(當血鈣血磷降低時也可以)。 | 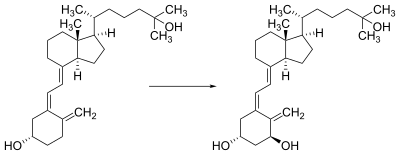
|
作用機理
[编辑]代謝活化
[编辑]
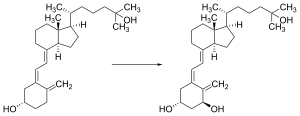
維他命D通過血流輸送到肝臟,它在這裡被轉化為前激素降鈣素,然後循環中的骨化二醇可在腎臟中轉化為骨化三醇,那是腎臟中維他命D的生物活性形式[190]。
無論是在皮膚中合成還是透過攝取而成,維他命D於肝臟中的位置25(分子的右上方)羥基化,以形成25-羥基膽鈣化固醇(骨化二醇/25(OH)D)[201]。該反應由CYP2R1這種人類基因微粒體酶的產物催化,並由肝細胞表達[202]。當製成後,該產物會被釋放到血漿中,並與稱為維他命D結合蛋白的α-球蛋白載體蛋白結合[203]。骨化二醇被輸送到腎臟的近端小管,它在1-α位置(分子的右下角)被羥基化,形成骨化三醇(1,25-二羥基膽鈣化固醇,1,2,5(OH)2D)。骨化二醇向骨化三醇的轉化是通過酶CYP27B1(25-羥基維他命D31-α-羥化酶)催化,這是人類基因「CYP27B1」的產物。CYP27B1活性的增加是透過甲狀旁腺激素以及低鈣或低磷酸鹽的環境[9][190]。
在腎臟的最後轉化步驟之後,骨化三醇會釋放到循環系統中。通過與維他命D結合蛋白的結合,骨化三醇被輸送到整個身體,包括腸道,腎臟和骨骼這些經典目標器官[21]。骨化三醇是維他命D受體中最有效的天然配體,它介導維他命D的大部分生理作用[9][190]。除腎臟外,骨化三醇還由某些其他細胞合成,包括免疫系統中的單核白血球至巨噬細胞。當單核白血球跟巨噬細胞合成時,骨化三醇局部作為細胞因子,通過刺激先天免疫系統調節針對微生物入侵者的身體防禦[190]。
鈍化
[编辑]骨化二醇和骨化三醇的活性可通過<span class="ilh-all " data-orig-title="維他命D324-羥化酶" data-lang-code="en" data-lang-name="英语" data-foreign-title="Vitamin D3 24-hydroxylase">[[:維他命D324-羥化酶|維他命D324-羥化酶]]的24位,分別形成分別骨鈣化醇(secalciferol)和(calcitetrol)進行羥基化來降低[201]。
基質之間的差異
[编辑]維他命D2(麥角鈣化醇)和維他命D3(膽鈣化醇)具有如上所述的相似作用機理[201]。維他命D2產生的代謝物於英文名稱上有時以「er-」或「ergo」作為為前綴來命名,使其與基於D3的配對物作區分[204]。
- 由維他命D2產生的代謝物往往與維他命D結合蛋白的結合較差。
- 維他命D3可以通過CYP27A1羥化為骨化二醇,但是維他命D2就不能。
- 麥角鈣化醇可以在位置24直接被羥基化。這種羥基化還導致更大程度的滅活:在24-羥基化作用後骨化三醇的活性降至原始水平的60%[205],骨鈣三醇轉化為鈣鈣鈦礦的活性降低了10倍[206]。
歷史
[编辑]美國研究人員埃爾默·麥柯倫和瑪格麗特·戴維斯於1914年在魚肝油中發現了一種物質,後來稱為「維他命A」[14]。英國醫生爱德华·梅兰比留意到以魚肝油餵養的狗沒有發展成佝僂病,並得出結論指它是維他命A,或可以預防這種疾病的一個密切相關的因素。1922年,麥柯倫測試了改良的魚肝油,其中維他命A被破壞了[14]。經改良的魚肝油治癒了患病的狗隻,因此麥柯倫得出結論,魚肝油中治癒佝僂病的因素不同於維他命A[207][208][209]。他把它稱為維他命D,因為它是第四個被命名的維他命[210][211]。最初人們並未意識到,它與其他維他命不同,維他命D可以由人體透過暴露於紫外線下合成。
1925年,當研究人員利用光照射7-脫氫膽固醇時,確立利用光照射7-脫氫膽固醇時,會產生了一種親脂性維他命(現在稱為維他命D3)[14]。阿爾弗雷德·法比安·赫斯指出:「光等於維他命D[212][213]。」德國格丁根大學的阿道夫·溫道斯,他於1928年因研究固醇的組成及其與維他命的關係而獲得諾貝爾化學獎,以表彰其在研究固醇與維他命之間關係的工作[214]。1929年,位於倫敦漢普斯特德的國立醫學研究所(NIMR)的一個小組正在研究目前尚未清楚的維他命D結構,以及類固醇的結構。他們跟約翰·伯頓·桑德森·霍爾丹、J·D·伯納爾及桃樂絲·霍奇金進行會議討論了可能的結構,這有助於使小組團結起來。X光晶體學分析顯示甾醇分子呈扁平狀,這跟溫道斯所領導的德國團隊提議的有所不同。1932年,奧托·羅森海姆(Otto Rosenheim)和哈羅德·金(Harold King)發表了一篇論文,提出了甾醇和膽汁酸的結構,這個論點立即被接受[215]。團隊成員羅伯特·本尼迪·鮑迪永、奧托·羅森海姆、哈羅德·金及肯尼斯·卡洛之間的非正式學術合作非常有成效,並導致維他命D的隔離和表徵的發現[216]。當時,英國醫學研究委員會的政策不是針對專利發現,而是認為醫學研究的結果應該向所有人開放。在1930年代,溫道斯進一步闡明了維他命D的化學結構[217]。
1923年,威斯康辛大學麥迪遜分校的美國生物化學家哈利·斯汀博克的研究顯示,紫外線照射增加了食物和其他有機物質中維他命D的含量[218][219]。在照射囓齒動物的食物後,斯汀博克發現囓齒動物的佝僂病得到治癒。維他命D缺乏是已知佝僂病的已知病因。斯汀博克於是利用自己的$300美元為其發明申請了專利。他把其技術用於食物,最讓人難忘的是用於牛奶。他的專利於1945年到期時,佝僂病在美國幾乎被淘汰了[220][221]。
1969年,在研究了腸道細胞的核碎片後,馬克·考斯勒(Mark Haussler)與安東尼·W·諾曼鑑定了一種稱為維他命D受體的維他命D特異性結合蛋白[222]。在1971–72年,維他命D進一步代謝以活性形式被發現。在肝臟中,維他命D被發現轉化為骨化二醇。骨化二醇然後被腎臟轉化為骨化三醇 — 維他命D於生物學上的活性形式[11]。骨化三醇作為一種激素在血液中循環,調節血液中鈣和磷酸鹽的濃度,促進骨骼的健康生長和重塑。維他命D代謝物—骨化二醇和骨化三醇,分別由東尼·諾曼及其同事於赫克托·德盧卡實驗室中的跟米高·F·霍利克領導的競賽團隊於實驗中確定[223][224][225]。
科研
[编辑]維他命D缺乏症在歐洲人口中普遍存在著[226]。歐洲正在研究與疾病發生率和飲食建議、食物強化、維他命D補充和日間少量暴露於陽光下的相關政策來評估維他命D的攝入量[56]。除了VDR激活外,各種不同的作用機制正在研究中,例如透過刺蝟的生物訊息傳遞,那是一種有關激素的形態發生[192]。
關於維他命D干預益處的證據出現互相矛盾[227],有一種觀點認為日曬的每天攝入量為4,000-12,000個IU,同時血清中的25-羥基維他命D水平為40-80ng/mL[228],而另一種觀點認為血清濃度高於50ng / mL是不合理的[228][22]。
截至2013年的證據,證據都不足以確定維他命D是否對癌症風險會有影響[229]。美國國家衛生研究院的膳食補充劑辦公室於2014年建立了一項維他命D計劃,以追踪當時的研究並向消費者提供教育[230]。他們進一步指出:「這些作用的大多數證據來自體外、動物和流行病學研究,而不是被認為更具決定性的隨機臨床試驗。直至此類試驗進行之前,將會進行現有關於公共衛生和患者護理問題牽連證據的討論[7]。」一些初步研究把低水平的維他命D與生命後期的疾病聯繫在一起[231]。一項綜合分析發現老年人的死亡率降低[17]。另一項涵蓋超過350,000人的綜合分析得出結論,在未經揀選的社區居民中個人補充維他命D不會使骨骼(總骨折)或非骨骼結果(心肌梗塞、缺血性心臟病、中風、結核、腦血管疾病、癌症)減少了15%以上,而且具有類似設計的進一步研究都不太可能改變這些結論[18]。
2019年的綜合分析發現,同時服用鈣和維他命D可能會增加中風的風險[232]。
COVID-19
[编辑]維他命D缺乏症已被證明可能會增加患上嚴重呼吸道感染的風險[129]。在2019冠状病毒病疫情期間,這在2020年引起了人們對該潛力重新產生興趣。一個對27項出版物的系統評價和綜合分析發現,維他命D缺乏症跟更高機會感染COVID-19的可能性並沒有關聯,但發現到維他命D缺乏症跟疾病的嚴重程度之間存在著正相關的關係,包括了住院率和死亡率的增加[233]。
2020年6月,美國美國國立衛生研究院發現沒有足夠的證據建議或反對使用維他命D補充劑作為專門預防或治療COVID-19[234]。同月,英國國家健康與護理卓越學院發現沒有證據支持或反對服用維他命D補充劑為專門預防或治療COVID-19[235]。這兩個組織都提出了一些建議,而這些建議是應繼續適用先前出於其他原因而補充維他命D建議(如骨骼和肌肉健康)。兩個組織都指出,由於COVID-19大流行期間的日照量較低,可能有更多的人需要補充劑[234][235],而英國國民保健署(NHS)已為COVID-19高危人群免費提供每天維他命D補充劑[236]。
COVID-19的主要併發症是急性呼吸窘迫綜合症(ARDS),可能是由於維他命D缺乏症而加劇[237],但這個關聯並不明確與冠狀病毒感染有關[237]。不同國家將於2020年進行許多試驗,以探討使用維他命D作為預防和治療SARS-CoV-2感染的潛力[237][137]。
参考文献
[编辑]- ^ 1.0 1.1 1.2 1.3 1.4 Holick MF. Sunlight and vitamin D for bone health and prevention of autoimmune diseases, cancers, and cardiovascular disease. The American Journal of Clinical Nutrition. December 2004, 80 (6 Suppl): 1678S–88S. PMID 15585788. doi:10.1093/ajcn/80.6.1678S
 .
.
- ^ 2.0 2.1 2.2 2.3 Holick MF. High prevalence of vitamin D inadequacy and implications for health. Mayo Clinic Proceedings. March 2006, 81 (3): 353–73. PMID 16529140. doi:10.4065/81.3.353
 .
.
- ^ Dietary Supplement Fact Sheet: Vitamin D. Office of Dietary Supplements (ODS). National Institutes of Health (NIH). [2010-04-11]. (原始内容存档于2012-02-13).
- ^ MacDonald, James. How Does the Body Make Vitamin D from Sunlight?. JSTOR Daily. 2019-07-18 [2019-07-22]. (原始内容存档于2020-12-22).
- ^ Holick MF, MacLaughlin JA, Clark MB, Holick SA, Potts JT, Anderson RR, et al. Photosynthesis of previtamin D3 in human skin and the physiologic consequences. Science. October 1980, 210 (4466): 203–5. Bibcode:1980Sci...210..203H. JSTOR 1685024. PMID 6251551. doi:10.1126/science.6251551.
- ^ 穿过窗户的阳光不能帮助人体产生维生素D. 奇客. [2019-03-06]. (原始内容存档于2020-12-22).
- ^ 7.0 7.1 7.2 7.3 7.4 Vitamin D Fact Sheet for Health Professionals. National Institutes of Health (NIH). 2016-02-11 [2017-06-06]. (原始内容存档于2016-12-31).
 本文含有此來源中屬於公有领域的内容。
本文含有此來源中屬於公有领域的内容。
- ^ Calvo MS, Whiting SJ, Barton CN. Vitamin D intake: a global perspective of current status. The Journal of Nutrition. February 2005, 135 (2): 310–6. PMID 15671233. doi:10.1093/jn/135.2.310
 .
.
- ^ 9.0 9.1 9.2 9.3 9.4 9.5 Norman AW. From vitamin D to hormone D: fundamentals of the vitamin D endocrine system essential for good health. The American Journal of Clinical Nutrition. August 2008, 88 (2): 491S–499S. PMID 18689389. doi:10.1093/ajcn/88.2.491S
 .
.
- ^ Lehmann U, Gjessing HR, Hirche F, Mueller-Belecke A, Gudbrandsen OA, Ueland PM, et al. Efficacy of fish intake on vitamin D status: a meta-analysis of randomized controlled trials. The American Journal of Clinical Nutrition. October 2015, 102 (4): 837–47. PMID 26354531. doi:10.3945/ajcn.114.105395
 .
.
- ^ 11.0 11.1 Holick MF, Schnoes HK, DeLuca HF, Suda T, Cousins RJ. Isolation and identification of 1,25-dihydroxycholecalciferol. A metabolite of vitamin D active in intestine. Biochemistry. July 1971, 10 (14): 2799–804. PMID 4326883. doi:10.1021/bi00790a023.
- ^ Vitamin D Tests. Lab Tests Online (USA). American Association for Clinical Chemistry. [2013-06-23]. (原始内容存档于2017-11-07).
- ^ Hollis BW. Assessment of vitamin D nutritional and hormonal status: what to measure and how to do it. Calcified Tissue International. January 1996, 58 (1): 4–5. PMID 8825231. S2CID 35887181. doi:10.1007/BF02509538.
- ^ 14.0 14.1 14.2 14.3 Wolf G. The discovery of vitamin D: the contribution of Adolf Windaus. The Journal of Nutrition. June 2004, 134 (6): 1299–302. PMID 15173387. doi:10.1093/jn/134.6.1299
 .
.
- ^ Pittas AG, Chung M, Trikalinos T, Mitri J, Brendel M, Patel K, et al. Systematic review: Vitamin D and cardiometabolic outcomes. Annals of Internal Medicine. March 2010, 152 (5): 307–14. PMC 3211092
 . PMID 20194237. doi:10.7326/0003-4819-152-5-201003020-00009.
. PMID 20194237. doi:10.7326/0003-4819-152-5-201003020-00009.
- ^ 16.0 16.1 Chung M, Balk EM, Brendel M, Ip S, Lau J, Lee J, et al. Vitamin D and calcium: a systematic review of health outcomes. Evidence Report/Technology Assessment. August 2009, (183): 1–420. PMC 4781105
 . PMID 20629479.
. PMID 20629479.
- ^ 17.0 17.1 17.2 17.3 17.4 Bjelakovic G, Gluud LL, Nikolova D, Whitfield K, Wetterslev J, Simonetti RG, et al. Vitamin D supplementation for prevention of mortality in adults. The Cochrane Database of Systematic Reviews (Systematic review). January 2014, 1 (1): CD007470. PMID 24414552. doi:10.1002/14651858.CD007470.pub3.
- ^ 18.0 18.1 18.2 18.3 18.4 18.5 18.6 Bolland MJ, Grey A, Gamble GD, Reid IR. The effect of vitamin D supplementation on skeletal, vascular, or cancer outcomes: a trial sequential meta-analysis. The Lancet. Diabetes & Endocrinology (Meta-analysis). April 2014, 2 (4): 307–20. PMID 24703049. doi:10.1016/S2213-8587(13)70212-2.
- ^ History of Vitamin D (页面存档备份,存于互联网档案馆) University of California, Riverside, Vitamin D Workshop.
- ^ Dorland's Illustrated Medical Dictionary, under Vitamin (Table of Vitamins)
- ^ 21.0 21.1 21.2 21.3 21.4 21.5 21.6 About Vitamin D (页面存档备份,存于互联网档案馆) Including Sections: History, Nutrition, Chemistry, Biochemistry, and Diseases. University of California Riverside
- ^ 22.0 22.1 22.2 22.3 Holick MF, Binkley NC, Bischoff-Ferrari HA, Gordon CM, Hanley DA, Heaney RP, Murad MH, Weaver CM. Evaluation, treatment, and prevention of vitamin D deficiency: an Endocrine Society clinical practice guideline. J Clin Endocrinol Metab. 2011-06-06, 96 (7): 1911–30. PMID 21646368. doi:10.1210/jc.2011-0385.
- ^ Houghton LA, Vieth R. The case against ergocalciferol (vitamin D2) as a vitamin supplement (PDF). The American Journal of Clinical Nutrition. October 2006, 84 (4): 694–7 [2012-01-02]. PMID 17023693. (原始内容存档 (PDF)于2012-07-03).
- ^ Holick, Michael F.; Biancuzzo, Rachael M.; Chen, Tai C.; Klein, Ellen K.; Young, Azzie; Bibuld, Douglass; Reitz, Richard; Salameh, Wael; Ameri, Allen; Tannenbaum, Andrew D. Vitamin D2Is as Effective as Vitamin D3in Maintaining Circulating Concentrations of 25-Hydroxyvitamin D. The Journal of Clinical Endocrinology & Metabolism (The Endocrine Society). 2008, 93 (3): 677–681. ISSN 0021-972X. doi:10.1210/jc.2007-2308.
- ^ 25.0 25.1 Bouillon R, Van Cromphaut S, Carmeliet G. Intestinal calcium absorption: Molecular vitamin D mediated mechanisms. Journal of Cellular Biochemistry. February 2003, 88 (2): 332–9. PMID 12520535. doi:10.1002/jcb.10360.
- ^ 26.0 26.1 Bell TD, Demay MB, Burnett-Bowie SA. The biology and pathology of vitamin D control in bone. Journal of Cellular Biochemistry. September 2010, 111 (1): 7–13. PMC 4020510
 . PMID 20506379. doi:10.1002/jcb.22661.
. PMID 20506379. doi:10.1002/jcb.22661.
- ^ 27.0 27.1 Watkins RR, Lemonovich TL, Salata RA. An update on the association of vitamin D deficiency with common infectious diseases. Canadian Journal of Physiology and Pharmacology. May 2015, 93 (5): 363–8. PMID 25741906. doi:10.1139/cjpp-2014-0352.
- ^ 28.0 28.1 Puchacz E, Stumpf WE, Stachowiak EK, Stachowiak MK. Vitamin D increases expression of the tyrosine hydroxylase gene in adrenal medullary cells. Brain Research. Molecular Brain Research. February 1996, 36 (1): 193–6. PMID 9011759. doi:10.1016/0169-328X(95)00314-I.
- ^ 29.0 29.1 Angeline ME, Gee AO, Shindle M, Warren RF, Rodeo SA. The effects of vitamin D deficiency in athletes. The American Journal of Sports Medicine. February 2013, 41 (2): 461–4. PMID 23371942. S2CID 21395800. doi:10.1177/0363546513475787.
- ^ 30.00 30.01 30.02 30.03 30.04 30.05 30.06 30.07 30.08 30.09 30.10 30.11 Institute of Medicine (IoM). 8, Implications and Special Concerns. Ross AC, Taylor CL, Yaktine AL, Del Valle HB (编). Dietary Reference Intakes for Calcium and Vitamin D. The National Academies Collection: Reports funded by National Institutes of Health. National Academies Press. 2011 [2020-08-19]. ISBN 978-0-309-16394-1. PMID 21796828. doi:10.17226/13050. (原始内容存档于2021-01-26).
- ^ 31.0 31.1 31.2 Vitamin D and Calcium: Updated Dietary Reference Intakes. Nutrition and Healthy Eating. Health Canada. 2008-12-05 [2018-04-28]. (原始内容存档于2017-06-14).
- ^ 32.0 32.1 32.2 Nutrient reference values for Australia and New Zealand (PDF). National Health and Medical Research Council. 2005-09-09 [2018-04-28]. (原始内容 (PDF)存档于2017-01-21).
- ^ 33.0 33.1 33.2 33.3 EFSA Panel on Dietetic Products, Nutrition and Allergies (NDA). Dietary reference values for vitamin D. EFSA Journal. 2016-06-29, 14 (10): e04547. doi:10.2903/j.efsa.2016.4547
 .
.
- ^ 34.0 34.1 EFSA Panel on Dietetic Products, Nutrition and Allergies (NDA). Scientific Opinion on the Tolerable Upper Intake Level of vitamin D. EFSA Journal (Submitted manuscript). 2012, 10 (7): 2813. doi:10.2903/j.efsa.2012.2813
 .
.
- ^ Federal Register May 27, 2016 Food Labeling: Revision of the Nutrition and Supplement Facts Labels. FR page 33982. (PDF). [2019-08-20]. (原始内容存档 (PDF)于2016-08-08).
 本文含有此來源中屬於公有领域的内容。
本文含有此來源中屬於公有领域的内容。
- ^ Daily Value Reference of the Dietary Supplement Label Database (DSLD). Dietary Supplement Label Database (DSLD). [2020-05-16]. (原始内容存档于2020-04-07).
- ^ 37.0 37.1 FDA provides information about dual columns on Nutrition Facts label. U.S. Food and Drug Administration (FDA). 2019-12-30 [2020-05-16]. (原始内容存档于2021-01-23).
 本文含有此來源中屬於公有领域的内容。
本文含有此來源中屬於公有领域的内容。
- ^ 38.0 38.1 38.2 Changes to the Nutrition Facts Label. U.S. Food and Drug Administration (FDA). 2016-05-27 [2020-05-16]. (原始内容存档于2019-04-22).
 本文含有此來源中屬於公有领域的内容。
本文含有此來源中屬於公有领域的内容。
- ^ Industry Resources on the Changes to the Nutrition Facts Label. U.S. Food and Drug Administration (FDA). 2018-12-21 [2020-05-16]. (原始内容存档于2020-12-25).
 本文含有此來源中屬於公有领域的内容。
本文含有此來源中屬於公有领域的内容。
- ^ Salleh A. Vitamin D food fortification on the table. Australian Broadcasting Corporation. 2012-06-12 [2020-08-13]. (原始内容存档于2020-12-22).
- ^ Vitamins and minerals – Vitamin D. National Health Service. 2015-02-18 [2016-07-21]. (原始内容存档于2017-10-30).
- ^ PHE publishes new advice on vitamin D. Public Health England. 2016-07-21 [2016-07-21]. (原始内容存档于2021-01-03).
- ^ Vitamin D (translated). Swedish National Food Agency. [2018-10-19]. (原始内容存档于2020-10-26) (瑞典语).
- ^ Vitamin-D-Bedarf bei fehlender endogener Synthese Deutsche Gesellschaft für Ernährung, January 2012
- ^ Pérez-López FR, Brincat M, Erel CT, Tremollieres F, Gambacciani M, Lambrinoudaki I, et al. EMAS position statement: Vitamin D and postmenopausal health. Maturitas. January 2012, 71 (1): 83–8. PMID 22100145. doi:10.1016/j.maturitas.2011.11.002.
- ^ 來自美國兒科學會官方報告。
- ^ 47.0 47.1 《中国居民膳食营养素参考摄入量速查手册》(2013版)Chinese DRIs Handbook
- ^ Doctor’s Orders: Don’t Become Vitamin D Deficient This Winter. [2020-06-23]. (原始内容存档于2020-12-22).
- ^ Institute of Medicine (US) Standing Committee on the Scientific Evaluation of Dietary Reference Intakes. DRI, Dietary reference intakes: for calcium, phosphorus, magnesium, vitamin D, and fluoride. Washington, D.C: National Academy Press. 1997: 250 [2020-08-14]. ISBN 978-0-309-06350-0. PMID 23115811. doi:10.17226/5776. (原始内容存档于2015-04-02).
- ^ 50.0 50.1 50.2 Holick MF. Evolutionary biology and pathology of vitamin D. Journal of Nutritional Science and Vitaminology. 1992,. Spec No: 79–83 [2020-08-19]. PMID 1297827. doi:10.3177/jnsv.38.Special_79
 . (原始内容存档于2020-12-22).
. (原始内容存档于2020-12-22).
- ^ 51.0 51.1 51.2 51.3 51.4 51.5 Keegan RJ, Lu Z, Bogusz JM, Williams JE, Holick MF. Photobiology of vitamin D in mushrooms and its bioavailability in humans. Dermato-Endocrinology. January 2013, 5 (1): 165–76. PMC 3897585
 . PMID 24494050. doi:10.4161/derm.23321.
. PMID 24494050. doi:10.4161/derm.23321.
- ^ 52.0 52.1 Wang T, Bengtsson G, Kärnefelt I, Björn LO. Provitamins and vitamins D₂and D₃in Cladina spp. over a latitudinal gradient: possible correlation with UV levels. Journal of Photochemistry and Photobiology. B, Biology (Submitted manuscript). September 2001, 62 (1–2): 118–22 [2020-08-14]. PMID 11693362. doi:10.1016/S1011-1344(01)00160-9. (原始内容存档于2020-05-28).
- ^ Haytowitz DB. Vitamin D in mushrooms (PDF). Nutrient Data Laboratory, US Department of Agriculture. 2009 [2018-04-16]. (原始内容存档 (PDF)于2021-02-01).
 本文含有此來源中屬於公有领域的内容。
本文含有此來源中屬於公有领域的内容。
- ^ Search, National Nutrient Database for Standard Reference Release 27. US Department of Agriculture, Agricultural Research Service. 2014 [2015-06-12]. (原始内容存档于2016-07-30).
 本文含有此來源中屬於公有领域的内容。
本文含有此來源中屬於公有领域的内容。
- ^ de Lourdes Samaniego-Vaesken M, Alonso-Aperte E, Varela-Moreiras G. Vitamin food fortification today. Food & Nutrition Research. 2012, 56: 5459. PMC 3319130
 . PMID 22481896. doi:10.3402/fnr.v56i0.5459.
. PMID 22481896. doi:10.3402/fnr.v56i0.5459.
- ^ 56.0 56.1 Spiro A, Buttriss JL. Vitamin D: An overview of vitamin D status and intake in Europe. Nutrition Bulletin. December 2014, 39 (4): 322–350. PMC 4288313
 . PMID 25635171. doi:10.1111/nbu.12108.
. PMID 25635171. doi:10.1111/nbu.12108.
- ^ Vitamin D for Milk and Milk Alternatives. Food and Drug Administration (FDA). 2016-07-15 [2017-02-22]. (原始内容存档于2020-12-22).
 本文含有此來源中屬於公有领域的内容。
本文含有此來源中屬於公有领域的内容。
- ^ Federal Register: Food Additives Permitted for Direct Addition to Food for Human Consumption; Vitamin D2. Food and Drug Administration, US Department of Health and Human Services. 2016-07-18 [2017-02-22]. (原始内容存档于2020-12-22).
 本文含有此來源中屬於公有领域的内容。
本文含有此來源中屬於公有领域的内容。
- ^ §172.379 Vitamin D2. Electronic Code of Federal Regulations. [2019-07-16]. (原始内容存档于2020-12-22).
 本文含有此來源中屬於公有领域的内容。
本文含有此來源中屬於公有领域的内容。
- ^ §172.380 Vitamin D3. Electronic Code of Federal Regulations. [2019-07-16]. (原始内容存档于2020-12-22).
 本文含有此來源中屬於公有领域的内容。
本文含有此來源中屬於公有领域的内容。
- ^ Dairy Milk alternatives. nutritionrefined. 2019-08-09. (原始内容存档于2020-12-22).
- ^ Alternative to dairy milk. osoblanco. 2020-01-16. (原始内容存档于2020-12-22).
- ^ Tripkovic L. Vitamin D2 vs. vitamin D3: Are they one and the same?. Nutrition Bulletin. 2013, 38 (2): 243–248. doi:10.1111/nbu.12029.
- ^ Alshahrani F, Aljohani N. Vitamin D: deficiency, sufficiency and toxicity. Nutrients. September 2013, 5 (9): 3605–16. PMC 3798924
 . PMID 24067388. doi:10.3390/nu5093605.
. PMID 24067388. doi:10.3390/nu5093605.
- ^ Biancuzzo RM, Clarke N, Reitz RE, Travison TG, Holick MF. Serum concentrations of 1,25-dihydroxyvitamin D2 and 1,25-dihydroxyvitamin D3 in response to vitamin D2 and vitamin D3 supplementation. The Journal of Clinical Endocrinology and Metabolism. March 2013, 98 (3): 973–9. PMC 3590486
 . PMID 23386645. doi:10.1210/jc.2012-2114.
. PMID 23386645. doi:10.1210/jc.2012-2114.
- ^ Borel P, Caillaud D, Cano NJ. Vitamin D bioavailability: state of the art. Critical Reviews in Food Science and Nutrition. 2015, 55 (9): 1193–205. PMID 24915331. S2CID 9818323. doi:10.1080/10408398.2012.688897.
- ^ Jakobsen J, Knuthsen P. Stability of vitamin D in foodstuffs during cooking. Food Chemistry. April 2014, 148: 170–5. PMID 24262542. doi:10.1016/j.foodchem.2013.10.043.
- ^ Walter F., PhD. Boron. The Parathyroid Glands and Vitamin F. Medical Physiology: A Cellular And Molecular Approaoch. Elsevier/Saunders. 2003: 1094. ISBN 978-1-4160-2328-9.
- ^ Rickets. National Health Service. 2012-03-08 [2012-07-09]. (原始内容存档于2017-10-11).
- ^ Munns CF, Shaw N, Kiely M, Specker BL, Thacher TD, Ozono K, et al. Global Consensus Recommendations on Prevention and Management of Nutritional Rickets. The Journal of Clinical Endocrinology and Metabolism. February 2016, 101 (2): 394–415. PMC 4880117
 . PMID 26745253. doi:10.1210/jc.2015-2175.
. PMID 26745253. doi:10.1210/jc.2015-2175.
- ^ Eriksen EF, Glerup H. Vitamin D deficiency and aging: implications for general health and osteoporosis. Biogerontology. 2002, 3 (1–2): 73–7. PMID 12014847. S2CID 22112344. doi:10.1023/A:1015263514765.
- ^ 72.0 72.1 72.2 72.3 72.4 72.5 Holick MF. Vitamin D deficiency. The New England Journal of Medicine. July 2007, 357 (3): 266–81. PMID 17634462. doi:10.1056/NEJMra070553.
- ^ 73.0 73.1 73.2 73.3 Brown JE, Isaacs J, Krinke B, Lechtenberg E, Murtaugh M. Nutrition Through the Life Cycle. Cengage Learning. 2013-06-28 [2020-08-14]. ISBN 978-1-285-82025-5. (原始内容存档于2023-03-19).
- ^ Schoenmakers I, Goldberg GR, Prentice A. Abundant sunshine and vitamin D deficiency. The British Journal of Nutrition. June 2008, 99 (6): 1171–3. PMC 2758994
 . PMID 18234141. doi:10.1017/S0007114508898662.
. PMID 18234141. doi:10.1017/S0007114508898662.
- ^ Lowe NM, Bhojani I. Special considerations for vitamin D in the south Asian population in the UK. Therapeutic Advances in Musculoskeletal Disease. June 2017, 9 (6): 137–144. PMC 5466148
 . PMID 28620422. doi:10.1177/1759720X17704430.
. PMID 28620422. doi:10.1177/1759720X17704430.
- ^ O'Connor MY, Thoreson CK, Ramsey NL, Ricks M, Sumner AE. The uncertain significance of low vitamin D levels in African descent populations: a review of the bone and cardiometabolic literature. Progress in Cardiovascular Diseases. 2013, 56 (3): 261–9. PMC 3894250
 . PMID 24267433. doi:10.1016/j.pcad.2013.10.015.
. PMID 24267433. doi:10.1016/j.pcad.2013.10.015.
- ^ Freedman BI, Register TC. Effect of race and genetics on vitamin D metabolism, bone and vascular health. Nature Reviews. Nephrology. June 2012, 8 (8): 459–66. PMID 22688752. S2CID 29026212. doi:10.1038/nrneph.2012.112.
- ^ Khalid AT, Moore CG, Hall C, Olabopo F, Rozario NL, Holick MF, et al. Utility of sun-reactive skin typing and melanin index for discerning vitamin D deficiency. Pediatric Research. September 2017, 82 (3): 444–451. PMC 5570640
 . PMID 28467404. doi:10.1038/pr.2017.114.
. PMID 28467404. doi:10.1038/pr.2017.114.
- ^ 79.0 79.1 Wagner CL, Greer FR. Prevention of rickets and vitamin D deficiency in infants, children, and adolescents. Pediatrics. November 2008, 122 (5): 1142–52. PMID 18977996. doi:10.1542/peds.2008-1862
 .
.
- ^ Lerch C, Meissner T. Lerch C , 编. Interventions for the prevention of nutritional rickets in term born children. The Cochrane Database of Systematic Reviews. October 2007, (4): CD006164. PMID 17943890. doi:10.1002/14651858.CD006164.pub2.
- ^ Zargar AH, Mithal A, Wani AI, Laway BA, Masoodi SR, Bashir MI, Ganie MA. Pseudovitamin D deficiency rickets--a report from the Indian subcontinent. Postgraduate Medical Journal. June 2000, 76 (896): 369–72. PMC 1741602
 . PMID 10824056. doi:10.1136/pmj.76.896.369.
. PMID 10824056. doi:10.1136/pmj.76.896.369.
- ^ Elidrissy AT. The Return of Congenital Rickets, Are We Missing Occult Cases?. Calcified Tissue International (Review). September 2016, 99 (3): 227–36. PMID 27245342. S2CID 14727399. doi:10.1007/s00223-016-0146-2.
- ^ Paterson CR, Ayoub D. Congenital rickets due to vitamin D deficiency in the mothers. Clinical Nutrition (Review). October 2015, 34 (5): 793–8. PMID 25552383. doi:10.1016/j.clnu.2014.12.006.
- ^ Oramasionwu GE, Thacher TD, Pam SD, Pettifor JM, Abrams SA. Adaptation of calcium absorption during treatment of nutritional rickets in Nigerian children (PDF). The British Journal of Nutrition. August 2008, 100 (2): 387–92. PMID 18197991. doi:10.1017/S0007114507901233.
- ^ Fischer PR, Rahman A, Cimma JP, Kyaw-Myint TO, Kabir AR, Talukder K, et al. Nutritional rickets without vitamin D deficiency in Bangladesh. Journal of Tropical Pediatrics. October 1999, 45 (5): 291–3. PMID 10584471. doi:10.1093/tropej/45.5.291
 .
.
- ^ 86.0 86.1 Dunnigan MG, Henderson JB. An epidemiological model of privational rickets and osteomalacia. The Proceedings of the Nutrition Society. November 1997, 56 (3): 939–56. PMID 9483661. doi:10.1079/PNS19970100
 .
.
- ^ Robertson I, Ford JA, McIntosh WB, Dunnigan MG. The role of cereals in the aetiology of nutritional rickets: the lesson of the Irish National Nutrition Survey 1943-8. The British Journal of Nutrition. January 1981, 45 (1): 17–22. PMID 6970590. doi:10.1079/BJN19810073
 .
.
- ^ Clements MR. The problem of rickets in UK Asians. Journal of Human Nutrition and Dietetics. 1989, 2 (2): 105–116. doi:10.1111/j.1365-277X.1989.tb00015.x.
- ^ 89.0 89.1 Pettifor JM. Nutritional rickets: deficiency of vitamin D, calcium, or both?. The American Journal of Clinical Nutrition. December 2004, 80 (6 Suppl): 1725S–9S. PMID 15585795. doi:10.1093/ajcn/80.6.1725S
 .
.
- ^ 90.0 90.1 Dunnigan MG, Henderson JB, Hole DJ, Barbara Mawer E, Berry JL. Meat consumption reduces the risk of nutritional rickets and osteomalacia. The British Journal of Nutrition. December 2005, 94 (6): 983–91. PMID 16351777. doi:10.1079/BJN20051558
 .
.
- ^ Cell Biology and Cancer Curriculum Supplement. Office of Science Education. [2010-08-24]. (原始内容存档于2010-06-08).
 本文含有此來源中屬於公有领域的内容。
本文含有此來源中屬於公有领域的内容。
- ^ Weick MT. A history of rickets in the United States. The American Journal of Clinical Nutrition. November 1967, 20 (11): 1234–41. PMID 4862158. doi:10.1093/ajcn/20.11.1234.
- ^ Garrison RH, Somer E. The Nutrition Desk Reference. McGraw-Hill. 1997 [2022-12-06]. ISBN 978-0-87983-826-3. (原始内容存档于2021-08-19).
- ^ Dupuis EM. Nature's Perfect Food: How Milk Became America's Drink. NYU Press. 2002-02-01 [2022-12-06]. ISBN 978-0-8147-1938-1. (原始内容存档于2021-08-19).
- ^ Teegarden D, Lyle RM, Proulx WR, Johnston CC, Weaver CM. Previous milk consumption is associated with greater bone density in young women. The American Journal of Clinical Nutrition. May 1999, 69 (5): 1014–7. PMID 10232644. doi:10.1093/ajcn/69.5.1014
 .
.
- ^ 96.0 96.1 96.2 Insel P, Ross D, Bernstein M, McMahon K. Discovering Nutrition. Jones & Bartlett Publishers. 2015-03-18 [2020-08-18]. ISBN 978-1-284-06465-0. (原始内容存档于2023-03-19).
- ^ Holick MF. Vitamin D: A millenium perspective. Journal of Cellular Biochemistry. February 2003, 88 (2): 296–307. PMID 12520530. doi:10.1002/jcb.10338.
- ^ Straube S, Andrew Moore R, Derry S, McQuay HJ. Vitamin D and chronic pain. Pain. January 2009, 141 (1–2): 10–3. PMID 19084336. S2CID 17244398. doi:10.1016/j.pain.2008.11.010.
- ^ Gaikwad M, Vanlint S, Mittinity M, Moseley GL, Stocks N. Does vitamin D supplementation alleviate chronic nonspecific musculoskeletal pain? A systematic review and meta-analysis. Clinical Rheumatology. May 2017, 36 (5): 1201–1208. PMID 26861032. S2CID 30189971. doi:10.1007/s10067-016-3205-1.
- ^ Theodoratou E, Tzoulaki I, Zgaga L, Ioannidis JP. Vitamin D and multiple health outcomes: umbrella review of systematic reviews and meta-analyses of observational studies and randomised trials. BMJ. April 2014, 348: g2035. PMC 3972415
 . PMID 24690624. doi:10.1136/bmj.g2035.
. PMID 24690624. doi:10.1136/bmj.g2035.
- ^ 101.0 101.1 101.2 Autier P, Boniol M, Pizot C, Mullie P. Vitamin D status and ill health: a systematic review. The Lancet. Diabetes & Endocrinology. January 2014, 2 (1): 76–89. PMID 24622671. doi:10.1016/S2213-8587(13)70165-7.
- ^ Hussain S, Singh A, Akhtar M, Najmi AK. Vitamin D supplementation for the management of knee osteoarthritis: a systematic review of randomized controlled trials. Rheumatology International. September 2017, 37 (9): 1489–1498. PMID 28421358. S2CID 23994681. doi:10.1007/s00296-017-3719-0.
- ^ 103.0 103.1 Maxmen A. Nutrition advice: the vitamin D-lemma (PDF). Nature. July 2011, 475 (7354): 23–5 [2012-01-02]. PMID 21734684. doi:10.1038/475023a
 . (原始内容存档 (PDF)于2020-08-03).
. (原始内容存档 (PDF)于2020-08-03).
- ^ Reid IR, Bolland MJ, Grey A. Effects of vitamin D supplements on bone mineral density: a systematic review and meta-analysis. Lancet. January 2014, 383 (9912): 146–55. PMID 24119980. doi:10.1016/s0140-6736(13)61647-5.
- ^ Avenell A, Mak JC, O'Connell D. Vitamin D and vitamin D analogues for preventing fractures in post-menopausal women and older men. The Cochrane Database of Systematic Reviews. April 2014, 4 (4): CD000227. PMC 7032685
 . PMID 24729336. doi:10.1002/14651858.CD000227.pub4.
. PMID 24729336. doi:10.1002/14651858.CD000227.pub4.
- ^ Bischoff-Ferrari HA, Willett WC, Orav EJ, Oray EJ, Lips P, Meunier PJ, et al. A pooled analysis of vitamin D dose requirements for fracture prevention (PDF). The New England Journal of Medicine. July 2012, 367 (1): 40–9 [2020-08-16]. PMID 22762317. S2CID 24338997. doi:10.1056/NEJMoa1109617. hdl:1871/48765. (原始内容存档 (PDF)于2020-12-15).
- ^ 107.0 107.1 Chung M, Lee J, Terasawa T, Lau J, Trikalinos TA. Vitamin D with or without calcium supplementation for prevention of cancer and fractures: an updated meta-analysis for the U.S. Preventive Services Task Force. Annals of Internal Medicine. December 2011, 155 (12): 827–38. PMID 22184690. doi:10.7326/0003-4819-155-12-201112200-00005
 .
.
- ^ Zhao JG, Zeng XT, Wang J, Liu L. Association Between Calcium or Vitamin D Supplementation and Fracture Incidence in Community-Dwelling Older Adults: A Systematic Review and Meta-analysis. JAMA. December 2017, 318 (24): 2466–2482. PMC 5820727
 . PMID 29279934. doi:10.1001/jama.2017.19344.
. PMID 29279934. doi:10.1001/jama.2017.19344.
- ^ Cranney A, Horsley T, O'Donnell S, Weiler H, Puil L, Ooi D, et al. Effectiveness and safety of vitamin D in relation to bone health. Evidence Report/Technology Assessment. August 2007, (158): 1–235. PMC 4781354
 . PMID 18088161.
. PMID 18088161.
- ^ Bolland MJ, Grey A, Gamble GD, Reid IR. Vitamin D supplementation and falls: a trial sequential meta-analysis. The Lancet. Diabetes & Endocrinology. July 2014, 2 (7): 573–80. PMID 24768505. doi:10.1016/S2213-8587(14)70068-3.
- ^ Shuler FD, Wingate MK, Moore GH, Giangarra C. Sports health benefits of vitamin d. Sports Health. November 2012, 4 (6): 496–501. PMC 3497950
 . PMID 24179588. doi:10.1177/1941738112461621.
. PMID 24179588. doi:10.1177/1941738112461621.
- ^ Byers T. Anticancer vitamins du Jour--The ABCED's so far. American Journal of Epidemiology (Review). July 2010, 172 (1): 1–3. PMC 2892535
 . PMID 20562190. doi:10.1093/aje/kwq112.
. PMID 20562190. doi:10.1093/aje/kwq112.
- ^ Feldman D, Krishnan AV, Swami S, Giovannucci E, Feldman BJ. The role of vitamin D in reducing cancer risk and progression. Nature Reviews. Cancer. May 2014, 14 (5): 342–57. PMID 24705652. S2CID 24164628. doi:10.1038/nrc3691.
- ^ Buttigliero C, Monagheddu C, Petroni P, Saini A, Dogliotti L, Ciccone G, Berruti A. Prognostic role of vitamin d status and efficacy of vitamin D supplementation in cancer patients: a systematic review. The Oncologist. 2011, 16 (9): 1215–27. PMC 3228169
 . PMID 21835895. doi:10.1634/theoncologist.2011-0098.
. PMID 21835895. doi:10.1634/theoncologist.2011-0098.
- ^ Li M, Chen P, Li J, Chu R, Xie D, Wang H. Review: the impacts of circulating 25-hydroxyvitamin D levels on cancer patient outcomes: a systematic review and meta-analysis. The Journal of Clinical Endocrinology and Metabolism. July 2014, 99 (7): 2327–36. PMID 24780061. doi:10.1210/jc.2013-4320
 .
.
- ^ Barbarawi M, Kheiri B, Zayed Y, Barbarawi O, Dhillon H, Swaid B, et al. Vitamin D Supplementation and Cardiovascular Disease Risks in More Than 83 000 Individuals in 21 Randomized Clinical Trials: A Meta-analysis. JAMA Cardiology. August 2019, 4 (8): 765–776. PMC 6584896
 . PMID 31215980. doi:10.1001/jamacardio.2019.1870.
. PMID 31215980. doi:10.1001/jamacardio.2019.1870.
- ^ Beveridge LA, Struthers AD, Khan F, Jorde R, Scragg R, Macdonald HM, et al. Effect of Vitamin D Supplementation on Blood Pressure: A Systematic Review and Meta-analysis Incorporating Individual Patient Data. JAMA Internal Medicine. May 2015, 175 (5): 745–54. PMC 5966296
 . PMID 25775274. doi:10.1001/jamainternmed.2015.0237.
. PMID 25775274. doi:10.1001/jamainternmed.2015.0237.
- ^ Hart PH. Vitamin D supplementation, moderate sun exposure, and control of immune diseases. Discovery Medicine. June 2012, 13 (73): 397–404 [2020-08-17]. PMID 22742645. (原始内容存档于2020-08-12).
- ^ Martineau AR, Cates CJ, Urashima M, Jensen M, Griffiths AP, Nurmatov U, et al. Vitamin D for the management of asthma. The Cochrane Database of Systematic Reviews. September 2016, 9: CD011511. PMC 6457769
 . PMID 27595415. doi:10.1002/14651858.cd011511.pub2.
. PMID 27595415. doi:10.1002/14651858.cd011511.pub2.
- ^ Paul G, Brehm JM, Alcorn JF, Holguín F, Aujla SJ, Celedón JC. Vitamin D and asthma. American Journal of Respiratory and Critical Care Medicine. January 2012, 185 (2): 124–32. PMC 3297088
 . PMID 22016447. doi:10.1164/rccm.201108-1502CI.
. PMID 22016447. doi:10.1164/rccm.201108-1502CI.
- ^ Del Pinto R, Pietropaoli D, Chandar AK, Ferri C, Cominelli F. Association Between Inflammatory Bowel Disease and Vitamin D Deficiency: A Systematic Review and Meta-analysis. Inflammatory Bowel Diseases. November 2015, 21 (11): 2708–17. PMC 4615394
 . PMID 26348447. doi:10.1097/MIB.0000000000000546.
. PMID 26348447. doi:10.1097/MIB.0000000000000546.
- ^ Guzman-Prado Y, Samson O, Segal JP, Limdi JK, Hayee B. Vitamin D Therapy in Adults With Inflammatory Bowel Disease: A Systematic Review and Meta-Analysis. Inflammatory Bowel Diseases. May 2020. PMID 32385487. doi:10.1093/ibd/izaa087.
- ^ Hewison M. Vitamin D and innate and adaptive immunity. Vitamins and the Immune System. Vitamins & Hormones 86. 2011: 23–62. ISBN 9780123869609. PMID 21419266. doi:10.1016/B978-0-12-386960-9.00002-2.
- ^ Beard JA, Bearden A, Striker R. Vitamin D and the anti-viral state. Journal of Clinical Virology. March 2011, 50 (3): 194–200. PMC 3308600
 . PMID 21242105. doi:10.1016/j.jcv.2010.12.006.
. PMID 21242105. doi:10.1016/j.jcv.2010.12.006.
- ^ Spector SA. Vitamin D and HIV: letting the sun shine in. Topics in Antiviral Medicine. 2011, 19 (1): 6–10. PMC 6148856
 . PMID 21852710.
. PMID 21852710.
- ^ Nnoaham KE, Clarke A. Low serum vitamin D levels and tuberculosis: a systematic review and meta-analysis. International Journal of Epidemiology. February 2008, 37 (1): 113–9. CiteSeerX 10.1.1.513.3969
 . PMID 18245055. doi:10.1093/ije/dym247.
. PMID 18245055. doi:10.1093/ije/dym247.
- ^ Luong K, Nguyen LT. Impact of vitamin D in the treatment of tuberculosis. The American Journal of the Medical Sciences. June 2011, 341 (6): 493–8. PMID 21289501. S2CID 18802134. doi:10.1097/MAJ.0b013e3182070f47.
- ^ Bergman P, Lindh AU, Björkhem-Bergman L, Lindh JD. Vitamin D and Respiratory Tract Infections: A Systematic Review and Meta-Analysis of Randomized Controlled Trials. PLOS ONE. 2013, 8 (6): e65835. Bibcode:2013PLoSO...865835B. PMC 3686844
 . PMID 23840373. doi:10.1371/journal.pone.0065835.
. PMID 23840373. doi:10.1371/journal.pone.0065835.
- ^ 129.0 129.1 129.2 Martineau AR, Jolliffe DA, Hooper RL, Greenberg L, Aloia JF, Bergman P, et al. Vitamin D supplementation to prevent acute respiratory tract infections: systematic review and meta-analysis of individual participant data. BMJ. February 2017, 356: i6583 [2020-08-17]. PMC 5310969
 . PMID 28202713. doi:10.1136/bmj.i6583. (原始内容存档于2021-02-02).
. PMID 28202713. doi:10.1136/bmj.i6583. (原始内容存档于2021-02-02).
- ^ Yakoob MY, Salam RA, Khan FR, Bhutta ZA. Vitamin D supplementation for preventing infections in children under five years of age. The Cochrane Database of Systematic Reviews. November 2016, 11: CD008824. PMC 5450876
 . PMID 27826955. doi:10.1002/14651858.cd008824.pub2.
. PMID 27826955. doi:10.1002/14651858.cd008824.pub2.
- ^ 131.0 131.1 Rhodes JM, Subramanian S, Laird E, Kenny RA. Editorial: low population mortality from COVID-19 in countries south of latitude 35 degrees North supports vitamin D as a factor determining severity. Alimentary Pharmacology & Therapeutics. June 2020, 51 (12): 1434–1437. PMC 7264531
 . PMID 32311755. doi:10.1111/apt.15777.
. PMID 32311755. doi:10.1111/apt.15777.
- ^ Grant WB, Lahore H, McDonnell SL, Baggerly CA, French CB, Aliano JL, Bhattoa HP. Evidence that Vitamin D Supplementation Could Reduce Risk of Influenza and COVID-19 Infections and Deaths. Nutrients. April 2020, 12 (4): 988. PMC 7231123
 . PMID 32252338. doi:10.3390/nu12040988.
. PMID 32252338. doi:10.3390/nu12040988.
- ^ 133.0 133.1 Ebadi M, Montano-Loza AJ. Perspective: improving vitamin D status in the management of COVID-19. European Journal of Clinical Nutrition. June 2020, 74 (6): 856–859. PMC 7216123
 . PMID 32398871. doi:10.1038/s41430-020-0661-0.
. PMID 32398871. doi:10.1038/s41430-020-0661-0.
- ^ D'Avolio A, Avataneo V, Manca A, Cusato J, De Nicolò A, Lucchini R, et al. 25-Hydroxyvitamin D Concentrations Are Lower in Patients with Positive PCR for SARS-CoV-2. Nutrients. May 2020, 12 (5): 1359. PMC 7285131
 . PMID 32397511. doi:10.3390/nu12051359.
. PMID 32397511. doi:10.3390/nu12051359.
- ^ Hastie CE, Mackay DF, Ho F, Celis-Morales CA, Katikireddi SV, Niedzwiedz CL, et al. Vitamin D concentrations and COVID-19 infection in UK Biobank. Diabetes & Metabolic Syndrome. May 2020, 14 (4): 561–565. PMC 7204679
 . PMID 32413819. doi:10.1016/j.dsx.2020.04.050.
. PMID 32413819. doi:10.1016/j.dsx.2020.04.050.
- ^ NICE. Key messages | COVID-19 rapid evidence summary: vitamin D for COVID-19 | Advice | NICE. www.nice.org.uk. [2020-06-29]. (原始内容存档于2020-12-15).
- ^ 137.0 137.1 137.2 International clinical trials assessing vitamin D in people with COVID-19. ClinicalTrials.gov, US National Library of Medicine. May 2020 [2020-05-20]. (原始内容存档于2020-10-06).
- ^ Anshul Jain, Rachna Chaurasia, Narendra Singh Sengar, Mayank Singh, Sachin Mahor & Sumit Narain. nature research Scientific Reports 2020 10:20191 OPEN ACCESS Analysis of vitamin D level among asymptonmatic and critically ill COVID-19 patients and its correlation with inflammatory markers (CC BY 4.0 creative commons). [2020-11-25]. doi:10.1038/s41598-020-77093-z. (原始内容存档于2020-12-07).
- ^ Seida JC, Mitri J, Colmers IN, Majumdar SR, Davidson MB, Edwards AL, et al. Clinical review: Effect of vitamin D3 supplementation on improving glucose homeostasis and preventing diabetes: a systematic review and meta-analysis. The Journal of Clinical Endocrinology and Metabolism (Review). October 2014, 99 (10): 3551–60. PMC 4483466
 . PMID 25062463. doi:10.1210/jc.2014-2136.
. PMID 25062463. doi:10.1210/jc.2014-2136.
- ^ Nakashima A, Yokoyama K, Yokoo T, Urashima M. Role of vitamin D in diabetes mellitus and chronic kidney disease. World Journal of Diabetes (Review). March 2016, 7 (5): 89–100. PMC 4781904
 . PMID 26981182. doi:10.4239/wjd.v7.i5.89.
. PMID 26981182. doi:10.4239/wjd.v7.i5.89.
- ^ Shaffer JA, Edmondson D, Wasson LT, Falzon L, Homma K, Ezeokoli N, et al. Vitamin D supplementation for depressive symptoms: a systematic review and meta-analysis of randomized controlled trials. Psychosomatic Medicine. April 2014, 76 (3): 190–6. PMC 4008710
 . PMID 24632894. doi:10.1097/psy.0000000000000044.
. PMID 24632894. doi:10.1097/psy.0000000000000044.
- ^ Balion C, Griffith LE, Strifler L, Henderson M, Patterson C, Heckman G, et al. Vitamin D, cognition, and dementia: a systematic review and meta-analysis. Neurology. September 2012, 79 (13): 1397–405. PMC 3448747
 . PMID 23008220. doi:10.1212/WNL.0b013e31826c197f.
. PMID 23008220. doi:10.1212/WNL.0b013e31826c197f.
- ^ Pathak K, Soares MJ, Calton EK, Zhao Y, Hallett J. Vitamin D supplementation and body weight status: a systematic review and meta-analysis of randomized controlled trials. Obesity Reviews. June 2014, 15 (6): 528–37. PMID 24528624. doi:10.1111/obr.12162.
- ^ Mallard SR, Howe AS, Houghton LA. Vitamin D status and weight loss: a systematic review and meta-analysis of randomized and nonrandomized controlled weight-loss trials. The American Journal of Clinical Nutrition. October 2016, 104 (4): 1151–1159. PMID 27604772. doi:10.3945/ajcn.116.136879
 .
.
- ^ 145.0 145.1 Aghajafari F, Nagulesapillai T, Ronksley PE, Tough SC, O'Beirne M, Rabi DM. Association between maternal serum 25-hydroxyvitamin D level and pregnancy and neonatal outcomes: systematic review and meta-analysis of observational studies. BMJ. March 2013, 346: f1169. PMID 23533188. doi:10.1136/bmj.f1169
 .
.
- ^ 146.0 146.1 Palacios C, De-Regil LM, Lombardo LK, Peña-Rosas JP. Vitamin D supplementation during pregnancy: Updated meta-analysis on maternal outcomes. The Journal of Steroid Biochemistry and Molecular Biology. November 2016, 164: 148–155. PMC 5357731
 . PMID 26877200. doi:10.1016/j.jsbmb.2016.02.008.
. PMID 26877200. doi:10.1016/j.jsbmb.2016.02.008.
- ^ Roth DE, Leung M, Mesfin E, Qamar H, Watterworth J, Papp E. Vitamin D supplementation during pregnancy: state of the evidence from a systematic review of randomised trials. BMJ. November 2017, 359: j5237. PMC 5706533
 . PMID 29187358. doi:10.1136/bmj.j5237.
. PMID 29187358. doi:10.1136/bmj.j5237.
- ^ 148.0 148.1 Palacios C, Kostiuk LK, Peña-Rosas JP. Vitamin D supplementation for women during pregnancy. The Cochrane Database of Systematic Reviews. July 2019, 7: CD008873. PMC 3747784
 . PMID 31348529. doi:10.1002/14651858.CD008873.pub4.
. PMID 31348529. doi:10.1002/14651858.CD008873.pub4.
- ^ 149.0 149.1 Wagner CL, Taylor SN, Dawodu A, Johnson DD, Hollis BW. Vitamin D and its role during pregnancy in attaining optimal health of mother and fetus. Nutrients. March 2012, 4 (3): 208–30. PMC 3347028
 . PMID 22666547. doi:10.3390/nu4030208.
. PMID 22666547. doi:10.3390/nu4030208.
- ^ Bi WG, Nuyt AM, Weiler H, Leduc L, Santamaria C, Wei SQ. Association Between Vitamin D Supplementation During Pregnancy and Offspring Growth, Morbidity, and Mortality: A Systematic Review and Meta-analysis. JAMA Pediatrics. July 2018, 172 (7): 635–645. PMC 6137512
 . PMID 29813153. doi:10.1001/jamapediatrics.2018.0302.
. PMID 29813153. doi:10.1001/jamapediatrics.2018.0302.
- ^ 151.0 151.1 151.2 European Food Safety Authority (EFSA) Panel on Dietetic Products, Nutrition and Allergies (NDA). Scientific opinion on the substantiation of health claims related to vitamin D and normal function of the immune system and inflammatory response (ID 154, 159), maintenance of normal muscle function (ID 155) and maintenance of normal cardiovascular function (ID 159) pursuant to Article 13(1) of Regulation (EC) No 1924/2006. EFSA Journal. 2010, 8 (2): 1468–85. doi:10.2903/j.efsa.2010.1468
 .
.
- ^ European Food Safety Authority (EFSA) Panel on Dietetic Products, Nutrition and Allergies (NDA). Scientific opinion on the substantiation of a health claim related to vitamin D and risk of falling pursuant to Article 14 of Regulation (EC) No 1924/2006 (PDF). EFSA Journal. 2011, 9 (9): 2382–2400 [2020-08-17]. doi:10.2903/j.efsa.2011.2382. (原始内容存档 (PDF)于2019-08-20).
- ^ Guidance for Industry: Food Labeling Guide. Food and Drug Administration (FDA). January 2013 [2020-08-17]. (原始内容存档于2020-12-22).
 本文含有此來源中屬於公有领域的内容。
本文含有此來源中屬於公有领域的内容。
- ^ Health Canada Scientific Summary on the U. S. Health Claim Regarding Calcium and Osteoporosis. Bureau of Nutritional Sciences Food Directorate, Health Products and Food Branch Health Canada. 2000-05-01 [2020-08-17]. (原始内容存档于2016-12-03).
- ^ Regulatory Systems of Health Claims in Japan (PDF). Japan Consumer Affairs Agency, Food Labelling Division. 2011-06-01 [2012-01-29]. (原始内容存档 (PDF)于2012-03-06).
|url-status=和|dead-url=只需其一 (帮助) - ^ Vitamin D. Nutrient Reference Values for Australia and New Zealand. Australian Ministry of Health. 2005-09-09 [2020-08-17]. (原始内容存档于2012-02-27).
|url-status=和|dead-url=只需其一 (帮助) - ^ Schöttker B, Jorde R, Peasey A, Thorand B, Jansen EH, Groot L, et al. Vitamin D and mortality: meta-analysis of individual participant data from a large consortium of cohort studies from Europe and the United States. BMJ. June 2014, 348 (jun17 16): g3656. PMC 4061380
 . PMID 24938302. doi:10.1136/bmj.g3656.
. PMID 24938302. doi:10.1136/bmj.g3656.
- ^ Tuohimaa P. Vitamin D and aging. The Journal of Steroid Biochemistry and Molecular Biology. March 2009, 114 (1–2): 78–84. PMID 19444937. S2CID 40625040. doi:10.1016/j.jsbmb.2008.12.020.
- ^ Tuohimaa P, Keisala T, Minasyan A, Cachat J, Kalueff A. Vitamin D, nervous system and aging. Psychoneuroendocrinology. December 2009,. 34 Suppl 1: S278–86. PMID 19660871. S2CID 17462970. doi:10.1016/j.psyneuen.2009.07.003.
- ^ Manya H, Akasaka-Manya K, Endo T. Klotho protein deficiency and aging. Geriatrics & Gerontology International. July 2010,. 10 Suppl 1 (Suppl 1): S80–7. PMID 20590845. doi:10.1111/j.1447-0594.2010.00596.x.
- ^ 161.0 161.1 Ross AC, Manson JE, Abrams SA, Aloia JF, Brannon PM, Clinton SK, et al. The 2011 report on dietary reference intakes for calcium and vitamin D from the Institute of Medicine: what clinicians need to know. The Journal of Clinical Endocrinology and Metabolism. January 2011, 96 (1): 53–8. PMC 3046611
 . PMID 21118827. doi:10.1210/jc.2010-2704.
. PMID 21118827. doi:10.1210/jc.2010-2704.
- ^ 162.0 162.1 162.2 Vitamin D 来自默克诊疗手册专业版
- ^ 163.0 163.1 163.2 163.3 Vieth R. Vitamin D supplementation, 25-hydroxyvitamin D concentrations, and safety (PDF). The American Journal of Clinical Nutrition. May 1999, 69 (5): 842–56 [2020-08-18]. PMID 10232622. doi:10.1093/ajcn/69.5.842. (原始内容存档 (PDF)于2012-07-03).
- ^ Tolerable Upper Intake Limits for Vitamins And Minerals (PDF). European Food Safety Authority. December 2006 [2020-08-18]. ISBN 978-92-9199-014-6. (原始内容 (PDF)存档于2019-05-06).
- ^ Schlingmann KP, Kaufmann M, Weber S, Irwin A, Goos C, John U, et al. Mutations in CYP24A1 and idiopathic infantile hypercalcemia. The New England Journal of Medicine. August 2011, 365 (5): 410–21. PMID 21675912. doi:10.1056/NEJMoa1103864.
- ^ De Paolis E, Scaglione GL, De Bonis M, Minucci A, Capoluongo E. CYP24A1 and SLC34A1 genetic defects associated with idiopathic infantile hypercalcemia: from genotype to phenotype. Clinical Chemistry and Laboratory Medicine. October 2019, 57 (11): 1650–1667. PMID 31188746. doi:10.1515/cclm-2018-1208
 .
.
- ^ Tebben PJ, Singh RJ, Kumar R. Vitamin D-Mediated Hypercalcemia: Mechanisms, Diagnosis, and Treatment. Endocrine Reviews. October 2016, 37 (5): 521–547. PMC 5045493
 . PMID 27588937. doi:10.1210/er.2016-1070.
. PMID 27588937. doi:10.1210/er.2016-1070.
- ^ Dahlquist DT, Dieter BP, Koehle MS. Plausible ergogenic effects of vitamin D on athletic performance and recovery. Journal of the International Society of Sports Nutrition (Review). 2015, 12: 33. PMC 4539891
 . PMID 26288575. doi:10.1186/s12970-015-0093-8.
. PMID 26288575. doi:10.1186/s12970-015-0093-8.
- ^ FDA Cautions on Accurate Vitamin D Supplementation for Infants (新闻稿). Food and Drug Administration (FDA). June 15, 2010 [2020-08-18]. (原始内容存档于2017-01-12).
|url-status=和|dead-url=只需其一 (帮助) 本文含有此來源中屬於公有领域的内容。
本文含有此來源中屬於公有领域的内容。
- ^ Olmos-Ortiz A, Avila E, Durand-Carbajal M, Díaz L. Regulation of calcitriol biosynthesis and activity: focus on gestational vitamin D deficiency and adverse pregnancy outcomes. Nutrients. January 2015, 7 (1): 443–80. PMC 4303849
 . PMID 25584965. doi:10.3390/nu7010443.
. PMID 25584965. doi:10.3390/nu7010443.
- ^ Holick MF. Photosynthesis of vitamin D in the skin: effect of environmental and life-style variables. Federation Proceedings. April 1987, 46 (5): 1876–82. PMID 3030826.
- ^ Deluca HF. History of the discovery of vitamin D and its active metabolites. BoneKEy Reports. January 2014, 3: 479. PMC 3899558
 . PMID 24466410. doi:10.1038/bonekey.2013.213.
. PMID 24466410. doi:10.1038/bonekey.2013.213.
- ^ 173.0 173.1 173.2 Holick MF. Vitamin D: importance in the prevention of cancers, type 1 diabetes, heart disease, and osteoporosis. The American Journal of Clinical Nutrition. March 2004, 79 (3): 362–71. PMID 14985208. doi:10.1093/ajcn/79.3.362
 .
.
- ^ Eyley SC, Williams DH. Photolytic production of vitamin D. The preparative value of a photo-sensitiser. Journal of the Chemical Society, Chemical Communications. 1975, (20): 858a. doi:10.1039/C3975000858A.
- ^ Crissey, SD; Ange, KD; Jacobsen, KL; Slifka, KA; Bowen, PE; Stacewicz-Sapuntzakis, M; Langman, CB; Sadler, W; Kahn, S. Serum concentrations of lipids, vitamin D metabolites, retinol, retinyl esters, tocopherols and selected carotenoids in twelve captive wild felid species at four zoos. The Journal of nutrition. 2003, 133 (1): 160–6. PMID 12514284.
- ^ Yahav, S; Buffenstein, R. Cholecalciferol supplementation alters gut function and improves digestibility in an underground inhabitant, the naked mole rat (Heterocephalus glaber), when fed on a carrot diet. The British journal of nutrition. 1993, 69 (1): 233–41. PMID 8384476. doi:10.1079/BJN19930025.
- ^ Stout, Sam D.; Agarwal, Sabrina C.; Stout, Samuel D. Bone loss and osteoporosis: an anthropological perspective. New York: Kluwer Academic/Plenum Publishers. 2003. ISBN 0-306-47767-X.
- ^ Crissey SD, Ange KD, Jacobsen KL, Slifka KA, Bowen PE, Stacewicz-Sapuntzakis M, et al. Serum concentrations of lipids, vitamin d metabolites, retinol, retinyl esters, tocopherols and selected carotenoids in twelve captive wild felid species at four zoos. The Journal of Nutrition. January 2003, 133 (1): 160–6. PMID 12514284. doi:10.1093/jn/133.1.160
 .
.
- ^ Holick MF. Chapter 4: Photobiology of Vitamin D. Feldman D, Wesley Pike J, Bouillon R, Giovannucci E, Goltzman D, Hewison M (编). Vitamin D: Volume 1: Biochemistry, Physiology and Diagnostics 4th. London, UK: Academic Press. 2018. ISBN 978-0-12-809965-0.
- ^ Ray CC. Q&A Sunshine Vitamin D. The New York Times. 2005-05-17 [2013-03-08]. (原始内容存档于2013-02-21).
- ^ Bolton J. UV FAQs. International Ultraviolet Association. [2020-08-19]. (原始内容存档于2013-05-30).
|url-status=和|dead-url=只需其一 (帮助) - ^ Holick MF. Vitamin D: the underappreciated D-lightful hormone that is important for skeletal and cellular health. Current Opinion in Endocrinology, Diabetes and Obesity. February 2002, 9 (1): 87–98. S2CID 87725403. doi:10.1097/00060793-200202000-00011.
- ^ Holick MF. Sunlight and vitamin D: both good for cardiovascular health. Journal of General Internal Medicine. September 2002, 17 (9): 733–5. PMC 1495109
 . PMID 12220371. doi:10.1046/j.1525-1497.2002.20731.x.
. PMID 12220371. doi:10.1046/j.1525-1497.2002.20731.x.
- ^ 184.0 184.1 Holick MF, Smith E, Pincus S. Skin as the site of vitamin D synthesis and target tissue for 1,25-dihydroxyvitamin D3. Use of calcitriol (1,25-dihydroxyvitamin D3) for treatment of psoriasis. Archives of Dermatology. December 1987, 123 (12): 1677–1683a. PMID 2825606. doi:10.1001/archderm.1987.01660360108022.
- ^ Anatomy of the skin. National Cancer Institute, US National Institutes of Health, Bethesda. 2016 [2016-12-19]. (原始内容存档于2021-01-28).
- ^ Vitamin D and Skin Health. LINUS PAULING INSTITUTE Micronutrient Information Center. Oregon State University. 2016-11-07 [2017-03-30]. (原始内容存档于2020-11-29).
- ^ Hume, Eleanor Margaret; Lucas, Nathaniel Sampson; Smith, Hannah Henderson. On the Absorption of Vitamin D from the Skin. Biochemical Journal. 1927, 21 (2): 362–367. PMC 1251921
 . PMID 16743844.
. PMID 16743844.
- ^ Dietary Reference Intakes for Calcium and Vitamin D (2011)Page 104. [2012-01-02]. (原始内容存档于2015-01-18).
- ^ Holick MF. Environmental factors that influence the cutaneous production of vitamin D (PDF). The American Journal of Clinical Nutrition. March 1995, 61 (3 Suppl): 638S–645S [2012-01-02]. PMID 7879731. (原始内容存档 (PDF)于2012-07-03).
- ^ 190.0 190.1 190.2 190.3 190.4 Adams, J. S.; Hewison, M. Update in Vitamin D. Journal of Clinical Endocrinology & Metabolism. 2010, 95 (2): 471–8. PMC 2840860
 . PMID 20133466. doi:10.1210/jc.2009-1773.
. PMID 20133466. doi:10.1210/jc.2009-1773.
- ^ Holick, MF. Sunlight and vitamin D for bone health and prevention of autoimmune diseases, cancers, and cardiovascular disease. The American Journal of Clinical Nutrition. 2004, 80 (6 Suppl): 1678S–88S [2012-01-02]. PMID 15585788. (原始内容存档于2012-08-20).
- ^ 192.0 192.1 Sarkar FH, Li Y, Wang Z, Kong D. The role of nutraceuticals in the regulation of Wnt and Hedgehog signaling in cancer. Cancer Metastasis Reviews. 2010, 29 (3): 383–64. PMC 2974632
 . PMID 20711635.
. PMID 20711635.
- ^ Hedgehog signaling and Vitamin D. Medscape.com. 2009-12-18 [2010-03-25]. (原始内容存档于2013-05-11).
- ^ Holick MF. The Vitamin D Solution: A 3-Step Strategy to Cure Our Most Common Health Problems. Penguin Publishing Group. 2010-04-01 [2022-12-06]. ISBN 978-1-101-22293-5. (原始内容存档于2022-04-16).
- ^ Agarwal SC, Stout SD. Bone Loss and Osteoporosis: An Anthropological Perspective. Springer Science & Business Media. 2011-06-28. ISBN 978-1-4419-8891-1. (原始内容存档 (PDF)于2006-01-29).
從猿類和猴子的生物學角度來看,可以理解其高25(OH)D濃度和相對較高的維他命D需求量是可以理解的—-牠們的身體表面面積通常相對於人類來說質量較大,而且牠們都是精通梳理毛髮的動物,經其口腔消耗從皮毛分泌的油脂中產生的維他命D。儘管人類皮膚中產生的許多維他命D被直接吸收,但鳥類和有毛皮的動物在梳理毛髮的時候,會從口腔獲得大部分維他命D(1946年—Bicknell和Prescott;1999年—Carpenter和Zhao)。維他命D是由皮膚油脂分泌到皮毛中產生的。口服的紫外線暴露的皮膚分泌物是許多動物獲取維他命D「營養素」的方式。儘管弗雷澤(Fraser,1983)認為皮膚吸收維他命D可能更自然,但從動物身上讓我們知道,口服維他命D具有同樣的生理意義。由於可以從暴露於紫外線的人體汗液和皮膚分泌物,也可以認為早期人類也可以透過舔皮膚經口腔獲得的某些維他命D。
- ^ Yahav S, Buffenstein R. Cholecalciferol supplementation alters gut function and improves digestibility in an underground inhabitant, the naked mole rat (Heterocephalus glaber), when fed on a carrot diet. The British Journal of Nutrition. January 1993, 69 (1): 233–41. PMID 8384476. doi:10.1079/BJN19930025
 .
.
- ^ 197.0 197.1 Holick MF. The vitamin D epidemic and its health consequences (PDF). The Journal of Nutrition. November 2005, 135 (11): 2739S–48S [2012-01-02]. PMID 16251641. doi:10.1093/jn/135.11.2739S. (原始内容存档 (PDF)于2017-11-18).
[Vitamin D3] is produced commercially by extracting 7-dehydrocholesterol from wool fat, followed by UVB irradiation and purification [...] [Vitamin D2] is commercially made by irradiating and then purifying the ergosterol extracted from yeast
- ^ Takeuchi A, Okano T, Sayamoto M, Sawamura S, Kobayashi T, Motosugi M, Yamakawa T. Tissue distribution of 7-dehydrocholesterol, vitamin D3 and 25-hydroxyvitamin D3 in several species of fishes. Journal of Nutritional Science and Vitaminology. February 1986, 32 (1): 13–22 [2020-08-20]. PMID 3012050. doi:10.3177/jnsv.32.13
 . (原始内容存档于2018-11-01).
. (原始内容存档于2018-11-01).
- ^ Cheng JB, Levine MA, Bell NH, Mangelsdorf DJ, Russell DW. Genetic evidence that the human CYP2R1 enzyme is a key vitamin D 25-hydroxylase. Proc Natl Acad Sci U S A. 2004-05-18, 101 (20): 7711–7715. Bibcode:2004PNAS..101.7711C. PMC 419671
 . PMID 15128933. doi:10.1073/pnas.0402490101.
. PMID 15128933. doi:10.1073/pnas.0402490101.
- ^ Laing, CJ and Cooke, NE. Vitamin D Binding Protein. In: Vitamin D (Vol. 1) David Feldman, Francis H. Glorieaux, J. Wesley Pike (eds.). Elsevier Press. 2005. pp 117-134.
- ^ 201.0 201.1 201.2 Bikle DD. Vitamin D metabolism, mechanism of action, and clinical applications. Chemistry & Biology. March 2014, 21 (3): 319–29. PMC 3968073
 . PMID 24529992. doi:10.1016/j.chembiol.2013.12.016.
. PMID 24529992. doi:10.1016/j.chembiol.2013.12.016.
- ^ Cheng JB, Levine MA, Bell NH, Mangelsdorf DJ, Russell DW. Genetic evidence that the human CYP2R1 enzyme is a key vitamin D 25-hydroxylase. Proceedings of the National Academy of Sciences of the United States of America. May 2004, 101 (20): 7711–5. Bibcode:2004PNAS..101.7711C. PMC 419671
 . PMID 15128933. doi:10.1073/pnas.0402490101.
. PMID 15128933. doi:10.1073/pnas.0402490101.
- ^ Laing CJ, Cooke NE. Section I: Ch. 8: Vitamin D Binding Protein. Feldman D, Glorieux FH, Pike JW (编). Vitamin D 1 2. Academic Press. 2004: 117–134 [2022-12-06]. ISBN 978-0122526879. (原始内容存档于2021-08-19).
- ^ IUPAC-IUB Joint Commission on Biochemical Nomenclature (JCBN): Nomenclature of vitamin D. Recommendations 1981. European Journal of Biochemistry. May 1982, 124 (2): 223–7. PMID 7094913. doi:10.1111/j.1432-1033.1982.tb06581.x.
- ^ Holick MF, Kleiner-Bossaller A, Schnoes HK, Kasten PM, Boyle IT, DeLuca HF. 1,24,25-Trihydroxyvitamin D3. A metabolite of vitamin D3 effective on intestine. The Journal of Biological Chemistry. October 1973, 248 (19): 6691–6. PMID 4355503.
- ^ Horst RL, Reinhardt TA, Ramberg CF, Koszewski NJ, Napoli JL. 24-Hydroxylation of 1,25-dihydroxyergocalciferol. An unambiguous deactivation process. The Journal of Biological Chemistry. July 1986, 261 (20): 9250–6. PMID 3013880.
- ^ Age-old children's disease back in force. Thestar.com. 2007-07-25 [2010-08-24]. (原始内容存档于2008-05-17).
- ^ Elena Conis. Fortified foods took out rickets. Los Angeles Times. 2006-07-24 [2010-08-24]. (原始内容存档于2012-03-02).
- ^ McClean, Franklin C.; Budy, Ann M. "Vitamin A, Vitamin D, Cartilage, Bones, and Teeth" in Harris, Robert S. (1963). Vitamins and Hormones, volume 21, pp. 51–52. London: Academic Press Partial view (页面存档备份,存于互联网档案馆) at Google Books.
- ^ Carere S. Age-old children's disease back in force. Toronto Star. 2007-07-25 [2010-08-24]. (原始内容存档于2008-05-17).
|url-status=和|dead-url=只需其一 (帮助) - ^ McClean FC, Budy AM. Vitamin A, Vitamin D, Cartilage, Bones, and Teeth. Vitamins and Hormones 21. Academic Press. 1964-01-28: 51–52 [2022-12-06]. ISBN 978-0-12-709821-0. (原始内容存档于2022-04-19).
- ^ History of Vitamin D. University of California at Riverside. 2011 [2014-05-09]. (原始内容存档于2017-10-16).
- ^ "Unraveling The Enigma Of Vitamin D" (页面存档备份,存于互联网档案馆) United States National Academy of Sciences
- ^ Adolf Windaus – Biography. Nobelprize.org. 2010-03-25 [2010-03-25]. (原始内容存档于2018-07-24).
- ^ Rosenheim O, King H. The Ring-system of sterols and bile acids. Part II. J. Chem. Technol. Biotechnol. 1932, 51 (47): 954–7. doi:10.1002/jctb.5000514702.
- ^ Askew FA, Bourdillon RB, Bruce HM, Callow RK, St. L. Philpot J, Webster TA. Crystalline Vitamin D. Proceedings of the Royal Society of London. Series B, Containing Papers of a Biological Character. 1932, 109 (764): 488–506. JSTOR 81571. doi:10.1098/rspb.1932.0008
 .
.
- ^ Hirsch AL. Industrial aspects of vitamin D. Feldman DJ, Pike JW, Adams JS (编). Vitamin D. Academic Press. 2011: 73 [2022-12-06]. ISBN 978-0-12-387035-3. (原始内容存档于2022-04-16).
- ^ Ziedonis AA, Mowery DC, Nelson RR, Bhaven NS. Ivory tower and industrial innovation: university-industry technology transfer before and after the Bayh-Dole Act in the United States. Stanford Business Books. 2004: 39–40 [2022-12-06]. ISBN 978-0-8047-4920-6. (原始内容存档于2022-03-14).
- ^ Arvids A. Ziedonis; Mowery, David C.; Nelson, Richard R.; Bhaven N. Sampat. Ivory tower and industrial innovation: university-industry technology transfer before and after the Bayh-Dole Act in the United States. Stanford, Calif: Stanford Business Books. 2004: [1]. ISBN 0-8047-4920-5.
- ^ Marshall J. Elbridge a Stuart: Founder of Carnation Company. Kessinger Publishing. September 2010 [2022-12-06]. ISBN 978-1-164-49678-6. (原始内容存档于2021-08-19).
- ^ Marshall, James. Elbridge A. Stuart Founder of the Carnation Company. Kessinger Publishing. 2005: 235. ISBN 978-1417988839.
- ^ Haussler MR, Norman AW. Chromosomal receptor for a vitamin D metabolite. Proceedings of the National Academy of Sciences of the United States of America. January 1969, 62 (1): 155–62. Bibcode:1969PNAS...62..155H. PMC 285968
 . PMID 5253652. doi:10.1073/pnas.62.1.155.
. PMID 5253652. doi:10.1073/pnas.62.1.155.
- ^ Holick MF, Schnoes HK, DeLuca HF. Identification of 1,25-dihydroxycholecalciferol, a form of vitamin D3 metabolically active in the intestine. Proceedings of the National Academy of Sciences of the United States of America. April 1971, 68 (4): 803–4. Bibcode:1971PNAS...68..803H. PMC 389047
 . PMID 4323790. doi:10.1073/pnas.68.4.803.
. PMID 4323790. doi:10.1073/pnas.68.4.803.
- ^ Norman AW, Myrtle JF, Midgett RJ, Nowicki HG, Williams V, Popják G. 1,25-dihydroxycholecalciferol: identification of the proposed active form of vitamin D3 in the intestine. Science. July 1971, 173 (3991): 51–4. Bibcode:1971Sci...173...51N. PMID 4325863. S2CID 35236666. doi:10.1126/science.173.3991.51.
- ^ Holick MF, DeLuca HF, Avioli LV. Isolation and identification of 25-hydroxycholecalciferol from human plasma. Archives of Internal Medicine. January 1972, 129 (1): 56–61. PMID 4332591. doi:10.1001/archinte.1972.00320010060005.
- ^ Cashman KD, Dowling KG, Škrabáková Z, Gonzalez-Gross M, Valtueña J, De Henauw S, et al. Vitamin D deficiency in Europe: pandemic?. The American Journal of Clinical Nutrition. April 2016, 103 (4): 1033–44. PMC 5527850
 . PMID 26864360. doi:10.3945/ajcn.115.120873.
. PMID 26864360. doi:10.3945/ajcn.115.120873.
- ^ Dankers W, Colin EM, van Hamburg JP, Lubberts E. Vitamin D in Autoimmunity: Molecular Mechanisms and Therapeutic Potential. Frontiers in Immunology. 2016, 7: 697. PMC 5247472
 . PMID 28163705. doi:10.3389/fimmu.2016.00697.
. PMID 28163705. doi:10.3389/fimmu.2016.00697.
- ^ 228.0 228.1 Heaney RP, Holick MF. Why the IOM recommendations for vitamin D are deficient. Journal of Bone and Mineral Research. March 2011, 26 (3): 455–7. PMID 21337617. S2CID 41510449. doi:10.1002/jbmr.328.
- ^ How is vitamin D being studied now in clinical cancer research?. National Cancer Institute, US National Institutes of Health. 2013-10-21 [2020-08-22]. (原始内容存档于2015-02-13).
- ^ ODS Vitamin D Initiative. Office of Dietary Supplements, US National Institutes of Health. 2014 [2020-08-22]. (原始内容存档于2021-01-26).
- ^ Pyrżak B, Witkowska-Sędek E, Krajewska M, Demkow U, Kucharska AM. Metabolic and immunological consequences of vitamin D deficiency in obese children. Body Metabolism and Exercise. Advances in Experimental Medicine and Biology 840. 2015: 13–9. ISBN 978-3-319-10249-8. PMID 25315624. doi:10.1007/5584_2014_81.
- ^ Khan SU, Khan MU, Riaz H, Valavoor S, Zhao D, Vaughan L, et al. Effects of Nutritional Supplements and Dietary Interventions on Cardiovascular Outcomes: An Umbrella Review and Evidence Map. Annals of Internal Medicine. August 2019, 171 (3): 190–198. PMC 7261374
 . PMID 31284304. doi:10.7326/m19-0341.
. PMID 31284304. doi:10.7326/m19-0341.
- ^ Pereira M, Dantas Damascena A, Galvão Azevedo LM, de Almeida Oliveira T, da Mota Santana J. Vitamin D deficiency aggravates COVID-19: systematic review and meta-analysis. Critical Reviews in Food Science and Nutrition. November 2020: 1–9. PMID 33146028. doi:10.1080/10408398.2020.1841090.
- ^ 234.0 234.1 Vitamin D | Coronavirus Disease COVID-19. COVID-19 Treatment Guidelines (US Centers for Disease Control and Prevention). [2020-10-03]. (原始内容存档于2021-01-27) (英语).
- ^ 235.0 235.1 Advisory statement on likely place in therapy | COVID-19 rapid evidence summary: vitamin D for COVID-19 | Advice | NICE. www.nice.org.uk. [2020-10-02]. (原始内容存档于2020-12-18).
- ^ Get vitamin D supplements if you're at high risk from coronavirus (COVID-19). nhs.uk. 2020-11-27 [2020-11-30]. (原始内容存档于2021-02-02) (英语).
- ^ 237.0 237.1 237.2 Quesada-Gomez JM, Entrenas-Castillo M, Bouillon R. Vitamin D receptor stimulation to reduce acute respiratory distress syndrome (ARDS) in patients with coronavirus SARS-CoV-2 infections: Revised Ms SBMB 2020_166. The Journal of Steroid Biochemistry and Molecular Biology. September 2020, 202: 105719. PMC 7289092
 . PMID 32535032. doi:10.1016/j.jsbmb.2020.105719.
. PMID 32535032. doi:10.1016/j.jsbmb.2020.105719.
衍生阅读
[编辑]- Ross, A.C/Taylor, C.L./Yaktine, A.L./Valle, H.B.D. (editors, 2011) Dietary Reference Intakes for Calcium and Vitamin D(页面存档备份,存于互联网档案馆). National Academies Press. ISBN 978-0-309-16394-1
- Rubin, A.L. (2011). Vitamin D for Dummies. Wiley Publishing. ISBN 978-0-470-89175-9
- Dietary Supplement Fact Sheet: Vitamin D(页面存档备份,存于互联网档案馆) from the U.S. National Institutes of Health
- Disagreement among experts about the correct vitamin D dose. (页面存档备份,存于互联网档案馆) (Nature News, July 6, 2011)
- 如何攝取維生素D?維生素D的好處與食物補充重點! (页面存档备份,存于互联网档案馆)
