倍他米松
 | |
 | |
| 臨床資料 | |
|---|---|
| 商品名 | Celestone、Eleuphrat及其他 |
| AHFS/Drugs.com | Monograph |
| MedlinePlus | a682799 |
| 核准狀況 | |
| 懷孕分級 | |
| 給藥途徑 | 口服給藥、外用藥物及肌肉注射 |
| ATC碼 | |
| 法律規範狀態 | |
| 法律規範 |
|
| 藥物動力學數據 | |
| 藥物代謝 | 肝臟CYP3A4 |
| 生物半衰期 | 36-54小時 |
| 排泄途徑 | 腎臟 (經由尿液排出人體) |
| 識別資訊 | |
| |
| CAS號 | 378-44-9 |
| PubChem CID | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| CompTox Dashboard (EPA) | |
| ECHA InfoCard | 100.006.206 |
| 化學資訊 | |
| 化學式 | C22H29FO5 |
| 摩爾質量 | 392.47 g·mol−1 |
| 3D模型(JSmol) | |
| |
| |
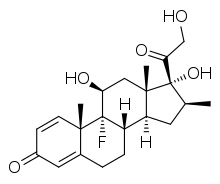
倍他米松(英語:Betamethasone)是一種類固醇藥物,[3]用於治療多種疾病,包括類風濕性關節炎和全身性紅斑狼瘡等風濕性疾病、皮膚炎和乾癬等皮膚病、氣喘和血管性水腫等過敏性疾病、促進早產嬰兒肺部發育、克隆氏症、白血病等癌症,以及與氟氫可的松聯合使用以治療腎上腺功能不全等。[3]給藥方式有口服、肌肉注射或在皮膚上塗抹(通常有霜劑、乳液或液體形式)。[3][4]
使用此藥物後嚴重的副作用有感染風險增加、肌肉無力、嚴重過敏反應和思覺失調。[3]長期使用可能會導致腎上腺功能不全。[3]長期使用後突然停藥可能會有嚴重性後果。[3]使用霜劑通常會導致毛髮增長和皮膚不適。[4]倍他米松屬於糖皮質素類藥物。[3]它是地塞米松的立體異構體,這兩種化合物僅在16位甲基的空間構型上有所不同(參見類固醇#命名法)。[5]
醫療用途
[編輯]倍他米松是一種皮質類固醇,有丸劑、注射劑、軟膏、乳膏、乳液、凝膠或皮膚用噴霧劑,以及用於頭皮的泡沫劑。[6]經注射給藥時,抗炎性作用約會在兩小時內開始,並持續7天。[3]
乳膏可用於緩解皮膚不適(例如皮膚炎引起的瘙癢和剝落)。它用作局部乾癬的治療,與二丙酸倍他米松(倍他米松衍生物)或是水楊酸的作用相似,或與卡泊三醇/倍他米松二丙酸組成複方劑使用。(參見卡泊三醇/二丙酸倍他米松#Regulation}})倍他米松磷酸鈉可作口服劑和注射劑,其適應症與其他類固醇相同。很多以倍他米松為基礎的藥物都含有戊酸酯類固醇。(如Betamethasone valerate與倍他米松二丙酸)
在一項隨機對照試驗中,倍他米松被證明可將與共濟失調微血管擴張症候群 (A-T) 相關的一些共濟失調症狀減輕28-31%。[7]
倍他米松也用於刺激胎兒肺臟成熟,以預防新生兒呼吸窘迫症候群 (IRDS) ,並降低早產兒顱內出血的發生率和死亡率。[8]
含有0.05%倍他米松的乳膏似乎可有效治療男孩的包莖問題,[9]而通常因此能避免包皮環切術。[10][11][12]此藥物已成為英國國民保健署體系中一些醫生的首選,用以避免包皮環切的治療方式。[13][14]
副作用
[編輯]在大面積皮膚、破損或裸露皮膚、皮膚皺褶或密封敷料之下長時間使用如倍他米松的皮質類固醇藥物,在極少數情況下可能會導致吸收過多,所產生的副作用例如有局部皮膚變薄,及導致腎上腺減少產生天然激素。
倍他米松也可在早產兒分娩前使用,以幫助其肺部發育。
當注射到人體硬膜外腔或脊柱時,可能會導致嚴重的副作用,如視力喪失、中風和癱瘓。[16]
藥理學
[編輯]形式
[編輯]倍他米松有多種化合物形式:二丙酸倍他米松(品牌有Diprosone、Diprolene、Celestamine、Procort(於巴基斯坦)等)、倍他米松磷酸鈉(於意大利,品牌名稱有Bentelan)和倍他米松二丙酸酯(品牌名稱有Audavate、Betnovate 、Celestone、Fucibet(夫西地酸/倍他米松二丙酸酯複方藥) )等。在美國和加拿大,倍他米松與克催瑪汝混合,以Lotrisone和Lotriderm的品牌銷售。它還與水楊酸組合用於治療乾癬(品牌名稱為Diprosalic)。在一些國家,它也與克催瑪汝和慶大黴素(兩者皆為(抗細菌藥)混合販售。
倍他米松磷酸鈉與醋酸倍他米松的混合物在美國以Celestone Soluspan的品牌名稱出售。[17]
社會與文化
[編輯]倍他米松的專利於1958年在美國提出申請,於1961年獲得,也於1961年取得美國的核准用於醫療用途。[3][18]此藥物的霜劑和軟膏已列入世界衛生組織基本藥物標準清單之中。[19]由於專利已過期,市面有其通用名藥物販售。[3]此藥物於2021年在美國最常用處方藥中排名第251,開立的處方箋數量超過100萬張。[20][21]
參見
[編輯]參考文獻
[編輯]- ^ Betamethasone Use During Pregnancy. Drugs.com. 2019-12-30 [2020-03-29]. (原始內容存檔於2020-12-01).
- ^ Betamethasone 500 microgram Soluble Tablets - Summary of Product Characteristics (SmPC). (emc). 2018-04-05 [2020-03-29]. (原始內容存檔於2020-03-29).
- ^ 3.00 3.01 3.02 3.03 3.04 3.05 3.06 3.07 3.08 3.09 Betamethasone. The American Society of Health-System Pharmacists. [2015-12-02]. (原始內容存檔於2015-12-08).
- ^ 4.0 4.1 Betamethasone topical. The American Society of Health-System Pharmacists. [2015-12-02]. (原始內容存檔於2015-12-08).
- ^ Antignac JP, Le Bizec B, Monteau F, Andre F. Differentiation of betamethasone and dexamethasone using liquid chromatography/positive electrospray tandem mass spectrometry and multivariate statistical analysis. Journal of Mass Spectrometry. January 2002, 37 (1): 69–75. Bibcode:2002JMSp...37...69A. PMID 11813313. doi:10.1002/jms.260.
- ^ Betamethasone Topical. MedlinePlus. 2020-03-19 [2020-03-29]. (原始內容存檔於2020-03-29).
- ^ Zannolli R, Buoni S, Betti G, Salvucci S, Plebani A, Soresina A, et al. A randomized trial of oral betamethasone to reduce ataxia symptoms in ataxia telangiectasia. Movement Disorders. September 2012, 27 (10): 1312–1316. PMID 22927201. S2CID 23696748. doi:10.1002/mds.25126.
- ^ Antenatal Corticosteroid Therapy for Fetal Maturation. ACOC Clinical. August 2017 [2024-03-31]. (原始內容存檔於2024-03-31).
- ^ Moreno G, Corbalán J, Peñaloza B, Pantoja T. Topical corticosteroids for treating phimosis in boys. The Cochrane Database of Systematic Reviews. September 2014, 9 (9): CD008973. PMC 10765470
 . PMID 25180668. doi:10.1002/14651858.CD008973.pub2.
. PMID 25180668. doi:10.1002/14651858.CD008973.pub2.
- ^ Van Howe RS. Cost-effective treatment of phimosis. Pediatrics. October 1998, 102 (4): E43. PMID 9755280. doi:10.1542/peds.102.4.e43
 . (原始內容存檔於2009-08-19). A review of estimated costs and complications of 3 phimosis treatments.
. (原始內容存檔於2009-08-19). A review of estimated costs and complications of 3 phimosis treatments.
- ^ Esposito C, Centonze A, Alicchio F, Savanelli A, Settimi A. Topical steroid application versus circumcision in pediatric patients with phimosis: a prospective randomized placebo controlled clinical trial. World Journal of Urology (Springer Science and Business Media LLC). April 2008, 26 (2): 187–190. PMID 18157674. S2CID 8922151. doi:10.1007/s00345-007-0231-2.
- ^ Zampieri N, Corroppolo M, Zuin V, Bianchi S, Camoglio FS. Phimosis and topical steroids: new clinical findings. Pediatric Surgery International. April 2007, 23 (4): 331–335. PMID 17308904. S2CID 22849471. doi:10.1007/s00383-007-1878-x.
- ^ Berdeu D, Sauze L, Ha-Vinh P, Blum-Boisgard C. Cost-effectiveness analysis of treatments for phimosis: a comparison of surgical and medicinal approaches and their economic effect. BJU International. February 2001, 87 (3): 239–244. PMID 11167650. S2CID 2161551. doi:10.1046/j.1464-410x.2001.02033.x
 .
.
- ^ Chu CC, Chen KC, Diau GY. Topical steroid treatment of phimosis in boys. The Journal of Urology. September 1999, 162 (3 Pt 1): 861–863. PMID 10458396. doi:10.1097/00005392-199909010-00078.
- ^ 15.0 15.1 15.2 15.3 15.4 15.5 15.6 betamethasone (PDF). F.A. Davis. 2017 [2017-03-07]. (原始內容存檔 (PDF)於2017-09-08).
- ^ FDA Drug Safety Communication: FDA requires label changes to warn of rare but serious neurologic problems after epidural corticosteroid injections for pain. FDA. 2014-04-23 [2016-08-15]. (原始內容存檔於2016-08-11).
- ^ Celestone Soluspan- betamethasone acetate and betamethasone sodium phosphate injection, suspension. DailyMed. 2019-11-18 [2020-03-29]. (原始內容存檔於2020-08-04).
- ^ Fischer J, Ganellin CR. Analogue-based Drug Discovery. John Wiley & Sons. 2006: 485 [2024-04-10]. ISBN 9783527607495. (原始內容存檔於2023-01-10).
- ^ World Health Organization. World Health Organization model list of essential medicines: 21st list 2019. Geneva: World Health Organization. 2019. hdl:10665/325771
 . WHO/MVP/EMP/IAU/2019.06. License: CC BY-NC-SA 3.0 IGO.
. WHO/MVP/EMP/IAU/2019.06. License: CC BY-NC-SA 3.0 IGO.
- ^ The Top 300 of 2021. ClinCalc. [2024-01-14]. (原始內容存檔於2024-01-15).
- ^ Betamethasone - Drug Usage Statistics. ClinCalc. [2024-01-14]. (原始內容存檔於2024-02-29).
