氯化鈉
| 氯化鈉 | |
|---|---|

| |

| |
| IUPAC名 Sodium chloride | |
| 英文名 | Sodium chloride |
| 別名 | 食鹽、石鹽、鹽、食用鹽 |
| 識別 | |
| CAS號 | 7647-14-5 |
| PubChem | 5234 |
| ChemSpider | 5044 |
| SMILES |
|
| InChI |
|
| InChIKey | FAPWRFPIFSIZLT-REWHXWOFAE |
| Beilstein | 3534976 |
| Gmelin | 13673 |
| EINECS | 231-598-3 |
| ChEBI | 26710 |
| RTECS | VZ4725000 |
| KEGG | D02056 |
| MeSH | Sodium+chloride |
| 性質 | |
| 化學式 | NaCl |
| 莫耳質量 | 58.44277 g·mol⁻¹ |
| 外觀 | 白色或無色晶體或粉末[1] |
| 密度 | 2.17 g/cm³ (固)[1] |
| 熔點 | 802.018 °C (1075.168 K)[1] |
| 沸點 | 1465 °C (1738.15 K)[1] |
| 溶解性(水) | 36.0 g/100 g (25 °C)[1] |
| 溶解性 | 微溶於乙醇(詳見「物理性質」一節)[1] |
| 折光度n D |
1.55 (500 nm)[2] |
| 結構 | |
| 晶體結構 | 面心立方結構[1] |
| 晶格常數 | a = 564 pm[3] |
| 配位幾何 | 八面體 |
| 危險性 | |
| 警示術語 | R:R36 |
| 安全術語 | S:無 |
| NFPA 704 | |
| 致死量或濃度: | |
LD50(中位劑量)
|
3 g/kg(口服,大鼠)[4] |
| 相關物質 | |
| 其他陰離子 | 氟化鈉、溴化鈉、 碘化鈉 |
| 其他陽離子 | 氯化鋰、氯化鉀、 氯化銣、氯化銫、 氯化鎂、氯化鈣、 氯化鋇 |
| 相關鹽 | 乙酸鈉 |
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |
氯化鈉(化學式:NaCl),是一種離子化合物。鈉離子和氯離子的原子質量分別為22.99和35.45g/mol,也就是說100g的氯化鈉中含有39.34 g的鈉和 60.66 g的氯。氯化鈉是海水中鹽分的主要組成部分,它的存在也使得海水有其特有的鹹味。氯化鈉也是細胞外液的主要鹽類,0.89%的氯化鈉水溶液俗稱為生理鹽水。其可食用的形態是食鹽的主要成分,多用於食物的調味和保存。
在工業中,主要用於製造氫氧化鈉和氯以及應用於聚氯乙烯、塑料、木漿(紙漿)等許多其他產品的生產過程。由於它可以降低水的熔點,偶爾也用於解凍冰凍的路面。
氯化鈉的pH是7。
生產[編輯]
各種化合物的生產[編輯]
氯化鈉是各種化學反應的生產中(不管是直接還是間接使用)不可缺少的原料。
氯鹼法[編輯]
由電解飽和食鹽水溶液製取氫氧化鈉、氯氣和氫氣的工業生產方法,是重要的基礎化學工業之一。其反應如下:
氨鹼法[編輯]
也叫索爾維法,是工業生產碳酸鈉的主要方法。此反應需要氯化鈉和石灰石,其產物是氯化鈣和碳酸鈉。
聯合制鹼法[編輯]
也叫侯氏制鹼法,同樣是工業生產碳酸鈉的主要方法。此反應需要氯化鈉、二氧化碳和氨氣,其產物是氮肥氯化銨和碳酸氫鈉,再經加熱使碳酸氫鈉分解為碳酸鈉。
硬水軟化[編輯]
硬水(如井水)含有大量的鎂離子和鈣離子。硬水有許多危害,包括降低洗衣液的效果和阻塞水管,因此需要用離子交換樹脂將其置換出來。氯化鈉用於更新已失效的離子交換樹脂,使其能重複使用。
晶體結構[編輯]

氯化鈉晶體的內部結構,是人類測試的第一個晶體結構[5]。氯化鈉的晶體形成立體對稱,每個離子有六個相鄰的離子,組成一個八面體。其晶體結構中,較大的氯離子排成立方最密堆積(ccp),較小的鈉離子則填充氯離子之間的八面體的空隙。每個離子周圍都被六個其他的離子包圍著。這種結構也存在於其他很多化合物中,稱為氯化鈉型結構。
| 名稱 | 英文名 | 代號 | 晶格結構 | 晶系 | 配位 | 舉例 | 示意圖(點擊可放大) |
|---|---|---|---|---|---|---|---|
| 氯化鈉結構 | NaCl structure | B1型 | 面心立方晶格 | 立方晶系 | [a] | [b] | 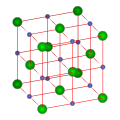
|
氯化鈉的晶體主要有帶正電荷的Na+和帶負電荷的Cl−組成,Na+和Cl−在相互垂直的3個方向上的平面上以1:1的比例均勻分布,每個方向上的平面上電荷的代數和為0,稱為「電性中和面」。「電性中和面」內靜電力較強,但相互平行的相鄰的「電性中和面」之間的靜電力較弱,導致氯化鈉晶體的解理沿著這3個互相垂直的方向產生。因此,當氯化鈉晶體受到外力發生破裂時,容易沿著這3個方向破裂開形成一個垂直的「三面凹角」。
性質[編輯]

物理性質[編輯]
氯化鈉在多數情況下是白色的粉末,其結晶是半透明的立方體,但也可能會因雜質而呈現出藍或紫的色調。氯化鈉的莫耳質量是58.443g/mol,熔點為801 °C(1,474 °F),沸點為1,465 °C(2,669 °F),密度是每立方厘米2.17克。莫氏硬度為2~2.5。[6][7]
氯化鈉易溶於水,常溫下在水中的溶解度是359克/升。食鹽水的物理性質與純水有較大的差異。常壓下,水鹽體系的低共熔點為−21.12 °C(−6.02 °F),低共熔物中鹽的質量分數為23.31%[c]。該質量分數的食鹽水沸點約為108.7 °C (227.7 °F)[8]。氯化鈉溶液的PH值不是正好等於7,而是視濃度,溫度及純度而定,介於5.6至8.4之間[9]。
依據sigma Aldrich 物質資料表: 氯化鈉水中溶解度為(25°C) 357 mg/ml, 100°C為 384 mg/ml。飽和食鹽水之密度為 (25°C) 1.202 g/ml。
依此換算25°C 飽和食鹽水每一立方公分含316.223毫克之氯化鈉。
(網路上之飽和生理食鹽水密度錯誤甚多,推估為教學現場密度考題衍生之錯誤)
| 氯化鈉在不同溶液中的溶解度 g / 1 kg ,25℃[10] | |
|---|---|
| 水 | 360 |
| 甲醯胺 | 94 |
| 甘油 | 83 |
| 1,2-丙二醇 | 71 |
| 甲酸 | 52 |
| 液氨 | 30.2 |
| 甲醇 | 14 |
| 乙醇 | 0.65 |
| 二甲基甲醯胺 | 0.4 |
| 1-丙醇 | 0.124 |
| 環丁碸 | 0.05 |
| 1-丁醇 | 0.05 |
| 異丙醇 | 0.03 |
| 1-戊醇 | 0.018 |
| 乙腈 | 0.003 |
| 丙酮 | 0.00042 |
| 溫度 | °C | 800 | 850 | 900 | 1000 | 1100 |
| 電導率 σ | S·m−1 | 3,58 | 3,75 | 3,90 | 4,17 | 4,39 |
化學性質[編輯]

氯化鈉是一種離子化合物,化學式為,代表鈉離子與氯離子的比例是一比一,之間靠離子鍵結合。鈉原子將其3s態電子轉移到氯原子的3d態上,兩者都達到穩定的電子結構。帶正電的鈉離子與帶負電的氯離子相互吸引,穩定的結合在一起[13]。
氯化鈉溶於水時,完全電離為鈉離子與氯離子[14]。他們會使純水靠氫鍵鍵合形成的正常結構(四面體排列)遭到破壞[15]。Na+與水分子的結合力大約是水分子間氫鍵的4倍[d]。[16]
從冷溶液中析出的鹽當中,每個鹽分子帶有兩個結晶水:NaCl·2H2O。
氯化鈉溶液的檢驗可分兩步完成。首先,向溶液中滴入硝酸酸化過的硝酸銀溶液,有白色沉澱(氯化銀)產生,證明有Cl-。然後用鉑絲蘸取少量溶液,置於酒精燈上灼燒,火焰呈黃色,可證含有Na+。[17]
| 製取金屬鈉 | |
| 電解飽和食鹽水 | |
| 和硝酸銀反應 | |
| 氯化鈉固體中加入濃硫酸 |
製法[編輯]
- 蒸發鹹水(如晾曬海水),在水沒有完全蒸乾前濾出氯化鈉晶體。適合大量生產。[18]
- 少量精製:將粗鹽溶解於水中,過濾掉不溶性雜質,再加精製劑如NaOH、Na2CO3 和CaCl2 等,使SO42−、Ca2+、Mg2+ 等可溶性雜質轉化成沉澱,並濾除。最後用鹽酸將pH調節至7以下,蒸乾溶液,得到氯化鈉晶體。
- 實驗室里的製備方法:將過量的鹽酸和氫氧化鈉,碳酸氫鈉,氧化鈉或碳酸鈉等鈉鹽的水溶液混合,或將過氧化氫與次氯酸鈉溶液混合,蒸乾溶液,析出氯化鈉晶體。
- HCl(aq)+NaOH(aq)→NaCl(aq)+H₂O(l)
- HCl(aq)+NaHCO₃(aq)→NaCl(aq)+CO₂(g)+H₂O(l)
- 2HCl(aq)+Na₂O(s)→2NaCl(aq)+H₂O(l)
- 4HCl(aq)+2Na₂O₂(s)→4NaCl(aq)+O₂(g)+2H₂O(l)
- 2HCl(aq)+Na₂CO₃(aq)→2NaCl(aq)+CO₂(g)+H₂O
- H₂O₂(aq)+NaClO(aq)→NaCl(aq)+O₂(g)+H₂O(l)
- 把金屬鈉放進鹽酸,蒸乾溶液,得到氯化鈉晶體。
- 2HCl(aq)+2Na(s)→2NaCl(aq)+H₂(g)
- 但此為爆炸性反應,一般不會使用。
- 把金屬鈉加熱,並放進氯氣中混合,得到氯化鈉晶體。
- 2Na(s)+Cl₂(g)→2NaCl(s)
用途[編輯]
| 此條目需要更新。 (2024年3月19日) |
氯化鈉的用途很廣,使用量也大。根據1974年的統計數據,美國生產的氯化鈉中只有2.7%作為家用食鹽出售,16.6%用於路面除冰[19],4.2%用於動物飼料,1.8%用於硬水軟化,剩餘60%以上均被用於工業生產[20]。

餐飲[編輯]
氯化鈉能產生人類能感知的鹹味,是一種常見的調味料。食鹽中一般含有97至99%的氯化鈉[21][22]。此外,海鹽及新鮮開採的石鹽(多數來自史前海洋)也含有微量的稀有元素,這些稀有元素通常對健康有益。
食鹽中的鈉是人體必需的營養素之一,但攝取過量的食鹽易得高血壓[23],或其它心血管疾病[24]。世界衛生組織建議,成年人每天應攝取少於2克的鈉,相當於5克食鹽[25]。
醫學[編輯]
氯化鈉對於地球上的生命非常重要。大部分生物組織中含有多種鹽類。鈉離子在體內負責調節神經衝動的傳導。血液中的鈉離子濃度直接關係到體液的安全水平的調節,濃度失常會導致高鈉血症或低血鈉症。[26]
0.9%的氯化鈉水溶液稱為生理鹽水,因為它與血漿有相同的滲透壓。生理鹽水是主要的體液替代物,廣泛用於治療及預防脫水[e],也用於靜脈注射治療及預防血量減少性休克。
工業[編輯]
氯化鈉是無機重化工業的基礎,在無機化工中,使用的食鹽比其他任何原料都要多[27]。其中,消耗食鹽最多的工藝是氯鹼法,該工藝通過電解食鹽水製備氫氧化鈉、氯氣和氫氣,通過電解熔鹽獲得金屬鈉和氯氣。氯氣主要被用於合成含氯有機化合物(如氯氟烴、聚氯乙烯)和消毒漂白,氫氧化鈉則被廣泛運用於無機化工和紙漿處理。另一種消耗食鹽量比較大的工藝是氨鹼法,該法通過往食鹽水中注入氨和二氧化碳來製備碳酸氫鈉,進而製備碳酸鈉。大部分碳酸鈉被用於製造玻璃。[28]
道路[編輯]
用於路面除冰是除了工業生產之外鹽的主要用途。
注釋[編輯]
參考資料[編輯]
- ^ 1.0 1.1 1.2 1.3 1.4 1.5 1.6 CRC Handbook of Chemistry and Physics 97th Edition. 2016-06-24: 4–85. ISBN 1-4987-5428-7 (英語).
- ^ RefractiveIndex.INFO: Refractive index of NaCl (Sodium chloride) (頁面存檔備份,存於網際網路檔案館)
- ^ W.T.Barrett, W.E.Wallace: Studies of NaCl-KCI Solid Solutions. I. Heats of Formation, Lattice Spacings, Densities, Schottky Defects and Mutual Solubilities. In: Journal of the American Chemical Society 76(2), 1954, S. 366–369, doi:10.1021/ja01631a014
- ^ Tucker, R. K.; Haegele, M. A. Comparative acute oral toxicity of pesticides to six species of birds. Toxicology and Applied Pharmacology. 1971, 20 (1): 57–65. ISSN 0041-008X. PMID 5110827. doi:10.1016/0041-008x(71)90088-3.
- ^ 氯化钠的晶体结构. 中國數字科技館. [2017-10-23]. (原始內容存檔於2020-05-02).
- ^ Sirdeshmukh, Dinker B.; Sirdeshmukh, Lalitha & Subhadra, K. G. Alkali halides: a handbook of physical properties. Springer. 2001: 65, 68 [2017-10-23]. ISBN 3-540-42180-7. (原始內容存檔於2016-09-04).
- ^ 氯化钠(NaCl)晶体. 吉林光正晶體有限公司. [2017-10-23]. (原始內容存檔於2017-10-24).
- ^ Elvers, B. et al. (ed.) (1991) Ullmann's Encyclopedia of Industrial Chemistry, 5th ed. Vol. A24, Wiley, p. 319, ISBN 978-3-527-20124-2.
- ^ L Shu, IJ Obagbemi, S Liyanaarachchi, D Navaratna, R Parthasarathy, V Jegatheesan (2016) Why does pH increase with CaCl2 as draw solution during forward osmosis filtration,Process Safety and Environmental Protection 104, 465–471
- ^ Burgess, J. Metal Ions in Solution. New York: Ellis Horwood. 1978. ISBN 0-85312-027-7.
- ^ G. Westphal, G. Kristen, W. Wegener, P. Ambatiello, H. Geyer, B. Epron, C. Bonal, G. Steinhauser, F. Götzfried: Sodium Chloride, in: Ullmanns Enzyklopädie der Technischen Chemie, Wiley-VCH Verlag GmbH & Co. KGaA, Weinheim 2012; doi:10.1002/14356007.a24_317.pub4.
- ^ Klewe, B.; Pedersen, B. The crystal structure of sodium chloride dihydrate. Acta Cryst. 1974, B30: 2363–2371. doi:10.1107/S0567740874007138.
- ^ 王昆林. 材料工程基础. 清華大學出版社. : 44. ISBN 7302070644.
- ^ Wood, Frank Osborne. Salt (NaCl). Encyclopædia Britannica online. [2013-10-09]. (原始內容存檔於2015-05-02).
- ^ Lincoln, S. F.; Richens, D. T. and Sykes, A. G. (2003) "Metal Aqua Ions" Comprehensive Coordination Chemistry II Volume 1, pp. 515–555. doi:10.1016/B0-08-043748-6/01055-0
- ^ 段振華. 高等学校研究生教材·高级食品化学. 中國輕工業出版社. 2012. ISBN 7501983844.
- ^ 氯化钠. 江西華亨生物科技有限公司. [2017-10-23]. (原始內容存檔於2017-10-23).
- ^ Salt (頁面存檔備份,存於網際網路檔案館), U.S. Geological Survey
- ^ Rastogi, Nina (16 February 2010) Does road salt harm the environment? (頁面存檔備份,存於網際網路檔案館) slate.com.
- ^ Westphal, Gisbert et al. (2002) "Sodium Chloride" in Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim doi:10.1002/14356007.a24_317.pub4.
- ^ Tesco Table Salt 750g. Tesco. [2010-12-05]. (原始內容存檔於2009-05-11).
Nutritional analysis provided with Tesco Table Salt states 38.9 percent sodium by weight which equals 97.3 percent sodium chloride
- ^ The international Codex Alimentarius Standard for Food Grade Salt (PDF). [2011-07-07]. (原始內容存檔 (PDF)於2012-03-14).
The content of NaCl shall not be less than 97% on a dry matter basis, exclusive of additives.
- ^ 科学生活:防控高血压为什么要“少吃盐”?. 中央政府入口網站. 科技日報. 2009-10-12 [2017-10-23]. (原始內容存檔於2017-10-24).
- ^ McCarron, David A. Dietary sodium and cardiovascular and renal disease risk factors: dark horse or phantom entry?. Nephrol Dial Transplant. 2008, 23 (7): 2133–7. PMC 2441768
 . PMID 18587159. doi:10.1093/ndt/gfn312.
. PMID 18587159. doi:10.1093/ndt/gfn312.
- ^ WHO issues new guidance on dietary salt and potassium. 世界衛生組織. 2013-01-31. (原始內容存檔於2016-07-20) (英語).
- ^ Osanai T, Fujiwara N, Saitoh M, et al. Relationship between salt intake, nitric oxide and asymmetric dimethylarginine and its relevance to patients with end-stage renal disease. Blood Purif. 2002, 20 (5): 466–8. PMID 12207094. doi:10.1159/000063555.
- ^ Dennis S. Kostick Salt (頁面存檔備份,存於網際網路檔案館), U.S. Geological Survey, 2008 Minerals Yearbook
- ^ N.N.Greenwood、A.Earnshaw著,曹庭禮等人譯. 元素化学. 高等教育出版社. 1997: 上冊108-112、144,中冊603-604.
參考文獻[編輯]
- Haynes, William M. (編). CRC Handbook of Chemistry and Physics 92nd. CRC Press. 2011. ISBN 978-1439855119.
參見[編輯]
外部連結[編輯]
| 維基共享資源中相關的多媒體資源:氯化鈉 |
| 維基教科書的食譜有以下內容:Salt |
- Salt (頁面存檔備份,存於網際網路檔案館) United States Geological Survey Statistics and Information
- Using Salt and Sand for Winter Road Maintenance. Road Management Journal. December 1997 [2020-02-14]. (原始內容存檔於2016-09-21).
- Calculators: surface tensions (頁面存檔備份,存於網際網路檔案館), and densities, molarities and molalities (頁面存檔備份,存於網際網路檔案館) of aqueous NaCl (and other salts)
- JtBaker MSDS
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||










