钛
钛被认为是一种稀有金屬,这是由于在自然界中其存在分散并难于提取。但其相对丰度在所有元素中居第十位。[5]鈦的礦石主要有鈦鐵礦及金紅石,廣佈於地殼及岩石圈之中。鈦亦同時存在於幾乎所有生物、岩石、水體及土壤中[6]。從主要礦石中萃取出鈦需要用到克羅爾法[7]或亨特法。鈦最常見的化合物是二氧化鈦,可用於製造白色顏料[8]。其他化合物還包括四氯化鈦(TiCl4,作催化劑及用於製造煙幕或空中文字)及三氯化鈦(TiCl3,用於催化聚丙烯的生產)[6]。
鈦能與鐵、鋁、釩或鉬等其他元素熔成合金,造出高強度的輕合金,在各方面有着廣泛的應用,包括宇宙航行(噴氣發動機、導彈及航天器)、軍事、工業程序(化工與石油製品、海水淡化及造紙)、汽車、農產食品、醫學(義肢、骨科移植及牙科器械與填充物)、運動用品、珠寶及手機等等。[6]
鈦最有用的兩個特性是,抗腐蝕性,及金屬中最高的強度-重量比[9]。在非合金的狀態下,鈦的強度跟某些鋼相若,但卻還要輕45%[10]。有兩種同素異形體[11]和五種天然的同位素,由46Ti到50Ti,其中豐度最高的是48Ti(73.8%)[12]。鈦的化學性質及物理性質和鋯相似,這是因為兩者的價電子數目相同,並於元素週期表中同屬一族。
特性[编辑]
物理性質[编辑]
在金屬元素中,鈦的比强度很高[11]。它是一種高強度但低質量的金屬,而且具有相當好的延展性(尤其是在無氧的環境下)[13]。钛的表面呈銀白色金屬光澤[14]。它的熔點相当地高(超過1,649攝氏度),所以是良好的耐火金屬材料。它具有順磁性,其電導率及熱導率皆甚低[6]。
商業等級的鈦(純度為99.2%)具有約為434百萬帕斯卡的極限抗拉強度,與低等級的鋼合金相若,但比鋼合金要輕45%[10]。鈦的密度比鋁高60%,但強度是常見的6061-T6鋁合金的兩倍[10]。鈦可被用於各種用途。某些鈦合金(例如βC)的抗拉強度達1,400兆帕斯卡[15]。然而,當鈦被加熱至430攝氏度以上時,強度會減弱[16]。
儘管比不上高等級的熱處理鋼,钛仍具有相當的硬度。钛不具磁性,同時是不良的導熱及導電體。用機械處理時需要注意,因為如不採用鋒利的器具及適當的冷卻手法,鈦會軟化,並留有壓痕。像鋼結構體一樣,鈦結構體也有疲勞極限,因此在某些應用上可保證持久耐用。[14]鈦合金的比勁度一般不如鋁合金及碳纖維等其他物料,所以較少應用於需要高剛度的結構上。
鈦具有两种同素異形體,在882攝氏度時,就會從六方最密堆積的α型轉變成體心立方的β型。[16]在到達臨界温度前,α型的比熱會隨着升温而暴增,但到達後會下降,然後在β型下不論温度地保持基本恆定。[16]跟鋯和鉿類似,鈦還存在一種ω態,在高壓時熱力學穩定,但也可能在常壓下以準穩態存在。此態一般是六邊形(理想)或三角形(扭曲),在軟性縱波聲頻光子導致β型(111)原子平面倒塌時能被觀測到。[17]
化學性質[编辑]
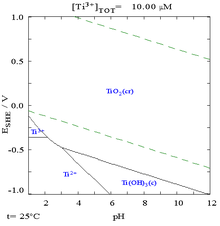
鈦的特性中,最為人稱道的就是它優良的抗腐蝕能力——它的抗蝕性幾乎跟鉑一樣好,但鈦会被热的稀硫酸、稀鹽酸和濃酸溶解。雖然以下的電位-pH圖指出鈦在熱力學上是一種活性很高的金屬[18],但是它與水及空氣的反應是非常緩慢的[6]。
鈦在曝露在高温空氣中時,會生成一層彩色的鈍氧化物保護膜,阻止氧化持續[6]。在最初形成時,保護層只有一至二納米厚,但會緩慢地持續增厚;四年間可達25納米厚[19]。但當鈦被置於高溫空氣中時,便很容易與氧產生反應[6]。
這個反應在空氣溫度達1200攝氏度時便會發生,而在純氧中最低只需610攝氏度,生成二氧化鈦[11]。因此不能在空氣中熔掉鈦,因為在到達熔點前鈦會先燃燒起來,所以只能在惰性氣體或真空中熔化鈦。在550攝氏度時,鈦會與氯氣結合[7]。鈦亦會與其他鹵素結合,並吸收氫氣[8]。
鈦也是少數會在純氮氣中燃燒的元素,達800攝氏度就會燃燒起來,生成一氮化鈦,導致脆化[20]。
實驗指出,天然鈦在受到氘核轟擊後會具有放射性,主要釋放出正電子及硬性γ射線[7]。
天然含量[编辑]
| 國家 | 千噸 | 百分比 |
|---|---|---|
| 1,513 | 13.1 | |
| 1,030 | 8.9 | |
| 3,830 | 33.1 | |
| 510 | 4.4 | |
| 562 | 4.9 | |
| 1,070 | 9.3 | |
| 502 | 4.3 | |
| 743 | 6.4 | |
| 492 | 4.3 | |
| 全球總計 | 11,563 | 100 |
自然中的鈦總是與其他元素結合成化合物。它是地殼中含量第九高的元素(質量佔地殼0.63%)[22],同時也是第七高的金屬。大部份的火成岩及由其演變成的沉積岩都含有鈦(生物及天然水體也含有鈦)[6][7]。實際上,在美國地質調查局分析過的801種火成岩中,784種含有鈦[22]鈦大約佔土壤的0.5至1.5%。[22]。
它分佈很廣,主要礦物為銳鈦礦、板鈦礦、鈦鐵礦、鈣鈦礦、金紅石、榍石及大部分鐵礦石[19]。這些礦物中,只有金紅石和鈦鐵礦具有經濟價值,但即使是這兩種礦物,它們的高濃度礦源仍是很難找。鐵鈦礦的重要礦源主要分佈於澳洲西部、加拿大、中國、印度、莫桑比克、新西蘭、挪威及烏克蘭[19]。北美洲及南非亦有大量開採金紅石,促使鈦金屬的年產量至九萬噸及二氧化鈦至四百三十萬噸[19]。據估計,鈦的貯藏量超過六億噸[19]。
鈦可以在隕石中找到,並且已在太陽及M型恆星處偵測到鈦[7];M型恆星是溫度最冷的恆星,表面溫度為3,200攝氏度[23]。在阿波羅17號任務從月球帶回的岩石中,二氧化鈦含量達12.1%[7]。鈦還可以在煤灰、植物,甚至人體中找到。[來源請求]
海中的鈦濃度大約是4x10−12M。在100°C,pH=7的水中,鈦濃度估計小於10−7M。鈦只有4+氧化態在空氣中是穩定的,但由於含鈦物種對水溶解度過低,且缺乏靈敏的光譜分析法,其在水溶液中之特性仍然未知。只有極少生物會累積高濃度的鈦,目前沒有證據顯示鈦在生物體的作用為何。[24]
同位素[编辑]
天然生的鈦有五種穩定的同位素:46Ti、47Ti、48Ti、49Ti及50Ti,其中最常見的是48Ti(天然豐度為73.8%)。現時已知鈦共有十一種放射性同位素,其中比較穩定的有44Ti(半衰期63年)、45Ti(半衰期184.8分鐘)、51Ti(半衰期5.76分鐘)及52Ti(半衰期1.7分鐘)。而剩下的其他放射性同位素,半衰期最長只有33秒,而大部份的半衰期更在半秒以下[12]。
鈦各同位素的原子重量,最輕有39.99u(40Ti),最重有57.966u(58Ti)。最常見的穩定同位素,48Ti,其主要衰變模式為電子捕獲,衰變產物為元素21(鈧)的同位素;而其次的衰變模式為β衰變,產物為元素23(釩)的同位素[12]。
鈦用氘核轟擊後會變成放射性物質,主要放射正子和短γ射線。[7]
化合物[编辑]

鈦主要以氧化數+4存在,[25]但是氧化數+3的鈦化合物也很常見。[26]通常,鈦在其錯合物中是八面體形分子構型[27][28],但是四氯化鈦為四面體結構,屬於特例。由于其高氧化态,+4價鈦化合物具有高度的共價性。[25]和大部分過渡金屬不同,簡單的+4價鈦水錯合物還未被發現。
氧化物,硫化物和醇鹽[编辑]
最重要的鈦氧化物是二氧化鈦。二氧化鈦以三種主要的晶形存在:銳鈦礦、板鈦礦、金紅石。這些都是反磁性固體,但在礦物中的外觀可能顏色較暗(請見金紅石)。銳鈦礦、金紅石的晶型結構主要由相互連接的TiO2八面體組成,TiO2八面體是以Ti為中心,周圍環繞六個氧原子。[29]
星彩藍寶石及紅寶石的星彩性來自於它們所含的二氧化鈦雜質[19]。鈦酸鹽是以二氧化鈦為原料的化合物。鈦酸鋇具有壓電性,因此可以被用於製造聲光轉換器[11]。酒精與四氯化鈦反應會生成鈦酯,可被用於製作防水纖維[11]。
目前已知有各種的鈦低氧化物,我們主要利用熱噴塗來減少所獲二氧化鈦的數目。五氧化三鈦,是一種紫色的半導體,含有+3價及+4價鈦,可在高溫下用氫氣還原二氧化鈦製得,[30]並當表面需要用二氧化鈦氣相塗覆時,在工業上使用:它像純一氧化鈦一樣會蒸發,而二氧化鈦會像鈦氧化物的混合物一般,蒸發並沉澱出具有可變折射率的塗層。[31]另外還有三氧化二鈦,為剛玉型結構,以及一氧化鈦,為岩鹽結構,不過其經常是非整比化合物。[32]
氮化物和碳化物[编辑]
氮化鈦是耐火過渡金屬氮化物的一員,且展現與其共價化合物類似的特性,包括:耐溫、超高硬度、導電導溫、高熔點。[33]
氮化鈦(TiN)具有與藍寶石及金剛砂相當的硬度(摩氏硬度9.0)[34],因此可作為各種切割工具的塗層,例如鑽頭[35]。它的其他應用還包括裝飾用金色塗料及半導體器件製造中銅導線界面的擴散阻障層[36]。
鹵化物[编辑]
四氯化鈦(氯化鈦(IV),TiCl4[37])是一種無色液體[38],也是二氧化鈦顏料製造過程的中間體[39]。作為一種路易斯酸,四氯化鈦在有機化學反應中有廣泛應用,例如向山羥醛反應[40]。在晶棒法中,四碘化钛(TiI4)用于生产高纯钛金属。[41]
鈦另有一種氧化數較低的氯化物,三氯化鈦(氯化鈦(III),TiCl3),用作合成聚烯烃的催化剂(见齐格勒-纳塔催化剂)和有机化学中的還原劑。[42][43]
有機金屬化合物[编辑]
二氯化二茂鈦是一種重要的碳-碳鍵形成催化劑。異丙醇鈦用於夏普萊斯不對稱環氧化反應。其他化合物還包括溴化鈦(用於冶金術、超合金及高溫用電線線路及塗層)和碳化鈦(用於高溫切割工具及塗層)[8]。
抗癌治療[编辑]
在含鉑藥物化療成功之後,鈦(IV)化合物是首批用於癌症治療的非鉑化合物。鈦化合物的優點在於其高效和低毒性。在生物環境中,水解產生安全且不活潑的二氧化鈦。儘管有這些優點,但第一批候選化合物未通過臨床試驗。進一步的發展導致可能具備有效性,選擇性和穩定性的含鈦藥物之產生。[44]其作用方式現在尚不清楚。
歷史[编辑]

1791年,鈦以含鈦礦物的形式在英格蘭的康沃爾郡被發現,發現者是英格蘭業餘礦物學家格雷戈爾(Reverend William Gregor),當時正業為負責康沃爾郡的克里特(Creed)教區的牧師[45]。他在鄰近的馬納坎教區中小溪旁找到了一些黑沙,後來他發現了那些沙會被磁鐵吸引[45],他意識到這種礦物(鈦鐵礦)包含着一種新的元素[8]。經過分析,發現沙裡面有兩種金屬氧化物;氧化鐵(沙受磁鐵吸引的原因)及一種他無法辨識的白色金屬氧化物(45.25%)[22]。意識到這種未被辨識的氧化物含有一種未被發現的金屬,格雷戈爾對康沃爾郡皇家地質學會及德國的《化學年刊》發表了這次的發現[45]。
大約就在同時,米勒·馮·賴興斯泰因(Franz-Joseph Müller von Reichenstein)也製造出類似的物質,但卻無法辨識它[8]。直到1795年,普魯士化學家克拉普羅特(Martin Heinrich Klaproth)獨立地從匈牙利的金紅石中再度發現到這種氧化物[45]。克拉普羅特發現到它含有一種新的物質,並以希臘神話中的泰坦(Titans)為其命名[23]。當他聽聞到格雷戈爾較早前的發現之後,克拉普羅特取得了一些馬納坎礦物的樣本,並證實它含鈦。[來源請求]
從各種含鈦礦物中提煉鈦的過程既費工又昂貴;不能像對其他金屬地用碳去還原鈦,因為鈦與碳加熱時會生成碳化鈦[45]。歷史上最早要到逾一世紀後的1910年才能製備出99.9%的純鈦,美國倫斯勒理工學院的亨特(Matthew A. Hunter)將四氯化鈦和钠一起加熱至700-800攝氏度,提煉出高純度的鈦,這種方法被稱為亨特法[7]。但是這時鈦的應用仍只限於實驗室,直到1932年克羅爾(William Justin Kroll)證明出可以利用鎂將四氯化鈦還原以提煉出鈦[46]。八年後他改良了這個過程,當中使用鎂甚至是鈉來還原鈦,後來被稱為克羅爾法[46]。儘管研究如何能更有效及便宜地提煉鈦的工作仍然持續(例如FFC劍橋法),但是鈦金屬的商業提煉還在使用克羅爾法[7][8]。

1925年,范·亞克(Anton Eduard van Arkel)及德·波耳(Jan Hendrik de Boer)發現了晶棒法(又稱碘化物精煉法),即與碘反應後再用熱燈絲從蒸氣中分離出純金屬[47],利用這個方法可生產出少量的超純鈦。
在1950年代至60年代年間,蘇聯率先將鈦用於軍事及潛艇用途(661型潛艇、705型核潛艇、M級核潛艇)[48],作為對冷戰的部份規劃[49]。自1950年代初起,鈦開始被用於各種軍事航空用途,尤其是製造高性能噴射機,最初的機體包括F-100超級軍刀及洛克希德A-12。[來源請求]
在美國,國防部意識到鈦這種金屬的戰略重要性[50],並支持了鈦早期的商業化行動[51]。在整個冷戰時期期間,鈦一直被美國政府視為戰略材料,國家防禦儲備中心內有大量海錦鈦庫存,直至2005年用盡為止[52]。現時世界最大的鈦生產商,是俄羅斯的VSMPO-Avisma,據估計這家公司的全球市場佔有率達29%[53]。
2006年美國國防部國防高等研究計劃署向兩家公司聯合撥款五百七十萬美元,研發製造鈦金屬粉末的新方法。在熱力與壓力下,這種粉末可用於製作各種強度高且重量輕的物件,從裝甲敷板到宇宙航行、運輸、化工用元件[54]。
製備[编辑]

處理鈦金屬主要分四個步驟[55]:一、把鈦礦石還原成“海綿體”(一種透氣的形態);二、製造鑄錠,熔化海綿體(或用海綿體加一種母合金)來形成鑄錠;三、初步製造,把鑄錠製成一般機械製品,如坯、棒、板、片、條及管;四、加工製造,把機械製品進一步加工成型。
由於鈦在高温時會與氧氣反應的關係,所以不能用還原反應來從氧化物中提煉鈦[14]。因此商業上提煉鈦金屬要用到克羅爾法,一種既繁複又昂貴的分批處理法。(鈦的市價相對地高,是因為在提煉的過程中,需要氧化另一種昂貴的金屬——鎂[56]。)在克羅爾法中,氧化物首先經過碳氯化,轉化成氯化物,過程中氯氣會在有碳的情況下,通過紅熱的金紅石或鈦鐵礦,生成四氯化鈦(TiCl4)。氯化物經分餾法濃縮及提純後,在800攝氏度的氬氣中被熔鎂還原成鈦[11]。
一種最近開發的提煉法,FFC劍橋法[57],日後有可能完全取代克羅爾法。此法的原料是粉末狀的二氧化鈦(一種精煉過的金紅石),而最後成品則會是鈦粉末或海綿體。假如在原料的粉末中混入粉末狀的氧化物,那麼成品就會是廉價鈦合金,這樣做比使用一般的多步熔化法要便宜得多。FFC劍橋法使鈦不像從前那樣的如此稀少和昂貴,可為航天工業及奢侈品市場提供更多的選擇,同時可取代一些製品中的鋁或特殊等級的鋼。[來源請求]
一般鈦合金是由還原反應所造出來的。例如,銅鈦合金(把加了銅的金紅石還原而成)、碳鈦鐵合金(把鈦鐵礦和焦炭用電爐還原而成)和錳鈦合金(金紅石加錳或氧化錳)都是經還原而成的[20]。
現時鈦與鈦合金共有大約50種指定品位,儘管市面上能容易買到的就只有六種[58]。美國材料試驗協會(ASTM)承認31種鈦金屬及合金品位,其中1至4號品位在商業上屬純鈦(非合金)。這四種品位以它們不同的抗拉強度區分,也就是含氧百分比,其中1號品位韌性最佳(抗拉強度低,含氧量0.18%),4號最差(抗拉強度高,含氧量0.40%)[19]。其餘品位皆為合金,每一種配方都有其特定的用途,例如韌性、強度、硬度、電阻、抗蠕變及抗腐蝕(特定某種介質或同時多種)[59]。
美國材料試驗協會所指定的品位及其他合金,亦會按照各種規格生產,例如宇宙航行及軍事規格(SAE-AMS, MIL-T)、ISO標準、各國的特定標準以及用家所需的規格(宇宙航行、軍事、醫學及工業用)[60]。
至於加工方面,鈦的所有焊接必需在氬或氦其中一種惰性氣體中進行,否則鈦會被空氣中的氧、氮或氫等氣體污染[16]。污染會引起各種情況,包括脆化,而脆化會減低焊接後的整體性,並導致連接失敗。商業純鈦的扁平產品(片、板)製造起來很容易,但處理時必須注意鈦金屬有“記憶”特性,有彈回原形的傾向。有幾種高強度合金更尤其如此[61][62]。鈦金屬一般可以用跟不鏽鋼一樣的機器及方法處理[16]。
用途[编辑]

鈦是鋼的一種合金用元素(鈦鐵),鈦會縮小鋼的晶粒尺寸,同時作為脫氧劑的鈦會減低鋼的含氧量;在不鏽鋼中加鈦會減低含碳量[6]。鈦常與其他金屬製成合金,這些金屬有鋁(改良晶粒大小)、釩、銅(硬化)、鎂及鉬等[63]。鈦的機械製品(片、板、管、線、鍛件、鑄件)在工業、宇宙航行、休閒及新興市場上都有應用。鈦粉在煙火製造上用於提供明亮的燃燒顆粒。[來源請求]
顏料、添加劑及塗料[编辑]

從地球表面被開採的鈦礦石中,約95%都被送往提煉成二氧化鈦(TiO2),俗稱鈦白(粉),一種超白的持久顏料,性質安定、無毒且覆蓋力佳,常被用於製造塗料、紙張、牙膏及塑膠[64],也是立可白的主要成分。二氧化鈦也被用於水泥、寶石、造紙用遮光劑[65]及石墨複合魚杆、高爾夫球桿的強化劑。[來源請求]
粉末狀的TiO2化學上具惰性,陽光下不褪色,而且很不透光:就是這些性質,使得它能夠為製造家用塑膠的灰色或棕色化學品帶來艷麗的純白色[8]。在自然中,二氧化鈦這種化合物可在銳鈦礦、板鈦礦及金紅石這幾種礦物中找到[6]。用二氧化鈦製成的塗料能夠耐高溫,輕度阻止塵污積聚,及抵受海洋環境帶來的影響[8]。純二氧化鈦的折射率非常高,而且對光學色散能力比鑽石還高[7]。除了作為一種很重要的顏料之外,二氧化鈦還會吸收紫外線,可用於防曬化妝品中。
奈米級二氧化鈦也會吸收紫外線,可製成光觸媒產品,有除臭、殺菌及消毒的功能。
最近,它還被用在空氣淨化器(過濾器塗層),及貼在建築物窗上的薄膜,這種薄膜在接觸到紫外線(太陽或人工)或空氣中的水份時,會產生帶高度活性的氧化還原物種,如羥基,能淨化空氣或保持窗面清潔[66]。
宇宙航行及航海[编辑]
由於它的高抗拉強度-密度比[11]、優良的抗腐蝕性[7]、抗疲乏性、抗裂痕性[67]及能夠在沒有蠕變的情況下抵受適度高溫,鈦合金被用於航空器、裝甲敷板、海軍艦隻、航天器與導彈[7][8]。在這些應用中,鈦與鋁、釩及其他元素所製成的合金,用於製造各種元件,包括關鍵的架構部件、防火牆、起落架、排氣管(直昇機)及液壓系統。事實上,約三分二的鈦金屬生產量被用於製造太空船引擎及構架[68]。SR-71“黑鳥”是最早在架構上廣泛使用鈦的機體,為現代軍用及商用機體的鈦應用鋪好了路。據估計,生產波音777要用59噸鈦,波音747要44噸,波音737要18噸,空中客車A340要32噸,空中客車A330要18噸,空中客車A320要12噸。空中巴士A380可能要用146噸,其中引擎要26噸[69]。在引擎應用上,鈦被用於轉子、壓縮機葉片、液壓系統元件及短艙。在航空應用的鈦合金中,鈦-6鋁-4釩佔幾乎50%[70]。
由於不易被海水腐蝕,鈦被用於製造螺槳軸、索具及用於海水淡化廠的換熱器[7];還被用於鹹水水族館的冷熱水器、釣魚線及潛水用刀。鈦被用於製造海洋監視部署的住房及其他元件,及用於以及科學用或軍用的監察儀。前蘇聯研發出主要用鈦製造潛艇的技術[71]。
工業[编辑]
化工及石油化工領域需要用到焊鈦製的管道及加工設備(換熱器、槽、加工用容器、閥),主要原因是鈦的抗腐蝕性。井內與鎳濕法冶金應用要用到特定的幾種合金,如鈦βC,因為需要高強度、高抗腐蝕性或兩者同時。製紙業某些會面對腐蝕性介質的生產設備會用到鈦,這些腐蝕性介質包括次氯酸鈉或濕氯氣(用於漂白)[72]。其他應用包括:超聲波焊接、熔錫波焊[73]及濺鍍靶材[74]。
四氯化鈦(TiCl4)是一種無色液體,在生產二氧化鈦的過程中的是一種重要的中間物,可用於生產齊格勒-納塔催化劑及製造鍍銥玻璃,還由於它在濕氣中會產生濃煙,所以可以用四氯化鈦來製造煙幕[14]。
消費品及建材[编辑]
鈦金屬被用於汽車,尤其是賽車(汽車或摩托),在這領域減低重量,但同時不失強度及剛度是極其重要的[75]。一般來說,鈦金屬對普通大眾的消費市場來說太昂貴了,很難會有銷路,所以它的主要市場是高檔產品,尤其是競賽用/高性能市場。最新款的Corvette跑車可選配鈦製排氣系統[76]。

鈦被用於各種體育用品:網球拍、高爾夫球杆桿頭、袋棍球棒手柄;板球、曲棍球、袋棍球及美式足球的頭盔上的護架;以及自行車的骨架及元件。儘管鈦並不是自行車生產的主流材料,但仍有運動選手及自行車冒險愛好者使用鈦製的自行車[77]。鈦合金亦被用於製造眼鏡框架[78],雖然這種鏡框會有點昂貴,但是它重量輕又很經久耐用,而且不會造成皮膚敏感。許多野外背包客都有鈦製的裝備,包括煮食用具、餐具、提燈及帳蓬的標樁[78]。雖然比傳統的鋼或鋁製的同類稍貴,這些鈦製品要輕得多但強度不減。蹄鐵匠也偏好使用鈦,因為鈦製的馬蹄鐵比鋼製的更輕且更耐用[78]。

由於它的耐久性,鈦製的名牌珠寶(尤其是鈦戒指)開始普遍起來[78]。鈦的惰性成了要選擇它的原因,特別是對有皮膚敏感或會在特定環境中(如游泳池)佩戴首飾的人。鈦的耐久性、輕重量、防凹性及耐腐蝕性,使它成為生產手錶外殼與錶帶的理想材料[78]。有些藝術家用鈦來製作藝術品,例如雕塑、裝飾品及家具[79]。
鈦偶爾會被用在有關建築的應用上:位於莫斯科高40米的加加林紀念柱,為紀念第一名太空人尤里·加加林而建造,就是以鈦建成的[80],選用鈦的原因是因為它吸引的顏色以及跟火箭技術的關連。西班牙的畢爾包古根漢美術館及美國喜瑞都的千禧圖書館分別是歐洲和北美最早使用鈦壁板護層的建築[68]。其他使用鈦壁板護層的建築還有位於美國科羅拉多州丹佛藝術博物館的漢密頓樓[81],及位於莫斯科高107米的征服太空紀念碑[82]。
比起槍支傳統上用的金屬(鋼、不鏽鋼及鋁),鈦的強度低質量較為優勝,加上在金屬製造上的發展,用鈦來製造槍支開始變得普遍。主要用途包括手槍支架及左輪手槍的轉輪。基於同樣的理由,筆記本電腦的主體也會用到鈦(例如蘋果的PowerBook系列)[83]。而2017年推出的智能手機Essential Phone將鈦合金作為手機邊框,是首部由鈦合金所組成機身的手機。[84]
有些高價位市場賣的工具,既輕量又耐腐蝕,例如鏟子及手電筒,也會用鈦合金製造。[來源請求]
珠寶[编辑]
由於其耐久性,鈦已成為更受設計師歡迎的珠寶(尤其是鈦戒指)[78]。它的低活性使其成為過敏症患者,或會在游泳池等環境中佩戴首飾的人之理想選擇。鈦與金合鑄可生產出能以24K金標示銷售的合金。此合金之硬度大約相當於14K金,且比純24K金更耐用。[85]
鈦的耐久度、較輕的重量、耐凹性以及耐蝕性使其很適合作為錶殼的材料。[78]有些藝術家會使用鈦製作雕塑、裝飾物和家具。[86]
鈦可經陽極氧化以改變表面氧化物的厚度,從而產生光學干涉條紋和各種鮮豔的顏色。[87]由於這種著色和低活性,鈦常被用作身體部位穿環。[88]
鈦在製造非流通硬幣和獎牌上用途較少。 於1999年,直布羅陀在千禧年慶典發布了世界上第一個鈦幣。[89]澳大利亞橄欖球聯盟的黃金海岸泰坦隊(Gold Coast Titans)為他們的年度最佳球員頒發了純鈦獎牌。[90]
醫學[编辑]
由於它的生物相容性(無毒及不被人體排斥),鈦在醫學上有廣泛應用,當中包括外科用具及植入物,例如替換髖骨框及球關節,最長可用20年[45]。這種用途的鈦一般與4%鋁[91]或6%鋁加4%釩製成合金。
鈦有一種固有的骨整合特性,活性生骨細胞會直接在鈦金屬表面上沉積鈣化為新生骨組織,最後會如同樹根與土壤一般結合得極為牢固,使得鈦製的牙科植入物能在原位上逗留50年之久。這種特性對整形植入物而言亦相當有用[45]。使用鈦的好處還有鈦較低的彈性模量(楊氏模量),與骨較為接近,植入物是以修補骨骼為目的而造。因此骨骼負重會更平均地分佈於骨及植入物之間,這樣會減低骨質流失的機會,因為如果負重不均就會有應力遮閉(骨骼應力因植入物而減低所導致的骨質流失),以及外科植入物與骨之間的義肢周骨折。然而,鈦合金的剛性仍是骨的兩倍,所以植入物周邊骨的受力仍是會大幅減少,並可能因此退化[92]。
由於鈦不具鐵磁性,有鈦植入物的病人能安全地接受核磁共振成像的檢查(這對有長期植入物的人士來說是很方便的)。準備植入人體的鈦要經過等離子弧的高溫加熱,移除表面原子,新露出的表面隨即被氧化[45]。
鈦被製成圖像導引手術用的外科器具,還有輪椅、丁形柺杖及其他需要高強度低重量的產品。[來源請求]
核廢料儲存[编辑]
由於其耐蝕性,鈦已被研究用以製成儲存核廢料之容器。可使用超過10萬年的容器被認為可透過最小化材料瑕疵的條件來製造。[93]鈦「滴水罩」也可以安裝在其他類型的容器上,以延長其使用壽命。[94]
生物修復[编辑]
「硬柄小皮傘」、「橙黃褐任傘」這兩種真菌可以把鈦污染泥土中之鈦金屬進行生物轉換。[95]
危害[编辑]

鈦沒有毒性,即使大劑量時也是如此,鈦在人體中不會發生任何自然作用[23]。據估計,人每天會攝取約0.8毫克鈦,但大部分都在沒有被吸收的情況下通過[23]。然而,含有矽土的組織會出現生物累積鈦的傾向。在植物中,一種未知的機制可能會用鈦來刺激碳水化合物的生產並促進生長。這可能解釋到為何大部分植物的含鈦量約為百萬分之1(ppm),而食用植物的含鈦量則約為2ppm,木賊及蕁麻更最高可達80ppm[23]。
粉末狀的鈦及刨削下來的鈦薄片很容易引起火災,而且在空氣中會因加熱而發生爆炸[96]。水及二氧化碳類的滅火法對燃燒中的鈦無效;必須改為使用D類乾粉滅火劑[8]。
當生產或處理氯氣時,必須小心注意鈦只能用在周圍沒有乾氯氣的地方,否則會引起鈦/氯火災[97]。即使是濕氯氣也是火災隱患,因為在異常的天氣狀況下濕氯氣可能會意外地變乾。
鈦未經氧化的新表面與液態氧接觸後可能會起火[98]。這種表面可以由經氧化的鈦表面跟硬物碰撞後所形成,或在力學應變導致的裂痕內形成。因此在液態氧的系統內使用鈦很可能有限制,例如宇宙航行工業就會有這種系統。[來源請求]
参考書目[编辑]
- Barksdale, Jelks. Titanium. Clifford A. Hampel (editor) (编). The Encyclopedia of the Chemical Elements. New York: Reinhold Book Corporation. 1968: 732–738. LCCN 68-29938.
- Emsley, John. Titanium. Nature's Building Blocks: An A-Z Guide to the Elements. Oxford, England, UK: Oxford University Press. 2001. ISBN 0198503407.
- Flower, Harvey M. Materials Science: A moving oxygen story. Nature. 2000, 407 (6802): 305–306. PMID 11014169. doi:10.1038/35030266.
- Greenwood, N. N.; Earnshaw, A. Chemistry of the Elements 2nd. Oxford: Butterworth-Heinemann. 1997. ISBN 0-7506-3365-4.
- Winter, Mark. Chemistry: Periodic table: Titanium. WebElements. 2006 [2006-12-10]. (原始内容存档于2008-05-16).
参考資料[编辑]
- ^ Prohaska, Thomas; Irrgeher, Johanna; Benefield, Jacqueline; Böhlke, John K.; Chesson, Lesley A.; Coplen, Tyler B.; Ding, Tiping; Dunn, Philip J. H.; Gröning, Manfred; Holden, Norman E.; Meijer, Harro A. J. Standard atomic weights of the elements 2021 (IUPAC Technical Report). Pure and Applied Chemistry. 2022-05-04. ISSN 1365-3075. doi:10.1515/pac-2019-0603 (英语).
- ^ Andersson, N.; et al. Emission spectra of TiH and TiD near 938 nm (PDF). J. Chem. Phys. 2003, 118: 10543. doi:10.1063/1.1539848. (原始内容 (PDF)存档于2012-02-09).
- ^ Weast, Robert. CRC, Handbook of Chemistry and Physics. Boca Raton, Florida: Chemical Rubber Company Publishing. 1984: E110. ISBN 0-8493-0464-4.
- ^ William L. Masterton; Cecile N. Hurley. Chemistry: Principles and Reactions 6th. Cengage Learning. 2008: 18. ISBN 0495126713.
- ^ 《無機化學》第四版。高等教育出版社.P375
- ^ 6.00 6.01 6.02 6.03 6.04 6.05 6.06 6.07 6.08 6.09 Titanium. Encyclopædia Britannica Concise. 2007.
- ^ 7.00 7.01 7.02 7.03 7.04 7.05 7.06 7.07 7.08 7.09 7.10 7.11 7.12 Lide, D. R. (编), CRC Handbook of Chemistry and Physics 86th, Boca Raton (FL): CRC Press, 2005, ISBN 0-8493-0486-5
- ^ 8.00 8.01 8.02 8.03 8.04 8.05 8.06 8.07 8.08 8.09 Krebs, Robert E. The History and Use of Our Earth's Chemical Elements: A Reference Guide (2nd edition). Westport, CT: Greenwood Press. 2006. ISBN 0313334382.
- ^ Matthew J. Donachie, Jr. TITANIUM: A Technical Guide. Metals Park, OH: ASM International. 1988: p.11. ISBN 0871703092.
- ^ 10.0 10.1 10.2 Barksdale 1968,第738頁
- ^ 11.0 11.1 11.2 11.3 11.4 11.5 11.6 Titanium. Columbia Encyclopedia 6th edition. New York: Columbia University Press. 2000–2006 [2009-06-16]. ISBN 978-0-7876-5015-5. (原始内容存档于2011-11-18).
- ^ 12.0 12.1 12.2 Barbalace, Kenneth L. Periodic Table of Elements: Ti - Titanium. 2006 [2006-12-26]. (原始内容存档于2012-07-14).
- ^ Titanium. Encyclopædia Britannica. 2006 [2006-12-29]. (原始内容存档于2008-11-18).
- ^ 14.0 14.1 14.2 14.3 Stwertka, Albert. Titanium. Guide to the Elements Revised. Oxford University Press. 1998: 81–82. ISBN 0-19-508083-1.
- ^ Matthew J. Donachie, Jr. TITANIUM: A Technical Guide. Metals Park, OH: ASM International. 1988. Appendix J, Table J.2. ISBN 0871703092.
- ^ 16.0 16.1 16.2 16.3 16.4 Barksdale 1968,第734頁
- ^ Sikka, S. K.; Vohra, Y. K., Chidambaram, R. Omega phase in materials. Progress in Materials Science. 1982, 27: 245–310. doi:10.1016/0079-6425(82)90002-0.
- ^ 18.0 18.1 Ignasi Puigdomenech, Hydra/Medusa Chemical Equilibrium Database and Plotting Software(2004)KTH Royal Institute of Technology, freely downloadable software at 存档副本. [2007-09-29]. (原始内容存档于2007-09-29).
- ^ 19.0 19.1 19.2 19.3 19.4 19.5 19.6 Emsley 2001,第453頁
- ^ 20.0 20.1 Titanium. Microsoft Encarta. 2005 [2006-12-29]. (原始内容存档于2006-10-27).
- ^ 引证错误:没有为名为
USGS的参考文献提供内容 - ^ 22.0 22.1 22.2 22.3 Barksdale 1968,第732頁
- ^ 23.0 23.1 23.2 23.3 23.4 Emsley 2001,第451頁
- ^ Buettner, K. M.; Valentine, A. M. Bioinorganic Chemistry of Titanium. Chemical Reviews. 2012, 112 (3): 1863. PMID 22074443. doi:10.1021/cr1002886.
- ^ 25.0 25.1 Greenwood 1997,第958頁
- ^ Greenwood 1997,第970頁
- ^ Greenwood & Earnshaw 1997,第960頁
- ^ Greenwood & Earnshaw 1997,第967頁
- ^ Greenwood & Earnshaw 1997,第961頁
- ^ Liu, Gang; Huang, Wan-Xia; Yi, Yong. Preparation and Optical Storage Properties of λTi3O5 Powder. Journal of Inorganic Materials. 2013-06-26, 28 (4): 425–430. doi:10.3724/SP.J.1077.2013.12309 (中文).
- ^ Bonardi, Antonio; Pühlhofer, Gerd; Hermanutz, Stephan; Santangelo, Andrea. A new solution for mirror coating in $γ$-ray Cherenkov Astronomy. Experimental Astronomy. 2014, 38 (1–2): 1–9. Bibcode:2014ExA....38....1B. arXiv:1406.0622
 . doi:10.1007/s10686-014-9398-x.
. doi:10.1007/s10686-014-9398-x.
- ^ Greenwood, Norman Neill; Earnshaw, Alan. Chemistry of the elements. 2016: 962. ISBN 978-0-7506-3365-9. OCLC 1040112384 (英语).
- ^ Saha, Naresh. Titanium nitride oxidation chemistry: An x-ray photoelectron spectroscopy study. Journal of Applied Physics. 1992, no. 7 (7): 3072–3079. Bibcode:1992JAP....72.3072S. doi:10.1063/1.351465.
- ^ Schubert, E.F. The hardness scale introduced by Friederich Mohs (PDF). [2010-12-10]. (原始内容 (PDF)存档于2010-06-03).],archive-web,
- ^ Truini, Joseph. Drill Bits. Popular Mechanics (Hearst Magazines). 1988-05, 165 (5): 91. ISSN 0032-4558.
- ^ Baliga, B. Jayant. Silicon carbide power devices. World Scientific. 2005: 91. ISBN 9812566058.
- ^ Seong, S.; et al. Titanium: industrial base, price trends, and technology initiatives. Rand Corporation. 2009: 10 [2021-12-17]. ISBN 978-0-8330-4575-1. (原始内容存档于2021-08-30).
- ^ Johnson, Richard W. The Handbook of Fluid Dynamics. Springer. 1998: 38–21. ISBN 3540646124.
- ^ Seong, S.; et al. Titanium: industrial base, price trends, and technology initiatives. Rand Corporation. 2009: 10. ISBN 083304575X.
- ^ Coates, Robert M.; Paquette, Leo A. Handbook of Reagents for Organic Synthesis. John Wiley and Sons. 2000: 93. ISBN 0470856254.
- ^ Greenwood & Earnshaw 1997,第965頁
- ^ Grimmett, M. Ross. Imidazole and benzimidazole synthesis. Academic Press. 1997: 155. ISBN 0123031907.
- ^ Gundersen, Lise-Lotte; Rise, Frode; Undheim, Kjell; Méndez Andino, José. Titanium(III) Chloride. Encyclopedia of Reagents for Organic Synthesis. 2007. ISBN 978-0471936237. doi:10.1002/047084289X.rt120.pub2.
- ^ Tshuva, Edit Y.; Miller, Maya. Chapter 8. Coordination Complexes of Titanium(IV) for Anticancer Therapy. Sigel, Astrid; Sigel, Helmut; Freisinger, Eva; Sigel, Roland K. O. (编). Metallo-Drugs: Development and Action of Anticancer Agents 18. Berlin: de Gruyter GmbH. 2018: 219–250 [2019-08-11]. ISBN 9783110470734. PMID 29394027. doi:10.1515/9783110470734-014. (原始内容存档于2021-04-24).
|journal=被忽略 (帮助) - ^ 45.0 45.1 45.2 45.3 45.4 45.5 45.6 45.7 Emsley 2001,第452頁
- ^ 46.0 46.1 Greenwood 1997,第955頁
- ^ van Arkel, A. E.; de Boer, J. H. Preparation of pure titanium, zirconium, hafnium, and thorium metal. Zeitschrift für anorganische und allgemeine Chemie. 1925, 148: 345 – 50.
- ^ Yanko, Eugene; Omsk VTTV Arms Exhibition and Military Parade JSC. Submarines: general information. 2006 [2006-12-26]. (原始内容存档于2016-03-10).
- ^ Stainless Steel World. VSMPO Stronger Than Ever (PDF). KCI Publishing B.V. July/August 2001: 16–19 [2007-01-02]. (原始内容 (PDF)存档于2006-10-05).
- ^ National Materials Advisory Board, Commission on Engineering and Technical Systems (CETS), National Research Council. Titanium: Past, Present, and Future. Washington, DC: national Academy Press. 1983: R9 [2010-12-17]. NMAB-392. (原始内容存档于2015-04-02).
- ^ Titanium Metals Corporation. Answers.com. Encyclopedia of Company Histories,. Answers Corporation. 2006 [2007-01-02]. (原始内容存档于2016-04-05).
- ^ Defense National Stockpile Center. Strategic and Critical Materials Report to the Congress. Operations under the Strategic and Critical Materials Stock Piling Act during the Period October 2004 through September 2005 (PDF). United States Department of Defense. 2006: 3304 [2010-12-17]. (原始内容 (PDF)存档于2008-12-19).
- ^ Bush, Jason. Boeing's Plan to Land Aeroflot. 商業周刊BusinessWeek]]. 2006-02-15 [2006-12-29]. (原始内容存档于2009-04-09).
- ^ DuPont. U.S. Defense Agency Awards $5.7 Million to DuPont and MER Corporation for New Titanium Metal Powder Process. 2006-12-09 [2009-08-01]. (原始内容存档于使用
|archiveurl=需要含有|archivedate=(帮助)).,archive-web, - ^ Matthew J. Donachie, Jr. TITANIUM: A Technical Guide. Metals Park, OH: ASM International. 1988. Chapter 4. ISBN 0871703092.
- ^ Barksdale 1968,第733頁
- ^ Chen, George Zheng; Fray, Derek J.; Farthing, Tom W. Direct electrochemical reduction of titanium dioxide to titanium in molten calcium chloride. Nature. 2000, 407: 361 – 64 [2009-06-19]. doi:10.1038/35030069. (原始内容存档于2008-12-10). Abstract (页面存档备份,存于互联网档案馆)
- ^ Matthew J. Donachie, Jr. TITANIUM: A Technical Guide. Metals Park, OH: ASM International. 1988: 16, Appendix J. ISBN 0871703092.
- ^ ASTM International. Annual Book of ASTM Standards (Volume 02.04: Non-ferrous Metals). West Conshohocken, PA: ASTM International. 2006. section 2. ISBN 0-8031-4086-X. ASTM International. Annual Book of ASTM Standards (Volume 13.01: Medical Devices; Emergency Medical Services). West Conshohocken, PA: ASTM International. 1998. sections 2 & 13. ISBN 0-8031-2452-X.
- ^ Matthew J. Donachie, Jr. TITANIUM: A Technical Guide. Metals Park, OH: ASM International. 1988. 13–16, Appendices H and J. ISBN 0871703092.
- ^ AWS G2.4/G2.4M:2007 Guide for the Fusion Welding of Titanium and Titanium Alloys. Miami: American Welding Society. 2006 [2010-12-18]. 原始内容存档于2013-03-29.,archive-web,
- ^ Titanium Metals Corporation. Titanium design and fabrication handbook for industrial applications. Dallas: Titanium Metals Corporation. 1997 [2010-12-18]. (原始内容存档于2009-02-09).,archive-web,
- ^ Hampel, Clifford A. The Encyclopedia of the Chemical Elements. Van Nostrand Reinhold. 1968: 738. ISBN 0442155980.
- ^ United States Geological Survey. USGS Minerals Information: Titanium. 2006-12-21 [2006-12-29]. (原始内容存档于2019-02-27).
- ^ Smook, Gary A. Handbook for Pulp & Paper Technologists (3rd edition). Angus Wilde Publications. 2002: 223. ISBN 0-9694628-5-9.
- ^ Stevens, Lisa; Lanning, John A.; Anderson, Larry G.; Jacoby, William A.; Chornet, Nicholas. Photocatalytic Oxidation of Organic Pollutants Associated with Indoor Air Quality. Air & Waste Management Association 91st Annual Meeting & Exhibition, San Diego. June 14–18, 1998.
- ^ Moiseyev, Valentin N. Titanium Alloys: Russian Aircraft and Aerospace Applications. Taylor and Francis, LLC. 2006: 196. ISBN 9780849332739.
- ^ 68.0 68.1 Emsley 2001,第454頁
- ^ Sevan, Vardan. Rosoboronexport controls titanium in Russia. Sevanco Strategic Consulting. 2006-09-23 [2006-12-26]. (原始内容存档于2023-08-27).,archive-web,
- ^ Matthew J. Donachie, Jr. TITANIUM: A Technical Guide. Metals Park, OH: ASM International. 1988: 13. ISBN 0871703092.
- ^ GlobalSecurity. GlobalSecurity.org. April 2006 [2008-04-23]. (原始内容存档于2021-08-24).
- ^ Matthew J. Donachie, Jr. TITANIUM: A Technical Guide. Metals Park, OH: ASM International. 1988. 11–16. ISBN 0871703092.
- ^ Kleefisch, E.W. (编). Industrial Application of Titanium and Zirconium. West Conshohocken, PA: ASTM International. 1981 [2010-12-22]. ISBN 0803107455. (原始内容存档于使用
|archiveurl=需要含有|archivedate=(帮助)).,archive-web, - ^ Rointan F. Bunshah, Editor. Handbook of Hard Coatings. Norwich, NY: William Andrew Inc. 2001: Ch. 8. ISBN 0815514387.
- ^ Bell, Tom; et al.. Heat Treating. Proceedings of the 20th Conference, 9–12 October 2000. ASM International. 2001: 141. ISBN 0871707276.
- ^ National Corvette Museum. Titanium Exhausts. 2006 [2006-12-26]. (原始内容存档于2013-01-03).
- ^ Davis, Joseph R. Metals Handbook. ASM International. 1998: 584. ISBN 0871706547.
- ^ 78.0 78.1 78.2 78.3 78.4 78.5 78.6 Donachie, Matthew J. Titanium: A Technical Guide. ASM International. 2000: 11, 255. ISBN 0871706865.
- ^ Fine Art and Functional Works in Titanium and Other Earth Elements. [2009-08-08]. (原始内容存档于2008-05-13).
- ^ Lütjering, Gerd; Williams, James Case. Appearance Related Applications. Titanium. 2007-06-12 [2010-12-22]. ISBN 9783540713975. (原始内容存档于2021-04-14).
- ^ Denver Art Museum, Frederic C. Hamilton Building. SPG Media. 2006 [2006-12-26]. (原始内容存档于2021-09-03).
- ^ Gruntman, Mike. Blazing the Trail: The Early History of Spacecraft and Rocketry. Reston, VA: American Institute of Aeronautics and Astronautics. AIAA: 457. ISBN 156347705X.
- ^ Apple PowerBook G4 400 (Original - Ti) Specs. [2009-08-08]. (原始内容存档于2012-04-03).
- ^ 鴻海、亞馬遜、騰訊力挺,Essential 鈦合金手機量產. [2017-08-10]. (原始内容存档于2020-11-27).
- ^ Gafner, G. The development of 990 Gold-Titanium: its Production, use and Properties (PDF). Gold Bulletin. 1989, 22 (4): 112–122. doi:10.1007/BF03214709. 原始内容存档于2010-11-29.
- ^ Fine Art and Functional Works in Titanium and Other Earth Elements. [2009-08-08]. (原始内容存档于2008-05-13).
- ^ Alwitt, Robert S. Electrochemistry Encyclopedia. 2002 [2006-12-30]. 原始内容存档于2008-07-02.
- ^ Body Piercing Safety. doctorgoodskin.com. [2009-08-01]. (原始内容存档于2021-09-02).
- ^ World Firsts | British Pobjoy Mint. www.pobjoy.com. [2017-11-11]. (原始内容存档于2021-08-20) (英语).
- ^ Turgeon, Luke. Titanium Titan: Broughton immortalised. The Gold Coast Bulletin. 2007-09-20. 原始内容存档于2013-09-28.
- ^ Orthopaedic Metal Alloys (页面存档备份,存于互联网档案馆). Totaljoints.info. Retrieved on 2010-09-27.
- ^ Titanium foams replace injured bones - Research News 09-2010-Topic 1 – Fraunhofer-Gesellschaft (页面存档备份,存于互联网档案馆). Fraunhofer.de. Retrieved on 2010-09-27.
- ^ Shoesmith, D. W.; Noel, J. J.; Hardie, D.; Ikeda, B. M. Hydrogen Absorption and the Lifetime Performance of Titanium Nuclear Waste Containers. Corrosion Reviews. 2000, 18 (4–5). doi:10.1515/CORRREV.2000.18.4-5.331.
- ^ Carter, L. J.; Pigford, T. J. Proof of Safety at Yucca Mountain. Science. 2005, 310 (5747): 447. PMID 16239463. doi:10.1126/science.1112786.
- ^ Elekes, Carmen Cristina; Busuioc, Gabriela. The Mycoremediation of Metals Polluted Soils Using Wild Growing Species of Mushrooms (PDF). Engineering Education. [2014-01-28]. (原始内容 (PDF)存档于2016-03-03).
- ^ Cotell, Catherine Mary; Sprague, J. A.; Smidt, F. A. ASM Handbook: Surface Engineering 10th. ASM International. 1994: 836. ISBN 087170384X.
- ^ Compressed Gas Association. Handbook of compressed gases 4th. Springer. 1999: 323. ISBN 0412782308.
- ^ Solomon, Robert E. Fire and Life Safety Inspection Manual. National Fire Prevention Association 8th. Jones & Bartlett Publishers. 2002: 45. ISBN 0877654727.
外部連結[编辑]
- 元素钛在洛斯阿拉莫斯国家实验室的介紹(英文)
- EnvironmentalChemistry.com —— 钛(英文)
- 元素钛在The Periodic Table of Videos(諾丁漢大學)的介紹(英文)
- 元素钛在Peter van der Krogt elements site的介紹(英文)
- WebElements.com – 钛(英文)
- “鈦:我們的下一種主要金屬”,《科技新時代》1950年8月號–最早一篇對公眾詳細報導鈦的文章(英文)
- 更乾淨更廉價地走向鈦的一條路線 (页面存档备份,存于互联网档案馆)(英文)
- 國際鈦協會 (页面存档备份,存于互联网档案馆)(英文)
- 鈦與其合金的冶金學——劍橋大學 (页面存档备份,存于互联网档案馆)(英文)
- 按國家區分的世界鈦精礦生產量 (页面存档备份,存于互联网档案馆)(英文)
- 火花中的真相:鈦還是樸實的老鋼?《科技新時代》雜誌(英文)
- archive-web,archive-is
- 神的金屬 (页面存档备份,存于互联网档案馆)(英文)
- http://baike.asianmetal.cn/metal/ti/application.shtml (页面存档备份,存于互联网档案馆)
| ||||||||||||||||||||||||||
| ||||||||||||||||||||||||
| 元素周期表 | |||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| IA 1 |
IIA 2 |
IIIB 3 |
IVB 4 |
VB 5 |
VIB 6 |
VIIB 7 |
VIIIB 8 |
VIIIB 9 |
VIIIB 10 |
IB 11 |
IIB 12 |
IIIA 13 |
IVA 14 |
VA 15 |
VIA 16 |
VIIA 17 |
VIIIA 18 | ||||||||||||||||||||
| 1 | H | He | |||||||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | |||||||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |||||
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |||||
| |||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||
| ||||||||||||



