铱
銥(拼音:yī,注音:ㄧ,粤拼:ji1;英語:Iridium),是一種化學元素,其化學符號为Ir,原子序數为77,原子量為192.217 u。銥是一種十分剛脆,銀白色的鉑系過渡金屬。銥是目前發現密度第二大的化學元素(僅次於鋨),以X射線晶體結構分析實驗測出的密度為22.56 g/cm3,在室內溫度及標準大氣壓的環境時,它以同樣的方式被計算出的密度較鋨高出了0.04g/cm3,銥是抗腐蝕性最高的金屬,甚至在攝氏2000度的高溫都還保留著抗腐蝕的特性。雖然只有某些融化的鹽類及鹵素對銥有腐蝕性,然而極細的銥粉末仍擁有較高的活性而且也是可燃的。
1803年,史密森·特南特在自然鉑礦石的不可溶雜質中發現了銥元素。由於該元素的鹽有眾多鮮豔的顏色,所以他根據希臘神話的彩虹女神伊里斯(Iris)把這新元素命名為「Iridium」。銥是地球地殼中最稀有的元素之一。其全球年產量及年消耗量只有三噸。自然存在的銥有191Ir和193Ir两种同位素,後者的丰度較高。銥的其他同位素都是不穩定同位素。
雖然銥可以形成有機金屬化合物和被拿來做為工業催化劑及研究中,最重要的銥化合物應用主要是和氯化合而成的酸類及鹽類。銥金屬會被應用是因其在高溫環境下的抗腐蝕性,像是在高效的火星塞,用作於半導體再結晶的坩堝中及氯鹼法的電極中。銥的放射性同位素則被應用於放射性同位素熱電機。
銥在隕石中的含量較地球的地殼還要來得高很多。因此,在K-T界線黏土層的高含銥量導致阿瓦雷茲推測在一次劇烈的隕石撞擊使恐龍及其他物種在六千六百萬年前滅絕。類似地,太平洋樣本中的銥的不規則也和兩百五十萬年前的Eltanin撞擊有關。
性質
[编辑]物理性質
[编辑]
銥屬於鉑系金屬,和鉑一樣呈白色,但夹杂少許黃色。銥堅硬易碎,熔點也非常高,所以很難鑄造和塑形。製造工序因此一般使用粉末冶金。[4]銥是唯一一種在1600 °C以上的空氣中仍保持優良力學性質的金屬。[5]其沸點極高,在所有元素中排第10位。銥在0.14 K以下會呈現超導體性質。[6]
銥的彈性模量仅次于鋨,為所有金屬中第二高。[5]其剪切模量很高,泊松比很低,因此具有很高的剛度,这使得銥非常难以加工生產。儘管生產不易且價格昂貴,但在現代科技所需的極端條件下,機械強度很高的銥元素仍然擁有多項應用。[5]
銥的密度在所有元素中排第二位,僅比鋨稍低(低約0.12%)。[7][8]由於两元素密度值十分相近且測量不易,所以其密度相对高低一度並沒有定論。[9]不過,X射線晶體學技術的發展使得测量密度時的準確度大大提高,最終以這種方法所得出銥和鋨的密度值分別為22.56 g/cm3和22.59 g/cm3。[10]
化學性質
[编辑]銥是抗腐蝕性最強的金屬之一:[11]它能夠在高溫下抵禦幾乎所有酸、鹼(包括濃硫酸、濃硝酸、磷酸、矽酸、鹽酸、氫氟酸、王水、逆王水、魔酸、氟銻酸、氫氧化鈉、氫氧化銫、熔融的鹼金屬),但是某些熔融鹽,如氰化鈉和氰化鉀[11]以及氧和鹵素(特別是氟)在高溫下還是可以侵蝕銥的。[12][13]
化合物
[编辑]| 氧化態[注 1] | |
|---|---|
| −3 | [Ir(CO) 3]3− |
| −1 | [Ir(CO) 3(PPh 3)]- |
| 0 | Ir 4(CO) 12 |
| +1 | [Ir(CO)Cl(PPh 3) 2] |
| +2 | IrCp 2 |
| +3 | IrCl 3 |
| +4 | IrO 2 |
| +5 | Ir 4F 20 |
| +6 | IrF 6 |
| +7 | [(η2 -O 2)IrO 2]+ |
| +8 | IrO 4 |
| +9 | [IrO 4]+ [2] |
銥的氧化態介于−3和+9间,最常見的氧化态为+3和+4。[4]高氧化態的化合物比較罕見,包括IrF
6和兩種混合氧化物Sr
2MgIrO
6及Sr
2CaIrO
6。[4][14]2009年,科學家利用基質隔離方法(在6 K的氬氣中)對過氧化銥配合物進行紫外線照射,製成了四氧化銥(IrO
4)。然而這一化合物預計在更高的溫度下無法穩定保持固體狀態。[15]铱的最高氧化态为+9,是所有已知元素中最高的,只存在于IrO+
4,它以气态形式出现,未知是否会形成任何盐。[2]
二氧化銥(IrO
2)為棕色粉末,是銥唯一一種性質已經過充分研究的氧化物。[4]三氧化二銥是一種黑藍色粉末,在硝酸中會氧化成IrO
2。[12]其他已知的化合物包括二硫化銥、二硒化銥、三硫化二銥和三硒化二銥等,另外也有研究指出IrS
3的存在。[4]銥還可以形成氧化態為+4和+5的銥酸,如K
2IrO
3和KIrO
3。在高溫下使銥與氧化鉀或超氧化鉀反應,就可取得這些銥酸盐。[16]
目前尚未發現化學式為Ir
xH
y的氫銥二元化合物,但有些已知配合物包含IrH4−
5和IrH3−
6離子,其中銥的氧化態分別為+1和+3。[17]科學家認為,Mg
6Ir
2H
11當中同時存在IrH4−
5以及含18個電子的IrH5−
4離子。[18]
銥並不形成一鹵化物和二鹵化物,而是會與每一種鹵素形成對應的三鹵化物IrX
3。[4]氧化態為+4或以上的鹵化物只有四氟化銥、五氟化銥和六氟化銥。[4]六氟化銥(IrF
6)是一種反應性很高的揮發性黃色固體,其分子結構呈八面體形。它在水中會分解,而且銥黑(即金屬銥粉末)可將其還原成晶體狀的四氟化銥(IrF
4)。[4]五氟化銥的特性相似,但它其實是一種四聚體Ir
4F
20,由四個角對角連接的八面體所形成。[4]
工業上最重要的銥化合物是六氯銥酸(H
2IrCl
6)及其銨鹽。[19]銥的純化過程、大多數銥化合物的生產初始步驟以及陽極塗層的製備過程都要用到這些化合物。IrCl2−
6離子呈棕黑色,能夠輕易還原成淺色的IrCl3−
6,且該反應可以逆轉。[19]三氯化銥(IrCl
3)常被用作其他Ir(III)化合物的製備原料。[4]氯和銥粉末在650 °C經氧化反應會形成無水三氯化銥,[19]而Ir
2O
3溶於氫氯酸中則可製成水合三氯化銥。另一種類似的製備原料是六氯銥酸銨((NH
4)
3IrCl
6)。三價銥配合物具抗磁性,分子結構一般為八面體型。[4]
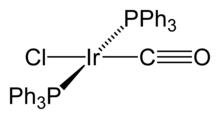
銥的有機化合物含有銥﹣碳鍵,其中銥的氧化態通常較低。比如,十二羰基四銥(Ir
4(CO)
12)是最常見兼最穩定的金屬羰基配合物,當中的銥就處於0氧化態。[4]十二羰基四銥中的每一個銥原子都與另外三個鍵合,形成四面體原子簇。一些重要的Ir(I)有機化合物都是以發現者命名的。這包括沃什卡配合物(IrCl(CO)[P(C
6H
5)
3]
2),它會與O
2分子鍵合,這種特性十分特殊。[20]克拉布特利催化劑(Crabtree's catalyst)是一種用於氫化反應的均相催化劑。[21]這些化合物都屬於平面正方形d8配合物,共有16個價電子,因此反應性很高。[22]
同位素
[编辑]銥有兩種自然穩定同位素:191Ir和193Ir,豐度分別為37.3%和62.7%。[23]已人工合成的放射性同位素共有34種,質量數從164至199不等。192Ir夾在兩個穩定同位素之間,也是最穩定的放射性同位素,半衰期為73.827天。這一同位素在近距離治療[24]和工業射線照相技術中具有用途,特別是在天然氣工業中用於無損檢測鋼鐵的焊接處。銥-192曾造成多宗輻射意外。另外有三個同位素的半衰期在一天以上:188Ir、189Ir和190Ir。[23]質量數低於191的同位素會同時進行β+衰變、α衰變以及質子發射,但有兩者除外:189Ir進行電子捕獲,而190Ir進行正電子發射。質量數高於191的同位素則進行β−衰變,其中192Ir會少量進行電子捕獲。[23]所有銥同位素都是在1934至2001年間發現的,其中最新發現的是171Ir。[25]
銥共有32種已知同核異構體,質量數介乎164到197。最穩定的同核異構體是192m2Ir,它會經同核異能躍遷,半衰期為241年,[23]因此比所有處於基態的放射性同位素都要穩定。最不穩定的異構體是190m3Ir,其半衰期只有2微秒。[23]191Ir是所有元素中首個被證實呈現穆斯堡爾效應的同位素。該同位素應用在穆斯堡爾光譜分析中,在物理學、化學、生物化學、冶金學和礦物學等領域都有用到。[26]
歷史
[编辑]
銥的發現與鉑以及其他鉑系元素息息相關。古埃塞俄比亞人[27]和南美洲各文化的人[28]自古便有使用自然產生的鉑金屬,當中必定含有少量其他鉑系元素,這也包括銥。17世紀西班牙征服者在今天的哥倫比亞喬科省發現了鉑,並將其帶到歐洲。[29]然而直到1748年,科學家才發現它並不是任何已知金屬的合金,而是一種全新的元素。[30]
當時研究鉑的化學家將它置於王水 (氫氯酸和硝酸的混合物)當中,從而產生可溶鹽。製成的溶液每次都留下少量深色的不可溶殘留物。[5]約瑟夫·普魯斯特曾以為這一殘留物是石墨。[5]法國化學家維多·科萊-德科提爾(Victor Collet-Descotils)、福爾克拉伯爵安東萬·弗朗索瓦(Antoine François, comte de Fourcroy)和路易·尼古拉·沃克朗(Louis Nicolas Vauquelin)在1803年也同樣觀察到了這一黑色殘留物,但因量太少而沒有進行進一步實驗。[5]
1803年,英國化學家史密森·特南特分析了殘留物,並推斷其中必含新的金屬元素。沃克朗把該粉末來回在酸鹼中浸洗,[11]取得了一種揮發性氧化物。他認為這是新元素的氧化物,並把新元素命名為「ptene」,源於希臘文的「πτηνος」(ptènos),即「有翼的」。[31][32]特南特則擁有更大量的殘留物,並在不久後辨認出兩種新元素,也就是鋨和銥。[5][11]在一連串用到氫氧化鈉和氫氯酸的反應之後,他製成了一種深紅色晶體(很可能是Na
2[IrCl
6]·nH
2O)。[32]銥的許多鹽都有鮮豔的顏色,所以特南特取希臘神話中的彩虹女神伊里斯(Ἶρις,Iris)之名,把銥命名為「Iridium」。[33]元素的發現被記錄在1804年6月21日致英國皇家學會的一封信中。[5][34]
1813年,英國化學家約翰·喬治·求爾德倫(John George Children)首次熔化銥金屬。[5]1842年,羅伯特·海爾(Robert Hare)首次取得高純度銥金屬。他量得的銥密度為21.8 g/cm3,並發現這一金屬幾乎不可延展,且硬度極高。1860年,亨利·愛丁·聖克萊爾·德維爾和朱爾·亨利·德布雷(Jules Henri Debray)第一次大量熔化銥。每公斤銥的熔化過程需要燃燒超過300升的純O
2和H
2。[5]
銥如此難熔化塑性,這大大限制了它的實際應用。約翰·艾薩克·霍金斯(John Isaac Hawkins)在1834年發明了裝有銥造筆尖的金質鋼筆。1880年,約翰·霍蘭德(John Holland)和威廉·洛弗蘭德·達德利(William Lofland Dudley)利用磷大大簡化了銥的熔化過程,並在美國申請了專利。英國莊信萬豐公司之後表示,他們早在1837年就開始使用類似的方法熔解銥,而且已在多個世界博覽會展出經熔融製成的銥。[5]奧托·佛斯納(Otto Feussner)在1993年第一次在熱電偶中使用銥﹣釕合金材料,使這種新型器材能夠測量高達2000 °C的溫度。[5]
1957年,魯道夫·穆斯堡爾在只含191Ir的固體金屬樣本中,發現原子能夠進行無反衝的γ射線共振發射及吸收。[35]他所進行的實驗是20世紀標誌性的物理實驗之一。[36]此現象稱為穆斯堡爾效應(其他呈現該效應的原子核也陸續被發現,如57Fe),是穆斯堡爾譜學的中心原理,在物理學、化學、生物化學、冶金學和礦物學中都有重要的應用。[26]論文發佈的僅僅3年之後,即1961年,穆斯堡爾就因這一發現獲得了諾貝爾物理學獎,時年32歲。[37]
存量
[编辑]

銥是地球地殼中最稀有的元素之一,平均質量比例只有百萬分之0.001。金的豐度是它的40倍,鉑是它的10倍,而銀和汞都是它的80倍。[4]碲的豐度與銥相近,另外只有三種穩定元素比銥更加稀有:錸、釕和銠,其中後兩者的豐度是銥的十分之一。[4]相比之下,銥在隕石裡的含量則高很多,一般在百萬分之0.5以上。[39]科學家相信,銥在整個地球的含量比在地殼中的含量高很多,但由於它密度高,而且具親鐵性,所以在地球仍處於熔融狀態時,就已沉到地球的內核了。[19]
銥在自然中以純金屬或合金的形態出現,尤其是各種比例的銥﹣鋨合金。[11]鎳和銅礦藏中含有鉑系金屬的硫化物(如(Pt,Pd)S)、碲化物(如PtBiTe)、銻化物(PdSb)和砷化物(如PtAs
2)。這些化合物中的鉑會被少量的銥和鋨元素取代。與其他鉑系元素一樣,銥可以形成自然鎳合金及銅合金。[40]
地殼中有三種地質結構的銥含量最高:火成岩、撞擊坑以及前二者演化而成的地質結構。最大的已知礦藏有南非的布殊維爾德火成雜岩體、[41]俄羅斯的諾里爾斯克及加拿大的索德柏立盆地等。美國有較小的銥礦藏。[41]銥也出現在次生礦藏中,與沖積層礦藏中的鉑以及其他鉑系元素結合。前哥倫布時期哥倫比亞喬科省居民所用的沖積層礦藏至今仍是鉑系元素的一大來源。截至2003年,並沒有數據記錄全球銥儲藏量。[11]
白堊紀﹣第三紀界線
[编辑]
6600萬年前形成的K-T界線記錄了從白堊紀到古近紀的轉捩點,此地層的黏土的銥含量異常高。[42]路易斯·阿爾瓦雷茨為首的研究團隊在1980年提出假說,指這一地層中的銥是小行星或彗星撞擊地球時帶來的。[42]這一理論稱為阿爾瓦雷茨假說,目前被公認為恐龍滅絕的最佳解釋。後來人們在中美洲尤卡坦半島地底發現了約6600萬年前形成的大型撞擊坑,即希克蘇魯伯隕石坑,這很可能就是阿爾瓦雷茨假說中那顆隕石的撞擊地點。[43][44]杜威·麥克林(Dewey M. McLean)等人則認為是火山活動把銥帶到地球表面的,因為地球深處存在更多的銥元素,而且許多火山至今仍在放出銥,如留尼旺島上的富爾奈斯火山。[45][46]
生產
[编辑]| 年份 | 消耗量(噸) | 價格(美元/金衡盎司)[47] |
|---|---|---|
| 2001 | 2.6 | 415.25 |
| 2002 | 2.5 | 294.62 |
| 2003 | 3.3 | 93.02 |
| 2004 | 3.60 | 185.33 |
| 2005 | 3.86 | 169.51 |
| 2006 | 4.08 | 349.45 |
| 2007 | 3.70 | 444.43 |
| 2008 | 3.10 | 448.34 |
| 2009 | 2.52 | 420.4 |
| 2010 | 10.40 | 642.15 |
銥是鎳和銅開採和提煉過程的副產品。在鎳和銅的電解精煉過程中,金、銀等貴金屬、鉑系元素以及硒和碲等非金屬元素都會積聚在正電極上。[47]這一泥狀物質要進入溶液才可把其中的金屬分離出來。具體方法取決於混合物的成份,但主要有兩種:加入過氧化鈉後溶於王水,或直接溶於氯和氫氯酸的混合溶液。[19][41]
要在溶解狀態下從其他鉑系金屬中分離出銥,需使(NH
4)
2IrCl
6沉澱,或用有機胺把IrCl2−
6萃取出來。[48]第一種分離方法類似於特南特所用的方法。第二種方法可以作為持續的溶劑提取過程,所以更適合工業規模的生產。兩種方法的產物都可用氫進行還原反應,產生粉末或海綿狀的銥金屬,再用粉末冶金技術來加工。[49][50]
過去數十年間的銥價格波動頗大。相對其他工業用金屬(如鋁和銅)來說,銥的全球市場量很小,所以價格很容易受產量、需求量、投機、囤積和產國政治等多方面變化的影響。由於屬性特殊,所以銥的價格會隨當今科技的變化而波動:用來製造大型單個晶體的銥製坩堝滯銷,導致銥價格在2001至2003年間下降。[47][51]2010至2014年,多個生產單個藍寶石晶體的工廠建立,促使銥價升至超過每盎司1000美元。這些藍寶石被用於電視LED背光燈中。[52]
應用
[编辑]銥的需求量從2009年的2.5噸升至2010年的10.4噸。這主要是因為電子相關應用的需求量從0.2噸升至6噸:銥製坩堝被廣泛用於大型高質量單個晶體的生產,而這些晶體的需求在這段時間大大提高。銥的消耗量預期將因為積累的坩堝庫存而飽和,這在2000年代也曾經發生過。其他重要應用還包括火花塞(2007年消耗0.78噸)、氯鹼法所用的電極(同年消耗1.1噸)以及化學催化劑(同年消耗0.75噸)。[47][53]
工業及醫學
[编辑]
3的分子結構
銥的應用大部份運用其高熔點、高硬度和抗腐蝕性質。銥金屬以及銥﹣鉑合金和鋨﹣銥合金的耗損很低,可用來製造多孔噴絲板。噴絲板用於把塑料聚合物擠壓成纖維,例如人造絲。[54]鋨﹣銥合金也可以用於指南針軸承和計重秤。[11]
銥的耐腐蝕、耐高溫性質很強,所以非常適合作為合金添加物。飛機引擎中的一些長期使用部件是由銥合金組成的,銥﹣鈦合金也被用作水底管道材料。[11]加入銥可提升鉑合金的硬度。純鉑的維氏硬度為56 HV,而含50%銥的鉑合金硬度可超過500 HV。[55][56]
銥也常被用於須承受高溫的儀器當中。比如,柴可拉斯基法使用銥製高溫坩堝,產生單個氧化物晶體,如藍寶石、釓鎵石榴石和釔鋁石榴石等。這些晶體被用於電腦記憶體和固態激光器零件當中。[57][58][5]銥合金能夠抵禦電弧侵蝕,所以是火花塞電觸頭的理想材料。[58][59]
Cativa催化法是把甲醇轉變為乙酸的過程,可使用銥化合物作為催化劑。[60]
放射性同位素銥-192在γ射線照相中是一種重要的能源,有助對金屬進行無損檢測。[61][62]另外,近距離治療利用192Ir所釋放的γ射線來治療癌症。這種治療方法把輻射源置於癌組織附近或裡面,可用於治療前列腺癌、膽管癌及子宮頸癌等。[11]
科學
[编辑]
1889年製成的國際米原器和國際公斤原器是由含90%鉑和10%銥的合金組成的,原器由位於巴黎附近的國際度量衡局保存。[11]米的定義在1960年改為氪的發射光譜中的一條譜線,[注 2][63],千克的定義在2019年5月20日修改後,千克原器已不再使用。[64]
航海家號、維京號、先鋒號和卡西尼-惠更斯號、伽利略號和新視野號等無人宇宙飛船都有使用含有銥的放射性同位素熱電機。由於熱電機要承受高達2000 °C的高溫,所以包裹著鈈-238同位素的容器是以既堅硬又耐高溫的銥所製。[5]
銥還被用於X射線望遠鏡中。[65]錢德拉X射線天文台的反射鏡上有一層60納米厚的銥塗層。在測試過多種金屬之後,銥的X射線反射能力證明比鎳、金和鉑都要優勝。這層銥的平滑程度要有幾個原子以內的準確度,須在氣態下在高真空環境中塗在鉻底層上。[66]
粒子物理學在反質子的產生過程中也用到銥。過程中,高強度質子束射向密度必須很高的「轉換目標體」。雖然可以使用鎢,但銥的優勝之處在於,它可以更穩定地承受入射粒子束使溫度升高時所造成的衝擊波。[67]

碳-氫鍵活化反應(C–H活化)是斷開碳-氫鍵的反應。這種鍵在以前曾被認為具有低反應性。科學家在1982年宣佈首次成功活化飽和烴中的C–H鍵,反應使用銥的有機配合物,使烴進行氧化加成。[68][69]
銥配合物可以用來催化不對稱氫化反應。這類催化劑已被用於合成天然產物,並能夠把本來難以氫化的基底(例如非官能團化烯烴等)氫化成其中一種對映異構體 。[70][71]
銥可以形成多種配合物,在有機發光二極體(OLED)當中起到作用。[72][73][74]
已淘汰的用途
[编辑]
銥﹣鋨合金曾被加入到鋼筆筆尖中。1834年開始,一些鋼筆生產商開始把銥安裝在金筆尖上,這是銥的首個主要應用。[5]自1944年起,著名的派克51鋼筆就有含釕﹣銥合金的筆尖,合金中的銥含量為3.8%。今天的鋼筆筆尖幾乎不再含有銥,而是含其他的金屬,例如鎢。[75]
銥﹣鉑合金曾經用於加農炮的點火孔和排氣孔。根據1867年巴黎世界博覽會的一份報告,莊信萬豐所展出的一份展品「曾在一把魏渥斯步槍中經歷超過3000發,仍無損無耗。所有知道火炮排氣孔損耗所導致的麻煩和花費的人,都會非常欣賞這一重要的應用」。[76]
「銥黑」是一種含有非常細緻銥粉末的染料,可以把瓷器染成很深的黑色。有19世紀的文獻稱「所有其他的黑色瓷器染料與它一比較,都變成了灰色」。[77]
安全
[编辑]成塊的銥金屬沒有生物用途亦無害,因為它不與生物組織反應。人體組織內的銥比例只有一兆(萬億)分之二十左右。[11]和大部份金屬一樣,銥的金屬細粉具有危險性。這樣的粉末會刺激組織,且容易在空氣中燃燒。[41]由於銥化合物的處理量一般都很低,所以人們對其毒性所知甚少。大部份銥化合物都不可溶,所以很難被人體吸收;[11]不過銥的可溶鹽,如各種鹵化銥,則具有毒性。[24]
192
Ir同位素和其他放射性同位素一樣是危險的。唯一的相關意外是在近距離治療時受該同位素輻射的意外照射。[24]192
Ir所放出的高能伽馬射線會提高患癌症的可能性。外照射可導致燒傷、輻射中毒甚至死亡。攝入192Ir可導致腸胃內膜燒傷。[78]進入體內的192Ir、192mIr和194mIr主要會積累在肝臟中,所放出的伽馬射線和β輻射會對身體造成損害。[39]
備註
[编辑]參考資料
[编辑]- ^ Prohaska, Thomas; Irrgeher, Johanna; Benefield, Jacqueline; Böhlke, John K.; Chesson, Lesley A.; Coplen, Tyler B.; Ding, Tiping; Dunn, Philip J. H.; Gröning, Manfred; Holden, Norman E.; Meijer, Harro A. J. Standard atomic weights of the elements 2021 (IUPAC Technical Report). Pure and Applied Chemistry. 2022-05-04. ISSN 1365-3075. doi:10.1515/pac-2019-0603 (英语).
- ^ 2.0 2.1 2.2 Wang, Guanjun; Zhou, Mingfei; Goettel, James T.; Schrobilgen, Gary G.; Su, Jing; Li, Jun; Schlöder, Tobias; Riedel, Sebastian. Identification of an iridium-containing compound with a formal oxidation state of IX. Nature. 2014, 514: 475–477. Bibcode:2014Natur.514..475W. PMID 25341786. doi:10.1038/nature13795.
- ^ Magnetic susceptibility of the elements and inorganic compounds 互联网档案馆的存檔,存档日期2012-01-12., in Lide, D. R. (编), CRC Handbook of Chemistry and Physics 86th, Boca Raton (FL): CRC Press, 2005, ISBN 0-8493-0486-5(英文)
- ^ 4.00 4.01 4.02 4.03 4.04 4.05 4.06 4.07 4.08 4.09 4.10 4.11 4.12 4.13 Greenwood, N. N.; Earnshaw, A. Chemistry of the Elements 2nd. Oxford: Butterworth–Heinemann. 1997: 1113–1143, 1294. ISBN 0-7506-3365-4. OCLC 48138330 (英语).
- ^ 5.00 5.01 5.02 5.03 5.04 5.05 5.06 5.07 5.08 5.09 5.10 5.11 5.12 5.13 5.14 Hunt, L. B. A History of Iridium (PDF). Platinum Metals Review. 1987, 31 (1): 32–41. (原始内容存档 (PDF)于2012-03-04) (英语).
- ^ Kittel, C. Introduction to Solid state Physics, 7th Edition. Wiley-India. 2004. ISBN 81-265-1045-5 (英语).
- ^ Arblaster, J. W. Osmium, the Densest Metal Known. Platinum Metals Review. 1995, 39 (4): 164 [2014-02-01]. (原始内容存档于2011-09-27) (英语).
- ^ Cotton, Simon. Chemistry of Precious Metals. Springer-Verlag New York, LLC. 1997: 78. ISBN 978-0-7514-0413-5 (英语).
- ^ Lide, D. R. CRC Handbook of Chemistry and Physics (70th Edn.). Boca Raton (FL):CRC Press. 1990 (英语).
- ^ Arblaster, J. W. Densities of osmium and iridium: recalculations based upon a review of the latest crystallographic data (PDF). Platinum Metals Review. 1989, 33 (1): 14–16 [2011-03-28]. (原始内容 (PDF)存档于2012-02-07) (英语).
- ^ 11.00 11.01 11.02 11.03 11.04 11.05 11.06 11.07 11.08 11.09 11.10 11.11 Emsley, J. Iridium. Nature's Building Blocks: An A–Z Guide to the Elements. Oxford, England, UK: Oxford University Press. 2003: 201–204. ISBN 0-19-850340-7 (英语).
- ^ 12.0 12.1 Perry, D. L. Handbook of Inorganic Compounds. CRC Press. 1995: 203–204. ISBN 1439814619 (英语).
- ^ Lagowski, J. J. (编). Chemistry Foundations and Applications 2. Thomson Gale. 2004: 250–251. ISBN 0028657233 (英语).
- ^ Jung, D.; Demazeau, Gérard. High Oxygen Pressure and the Preparation of New Iridium (VI) Oxides with Perovskite Structure: Sr
2MIrO
6 (M = Ca, Mg). Journal of Solid State Chemistry. 1995, 115 (2): 447–455. Bibcode:1995JSSCh.115..447J. doi:10.1006/jssc.1995.1158 (英语). - ^ Gong, Y.; Zhou, M.; Kaupp, M.; Riedel, S. Formation and Characterization of the Iridium Tetroxide Molecule with Iridium in the Oxidation State +VIII. Angewandte Chemie International Edition. 2009, 48 (42): 7879–7883. doi:10.1002/anie.200902733 (英语).
- ^ Gulliver, D. J; Levason, W. The chemistry of ruthenium, osmium, rhodium, iridium, palladium and platinum in the higher oxidation states. Coordination Chemistry Reviews. 1982, 46: 1–127. doi:10.1016/0010-8545(82)85001-7 (英语).
- ^ Holleman, A. F.; Wiberg, E.; Wiberg, N. Inorganic Chemistry, 1st Edition. Academic Press. 2001. ISBN 0-12-352651-5. OCLC 47901436 (英语).
- ^ Černý, R.; Joubert, J.-M.; Kohlmann, H.; Yvon, K. Mg
6Ir
2H
11, a new metal hydride containing saddle-like IrH5−
4 and square-pyramidal IrH4−
5 hydrido complexes. Journal of Alloys and Compounds. 2002, 340 (1–2): 180–188. doi:10.1016/S0925-8388(02)00050-6 (英语). - ^ 19.0 19.1 19.2 19.3 19.4 Renner, H.; Schlamp, G.; Kleinwächter, I.; Drost, E.; Lüschow, H. M.; Tews, P.; Panster, P.; Diehl, M.; Lang, J.; Kreuzer, T.; Knödler, A.; Starz, K. A.; Dermann, K.; Rothaut, J.; Drieselman, R. Platinum group metals and compounds. Ullmann's Encyclopedia of Industrial Chemistry. Wiley. 2002. doi:10.1002/14356007.a21_075 (英语).
- ^ Vaska, L.; DiLuzio, J.W. Carbonyl and Hydrido-Carbonyl Complexes of Iridium by Reaction with Alcohols. Hydrido Complexes by Reaction with Acid. Journal of the American Chemical Society. 1961, 83 (12): 2784–2785. doi:10.1021/ja01473a054 (英语).
- ^ Crabtree, R. H. Iridium compounds in catalysis. Accounts of Chemical Research. 1979, 12 (9): 331–337. doi:10.1021/ar50141a005 (英语).
- ^ Crabtree, R. H. The Organometallic Chemistry of the Transition Metals (PDF). Wiley. 2005. ISBN 0471662569. OCLC 224478241. (原始内容 (PDF)存档于2012-11-19) (英语).
- ^ 23.0 23.1 23.2 23.3 23.4 Audi, G.; Bersillon, O.; Blachot, J.; Wapstra, A.H. The NUBASE Evaluation of Nuclear and Decay Properties. Nuclear Physics A (Atomic Mass Data Center). 2003, 729: 3–128. Bibcode:2003NuPhA.729....3A. doi:10.1016/j.nuclphysa.2003.11.001 (英语).
- ^ 24.0 24.1 24.2 Mager Stellman, J. Iridium. Encyclopaedia of Occupational Health and Safety. International Labour Organization. 1998: 63.19. ISBN 978-92-2-109816-4. OCLC 35279504 (英语).
- ^ Arblaster, J. W. The discoverers of the iridium isotopes: the thirty-six known iridium isotopes found between 1934 and 2001. Platinum Metals Review. 2003, 47 (4): 167–174 [2014-02-01]. (原始内容存档于2009-01-06) (英语).
- ^ 26.0 26.1 Chereminisoff, N. P. Handbook of Ceramics and Composites. CRC Press. 1990: 424. ISBN 0-8247-8006-X (英语).
- ^ Ogden, J. M. The So-Called 'Platinum' Inclusions in Egyptian Goldwork. The Journal of Egyptian Archaeology. 1976, 62: 138–144. JSTOR 3856354. doi:10.2307/3856354 (英语).
- ^ Chaston, J. C. The Powder Metallurgy of Platinum. Platinum Metals Rev. 1980, 24 (21): 70–79 (英语).
- ^ McDonald, M. The Platinum of New Granada: Mining and Metallurgy in the Spanish Colonial Empire. Platinum Metals Review. 959, 3 (4): 140–145 [2014-02-01]. (原始内容存档于2011-06-09) (英语).
- ^ Juan, J.; de Ulloa, A. Relación histórica del viage a la América Meridional 1. 1748: 606 (西班牙语).
- ^ Thomson, T. A System of Chemistry of Inorganic Bodies. Baldwin & Cradock, London; and William Blackwood, Edinburgh. 1831: 693.
- ^ 32.0 32.1 Griffith, W. P. Bicentenary of Four Platinum Group Metals. Part II: Osmium and iridium – events surrounding their discoveries. Platinum Metals Review. 2004, 48 (4): 182–189. doi:10.1595/147106704X4844 (英语).
- ^ Weeks, M. E. Discovery of the Elements 7. Journal of Chemical Education. 1968: 414–418. ISBN 0-8486-8579-2. OCLC 23991202 (英语).
- ^ Tennant, S. On Two Metals, Found in the Black Powder Remaining after the Solution of Platina. Philosophical Transactions of the Royal Society of London. 1804, 94: 411–418. JSTOR 107152. doi:10.1098/rstl.1804.0018 (英语).
- ^ Mössbauer, R. L. Gammastrahlung in Ir191. Zeitschrift für Physik A. 1958, 151 (2): 124–143. Bibcode:1958ZPhy..151..124M. doi:10.1007/BF01344210 (德语).
- ^ Trigg, G. L. Landmark Experiments in Twentieth Century Physics. Courier Dover Publications. 1995: 179–190. ISBN 0-486-28526-X. OCLC 31409781 (英语).
- ^ Waller, I. The Nobel Prize in Physics 1961: presentation speech. Nobel Lectures, Physics 1942–1962. Elsevier. 1964. (原始内容存档于2008-10-13) (英语).
- ^ Scott, E. R. D.; Wasson, J. T.; Buchwald, V. F. The chemical classification of iron meteorites—VII. A reinvestigation of irons with Ge concentrations between 25 and 80 ppm. Geochimica et Cosmochimica Acta. 1973, 37 (8): 1957–1983. Bibcode:1973GeCoA..37.1957S. doi:10.1016/0016-7037(73)90151-8 (英语).
- ^ 39.0 39.1 Iridium (PDF). Human Health Fact Sheet. Argonne National Laboratory. 2005 [2014-04-15]. (原始内容存档 (PDF)于2014-02-01) (英语).
- ^ Xiao, Z.; Laplante, A. R. Characterizing and recovering the platinum group minerals—a review. Minerals Engineering. 2004, 17 (9–10): 961–979. doi:10.1016/j.mineng.2004.04.001 (英语).
- ^ 41.0 41.1 41.2 41.3 Seymour, R. J.; O'Farrelly, J. I. Platinum-group metals. Kirk Othmer Encyclopedia of Chemical Technology. Wiley. 2001. doi:10.1002/0471238961.1612012019052513.a01.pub2 (英语).
- ^ 42.0 42.1 Alvarez, L. W.; Alvarez, W.; Asaro, F.; Michel, H. V. Extraterrestrial cause for the Cretaceous–Tertiary extinction. Science. 1980, 208 (4448): 1095–1108. Bibcode:1980Sci...208.1095A. PMID 17783054. doi:10.1126/science.208.4448.1095 (英语).
- ^ Hildebrand, A. R.; Penfield, Glen T.; Kring, David A.; Pilkington, Mark; Zanoguera, Antonio Camargo; Jacobsen, Stein B.; Boynton, William V. Chicxulub Crater; a possible Cretaceous/Tertiary boundary impact crater on the Yucatan Peninsula, Mexico. Geology. 1991, 19 (9): 867–871. Bibcode:1991Geo....19..867H. doi:10.1130/0091-7613(1991)019<0867:CCAPCT>2.3.CO;2 (英语).
- ^ Frankel, C. The End of the Dinosaurs: Chicxulub Crater and Mass Extinctions. Cambridge University Press. 1999. ISBN 0-521-47447-7. OCLC 40298401 (英语).
- ^ Ryder, G.; Fastovsky, D. E.; Gartner, S. The Cretaceous-Tertiary Event and Other Catastrophes in Earth History. Geological Society of America. 1996: 47. ISBN 0-8137-2307-8 (英语).
- ^ Toutain, J.-P.; Meyer, G. Iridium-Bearing Sublimates at a Hot-Spot Volcano (Piton De La Fournaise, Indian Ocean). Geophysical Research Letters. 1989, 16 (12): 1391–1394. Bibcode:1989GeoRL..16.1391T. doi:10.1029/GL016i012p01391 (英语).
- ^ 47.0 47.1 47.2 47.3 Platinum-Group Metals 互联网档案馆的存檔,存档日期2016-02-16.. U.S. Geological Survey Mineral Commodity Summaries(英文)
- ^ Gilchrist, Raleigh. The Platinum Metals. Chemical Reviews. 1943, 32 (3): 277–372. doi:10.1021/cr60103a002 (英语).
- ^ Ohriner, E. K. Processing of Iridium and Iridium Alloys. Platinum Metals Review. 2008, 52 (3): 186–197. doi:10.1595/147106708X333827 (英语).
- ^ Hunt, L. B.; Lever, F. M. Platinum Metals: A Survey of Productive Resources to industrial Uses (PDF). Platinum Metals Review. 1969, 13 (4): 126–138 [2014-02-01]. (原始内容 (PDF)存档于2008-10-29) (英语).
- ^ Hagelüken, C. Markets for the catalysts metals platinum, palladium, and rhodium (PDF). Metall. 2006, 60 (1–2): 31–42. (原始内容 (PDF)存档于2009-03-04) (英语).
- ^ Platinum 2013 Interim Review (PDF). Johnson Matthey. Johnson Matthey Plc. [2014-01-10]. (原始内容存档 (PDF)于2014-01-10) (英语).
- ^ Jollie, D. Platinum 2008 (PDF). Johnson Matthey. 2008 [2008-10-13]. ISSN 0268-7305. (原始内容 (PDF)存档于2008-10-29) (英语).
- ^ Egorova, R. V.; Korotkov, B. V.; Yaroshchuk, E. G.; Mirkus, K. A.; Dorofeev N. A.; Serkov, A. T. Spinnerets for viscose rayon cord yarn. Fibre Chemistry. 1979, 10 (4): 377–378. doi:10.1007/BF00543390 (英语).
- ^ Darling, A. S. Iridium Platinum Alloys (PDF). Platinum Metals Review. 1960, 4 (l): 18–26 [2008-10-13]. (原始内容 (PDF)存档于2008-10-29) (英语).
- ^ Biggs, T.; Taylor, S. S.; van der Lingen, E. The Hardening of Platinum Alloys for Potential Jewellery Application. Platinum Metals Review. 2005, 49 (1): 2–15. doi:10.1595/147106705X24409 (英语).
- ^ Crookes, W. On the Use of Iridium Crucibles in Chemical Operations. Proceedings of the Royal Society of London. Series A, Containing Papers of a Mathematical and Physical Character. 1908, 80 (541): 535–536. Bibcode:1908RSPSA..80..535C. JSTOR 93031. doi:10.1098/rspa.1908.0046 (英语).
- ^ 58.0 58.1 Handley, J. R. Increasing Applications for Iridium (PDF). Platinum Metals Review. 1986, 30 (1): 12–13 [2014-02-01]. (原始内容 (PDF)存档于2012-04-02) (英语).
- ^ Stallforth, H.; Revell, P. A. Euromat 99. Wiley-VCH. 2000. ISBN 978-3-527-30124-9 (英语).
- ^ Cheung, H.; Tanke, R. S.; Torrence, G. P. Acetic acid. Ullmann's Encyclopedia of Industrial Chemistry. Wiley. 2000. doi:10.1002/14356007.a01_045 (英语).
- ^ Halmshaw, R. The use and scope of Iridium 192 for the radiography of steel. British Journal of Applied Physics. 1954, 5 (7): 238–243. Bibcode:1954BJAP....5..238H. doi:10.1088/0508-3443/5/7/302 (英语).
- ^ Hellier, Chuck. Handbook of Nondestructive Evlaluation. The McGraw-Hill Companies. 2001. ISBN 978-0-07-028121-9 (英语).
- ^ Penzes, W. B. Time Line for the Definition of the Meter. National Institute for Standards and Technology. 2001 [2008-09-16]. (原始内容存档于2008-09-16) (英语).
- ^ General section citations: Recalibration of the U.S. National Prototype Kilogram, R. S. Davis, Journal of Research of the National Bureau of Standards, 90, No. 4, July–August 1985 (5.5 MB PDF, here 互联网档案馆的存檔,存档日期2011-06-03.); and The Kilogram and Measurements of Mass and Force, Z. J. Jabbour et al., J. Res. Natl. Inst. Stand. Technol. 106, 2001, 25–46 (3.5 MB PDF, here 互联网档案馆的存檔,存档日期2011-06-04.) (英文)
- ^ Ziegler,, E.; Hignette, O.; Morawe, Ch.; Tucoulou, R. High-efficiency tunable X-ray focusing optics using mirrors and laterally-graded multilayers. Nuclear Instruments and Methods in Physics Research Section A: Accelerators, Spectrometers, Detectors and Associated Equipment. 2001,. 467–468: 954–957. Bibcode:2001NIMPA.467..954Z. doi:10.1016/S0168-9002(01)00533-2 (英语).
- ^ Face-to-Face with Jerry Johnston, CXC Program Manager & Bob Hahn, Chief Engineer at Optical Coating Laboratories, Inc., Santa Rosa, CA. Harvard-Smithsonian Center for Astrophysics; Chandra X-ray Center. 1995 [2008-09-24]. (原始内容存档于2008-07-05) (英语).
- ^ Möhl, D. Production of low-energy antiprotons. Zeitschrift Hyperfine Interactions. 1997, 109: 33–41. Bibcode:1997HyInt.109...33M. doi:10.1023/A:1012680728257 (英语).
- ^ 68.0 68.1 Janowicz, A. H.; Bergman, R. G. Carbon-hydrogen activation in completely saturated hydrocarbons: direct observation of M + R-H -> M(R)(H). Journal of the American Chemical Society. 1982, 104 (1): 352–354. doi:10.1021/ja00365a091 (英语).
- ^ 69.0 69.1 Hoyano, J. K.; Graham, W. A. G. Oxidative addition of the carbon-hydrogen bonds of neopentane and cyclohexane to a photochemically generated iridium(I) complex. Journal of the American Chemical Society. 1982, 104 (13): 3723–3725. doi:10.1021/ja00377a032 (英语).
- ^ Källström, K; Munslow, I; Andersson, P. G. Ir-catalysed asymmetric hydrogenation: Ligands, substrates and mechanism. Chemistry – A European Journal. 2006, 12 (12): 3194–3200. PMID 16304642. doi:10.1002/chem.200500755 (英语).
- ^ Roseblade, S. J.; Pfaltz, A. Iridium-catalyzed asymmetric hydrogenation of olefins. Accounts of Chemical Research. 2007, 40 (12): 1402–1411. PMID 17672517. doi:10.1021/ar700113g (英语).
- ^ Wang, X.; Andersson, M. R.; Thompson, M. E.; Inganäsa, O. Electrophosphorescence from substituted poly(thiophene) doped with iridium or platinum complex. Thin Solid Films. 2004, 468 (1–2): 226–233. Bibcode:2004TSF...468..226W. doi:10.1016/j.tsf.2004.05.095 (英语).
- ^ Tonzetich, Zachary J. Organic Light Emitting Diodes—Developing Chemicals to Light the Future (PDF). Journal of Undergraduate Research (Rochester University). 2002, 1 (1) [2008-10-10]. (原始内容 (PDF)存档于2008-10-29) (英语).
- ^ Holder, E.; Langefeld, B. M. W.; Schubert, U. S. New Trends in the Use of Transition Metal-Ligand Complexes for Applications in Electroluminescent Devices. Advanced Materials. 2005-04-25, 17 (9): 1109–1121. doi:10.1002/adma.200400284 (英语).
- ^ Mottishaw, J. Notes from the Nib Works—Where's the Iridium?. The PENnant. 1999, XIII (2). (原始内容存档于2009-08-19) (英语).
- ^ Crookes, W. (编). The Paris Exhibition. The Chemical News and Journal of Physical Science. 1867, XV: 182 (英语).
… has been used in a Withworth gun for more than 3000 rounds, and scarcely shows signs of wear yet. Those who know the constant trouble and expense which are occasioned by the wearing of the vent-pieces of cannon when in active service, will appreciate this important adaptation.
- ^ Pepper, J. H. The Playbook of Metals: Including Personal Narratives of Visits to Coal, Lead, Copper, and Tin Mines, with a Large Number of Interesting Experiments Relating to Alchemy and the Chemistry of the Fifty Metallic Elements. Routledge, Warne, and Routledge. 1861: 455 (英语).
- ^ Radioisotope Brief: Iridium-192 (Ir-192) (PDF). Radiation Emergencies. Centers for Disease Control and Prevention. 2004-08-18 [2008-09-20]. (原始内容存档 (PDF)于2008-10-29) (英语).
外部連結
[编辑]- 元素铱在洛斯阿拉莫斯国家实验室的介紹(英文)
- EnvironmentalChemistry.com —— 铱(英文)
- 元素铱在The Periodic Table of Videos(諾丁漢大學)的介紹(英文)
- 元素铱在Peter van der Krogt elements site的介紹(英文)
- WebElements.com – 铱(英文)
- (英文)大英百科全书的铱 (页面存档备份,存于互联网档案馆)
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||
| ||||||



