固体


固體( 英語:solid )是物質存在的一種狀態,是四種基本物质状态之一。與液體和氣體相比,固體有固定的體積及形狀[1],形狀也不會隨著容器形狀而改變。固體的質地較液體及氣體堅硬,固體的原子之間有緊密的結合。固體可能是晶体,其空間排列是有規則的晶格排列(例如金屬及冰),也可能是無定形體,在空間上是不規則的排列(例如玻璃)。一般而言,固体是宏观物体,一个物体要达到一定的大小才能夠被称为固体,但是对其大小無明确的规定。
物理學中研究固體的分支稱為固体物理学,是凝聚态物理学的主要分支之一。材料科学探討各種常見固體的物理及化學特性。固體化學研究固體結構、性質、合成、表徵等的一門化學分支,也和一些固體材料的化學合成有關。
特性[编辑]
固體有三種特性:
儘管任何固體都有熱能,粒子間可以相互震動,此粒子運動幅度相當的小,很難靠感覺來觀察。
通过其组成部分之间相互作用,固体的特性可能与组成它的粒子的特性有很大区别。
微觀描述[编辑]

固体可依其原子、分子或離子的排列方式是否有特定週期性的規則,分類為晶體或無定形體(非晶体),而晶体又分为单晶体和多晶体[2]。固體是結晶體或是無定形體,和其材料及冷卻凝固的條件有關,緩慢冷卻形成的固體比較容易形成結晶體,而快速冷卻形成的固體比較容易形成無定形體。
有些物質中只含有一種化合物,像冰塊或氯化鈉等,但也有許多物體是由多種化合物所組成,像岩石就是由許多不同的的礦物及准矿物所組成,無法用一個化學式來表示其中的成份,而木材是自然形成的有機材料,主要由纤维素及木質素所組成。複合材料是由多種材料所組成,可藉由材料及成份的調整來達到預期的特性。
晶体[编辑]
晶體是排列規則的固體,当整个晶体内原子都按周期性規則排列时,稱為单晶,例如氯化鈉、天然水晶、鑽石等。不過大部份固體的晶體大小都遠小於可用肉眼判識的大小,肉眼可見的固體其實是由許多稱為晶粒的“小单晶體”所組成,晶粒最小可以到數奈米。粗晶、微晶、纳米晶指的就是晶粒的大小。[3]
由許多晶粒組成的固體稱為多晶,常見的石头、金屬、陶瓷都是多晶。結晶體的晶体结构和其材料及冷卻凝固的條件有關。例如鋼在慢速冷卻時會形成波來鐵,若經過淬火的快速冷卻,會形成馬氏體[4]。
非晶体[编辑]
准晶[编辑]
准晶体是一种介于晶体和非晶体之间的固体。[5]
固體的類別[编辑]
依固體組成的原子(或原子團)不同,原子之間的作用力也隨之不同:例如氯化鈉是由氯離子和鈉離子組成,氯離子和鈉離子之間會形成離子鍵。像鑽石或矽的固體,原子和原子之間共同使用它們的外層電子,形成成共價鍵。金屬中的原子之間會形成金屬鍵,原子的價電子會形成自由電子。大部份的有機化合物分子間的作用力是凡得瓦力,主因是在分子中的電荷分佈不平均所造成。固體的特性受原子之間作用力的影響很大[6]。
金屬[编辑]
一般而言,金屬是電及熱的良導體。元素週期表中由硼畫一條線至Og,線左側的元素都是金屬。合金是指由二種或二種以上元素混合而成,以金屬為其主要成份,且有金屬特性的混合物[7]。
人類自史前時代就開始使用金屬,像青銅時代及鐵器時代就開始以器具使用的金屬種類為其時代名稱。金屬由於其強度及可靠度良好,已廣為使用在各領域中,例如建築物的結構、車輛的結構、許多工具及設備、管線、道路標誌及鐵軌等。鐵和鋁是最常使用的二種金屬,也是地殼中豐度最高的二種金屬元素。在使用時,鐵一般會和其他元素形成合金,其中最常使用的鋼,其碳含量最多會到2.1%,而隨著碳含量的增加,合金的硬度也會逐漸提高[8]。
礦物[编辑]

礦物是存在於自然界中,在高壓下經過許多地质過程後形成的固體。礦物必需有晶体结构以及一致性物理性質。礦物的成份約有數千種廣,範圍從純元素、簡單鹽類,也可以是複雜的矽酸鹽。礦物和岩石不同,後者是由許多的礦物及准矿物所組成,無法用化學式來表示。地殼中岩石的主要成份包括石英、长石、雲母、綠泥石、高嶺石、方解石、綠簾石、橄榄石、普通辉石、角闪石、磁鐵礦、赤铁矿、褐铁矿等。其中石英、长石及雲母是常見的礦物,其他的礦物只在一些特定區域才能找到。礦物中最多的是矽酸鹽,約佔一般岩石的95%,主要是由氧和矽組成,也包括鋁、鎂、鐵、鈣及其他金屬。
陶瓷[编辑]
陶瓷材料是由無機化合物所組成,通常是元素的氧化物。陶瓷不容易發生化學反應,一般而言是可以耐酸耐腐蝕的材料。陶瓷一般可耐1000至1600 °C的高溫,不過像氮化物、硼化物及碳化物等不含氧的無機化合物其耐溫範圍更高。陶瓷一般會有高硬度、高耐磨性、抗腐蝕,但其脆性大[9]。
傳統的陶瓷原料包括像高嶺石之類的黏土礦物,較後期的陶瓷原料則包括氧化鋁(礬土),現代的陶瓷原料或稱為先進陶瓷原料包括有碳化矽及碳化鎢.兩者的耐磨性都很好,因此可用在像採礦設備中的粉碎用機械中。
大部份的陶瓷(包括礬土及其相關化合物)都是用粉末原料成形而成,因此可以得到細粒度的多晶微結構,容易散射可見光範圍的電磁波,因此陶瓷一般都是不透明的材料。
玻璃陶瓷[编辑]

玻璃陶瓷兼具有无定形体的玻璃及晶體的陶瓷的許多特性,其成形方式類似玻璃,再利用熱處理的方式使其部份產生结晶,因此其中同時有无定形体及晶體均勻分佈。
當閃電擊中砂粒中的晶粒時,也會產生玻璃陶瓷。閃電帶來的大量及快速的熱能會使溫度到約2500 °C,會產生中空、分支樹根狀的閃電熔岩。
有机固体[编辑]
有机化学是研究有機化合物的結構、性質、組成、反應及製備等。有機化合物的主要成份為碳和氫,但也包括氧、氮及鹵素(氟、氯、溴、碘),有些有機化合物還含有磷和硫等,有机固體的例子有木材、石蠟、萘及許多的聚合物和塑膠等。
木材[编辑]
木材是像乔木和灌木能够次级生长的植物所形成的木质化组织。这些植物在初生生长结束后,根茎中的维管形成层开始活动,向外发展出韧皮,向内发展出木材。木材是维管形成层向内的发展出植物组织的统称,包括木质部和木質线。
木材為林業主產物,对于人类生活起着很大的支持作用。根据木材性质的不同,可以用在不同的應用中。
聚合物[编辑]

聚合物(Polymer)是指具有非常大的分子量的化合物,分子間由結構單位、或單體經由共價鍵連接在一起。這個字眼(polymer)是出自於希臘字:polys代表的是多,而meros 代表的是小單位(part)[10],所以很多小單位連結在一起的這種特別的分子,我們稱之為聚合物[11]。需要更多的資訊,可以參考塑膠、DNA和高分子。
生物材料[编辑]
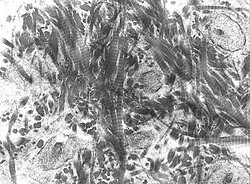
許多自然界的材料都可以視為複雜的複合材料,而且各自有其特殊的性質。這些材料歷經數百萬年的演變,許多科學家也從中得到靈感來設計先進材料。生物材料的特徴包括结构层次(structural hierarchy)、多功能性及自我修复的能力。自我組織也是生物材料的基本特性之一,藉此才能由分子層次逐漸組合為各種生物材料,自組裝也是在進行一些高效能生物材料的化學合成時,逐漸開始使用的方法之一。
複合材料[编辑]

複合材料是由金屬材料、陶瓷材料或高分子材料等兩種或兩種以上的材料,經過複合工藝而製備的多相材料。其中包括連續相的基體,和被基體包容,用來提昇材料性能的相增強體。
複合材料的應用範圍很廣,包括建築工程中常用的鋼筋混凝土,及用在太空梭的航天飞机隔热系统中,在太空梭返航回到地球時避免表面過熱的絕熱瓦,太空梭機鼻及機翼前緣會使用強化碳-碳的淺灰色材料,可以承受返航時高達1510 °C的溫度。強化碳-碳是一種由浸漬在酚醛樹脂的石墨人造絲製成的層疊複合材料。在高溫的高壓釜中處理後,層疊會熱分解,人造絲會釋出碳,再在真空下浸漬在糠醇中,糠醇也會釋出碳。為了反覆利用時的抗氧化能力,會用碳化矽作為強化碳-碳的外層。
半导体[编辑]
半导体是電阻率介於金屬導體和非金屬絕緣體之間的物質,在週期表硼往右下的對角線上.其左邊是金屬導體,其右邊是絕緣體。
半導體元件是近代電子學的基礎,包括收音機、電腦、電視中都有半導體元件。半導體元件包括電晶體、太陽能電池、二極體及積體電路。大陽能光電板是大型的半導體元件,直接將光能轉換為電能。
在金屬導體中,電流是由於電子的流動所造成,但在半導體中,電流是由於材料能带结构中的電子流動以及帶正電電洞流動所造成。常見的半導體材料包括矽、鍺及砷化鎵。
纳米材料[编辑]
許多固體當其大小為幾個納米時,其特性也會隨之改變。例如金和矽分別是金色和灰色,但金和矽的納米料子都是紅色,大小為約2.5納米的金納米粒子,其熔點約為300°C,遠低於金塊的熔點1064°C[12]。金屬的納米線其強度也比一般大小下的相同金屬要大[13][14]。
納米材料有高表面積,適用在許多和能源相關的應用中,例如納米的鉑金屬可以作為車用燃料的催化劑,也可以用在質子交換膜燃料電池中、鑭、鈰、錳、鎳的氧化物形成的陶瓷或金屬陶瓷可用在固体氧化物燃料电池(SOFC)、鋰和鈦的納米顆粒可用在鋰離子電池或钛酸锂电池中、矽納米粒子已被證實可以大幅提昇鋰離子電池在膨胀/收缩周期中的儲存容量。矽納米顆粒也用在新形式的太陽能電池中,太陽能電池中多晶矽基板上矽量子點的薄膜沉积可以增加60%輸出電壓,此應用中納米顆粒或薄膜的表面積也使其吸收輻射量達到最大值。
物理性質[编辑]
固體的物理性質包括氣味、顏色、體積、密度、熔點、沸點、比熱、室溫下的形態(固體、液體或氣體)、硬度、多孔性、折射率等。以下探討一些固體的材料性質。
世界上最輕的固體是飛行石墨,其密度小于0.2 mg/cm³[15],比微晶格(0.9 mg/cm³ )和气凝胶(1.9 mg/cm³)的密度都小。
力學[编辑]

材料的力學性質是和其材料強度及抵抗變形的能力有關,像許多結構中使用钢梁的原因是因為钢的高強度,在結構中受力時不會斷裂,也不會有顯著的彎曲。
力學性質包括彈性、塑性、抗拉強度、抗壓強度、抗剪強度、断裂韧性及延展性(脆性材料的延展性低)及压入硬度。固體力學是研究固體在外在施力及溫度變化下的行為。
固體和流體不同,不會有宏觀的流動現象。固體有一定的形狀,若其形狀變化,和其原有形狀不同,稱為形變,形變和原有尺寸的比例稱為應變。若材料受到的應力非常小,幾乎所有固體都會滿足胡克定律,其應變和應力成正比,比例係數為彈性模量或楊氏模量,這類的變形是在線彈性的範圍內。物體受力時的形變可分為以下的三種:
- 彈性:當外力移除後,物體會恢復成原來形變前的狀態。
- 粘弹性:材料同時有彈性及阻尼,因此當外力移除後,物體會接近原來形變前的狀態,但不會完全恢復形變前的狀態,需額外施力克服阻尼的影響。其應力-應變曲線會有遲滯現象,表示其力學上的響應為一個和時間有關的響應。
- 塑性:當外力造成的應力超過一定範圍時,物體會產生不可逆的永久形變,外力移除後,物體無法恢復成原來形變前的狀態。
許多材料高溫下的強度會下降,防火材料是指高溫下仍可維持其強度的材料,可用一些有特殊要求的應用中。例如玻璃陶瓷有優異的力學性質,而且可以承受超過1000 °C的反覆性快速溫度變化,適用在檯面烹飪中。在航太工業中,飛機或太空船外層使用的材料需要可以耐熱衝擊,因此會使用由有機聚合物紡出的合成纖維,有聚合物/陶瓷/金屬的複合材料或是纤维增强塑料。
熱學[编辑]

由於固體有熱能,其原子會在固體中特定位置的周圍振動,晶體或是無定形體的晶格振動頻率頻譜是固體動力學的基礎,原子的振動幅度是原子等級的大小,因此需用特殊的儀器才能觀察,例如光譜學相關的儀器。
固體的熱學性質包括熱導率,是指一固體热传导的能力。固體的熱學性質也包括比熱容,是指固體以熱能方式儲存能量的能力。
熱電效應包括三個在金屬中溫度和電壓之間的轉換效應:塞貝克效應、帕爾帖效應及湯姆森效應,前二個是在二種不同金屬介質中,溫度差和電壓之間的轉換效應,湯姆森效應則是一金屬兩端溫度不同時,金屬兩端會形成電勢差的效應。
電學[编辑]
電學性質包括電導率、電阻率、阻抗及電容,金屬及合金是電的導體,而玻璃及陶瓷是電的絕緣體,前者電導率高,後者電導率低,而半導體介於二者之間。金屬的導電是因為其中的電子,半導體的導電是電子和電洞,而快离子导体的導電性是由離子造成。
大部份導體的電阻率會隨著溫度的下降而降低,只是電阻率最終會是一個不為零的值。有些材料有超導體的特性,當在溫度低於其臨界溫度時,電阻率會突然降為零。低溫下有超導特性的材料包括錫和鋁等金屬、許多金屬合金、一些重度摻雜的半導體及特定的陶瓷。一個由超導體形成的線圈,可以在沒有電壓源的條件下,讓電流在線圈內持續流動。
介電質是一種可以電極化的絕緣體,可以用在電容器中。電容器是利用二片距離很近的導體來儲存能量的電子零件,二片導體之間即為介電質,因此二片導體會產生大小相同,極性相反的電荷,在電路中電容器常作為能量儲存元件,因此電容器的阻抗會隨著頻率而不同,電容器也常用在濾波器中,去分離高頻及低頻訊號。
機電特性[编辑]
壓電性是指晶體在受到應力後會產生電壓的特性,在有壓電性的晶體中,若施加電壓也會產生微小的形變。像橡膠、木材、頭髮及絲等聚合物都有壓電性,而聚偏二氟乙烯聚合物的壓電性要比石英高出許多。壓電性材料的形變特性使其適用在像高壓源、喇叭、雷射.及其他化學、生物及聲光的感測器及換能器。
光學[编辑]
有些材料會允許可見光穿透,例如玻璃,有些材料則會反射可見光,例如金屬。
許多材料會允許一定波長範圍的電磁波通過,反射其他波長範圍的電磁波。例如窗戶的玻璃會設計成可以讓可見光穿透,但會反射大部份會造成曬傷的紫外線,此特性可以用來作頻率選擇的光濾鏡,可以調整入射光的顏色。
在一些特定的應用時,需同時考慮材料的光學和力學特性。例如紅外線導引飛彈的感測器需放在一個允許紅外線穿透的外殼內,目前會使用單晶蓝宝石作為高速紅外線導引飛彈的外殼,但無法讓整個中紅外線(3–5 µm)範圍內的紅外線都穿透此材料,在室溫下若波長約超過4.5 µm,穿透能力就開始下降。雖然在室溫下蓝宝石的強度比其他和中紅外線的材料會好,但若超過600°C時其強度會變差。因此長期以來都要在光學特性和力學的耐久性上取捨,不過使用透明陶瓷或光學奈米材料可以減少這類的問題。
受導引的光波傳輸和光纖領域有關,也和玻璃是否可以同時傳送多個頻率的信號(多模光導)有關,理想情形下光訊號強度維持不變,而信號之間不會有干涉。光導是積體光電子電路的一部份,或是光學通訊系統的傳輸介質。
光電特性[编辑]
太陽能電池是可以將光能轉換為電能的設備,太陽能電池會利用吸光性材料用光子激發電子和電洞,再讓電子和電洞往不同方向移動來傳導電流。上述的效應稱為光電效應,此一領域稱為光電工程。
太陽能電池有許多不同的應用,最常見的是用在需要電源,但又無法連接到輸電網路的情形,例如地球軌道上的衛星、掌上式計算機、手表、衛星電話或距離很遠的打水泵浦。近來也開始將太陽能電池產生的能量透過變頻器轉換為交流電壓,輸送到輸電網路,太陽能電池不只是一個獨立的電源,也可以是輸電網路的一部份。
所有的太陽能電池都需要在電池結構中有可以吸收光線的材料,用來吸收光子,利用光電效應產生電子。由於太陽光中特定頻率範圍的光才能穿過大氣層,到達地表,太陽能電池中的吸光性材料會選用在可吸收這些頻率光子的材料,不過若太陽能電池是放置在大氣層外,則需針對大氣層的太陽光頻率分佈來選擇太陽能電池的材質。
磁學[编辑]
參見[编辑]
參考資料[编辑]
- ^ 田战省. 身边的科学/电与磁. 陕西: 陕西科学技术出版社. 2004: p.6 [2013-04-17]. ISBN 7536938829. (原始内容存档于2015-05-03).
- ^ 王昆林. 材料工程基础. 北京: 清华大学出版社有限公司. 2003: p.54 [2013-04-16]. ISBN 7302070644. (原始内容存档于2015-05-03).
- ^ 单晶体与多晶体. 中国数字科技馆. [2017-05-17]. (原始内容存档于2017-01-15).
- ^ Robert William Kerr Honeycombe, Harshad Kumar Dharamshi Hansraj Bhadeshia, 蔡明欽. 鋼-顯微組織與性質. 台北: 五南圖書出版股份有限公司. 2004: p.168 [2013-04-18]. ISBN 9571137812. (原始内容存档于2015-05-02).
- ^ 王昆林. 材料工程基础. 清华大学出版社. 2003: 74. ISBN 7302070644.
- ^ 王昆林,材料工程基础,p.43
- ^ 冯之敬. 制造工程与技术原理. 北京: 清华大学出版社有限公司. 2004: p.19 [2013-04-20]. ISBN 7302081204. (原始内容存档于2015-05-03).
- ^ 冯之敬,制造工程与技术原理,p.31
- ^ 冯之敬,制造工程与技术原理,p.72
- ^ Online Etymology Dictionary. [2013-04-23]. (原始内容存档于2007-10-16).
- ^ IUPAC. "Glossary of Basic Terms in Polymer Science". Pure Appl. Chem. 1996, 68, 2287-2311.
- ^ Buffat, Ph.; Borel, J.-P. Size effect on the melting temperature of gold particles. Physical Review A. 1976, 13 (6): 2287. Bibcode:1976PhRvA..13.2287B. doi:10.1103/PhysRevA.13.2287.
- ^ Walter H. Kohl. Handbook of materials and techniques for vacuum devices. Springer. 1995: 164–167. ISBN 1-56396-387-6.
- ^ Shpak, Anatoly P; Kotrechko, Sergiy O; Mazilova, Tatjana I; Mikhailovskij, Igor M. Inherent tensile strength of molybdenum nanocrystals. Science and Technology of Advanced Materials (free-download pdf). 2009, 10 (4): 045004. Bibcode:2009STAdM..10d5004S. doi:10.1088/1468-6996/10/4/045004.
- ^ Christian-Albrechts-Universitaet zu Kiel. World Record: Lightest Material in the World Produced. www.sciencedaily.com. 2012-07-12 [2013-04-18]. (原始内容存档于2012-07-21).
| ||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||



