原子
| 氦原子 | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||
| 氦原子結構示意圖。圖中灰階顯示對應電子雲於1s原子軌域之機率密度函數的積分強度。而原子核僅為示意,質子以粉紅色、中子以紫色表示。事實上,原子核(與其中之核子的波函數)也是球型對稱的。 (對於更複雜的原子核則非如此) | ||||||||||
| 分类 | ||||||||||
| ||||||||||
| 性质 | ||||||||||
|
原子(英語:atom)是构成化学元素的普通物质[2][3]的最小单位[4];原子也是化学变化中最小的粒子及元素化學性質的最小單位。
一粒正原子包含有一粒緻密的原子核及若干圍繞在原子核周圍帶負電的電子。而反原子的原子核帶負電,周圍的反電子帶「正電」。正原子的原子核由帶正電的質子和電中性的中子組成。反原子的原子核中的反質子帶負電,從而使反原子的原子核帶負電。當質子數與電子數相同時,這原子就是電中性,称为中性原子[5](英語:neutral atom)[6];否則,就是帶有正電荷或者負電荷的離子。根據質子和中子數量的不同,原子的類型也不同:質子數決定了該原子屬於哪種元素,而中子數則確定了該原子是此元素的哪種同位素。
原子的英语 atom 是從古希臘語:ἄτομος(atomos,“不可切分的”)轉化而來。很早以前,希臘和印度的哲學家就提出了原子的不可切分的概念。 17和18世紀時,化學家發現了物理學的根據:對於某些物質,不能通過化學手段將其繼續的分解。 19世紀晚期和20世紀早期,物理學家發現了亞原子粒子以及原子的內部結構,由此證明原子並不是不能進一步切分。 量子力學原理能夠為原子提供很好的模型。 [7][8]
與日常體驗相比,原子是極小的物體,其質量也很微小,以至於只能以特殊儀器才能觀測到單粒原子,如扫描隧道显微镜。原子的99.9%的重量集中在原子核,[9]其中的质子和中子有著相近的質量。每種元素至少有一種不穩定的同位素,可以放射性衰變。這直接導致核轉化,即原子核中的中子數或質子數發生變化。[10]原子佔據一組穩定的能級,或稱為軌道。當它們吸收和放出中子的時候,中子也可以在不同能級之間跳躍,此時吸收或放出原子的能量與能級之間的能量差相等。電子決定元素的化學特性,並且對中子的磁性有很大的影響。
历史[编辑]
| 此章節需要提供更多來源,否則內容可能無法查證。 (2015年2月9日) |
大约在两千五百年前,希腊哲学家对物质的组成问题争论不休。原子派认为物质在无数次分割之后,最终会小到无法分割。原子(atom)一词源自希腊语,意思是“不可分割”。在1803年到1807年之间,英国化学家道尔顿发展了这些观点并将它用在它的原子学说中。他相信原子既不能创造也不能消灭。任一元素所含的原子都一样。[來源請求]
关于物质是由离散单元组成且能任意分割的概念流传了几千年,但这些想法只是基于抽象的、哲学的推理,而非实验和实证观察。随着时间的推移以及文化及学派的转变,哲学上原子的性质也有着很大的改变而这种改变往往还带有一些精神因素。尽管如此,对于原子的基本概念在数千年后仍然有化学家采用,因为它能够很简洁阐述一些化学界的新发现。[11]
原子論[编辑]
原子论(英語:atomism,来自古希腊语 ἄτομον,atomos,含义为“不可分割”[12])是在一些古代传统中发展出的一种自然哲学[來源請求]。原子论者将自然世界理论化为由两基本部分所构成:不可分割的原子和空无的虚空(void)[來源請求]。原子论的创始人是古希腊人留基伯,他是德谟克利特的老师。古代学者在论及原子论时,通常是把他们俩人的学说混在一起的。留基伯的学说由他的学生德谟克利特发展和完善,因此公认德谟克利特为原子论的主要代表[13]。
原子论的主要内容是:宇宙的本原是原子和虚空,原子不可构造且永恒不变。原子有两种属性:大小和形状。它们在数量上是无限的。原子按一定的形状、次序和位置,在空无(empty)中通过移动和碰撞,结合和分离,与一粒或以上其他原子相钩结而形成聚簇(cluster)。不同形状、排列和位置的聚簇构成世界上各种宏观物质(substance)。德谟克利特认为,运用上述原子论的思想,就可以解释世间万物为什么会有重量、形状、尺寸等客观特性;不仅如此,他还认为,另一些特性,比如气味,只有当物体的原子和人鼻互相作用时才显示出来。
对原子概念的记述可以上溯到古印度和古希腊。有人将印度的耆那教的原子论认定为开创者大雄在公元前6世纪提出,并将与其同时代的彼浮陀伽旃延和顺世派先驱阿夷陀翅舍钦婆罗的元素思想也称为原子论[來源請求]。正理派和胜论派后来发展出了原子如何组合成更复杂物体的理论[來源請求]。在西方,对原子的记述出现在公元前5世纪留基伯和德谟克利特的著作中。对于印度文化影响希腊还是反之,亦或二者独立演化是有争议[來源請求]。
科學理論[编辑]
直到化学作为一门科学开始发展的时候,对原子才有更进一步的理解。1661年,自然哲学家罗伯特·波义耳出版了《怀疑的化学家》一书,书中他声称物质是由不同的“微粒”或原子自由组合构成的,而并不是由诸如气、土、火、水等基本元素构成。[14]1789年,既是法国贵族,又是科学研究者的拉瓦锡定义了元素一词,从此,元素就用来表示化学变化中的最小的单位。[15]
1803年道尔顿创立科学原子论,并在1803年12月与1804年1月在英国皇家学会作关于原子论的演讲,其中全面阐释了他的原子论思想。其要点为:1.化学元素均由不可再分的微粒组成。这种微粒称为原子。原子在一切化学变化中均保持其不可再分性。2.同一元素的所有原子,在质量和性质上都相同;不同元素的原子,在质量和性质上都不相同。3.不同的元素化合时,这些元素的原子按简单整数比结合成化合物。尽管从现在的观点来看,道尔顿的观点非常简洁有力(当然存在着错误)但是由于缺乏实验证据和表述不力,这一观点直到20世纪初才獲广泛接受。
现代原子理论[编辑]

道尔顿的理想没有涉及原子内部结构。随后,在1897年,发现了第一粒亚原子粒子──电子。1911年,新西兰物理学家卢瑟福发现每一粒原子都含有一粒比重很大并且带正电的原子核,他隨後在1919年發現了原子核內部帶正電的質子。1932年英國物理學家查德威克发现不帶電的中子。现代化学认为原子由原子核及绕核旋转的电子构成。原子核中含有许多质子和中子。质子和中子要比电子重約1836倍。质子的带电量是一单位正电荷,电子是一单位负电荷,中子不带电。
1803年,英语教师及自然哲学家約翰·道爾頓用原子的概念解释了为什么不同元素总是呈整数倍反应,即倍比定律;也解释了为什么某些气体比另外一些更容易溶于水。他提出每一种元素只包含唯一一种原子,而这些原子相互结合起来就形成了化合物。[16][17]
1827年,英國植物學家羅伯特·布朗在使用显微镜观察水面上花粉的时候,发现它们的运动不规则,进一步证明了微粒学说。后来,这现象称为布朗运动。德绍儿克思在1877年提出这种现象是由于水分子的热运动而导致的。1905年,爱因斯坦提出了第一个数学分析的方法,证明了这猜想。[18][19][20]
在关于阴极射线的工作中,物理学家約瑟夫·汤姆孙发现了电子以及它的亚原子特性,粉碎了一直以来认为原子不可再分的设想。[21]汤姆孙认为电子是平均分布在整粒原子上,就如同散布在均匀的正电荷海洋中,它们的负电荷与那些正电荷相互抵消。这也叫做梅子布丁模型。
然而,在1909年,在物理学家卢瑟福的指导下,研究者们用氦离子轰击金箔。他们意外的发现有很小一部分离子的偏转角度远远大于使用汤姆孙假设所预测值。卢瑟福根据这金箔实验的结果提出原子中大部分质量和正电荷都集中在位于原子中心的原子核当中,电子则像行星围绕太阳一样围绕着原子核。带正电的氦离子在穿越原子核附近时,就会大角度被反射。[22]
1913年,放射化学家弗雷德里克·索迪在放射性衰变产物的实验中发现元素周期表中各位置不只有一种原子。[23] 玛格丽特·陶德创造了同位素一词来表示同一种元素不同种类的原子。在研究离子气体的过程中,汤姆孙发明了一种新技术,可以用来分离不同同位素,最终导致了稳定同位素的发现。[24]
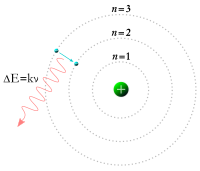
与此同时,物理学家玻尔重新审视了卢瑟福的模型,他认为电子应该位于确定的轨道之中,并且能够在不同轨道之间跳跃,而不是像先前认为那样可以自由的向内或向外移动。电子在这些固定轨道间跳跃时,必须吸收或者释放特定的能量。[25]当热源产生的一束光穿过棱镜时,能够产生多彩的光谱。应用轨道跃迁的理论就能够很好的解释光谱中存在的位置不变的线条。[26]
1916年,吉爾伯特·路易斯发现化学键的本质就是两粒原子间电子的相互作用。[27]众所周之,元素的化学性质按照周期律反复的循环。[28]1919年,美国化学家歐文·朗繆爾提出原子中的电子以某种性质相互连接或者说相互聚集。一组电子占有一層特定的电子层。[29]
1926年,薛定谔用路易·德布罗意于1924年提出的波粒二象性假说,建立了原子的数学模型,用来将电子描述为三维波形。使用波形来描述电子的一个直接后果就是在数学上不能够同时得到位置和动量的精确值,1926年,海森堡建立了相关的方程,这也就是后来著名的不确定性原理。这概念描述的是,对于测量的某个位置,只能得到一个不确定的动量范围,反之亦然。尽管这模型很难想象,但它能够解释一些以前观测到却不能解释的原子的性质,例如比氢更大的原子的谱线。因此,人们不再使用原子的行星模型,而更倾向于将原子轨道视为电子存在概率的区域。[30][31]
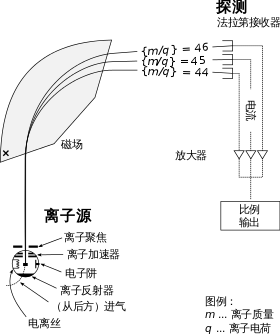
发明质谱使得科学家可以直接测量原子的准确质量。该设备使用磁体弯曲一束离子,而偏转量取决于原子的质荷比。弗朗西斯·阿斯顿使用质谱证实了同位素有着不同的质量,并且同位素间的质量差都为整数,称为整数规则。[32]1932年,詹姆斯·查德威克发现了中子,解释了这问题。中子是中性的粒子,质量与质子相仿。同位素则重新定义为质子数相同而中子数不同的元素。[33]
1950年代,随着粒子加速器及粒子探测器的发展,科学家们可以研究高能粒子间的碰撞。[34]他们发现中子和质子是强子的一种,由更小的夸克微粒构成。核物理的标准模型也随之发展,能够成功的在亚原子水平解释整粒原子核以及亚原子粒子之间的相互作用。[35]
1985年左右,朱棣文及其同事在贝尔实验室开发了一种新技术,能够使用激光来冷却原子。威廉·丹尼尔·菲利普斯团队设法将钠原子置于一个磁阱中。这两个技术加上由克洛德·科昂-唐努德日团队基于多普勒效应开发的一种方法,可以将少量的原子冷却至微开尔文的温度范围,这样就可以很高精度研究原子,这也直接导致玻斯-爱因斯坦凝聚的发现。[36]
历史上认为单一原子过于微小,不能以科学研究。最近,科学家已经成功用单一金属原子与一粒有机配体连接形成单电子晶体管。[37]一些实验用激光冷却的方法将原子减速并捕获,这些实验能够提升對物质的認知。[38]
原子的组成[编辑]
原子是由带正电荷的原子核和带负电荷的电子构成。原子核所带的正电荷数(即核电荷数)与原子核外电子所带的负电子数相等,故原子呈电中性。原子可以构成分子,也可以形成离子,也可以直接构成物质。
构成原子的三种粒子(质子、中子、电子)的基本数据:
| 原子的组成 | 原子核 | 电子 | |
|---|---|---|---|
| 质子 | 中子 | ||
| 电性和电量 | 1粒质子带1单位正电荷 | 电中性 | 1粒电子带1单位负电荷 |
| 质量(kg) | |||
| 相对原子质量 | 1.007 | 1.008 | |
亚原子粒子[编辑]
尽管原子的英文名称(atom)本意是不能繼續分割的最小粒子,但是在现代科学领域,原子实际上包含了很多不同的亚原子粒子:电子,质子和中子。氢-1原子和带一粒正电荷的氢正离子例外,前者没有中子,后者沒有电子。
质子有一粒正电荷,质量是电子质量的1836倍,为公斤,然而部分质量可以转化为原子结合能。中子不带电荷,自由中子的质量是电子质量的1839倍,为公斤。[39]中子和质子的尺寸相仿,均在m这一数量级,但它们的表面并没能精确定义。[40]
在物理学标准模型理论中,质子和中子都由名叫夸克的基本粒子构成。夸克是费米子的一种,也是构成物质的两種基本组分之一。另一基本组份称轻子,电子就是轻子的一种。夸克共有六种,每一种都带有分数的电荷,不是就是。质子就是由两粒上夸克和一粒下夸克组成,而中子则是由一粒上夸克和两粒下夸克组成。这区别就解释了为什么中子和质子电荷和质量均有差别。夸克由强相互作用结合在一起的,由胶子作中介。胶子是规范玻色子的一员,是一种用来传递力的基本粒子。[41][42]
原子核[编辑]

原子核是原子中所有的质子和中子构成的,结合起来很小,它们一起也可以称为核子。质子带正电荷,中子不显电性,故原子核的正电荷由质子数决定。原子核的半径约等于fm其中是核子的总数。[43]原子半径的数量级大约是105fm,因此原子核半径远远小于原子半径。能在短距离上起作用的残留强力將核子束缚在一起。当距离小于2.5fm的时候,强力远远大于静电力,因此它能够克服带正电的质子间的相互排斥。[44]
同种元素的原子带有相同数量的质子,这数也称原子序数。而对于某种特定的元素,中子数是可以变化的,这也就决定了该原子是这种元素的哪一种同位素。质子数量和中子数量决定了该原子是这种元素的哪一种核素。中子数决定了该原子的稳定程度,一些同位素能自发放射性衰变。[45]
中子和质子都是费米子的一种,根据量子力学中的泡利不相容原理,不可能有完全相同的两粒费米子同时拥有一样量子物理态。因此,原子核每粒质子都占用不同的能级,中子的情况也与此相同。不过泡利不相容原理并没有禁止质子和中子有相同量子态。[46]

如果原子核的质子数和中子数不相同,该原子核很易放射性衰变到更低的能级,拉近质子数和中子数。因此,质子数和中子数相同或很相近的原子更加不易衰变。然而,当原子序数逐渐增加时,质子间排斥力增强,需要更多中子來稳定原子核,所以对上述趋势有所影响。原子序数大于20时,就找不到质子数与中子数相等而又稳定的原子核了。随着Z增加,中子和质子的比例逐渐趋于1.5。[46]
原子核中的质子数和中子数也是可以变化的,不过因为它们之间的力很强,所以需要很高的能量,当多粒粒子聚集形成更重的原子核时,就会发生核聚变,例如两粒核之间的高能碰撞。在太阳的核心,质子需要3-10KeV的能量才能够克服它们之间的相互排斥,也就是库仑障壁,进而融合起来形成新的核。[47]与此相反的过程是核裂变,在核裂变中,一个核通常是经过放射性衰变,分裂成为两粒更小的核。使用高能的亚原子粒子或光子轰击也能够改变原子核。如果在过程中,原子核的质子数变了,此原子就变成另一种元素的原子。[48][49]
如果核聚变后产生的原子核质量小于聚变前原子质量的总和,那么根据爱因斯坦的质能方程,质量的差就以能量形式释放出來。这差别实际是原子核之间的结合能。[50]
对于两粒原子序数在铁或镍之前的原子核来说,它们之间的核聚变是放热过程,也就是说过程释放的能量大于将它们连在一起的能量。[51]正是因为如此,才确保了恒星中的核聚变能够自我维持。对于更重一些的原子来说,结合能开始减少,也就是说它们的核聚变会是吸热过程。因此,这些更重的原子不能以核聚变产能,也就不能够维持恒星的流体静力平衡。[46]
电子云[编辑]

在原子中,电子和质子以电磁力相互吸引,也正是这道力将电子束缚在环绕着原子核的静电位势阱中,要从这势阱中逃逸则需要外部能量。电子离原子核越近,吸引力则越大。因此,与外层电子相比,离核近的电子需要更多能量才能够逃逸。[52]
原子轨道则是描述电子在核内的概率分布的数学方程。在实际中,只有一组离散的(或量子化的)轨道存在,其他可能的形式会很快的坍塌成更稳定的形式。[53]这些轨道可以有一个或以上的环或节点,并且它们的大小,形状和空间方向都有不同。[54]

每條原子轨道都对应一粒电子的能级。电子可以吸收一粒有足够能量的光子而跃迁到更高的能级。同样,通过自发辐射,在高能级态的电子也可以跃迁回低能级态,放出光子。这些典型的能量,也就是不同量子态之间的能量差,可以用来解释原子谱线。[53]
在原子核中除去或增加一粒电子所需要的能量远远小于核子的结合能,这些能量称为电子结合能。例如:夺去氢原子中基态电子只需要13.6eV。[55]当电子数与质子数相等时,原子是电中性的。如果电子数大于或小于质子数时,该原子就会称为离子。原子最外层电子可以移动至相邻的原子,也可以由两粒原子所共有。正是由于有了这种机理,原子才能够键合形成分子或其他种类的化合物,例如离子或共价的网状晶体。[56]
性质[编辑]
核性质[编辑]
根据定义,有相同质子数的原子即属同一元素,质子数相同而中子数不同的则是同一元素的不同同位素。例如,所有的氢原子都只有一粒质子,但氢原子的同位素有几种,分别含有零粒中子(氢-1,目前最常见的类型,有时也称为氕),一粒中子(氘),两粒中子(氚)以及更多中子。[57]原子序数从1(氢)到118(Og)均为已知元素。[58]对于所有原子序数大于82的同位素都有放射性。[59][60]
地球上自然存在约339种核素,其中255种是稳定的,约占总数79%。[61]80种元素有一種或以上的稳定同位素。第43号元素、第61号元素及所有原子序数大于等于83的元素没有稳定的同位素。有十六种元素只含有一个稳定的同位素,而拥有同位素最多的元素,锡,则有十个同位素。[62]
同位素的稳定性不只受到质子数与中子数之比的影响,也受到所谓幻数的影响,实际上幻数就代表了全满的量子层。这些量子层对应于原子核层模型中一组能级。在已知的269种稳定核素中,只有四種同时有奇数粒质子和奇数粒中子。它们是2H, 6Li, 10B和14N;对于放射性核素来说,也只有5种奇-奇核素的半衰期超过一亿年:40K, 50V, 138La,176Lu和180mTa。这是因为对于大多数奇-奇核素来说,很易会β衰变,产生更稳定的偶-偶核素。[62]
质量[编辑]
因为原子质量的绝大部分是质子和中子的质量,所以质子和中子数量的总和叫做质量数。原子的静止质量通常用统一原子质量单位(u)来表示,也称作道尔顿(Da)。这单位定义为电中性的碳12质量的十二分之一,约为公斤。[63]氢最轻的同位素氕是最轻的原子,重约1.007825u。[64]原子质量约是质量数与原子质量单位的乘积。[65]最重的稳定原子是铅-208,[59]质量为207.9766521u。[66]就算是最重的原子,化学家也很难直接操作之,所以它们通常使用另一单位,摩尔,簡稱摩。摩的定义是对于任何元素,一摩总是有同样数量的原子,约。如果元素的原子质量为1u,一摩该原子的质量就为0.001kg,也就是1克。例如,碳的原子质量是12u,一摩碳的质量则是0.012kg。[63]
大小[编辑]
原子并没有精确定义的最外层,只有当两粒原子形成化学键后,测量两粒原子核间的距离,才能得到原子半径的近似值。影响原子半径的因素很多,包括在元素周期表的位置,化学键的类型,周围的原子数(配位数)以及自旋。[67]在元素周期表中,原子的半径变化的大体趋势是自上而下增加,而从左至右减少。[68]因此,最小的原子是氦,半径32pm;最大的原子是铯,半径为225pm。[69]因为这样的尺寸远远小于可见光的波长(约400-700nm),所以不能够通过光学显微镜来观测它们。然而,使用扫描隧道显微镜我们能够观察到单粒原子。
可以看到:原子的体积很小。一根人的头发的直径大约是一百万粒原子。[70]一滴水则大约有二十垓()粒氧原子以及两倍的氢原子。[71]一克拉钻石重量为kg,含有约100垓粒碳原子。[72]如果苹果放大到地球的大小,苹果中的原子就大约有原来苹果那么大。[73]
放射性[编辑]

每种元素都有一个或以上同位素有不稳定的原子核,从而能放射性衰变,在这个过程中,原子核可释放出粒子或电磁辐射。原子核半径大于强力的作用半径时就可能會放射性衰变,而强力的作用半径仅为几飞米。[74]
- α衰变:原子核释放一粒α粒子,即含有两粒质子和两粒中子的氦原子核。衰变产生原子序数低一些的新元素。
- β衰变:弱相互作用的现象,过程中中子转变成质子或者质子转变成中子。前者亦释放一粒电子和一粒反中微子,后者则释放一粒正电子和一粒中微子。所释放的电子或正电子叫β粒子。因此,β衰变能够使得该原子的原子序数增加或减少一。
- γ衰变:原子核的能级降低,释放出电磁波辐射,通常在释放了α粒子或β粒子后发生。
其它比较罕见的放射性衰变还包括:释放中子或质子,释放核子团或电子团,通过内转换产生高速的电子而非β射线以及高能的光子而非伽马射线。
每一个放射性同位素都有一个特征衰变期间,即半衰期。半衰期就是一半样品发生衰变所需要的时间。这是一种指数衰减,即样品在每一个半衰期内恒定的衰变50%,换句话说,当两次半衰期之后,就只剩下25%的起始同位素了。[74]
磁矩[编辑]
基本微粒都有一个固有性质,就像在宏观物理中围绕质心旋转的物体都有角动量一样,在量子力学叫自旋。但是严格来说,这些微粒仅仅是一些点,不能够旋转。自旋的单位是约化普朗克常数(),电子、质子和中子的自旋都是½。在原子里,电子围绕原子核运动,所以除了自旋,它们还有轨道角动量。而对于原子核来说,轨道角动量是起源于自身的自旋。[77]
正如旋转的带电物体能够产生磁场一样,原子所产生的磁场,即它的磁矩,就是由这些不同的角动量决定的。然后,自旋对它的影响应该是最大的。因为电子的一个性质就是要符合泡利不相容原理,即不能有两粒位于同样量子态的电子,所以当电子成对时,总是一个自旋朝上而另外一个自旋朝下。这样,它们产生的磁场相互抵消。对于某些带有偶数电子的原子,总的磁偶极矩会减少至零。[78]
对于铁磁元素,例如铁,电子总数为奇数,会产生净磁矩。同时,因为相邻原子轨道重叠等原因,当未成对电子都朝向同一个方向时,体系的总能量最低,这个过程称为交换相互作用。当这些铁磁性元素的磁动量都统一朝向后,整个材料就会拥有一个宏观可以测量的磁场。顺磁性材料中,在没有外部磁场的情况下,原子磁矩都是随机分布的;施加了外部磁场以后,所有原子都会统一朝向,产生磁场。[79][78]
原子核也可以存在净自旋。由于热平衡,这些原子核通常都随机朝向。但一些元素,例如氙-129,一部分核自旋也可能极化,这状态叫做超极化,在核磁共振成像中有很重要的用途。[80][81]
能級[编辑]
原子中,电子的势能与它离原子核的距离成反比。测量电子的势能,通常的测量将让该电子脱离原子所需要的能量,单位是电子伏特(eV)。在量子力学模型中,电子只能占据一组以原子核为中心的状态,每一个状态就对应于一个能级。最低的能级就叫做基态,而更高的能级就叫做激发态。[82]
电子要在两个能级之间跃迁的前提是它要吸收或者释放能量,该能量还必须要和这两个能级之间的能量差一致。因为释放的光子能量只与光子的频率有关,并且能级是不连续的,所以在电磁波谱中就会出现一些不连续的带。[83]每種元素都有特征波谱,特征波谱取决于核电荷的多少,电子的填充情况,电子间的电磁相互作用以及一些其他的因素。[84]

当一束全谱的光经过一团气体或者一团等离子体后,原子会吸收一些光子,使得这些原子内的电子跃迁。而在激发态的电子则会自发的返回低能态,能量差作为光子释放至随机方向。前者就使那些原子有了类似于滤镜的功能,观测者在最后接收到的光谱中会发现一些黑色的吸收能带。而后者能够使那些与光线不在同一条直线上的观察者观察到一些不连续的谱线,实际就是那些原子的发射谱线。用光谱学测量这些谱线就可知该物质的组成以及物理性质。[85]
仔细分析谱线后,科学家发现一些谱线有着精细结构的裂分。这是因为自旋与最外层电子运动间的相互作用,也称作自旋-轨道耦合。[86]当原子位于外部磁场中时,谱线能够裂分成三个或多个部分,这现象叫塞曼效应,其原因是原子的磁矩及其电子与外部磁场的相互作用。一些原子拥有许多相同能级电子排布,因而只产生一条谱线。当这些原子安置在外部磁场中时,这几种电子排布的能级就有了一些细小区别,这样就出现了裂分。[87]外部电场也能导致类似的现象发生,成为斯塔克效应。[88]
如果一粒电子在激发态,一粒有恰当能量的光子能够使得该电子受激辐射,释放出一粒拥有相同能量的光子,其前提就是电子返回低能级所释放出来的能量必须要与之作用的光子的能量一致。此时,受激释放的光子与原光子向同一个方向运动,也就是说这两粒光子的波是同步的。利用这个原理,人们设计出了激光,用来产生一束拥有很窄频率相干光源。[89]
化合价[编辑]
单粒原子的电子层最外层一般称为价层,其中的电子称为价电子。价电子粒数决定了这原子与其他原子成键的性质。原子能发生化学反应的一个统一趋势是使其价层全满或者全空。[90]
化学元素通常写在化学周期表中,用来表明它们有周期重复的一些化学性质。通常,拥有相同数量价电子的元素形成一组,在元素周期表中占相同的一列。而元素周期表中的横排则与量子层的电子填充情况相对应。周期表最右边的元素价层都全满,它们在化学反应中表现出一定的惰性,称为惰性气体。[91][92]
态[编辑]

物质很多不同的相态之中都存在原子,这些相态都由一定的物理条件所决定,例如温度与压强。通过改变这些条件,物质可以在固体、液体、气体与等离子体之间转换。[93]在同一种相态中,物质也可以有不同的形态,例如固态的碳就有石墨和金刚石两种形态。[94]
当温度很靠近绝对零度时,原子可以形成玻斯-爱因斯坦凝聚态。[95][96]这些超冷的原子可视为超原子,使得科学家可以研究量子力学的一些基本原理。[97]
测定[编辑]

扫描隧道显微镜是用来在原子級數观测物体表面的仪器。它利用了量子穿隧效应,使电子能穿越平时不能克服的障碍。在操作中,电子能够隧穿介于两塊平面金属电极间的真空。每塊电极表面吸附有一粒原子,使得穿隧电流密度大到可以测量。扫描時保持电流恒定,可以得到探针末端上下位移与横向位移间关系的图。计算证明扫描隧道显微镜所得到的显微图像能够分辨出单粒原子。在低偏差的情况下,显微图像显示的是对相近能级的电子轨道的一种空间平均后的尺寸,这些相近的能级也就是费米能中的局部态密度。[98][99]
原子失去电子时就电离了。这多余的电荷會偏折它在磁场运行的轨迹。这偏转角度由原子质量决定。质谱仪就用这原理测定离子的质荷比。如果样品里有多种同位素,质谱可以通过测量不同离子束的强度来推导同位素的比例。使原子气化的技术包括电感耦合等离子体原子发射光谱以及电感耦合等离子体质谱法。这两种技术都使用了气态或等离子态的样品。[100]
另一有侷限的方法是电子能量损失谱,它是通过测量透射电子显微镜中电子束穿越一个样品后所损失的能量。原子探针显像具有三维亚纳米级的分辨率,也可以通过飞行时间质谱仪来鉴定单粒的原子。[101]
激发态光谱可以用来研究远距离恒星的元素组成。观测来自恒星的光谱中特殊的波长,可以得到气体状态下原子的量子转变。使用同种元素的气体放电灯,可以得到相同的颜色。[102]氦元素就是以这种手段在太阳的光谱中发现,比在地球上发现早了23年。[103]
起源和现状[编辑]
核合成[编辑]
稳定的质子和电子在大爆炸后的一秒钟内出现。在接下来的三分钟之内,太初核合成产生了宇宙中大部分的氦、锂和氘,有可能也产生了一些铍和硼。[104][105][106]在理论上,最初的原子(有束缚的电子)是在大爆炸后大约38万年产生的,这个时代称为重新结合,在这时宇宙已经冷却到足以使电子与原子核结合了。[107]自从那时候开始,原子核就开始在恒星中通过核聚变的过程结合,产生直到铁的元素。[108]
像锂-6那样的同位素是在太空中通过宇宙射线散裂产生的。[109]这种现象在高能量的质子撞击原子核时会发生,射出大量核子。比铁重的元素在超新星中通过r-过程产生,或在AGB星中通过s-过程产生,两种过程中原子核都會捕获中子。[110]像铅那样的元素,大都是从更重的元素通过核衰变产生的。[111]
地球[编辑]
大部分组成地球及其居民的原子,都是在太阳系刚形成的时候就已经存在了。还有一部分的原子是核衰变的结果,它们的相对比例可以用来通过放射性定年法决定地球的年龄。[112][113]大部分地壳中的氦都是α衰变的产物。[114]
地球上有很少的原子既不是在一开始就存在的,也不是放射性衰变的结果。碳-14是大气中的宇宙射线所产生的。[115]有些地球上的原子是核反应堆或核爆炸的产物,要么是特意制造的,要么是副产物。[116][117]在所有超铀元素──原子序数大于92的元素中,只有钚和镎在地球中自然出现。[118][119]超铀元素的寿命比地球现在的年龄短[120],因此许多这类的元素都早已衰变了,只有微量的钚-244例外[112]。钚和镎的自然矿藏是在铀矿中通过中子俘获产生的。[121]
地球有约粒原子。[122]地球大气层有少量惰性气体原子,如氩和氖。大气层剩下的99%的部分,是以分子的形式束缚的,包括二氧化碳、双原子的氧气和氮气。在地球表面,原子结合并形成了各种各样的化合物,包括水、盐、硅酸盐和氧化物。原子也可以结合起来组成不含独立分子的物质,包括晶体和液态或固态金属。[123][124]
罕见和理论形式[编辑]
虽然原子序数大于82(铅)的元素已知有放射性,但是对于原子序数大于103的元素,提出了“稳定岛”的概念。这些超重元素中可能有原子核相对来说比其它原子核稳定。[125]最有可能的稳定超重元素是Ubh,它有126粒质子和184粒中子。[126]
各種粒子都有对应的反物质粒子,电荷相反;正电子就是带有正电荷的反电子,反质子就是与质子对等,但带有负电荷的粒子。不知道什么原因,宇宙中反物质非常稀少,在自然界没有发现任何反原子。[127][128]然而,1996年,在日内瓦的欧洲核子研究中心,首次合成了反氢──氢的反物质。[129][130]
把原子中的质子、中子或电子用相等电荷的其它粒子代替,可以形成奇异原子。例如,可以把电子用质量更大的緲子代替,形成緲子原子。这些类型的原子可以用来测试物理学的基本预言。[131][132][133]
参阅[编辑]
参考文献[编辑]
引用[编辑]
- ^ Matthew Champion, As.r.html "Re: How many atoms make up the universe?"[永久失效連結], 1998
- ^ 吴岳良. “两暗一新”暗物质、暗能量、新理论 (PDF). 中国科学院理论物理研究所. 2010-03-18 [2022-05-18]. (原始内容 (PDF)存档于2020-05-24) (中文(简体)).
可见宇宙有普通物质(ORDINARY MATTER)和普通能量(ORDINARY ENERGY),黑暗宇宙有暗物质(DARK MATTER)和暗能量(DARK ENERGY)
- ^ 時時. 「這應該是不可能的」科學家發現不含暗物質的神秘星系. 地球圖輯隊. 2018-04-02 [2022-05-18] (中文(繁體)).
銀河系的暗物質比肉眼看得到的普通物質(ordinary matter)在整體的質量上多了 30倍。
- ^ McSween Jr H, Huss G. Cosmochemistry[M]. Cambridge University Press, 2021. p. 419
- ^ 存档副本. [2023-08-04]. (原始内容存档于2023-08-04).
- ^ Scientific American. Scientific American Science Desk Reference. Wiley. 1999: 62. ISBN 9780471356752.
- ^ Haubold, Hans; Mathai, AM. Microcosmos: From Leucippus to Yukawa. Structure of the Universe. Common Sense Science. 1998 [2008-01-17]. (原始内容存档于2008-10-01).
- ^ Harrison (2003:123–139 ).
- ^ 大部分同位素中核子(原子核内质子与中子之和)比電子多。以氫-1為例,只有一個電子和核子(质子),則質子重量是總質量的或99.95 %
- ^ Staff. Radioactive Decays. Stanford Linear Accelerator Center, Stanford University. 2007-08-01 [2007-01-02]. (原始内容存档于2009-06-07).
- ^ Ponomarev (1993:14–15).
- ^ atom. Online Etymology Dictionary. [2015-02-09]. (原始内容存档于2015-03-20).
- ^ 古希腊原子论的科学意义:由基本的物质微粒解释宏观经验现象. 静思--中科院研究生院教授,博士生导师. [2010-02-05]. (原始内容存档于2021-06-14).
- ^ Siegfried (2002:42–55).
- ^ Lavoisier's Elements of Chemistry. Elements and Atoms. Le Moyne College, Department of Chemistry. [2007-12-18]. (原始内容存档于2007-05-01).
- ^ Wurtz (1881:1–2).
- ^ Dalton (1808).
- ^ Einstein, Albert. Über die von der molekularkinetischen Theorie der Wärme geforderte Bewegung von in ruhenden Flüssigkeiten suspendierten Teilchen (PDF). Annalen der Physik. 1905年5月, 322 (8): 549–560 [2007-02-04]. Bibcode:1905AnP...322..549E. doi:10.1002/andp.19053220806. (原始内容 (PDF)存档于2006-03-18) (德语).
- ^ Mazo (2002:1–7).
- ^ Lee, Y. K.; Hoon, Kelvin. Brownian Motion. Imperial College, London. 1995 [2007-12-18]. (原始内容存档于2007-12-18).
- ^ The Nobel Foundation. J.J. Thomson. Nobelprize.org. 1906 [2007-12-20]. (原始内容存档于2013-05-12).
- ^ Rutherford, E. The Scattering of α and β Particles by Matter and the Structure of the Atom. Philosophical Magazine. 1911, 21: 669–88 [2008-01-18]. (原始内容存档于2007-02-05).
- ^ Frederick Soddy, The Nobel Prize in Chemistry 1921. Nobel Foundation. [2008-01-18]. (原始内容存档于2008-04-09).
- ^ Thomson, Joseph John. Rays of positive electricity. Proceedings of the Royal Society. 1913, A 89: 1–20 [2007-01-18]. (原始内容存档于2019-03-08).
- ^ Stern, David P. The Atomic Nucleus and Bohr's Early Model of the Atom. NASA Goddard Space Flight Center. 2005-05-16 [2007-12-20]. (原始内容存档于2007-08-20).
- ^ Bohr, Niels. Niels Bohr, The Nobel Prize in Physics 1922, Nobel Lecture. The Nobel Foundation. 1922-12-11 [2008-02-16]. (原始内容存档于2008-04-15).
- ^ Lewis, Gilbert N. The Atom and the Molecule. Journal of the American Chemical Society. 1916年4月, 38 (4): 762–786. doi:10.1021/ja02261a002.
- ^ Scerri, Eric R. The Periodic Table. Oxford University Press US. 2007: 205–226. ISBN 0195305736.
- ^ Langmuir, Irving. The Arrangement of Electrons in Atoms and Molecules. Journal of the American Chemical Society. 1919, 41 (6): 868–934 [2008-09-01]. (原始内容存档于2008-12-10).
- ^ Brown, Kevin. The Hydrogen Atom. MathPages. 2007 [2007-12-21]. (原始内容存档于2008-05-13).
- ^ Harrison, David M. The Development of Quantum Mechanics. University of Toronto. 2000年3月 [2007-12-21]. (原始内容存档于2007-12-25).
- ^ Aston, Francis W. The constitution of atmospheric neon. Philosophical Magazine. 1920, 39 (6): 449–55.
- ^ Chadwick, James. Nobel Lecture: The Neutron and Its Properties. Nobel Foundation. 1935-12-12 [2007-12-21]. (原始内容存档于2007-10-12).
- ^ Kullander, Sven. Accelerators and Nobel Laureates. The Nobel Foundation. 2001-08-28 [2008-01-31]. (原始内容存档于2008-04-13).
- ^ Staff. The Nobel Prize in Physics 1990. The Nobel Foundation. 1990-10-17 [2008-01-31]. (原始内容存档于2008-05-14).
- ^ Staff. The Nobel Prize in Physics 1997. Nobel Foundation. 1997-10-15 [2008-02-10]. (原始内容存档于2008-04-09).
- ^ Park, Jiwoong; et al. Coulomb blockade and the Kondo effect in single-atom transistors. Nature. 2002, 417 (6890): 722–25 [2008-01-03]. Bibcode:2002Natur.417..722P. doi:10.1038/nature00791. (原始内容存档于2008-01-12).
- ^ Domokos, P.; Janszky, J.; Adam, P. Single-atom interference method for generating Fock states. Physical Review a. 1994, 50: 3340–44 [2008-01-03]. Bibcode:1994PhRvA..50.3340D. doi:10.1103/PhysRevA.50.3340. (原始内容存档于2018-10-05).
- ^ Woan (2000:8).
- ^ MacGregor (1992:33–37).
- ^ Particle Data Group. The Particle Adventure. Lawrence Berkeley Laboratory. 2002 [2007-01-03]. (原始内容存档于2007-01-04).
- ^ Schombert, James. Elementary Particles. University of Oregon. 2006-04-18 [2007-01-03]. (原始内容存档于2011-08-21).
- ^ Jevremovic (2005:63).
- ^ Pfeffer (2000:330–336).
- ^ Wenner, Jennifer M. How Does Radioactive Decay Work?. Carleton College. 2007-10-10 [2008-01-09]. (原始内容存档于2008-05-11).
- ^ 46.0 46.1 46.2 Raymond, David. Nuclear Binding Energies. New Mexico Tech. 2006-04-07 [2007-01-03]. (原始内容存档于2002-12-01).
- ^ Mihos, Chris. Overcoming the Coulomb Barrier. Case Western Reserve University. 2002-07-23 [2008-02-13]. (原始内容存档于2006-09-12).
- ^ Staff. ABC's of Nuclear Science. Lawrence Berkeley National Laboratory. 2007-03-30 [2007-01-03]. (原始内容存档于2006-12-05).
- ^ Makhijani, Arjun; Saleska, Scott. Basics of Nuclear Physics and Fission. Institute for Energy and Environmental Research. 2001-03-02 [2007-01-03]. (原始内容存档于2007-01-16).
- ^ Shultis et al (2002:72–6).
- ^ Fewell, M. P. The atomic nuclide with the highest mean binding energy. American Journal of Physics. 1995, 63 (7): 653–58 [2007-02-01]. Bibcode:1995AmJPh..63..653F. doi:10.1119/1.17828. (原始内容存档于2011-03-22).
- ^ 歐風烈. 陽陰宇宙: 重新思考我們對宇宙的想法. Fong Lieh Ou(Showwe Information Co Ltd). 1 December 2018: 407– [2019-04-11]. ISBN 978-957-43-6142-7. (原始内容存档于2022-04-04).
- ^ 53.0 53.1 Brucat, Philip J. The Quantum Atom. University of Florida. 2008 [2007-01-04]. (原始内容存档于2006-12-07).
- ^ Manthey, David. Atomic Orbitals. Orbital Central. 2001 [2008-01-21]. (原始内容存档于2008-01-10).
- ^ Herter, Terry. Lecture 8: The Hydrogen Atom. Cornell University. 2006 [2008-02-14]. (原始内容存档于2008-04-15).
- ^ Smirnov (2003:249–72).
- ^ Matis, Howard S. The Isotopes of Hydrogen. Guide to the Nuclear Wall Chart. Lawrence Berkeley National Lab. 2000-08-09 [2007-12-21]. (原始内容存档于2007-12-18).
- ^ Weiss, Rick. Scientists Announce Creation of Atomic Element, the Heaviest Yet. Washington Post. 2006-10-17 [2007-12-21]. (原始内容存档于2011-08-21).
- ^ 59.0 59.1 Sills (2003:131–134).
- ^ Dumé, Belle. Bismuth breaks half-life record for alpha decay. Physics World. 2003-04-23 [2007-12-21]. (原始内容存档于2007-12-14).
- ^ Lindsay, Don. Radioactives Missing From The Earth. Don Lindsay Archive. 2000-07-30 [2007-05-23]. (原始内容存档于2007-04-28).
- ^ 62.0 62.1 CRC Handbook (2002).
- ^ 63.0 63.1 Mills et al (1993).
- ^ Chieh, Chung. Nuclide Stability. University of Waterloo. 2001-01-22 [2007-01-04]. (原始内容存档于2007-08-30).
- ^ Atomic Weights and Isotopic Compositions for All Elements. National Institute of Standards and Technology. [2007-01-04]. (原始内容存档于2006-12-31).
- ^ Audi, G.; Wapstra, A. H.; Thibault C. The Ame2003 atomic mass evaluation(II). Nuclear Physics. 2003, A729: 337–676 [2008-02-07]. (原始内容存档于2008-09-16).
- ^ Shannon, R. D. Revised effective ionic radii and systematic studies of interatomic distances in halides and chalcogenides. Acta Crystallographica, Section a. 1976, 32: 751 [2007-01-03]. Bibcode:1976AcCrA..32..751S. doi:10.1107/S0567739476001551. (原始内容存档于2007-09-30).
- ^ Dong, Judy. Diameter of an Atom. The Physics Factbook. 1998 [2007-11-19]. (原始内容存档于2007-11-04).
- ^ Zumdahl (2002).
- ^ Staff. Small Miracles: Harnessing nanotechnology. Oregon State University. 2007 [2007-01-07]. (原始内容存档于2007-12-04).—describes the width of a human hair as 105 nm and 10 carbon atoms as spanning 1 nm.
- ^ Padilla et al(2002:32)—"There are 2,000,000,000,000,000,000,000 (that's 2 sextillion) atoms of oxygen in one drop of water—and twice as many atoms of hydrogen."
- ^ A carat is 200 milligrams. By definition, Carbon-12 has 0.012 kg per mole. The Avogadro constant defines 6 × 1023 atoms per mole.
- ^ Feynman (1995).
- ^ 74.0 74.1 Radioactivity. Splung.com. [2007-12-19]. (原始内容存档于2007-12-04).
- ^ L'Annunziata (2003:3–56).
- ^ Firestone, Richard B. Radioactive Decay Modes. Berkeley Laboratory. 2000-05-22 [2007-01-07]. (原始内容存档于2006-09-29).
- ^ Hornak, J. P. Chapter 3: Spin Physics. The Basics of NMR. Rochester Institute of Technology. 2006 [2007-01-07]. (原始内容存档于2007-05-26).
- ^ 78.0 78.1 Schroeder, Paul A. Magnetic Properties. University of Georgia. 2000-02-25 [2007-01-07]. (原始内容存档于2007-04-29).
- ^ Goebel, Greg. [4.3] Magnetic Properties of the Atom. Elementary Quantum Physics. In The Public Domain website. 2007-09-01 [2007-01-07]. (原始内容存档于2011-08-21).
- ^ Yarris, Lynn. Talking Pictures. Berkeley Lab Research Review. 1997 [2008-01-09]. (原始内容存档于2008-01-13).
- ^ Liang and Haacke (1999:412–26).
- ^ Zeghbroeck, Bart J. Van. Energy levels. Shippensburg University. 1998 [2007-12-23]. (原始内容存档于2005-01-15).
- ^ Fowles (1989:227–233).
- ^ Martin, W. C.; Wiese, W. L. Atomic Spectroscopy: A Compendium of Basic Ideas, Notation, Data, and Formulas. National Institute of Standards and Technology. 2007年5月 [2007-01-08]. (原始内容存档于2007-02-08).
- ^ Atomic Emission Spectra—Origin of Spectral Lines. Avogadro Web Site. [2006-08-10]. (原始内容存档于2006-02-28).
- ^ Fitzpatrick, Richard. Fine structure. University of Texas at Austin. 2007-02-16 [2008-02-14]. (原始内容存档于2011-08-21).
- ^ Weiss, Michael. The Zeeman Effect. University of California-Riverside. 2001 [2008-02-06]. (原始内容存档于2008-02-02).
- ^ Beyer (2003:232–236).
- ^ Watkins, Thayer. Coherence in Stimulated Emission. San José State University. [2007-12-23]. (原始内容存档于2008-01-12).
- ^ Reusch, William. Virtual Textbook of Organic Chemistry. Michigan State University. 2007-07-16 [2008-01-11]. (原始内容存档于2007-10-29).
- ^ Husted, Robert; et al. Periodic Table of the Elements. Los Alamos National Laboratory. 2003-12-11 [2008-01-11]. (原始内容存档于2008-01-10).
- ^ Baum, Rudy. It's Elemental: The Periodic Table. Chemical & Engineering News. 2003 [2008-01-11]. (原始内容存档于2011-08-21).
- ^ Goodstein (2002:436–438).
- ^ Brazhkin, Vadim V. Metastable phases, phase transformations, and phase diagrams in physics and chemistry. Physics-Uspekhi. 2006, 49: 719–24. Bibcode:2006PhyU...49..719B. doi:10.1070/PU2006v049n07ABEH006013.
- ^ Myers (2003:85).
- ^ Staff. Bose-Einstein Condensate: A New Form of Matter. National Institute of Standards and Technology. 2001-10-09 [2008-01-16]. (原始内容存档于2008-01-03).
- ^ Colton, Imogen; Fyffe, Jeanette. Super Atoms from Bose-Einstein Condensation. The University of Melbourne. 1999-02-03 [2008-02-06]. (原始内容存档于2007-08-29).
- ^ Jacox, Marilyn; Gadzuk, J. William. Scanning Tunneling Microscope. National Institute of Standards and Technology. 1997年11月 [2008-01-11]. (原始内容存档于2008-01-07).
- ^ The Nobel Prize in Physics 1986. The Nobel Foundation. [2008-01-11]. (原始内容存档于2008-09-17).—in particular, see the Nobel lecture by G. Binnig and H. Rohrer.
- ^ Jakubowski, N.; Moens, L.; Vanhaecke, F. Sector field mass spectrometers in ICP-MS. Spectrochimica Acta Part B: Atomic Spectroscopy. 1998, 53 (13): 1739–63. Bibcode:1998AcSpe..53.1739J. doi:10.1016/S0584-8547(98)00222-5.
- ^ Müller, Erwin W.; Panitz, John A., McLane, S. Brooks. The Atom-Probe Field Ion Microscope. Review of Scientific Instruments. 1968, 39 (1): 83–86. Bibcode:1968RScI...39...83M. ISSN 0034-6748. doi:10.1063/1.1683116.
- ^ Lochner, Jim; Gibb, Meredith; Newman, Phil. What Do Spectra Tell Us?. NASA/Goddard Space Flight Center. 2007-04-30 [2008-01-03]. (原始内容存档于2008-01-16).
- ^ Winter, Mark. Helium. WebElements. 2007 [2008-01-03]. (原始内容存档于2007-12-30).
- ^ Croswell, Ken. Boron, bumps and the Big Bang: Was matter spread evenly when the Universe began? Perhaps not; the clues lie in the creation of the lighter elements such as boron and beryllium. New Scientist. 1991, (1794): 42 [2008-01-14]. (原始内容存档于2008-02-07).
- ^ Copi, Craig J.; Schramm, David N.; Turner, Michael S. Big-Bang Nucleosynthesis and the Baryon Density of the Universe (PDF). Science. 1995, 267: 192–99 [2008-01-13]. Bibcode:1995Sci...267..192C. PMID 7809624. arXiv:astro-ph/9407006
 . doi:10.1126/science.7809624. (原始内容存档 (PDF)于2008-02-27).
. doi:10.1126/science.7809624. (原始内容存档 (PDF)于2008-02-27).
- ^ Hinshaw, Gary. Tests of the Big Bang: The Light Elements. NASA/WMAP. 2005-12-15 [2008-01-13]. (原始内容存档于2008-01-17).
- ^ Abbott, Brian. Microwave (WMAP) All-Sky Survey. Hayden Planetarium. 2007-05-30 [2008-01-13]. (原始内容存档于2013-02-13).
- ^ F. Hoyle. The synthesis of the elements from hydrogen. Monthly Notices of the Royal Astronomical Society. 1946, 106: 343–83 [2008-01-13]. Bibcode:1946MNRAS.106..343H. (原始内容存档于2008-03-05).
- ^ Knauth, D. C.; Federman, S. R.; Lambert, David L.; Crane, P. Newly synthesized lithium in the interstellar medium. Nature. 2000, 405: 656–58. doi:10.1038/35015028.
- ^ Mashnik, Stepan G. On Solar System and Cosmic Rays Nucleosynthesis and Spallation Processes. Cornell University. 2000年8月 [2008-01-14]. (原始内容存档于2015-03-19).
- ^ Kansas Geological Survey. Age of the Earth. University of Kansas. 2005-05-04 [2008-01-14]. (原始内容存档于2008-07-05).
- ^ 112.0 112.1 Manuel (2001:407–430,511–519).
- ^ Dalrymple, G. Brent. The age of the Earth in the twentieth century: a problem (mostly) solved. Geological Society, London, Special Publications. 2001, 190: 205–21 [2008-01-14]. Bibcode:2001GSLSP.190..205D. doi:10.1144/GSL.SP.2001.190.01.14. (原始内容存档于2007-11-11).
- ^ Anderson, Don L.; Foulger, G. R.; Meibom, Anders. Helium: Fundamental models. MantlePlumes.org. 2006-09-02 [2007-01-14]. (原始内容存档于2007-02-08).
- ^ Pennicott, Katie. Carbon clock could show the wrong time. PhysicsWeb. 2001-05-10 [2008-01-14]. (原始内容存档于2007-12-15).
- ^ Yarris, Lynn. New Superheavy Elements 118 and 116 Discovered at Berkeley Lab. Berkeley Lab. 2001-07-27 [2008-01-14]. (原始内容存档于2008-01-09).
- ^ Diamond, H.; et al. Heavy Isotope Abundances in Mike Thermonuclear Device (subscription required). Physical Review. 1960, 119: 2000–04 [2008-01-14]. Bibcode:1960PhRv..119.2000D. doi:10.1103/PhysRev.119.2000. (原始内容存档于2011-11-12).
- ^ Poston Sr., John W. Do transuranic elements such as plutonium ever occur naturally?. Scientific American. 1998-03-23 [2008-01-15]. (原始内容存档于2008-10-01).
- ^ Keller, C. Natural occurrence of lanthanides, actinides, and superheavy elements. Chemiker Zeitung. 1973, 97 (10): 522–30 [2008-01-15]. (原始内容存档于2008-10-01).
- ^ Marco (2001:17).
- ^ Oklo Fossil Reactors. Curtin University of Technology. [2008-01-15]. (原始内容存档于2007-12-18).
- ^ Weisenberger, Drew. How many atoms are there in the world?. Jefferson Lab. [2008-01-16]. (原始内容存档于2007-10-22).
- ^ Pidwirny, Michael. Fundamentals of Physical Geography. University of British Columbia Okanagan. [2008-01-16]. (原始内容存档于2008-01-21).
- ^ Anderson, Don L. The inner inner core of Earth. Proceedings of the National Academy of Sciences. 2002, 99 (22): 13966–68 [2008-01-16]. Bibcode:2002PNAS...9913966A. PMID 12391308. doi:10.1073/pnas.232565899.
- ^ Anonymous. Second postcard from the island of stability. CERN Courier. 2001-10-02 [2008-01-14]. (原始内容存档于2008-02-03).
- ^ Jacoby, Mitch. As-yet-unsynthesized superheavy atom should form a stable diatomic molecule with fluorine. Chemical & Engineering News. 2006, 84 (10): 19 [2008-01-14]. (原始内容存档于2012-07-15).
- ^ Koppes, Steve. Fermilab Physicists Find New Matter-Antimatter Asymmetry. University of Chicago. 1999-03-01 [2008-01-14]. (原始内容存档于2008-07-19).
- ^ Cromie, William J. A lifetime of trillionths of a second: Scientists explore antimatter. Harvard University Gazette. 2001-08-16 [2008-01-14]. (原始内容存档于2006-09-03).
- ^ Hijmans, Tom W. Particle physics: Cold antihydrogen. Nature. 2002, 419: 439–40. doi:10.1038/419439a.
- ^ Staff. Researchers 'look inside' antimatter. BBC News. 2002-10-30 [2008-01-14]. (原始内容存档于2007-02-22).
- ^ Barrett, Roger; Jackson, Daphne; Mweene, Habatwa. The Strange World of the Exotic Atom. New Scientist. 1990, (1728): 77–115 [2008-01-04]. (原始内容存档于2007-12-21).
- ^ Indelicato, Paul. Exotic Atoms. Physica Scripta. 2004, T112: 20–26. Bibcode:2004PhST..112...20I. arXiv:physics/0409058
 . doi:10.1238/Physica.Topical.112a00020.
. doi:10.1238/Physica.Topical.112a00020.
- ^ Ripin, Barrett H. Recent Experiments on Exotic Atoms. American Physical Society. 1998年7月 [2008-02-15]. (原始内容存档于2008-10-02).
来源[编辑]
- 书籍
- L'Annunziata, Michael F. Handbook of Radioactivity Analysis. Academic Press. 2003. ISBN 978-0-12-436603-9.
- Beyer, H. F.; Shevelko, V. P. Introduction to the Physics of Highly Charged Ions. CRC Press. 2003. ISBN 978-0-7503-0481-8.
- Choppin, Gregory R.; Liljenzin, Jan-Olov; Rydberg, Jan. Radiochemistry and Nuclear Chemistry. Elsevier. 2001. ISBN 978-0-7506-7463-8.
- Dalton, J. A New System of Chemical Philosophy, Part 1. London and Manchester: S. Russell. 1808.
- Demtröder, Wolfgang. Atoms, Molecules and Photons: An Introduction to Atomic- Molecular- and Quantum Physics 1st Edition. Springer. 2002. ISBN 978-3-540-20631-6.
- Feynman, Richard. Six Easy Pieces. The Penguin Group. 1995. ISBN 978-0-14-027666-4.
- Fowles, Grant R. Introduction to Modern Optics. Courier Dover Publications. 1989. ISBN 978-0-486-65957-2.
- Gangopadhyaya, Mrinalkanti. Indian Atomism: History and Sources. Atlantic Highlands, New Jersey: Humanities Press. 1981. ISBN 0-391-02177-X.
- Goodstein, David L. States of Matter. Courier Dover Publications. 2002. ISBN 978-0-486-49506-4.
- Harrison, Edward Robert. Masks of the Universe: Changing Ideas on the Nature of the Cosmos. Cambridge University Press. 2003. ISBN 978-0-521-77351-5.
- Jevremovic, Tatjana. Nuclear Principles in Engineering. Springer. 2005. ISBN 978-0-387-23284-3.
- Lequeux, James. The Interstellar Medium. Springer. 2005. ISBN 978-3-540-21326-0.
- Liang, Z.-P.; Haacke, E. M. Webster, J. G. , 编. Encyclopedia of Electrical and Electronics Engineering: Magnetic Resonance Imaging (PDF) vol. 2. John Wiley & Sons. 1999: 412–26 [2008-01-09]. ISBN 978-0-471-13946-1. [失效連結]
- MacGregor, Malcolm H. The Enigmatic Electron. Oxford University Press. 1992. ISBN 978-0-19-521833-6.
- Manuel, Oliver. Origin of Elements in the Solar System: Implications of Post-1957 Observations. Springer. 2001. ISBN 978-0-306-46562-8.
- Mazo, Robert M. Brownian Motion: Fluctuations, Dynamics, and Applications. Oxford University Press. 2002. ISBN 978-0-19-851567-8.
- Mills, Ian; Cvitaš, Tomislav; Homann, Klaus; Kallay, Nikola; Kuchitsu, Kozo. Quantities, Units and Symbols in Physical Chemistry 2nd edition. Oxford: International Union of Pure and Applied Chemistry, Commission on Physiochemical Symbols Terminology and Units, Blackwell Scientific Publications. 1993. ISBN 978-0-632-03583-0.
- Myers, Richard. The Basics of Chemistry. Greenwood Press. 2003. ISBN 978-0-313-31664-7.
- Padilla, Michael J.; Miaoulis, Ioannis; Cyr, Martha. Prentice Hall Science Explorer: Chemical Building Blocks. Upper Saddle River, New Jersey USA: Prentice-Hall, Inc. 2002. ISBN 978-0-13-054091-1.
- Pauling, Linus. The Nature of the Chemical Bond. Cornell University Press. 1960. ISBN 978-0-8014-0333-0.
- Pfeffer, Jeremy I.; Nir, Shlomo. Modern Physics: An Introductory Text. Imperial College Press. 2000. ISBN 978-1-86094-250-1.
- Ponomarev, Leonid Ivanovich. The Quantum Dice. CRC Press. 1993. ISBN 978-0-7503-0251-7.
- Shultis, J. Kenneth; Faw, Richard E. Fundamentals of Nuclear Science and Engineering. CRC Press. 2002. ISBN 978-0-8247-0834-4.
- Siegfried, Robert. From Elements to Atoms: A History of Chemical Composition. DIANE. 2002. ISBN 978-0-87169-924-4.
- Sills, Alan D. Earth Science the Easy Way. Barron's Educational Series. 2003. ISBN 978-0-7641-2146-3.
- Smirnov, Boris M. Physics of Atoms and Ions. Springer. 2003. ISBN 978-0-387-95550-6.
- Teresi, Dick. Lost Discoveries: The Ancient Roots of Modern Science. Simon & Schuster. 2003: 213–214 [2008-09-16]. ISBN 074324379X. (原始内容存档于2020-07-13).
- Various. Lide, David R. , 编. Handbook of Chemistry & Physics 88th edition. CRC. 2002 [2008-05-23]. ISBN 0849304865. (原始内容存档于2018-04-30).
- Woan, Graham. The Cambridge Handbook of Physics. Cambridge University Press. 2000. ISBN 978-0-521-57507-2.
- Wurtz, Charles Adolphe. The Atomic Theory. New York: D. Appleton and company. 1881.
- Zaider, Marco; Rossi, Harald H. Radiation Science for Physicians and Public Health Workers. Springer. 2001. ISBN 978-0-306-46403-4.
- Zumdahl, Steven S. Introductory Chemistry: A Foundation 5th edition. Houghton Mifflin. 2002 [2008-02-05]. ISBN 978-0-618-34342-3. (原始内容存档于2008-03-04).
外部链接[编辑]
| 维基共享资源中相关的多媒体资源:原子 |
- (简体中文)中国科普博览──核能博物馆 (页面存档备份,存于互联网档案馆),中国科学院主编。
- 一滴水中的原子
- (英文) Francis, Eden. Atomic Size. Clackamas Community College. 2002 [2008-09-16]. (原始内容存档于2009-02-05).
- (英文) Freudenrich, Craig C. How Atoms Work. How Stuff Works. [2008-09-16]. (原始内容存档于2009-02-05).
- (英文) Anonymous. The atom. Science aid+. 2007 [2007-01-09]. (原始内容存档于2011-08-21).
- (英文) Anonymous. Atoms and Atomic Structure. BBC. 2006-01-03 [2008-09-16]. (原始内容存档于2007-01-02).
- (英文) Various. Physics 2000, Table of Contents. University of Colorado. 2006-01-03 [2008-09-16]. (原始内容存档于2008-01-14).
- (英文) Various. What does an atom look like?. University of Karlsruhe. 2006-02-03 [2008-09-16]. (原始内容存档于2010-04-17).
| |||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||









![{\displaystyle 1.07\cdot {\sqrt[{3}]{A}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/d5c4693ed96684d0bfaa35b5760855169e171ed4)











