一氧化二氮
此條目需要补充更多来源。 (2014年1月24日) |
| 一氧化二氮 | |
|---|---|
| |
| |
| |
| IUPAC名 Nitrous oxide 氧化亞氮 | |
| 别名 | 笑氣 |
| 识别 | |
| CAS号 | 10024-97-2 |
| PubChem | 948 |
| ChemSpider | 923 |
| SMILES |
|
| InChI |
|
| Beilstein | 8137358 |
| Gmelin | 2153410 |
| UN编号 | 1070(壓縮氣體) 2201(液體) |
| ChEBI | 17045 |
| RTECS | QX1350000 |
| DrugBank | DB06690 |
| KEGG | D00102 |
| 性质 | |
| 化学式 | N2O |
| 摩尔质量 | 44.0128 g·mol⁻¹ |
| 外观 | 无色气体 |
| 密度 | 1.2228 g/cm3(液态) 1.8 g/L(气态,标准状态) |
| 熔点 | -90.86 °C (182.29 K) |
| 沸点 | -88.48 °C (184.67 K) |
| 溶解性(水) | 0.15 g/100 ml (15 °C) |
| 溶解性 | 易溶於乙醇,醚,硫酸 |
| log P | 0.35 |
| 蒸氣壓 | 5150 kPa (20 °C) |
| 结构 | |
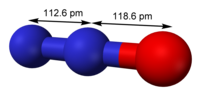
| 分子构型 | 直线型 |
| 偶极矩 | 0.166D |
| 热力学 | |
| ΔfHm⦵298K | +82.05 |
| 药理学 | |
| 妊娠分类 | C(美) |
| 药代动力学: | |
| 5 分钟 | |
| 危险性 | |
| 警示术语 | R:R8 |
| 安全术语 | S:S38 |
| 欧盟编号 | 氧化劑 [O] |
| NFPA 704 | |
| 闪点 | 非易燃 |
| 相关物质 | |
| 相关化学品 | 一氧化氮、二氧化氮、三氧化二氮、四氧化二氮、五氧化二氮、硝酸、亞硝酸 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
一氧化二氮,又稱氧化亞氮(英語:Nitrous oxide),俗称笑气,化学式為N2O,是一種无色有甜味气体,在一定条件下能支持燃烧,但在室温下稳定,有轻微麻醉作用,其麻醉作用于1799年由英国化学家汉弗莱·戴维发现[1]。该气体早期被用于牙科手术的麻醉,現用在外科手術和牙科。“笑氣”的名稱是由於吸入它會感到欣快,并能致人发笑。一氧化二氮能溶于水、乙醇、乙醚及浓硫酸,但不与水反应。它可以用來作為火箭和賽車的氧化劑,以及增加發動機的輸出功率。在食品行业中,氧化亚氮可作为添加剂,用于打发奶泡与制作咖啡。一氧化二氮是强温室气体。现笑气被用在很多娱乐场所[2]。
历史
一氧化二氮最早是在1772年由英国化学家约瑟夫·普利斯特里合成,他将之称为“燃素的亚硝酸气”[3]。普利斯特里将这一发现写进了他的书《不同类型气体的实验与观察》(1775年),在书中他描述了通过加热铁屑和硝酸的混合物来制备这种气体[4]。
18世纪90年代,汉弗莱·戴维和他的朋友,包括诗人柯爾律治和罗伯特·骚塞试验了这种气体。他们發現一氧化二氮能使病人丧失痛觉,而且吸入后仍然可以保持意識,不会神智不清(现代研究表明吸入过量一氧化二氮後会使人神智不清)。
1844年12月11日,一氧化二氮首次被当作麻醉剂在医学治疗中使用,牙医霍勒斯·威尔士在拔牙过程中使用一氧化二氮减轻病人疼痛[5]。
制备
工业生产
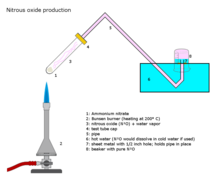
工业上在约250°C的温度下小心加热硝酸铵可以生成一氧化二氮和水蒸汽。[6][7]
添加各种磷酸盐有利于在稍低的温度下形成更纯的气体。该反应可能难以控制,从而导致爆炸。[8]
实验室制备
硝酸铵的分解也是制备气体的常用实验室方法。同样也可以通过加热硝酸钠和硫酸铵的混合物制得:[9]
另一种方法涉及尿素、硝酸和硫酸的反应:[10]
据报道,可用二氧化锰-三氧化二铋催化剂直接氧化氨:[11]参考奥斯特瓦尔德法。
盐酸羟胺与亚硝酸钠反应生成一氧化二氮。如果将亚硝酸盐添加到羟胺溶液中,则唯一剩余的副产物是盐水。但是,如果将羟胺溶液添加到亚硝酸盐溶液中(亚硝酸盐过量),则会形成有毒的高级氮氧化物:
连二次硝酸会分解为一氧化二氮和水,在25°C,pH值1–3时的半衰期为16天。 [12]
結構与性质
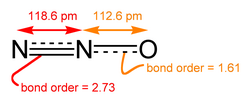
一氧化二氮的分子是直线型结构。其中一个氮原子与另一个氮原子相连,而第二个氮原子又与氧原子相连。它可以被认为是
- 和
的共振杂化体。
一氧化二氮可以被氧化为更高价的氮氧化物,如一氧化氮NO和二氧化氮NO2。
将一氧化二氮与沸腾汽化的碱金属反应可以生成一系列的亚硝酸盐,在高温下,一氧化二氮也可以氧化有机物。
應用
一氧化二氮是一種助燃劑,最初用在幫助二戰時德軍飛機迅速逃離戰場,現今用於改裝汽車上,用於直線加速。
增加車輛速度
使用氮氧加速系统的改裝車輛將一氧化二氮送入引擎,遇熱分解成氮氣和氧氣,提高引擎燃燒率,增加速度。氧气有助燃作用,加快燃料燃烧。
火箭氧化劑
一氧化二氮可以用作火箭氧化劑。比其他氧化劑更好的地方是因為它是無毒的,在室溫下穩定,易於儲存和相對安全地進行飛行。第二個好處是可以很容易分解成幫助呼吸的空氣。
用作麻醉劑
醫生會讓病人吸入一氧化二氮和氧氣,以降低對疼痛的感覺,同時讓病人在清醒狀態。
食品加工
因不易与奶油中的成分发生反应,多用做奶油发泡剂。
安全性
人可能因為在吸入笑氣时氧氣過少而引起突然的窒息。暴露於笑氣中會短時間導致智力,視聽能力,手的靈活度降低。長期接觸可引起維生素B群缺乏症,肌肉麻痺等。
一氧化二氮的主要安全隐患在于,它是一种有分解性的麻醉剂,而且通常以加压液化的形式储存。在正常儲存時,它是很稳定的,使用起来也很安全。但是如果错误地使用,它会很容易分解而且很有可能爆炸。液态的一氧化二氮是有机物的良好溶剂,不过用它制成溶液有可能会生成一些对外界刺激敏感的爆炸性物质。一部分火箭事故由于一氧化二氮被燃料污染而发生,少量的一氧化二氮和燃料的混合物发生爆炸,随即引起剩余一氧化二氮的爆炸性分解。
監管
在中華人民共和國,笑气被列入《危险化学品目录(2015版)》,其仍可被用作食品添加剂以及医用麻醉剂。[13]
与环境的關聯
氮氧化物,当然也包括一氧化二氮,是一类温室气体。因此,氮氧化物是控制温室气体排放时(比如京都议定书)的主要对象。一氧化二氮本身是排在二氧化碳、甲烷之后的第三大温室气体。它所能造成的温室效应的效果大约是二氧化碳的200倍[14][15]。在自然条件下,一氧化二氮主要从土壤和海洋中排出。人类耕作、生产、使用氮肥、生产尼龙还有燃烧化石燃料和其他有机物的过程增加了一氧化二氮的排放量。
參考文獻
- ^ 陳炳聖. 《萬物簡史》. 源樺. 2007. ISBN 986828421X.
- ^ 東方日報. 潮興吸笑氣京酒吧無王管. 2016-07-21 [2017-05-29]. (原始内容存档于2021-07-28).
- ^ Keys, T.E. The Development of Anesthesia. Anesthesiology. 1941, 2 (5): 552–574 [2017-08-26]. Bibcode:1982AmSci..70..522D. doi:10.1097/00000542-194109000-00008. (原始内容存档于2014-01-12).
- ^ Priestley J. Experiments and Observations on Different Kinds of Air 2 (3). 1776 [2017-08-26]. (原始内容存档于2022-05-12).
- ^ Erving, H. W. The Discoverer of Anæsthesia: Dr. Horace Wells of Hartford.. The Yale Journal of Biology and Medicine. 1933, 5 (5): 421–430. PMC 2606479
 . PMID 21433572.
. PMID 21433572.
- ^ Parmon, V. N.; Panov, G. I.; Uriarte, A.; Noskov, A. S. Nitrous oxide in oxidation chemistry and catalysis application and production. Catalysis Today. 2005, 100 (2005): 115–131. doi:10.1016/j.cattod.2004.12.012.
- ^ Holleman, A. F.; Wiberg, E. Inorganic Chemistry. San Diego: Academic Press. 2001. ISBN 978-0-12-352651-9.
- ^ Nitrous oxide plant. Sanghi Organization. [18 December 2013]. (原始内容存档于27 November 2013).
- ^ "Nitrogen Family" (页面存档备份,存于互联网档案馆). chemistry.tutorvista.com
- ^ "Preparation of Nitrous Oxide from Urea, Nitric Acid and Sulfuric Acid" (页面存档备份,存于互联网档案馆).
- ^ Suwa T, Matsushima A, Suziki Y, Namina Y. Manufacture of Nitrous Oxide by the Catalytic Oxidation of Ammonia. The Journal of the Society of Chemical Industry, Japan. 1961, 64 (11): 1879–1888. doi:10.1246/nikkashi1898.64.11_1879
 .
.
- ^ Egon Wiberg, Arnold Frederick Holleman (2001) Inorganic Chemistry, Elsevier ISBN 0-12-352651-5
- ^ 年轻人滥用笑气该怎么管?-新华网. 新华网_让新闻离你更近. 2023-04-13 [2023-09-26]. (原始内容存档于2023-10-25) (中文).
- ^ Manage the Nitrogen Cycle. NAE Grand Challenges for Engineering. National Academy of Engineering. [2021-04-21]. (原始内容存档于2022-08-16).
- ^ Nicole Mortillaro. Nitrous oxide, more harmful to the climate than CO2, increasing in atmosphere, study finds [研究發現 : 比起二氧化碳,在大氣中增加的一氧化二氮對氣候影響更大]. 臺灣氣候變遷推估資訊與調適知識平台計畫. 由李宣融翻译 (CBC News). 2020-10-23 [2022-08-16]. (原始内容存档于2022-08-16).
外部連結
- 從ㄎㄧㄤ掉變癱掉:「毒害」年輕人的笑氣濫用 (页面存档备份,存于互联网档案馆)滲透校園、派對助興,被低估的成癮物質
- 肢體無力竟是吸食「笑氣」!醫:嚴重恐昏迷成植物人、致死 (页面存档备份,存于互联网档案馆)
- 肢體無力 醫師察覺竟是吸食笑氣 長庚呼籲 重視青少年笑氣濫用問題 (页面存档备份,存于互联网档案馆)
- 少女吸「笑氣」神經受損坐輪椅/長庚6年內收治9名青少年患者 最久吸食時間逾6個月 (页面存档备份,存于互联网档案馆)
- 長期吸笑氣恐尿失禁致死 醫籲政府重視青少年濫用問題 (页面存档备份,存于互联网档案馆)
- 吸食笑氣上癮 17歲少女脊髓神經受損,站都站不住 (页面存档备份,存于互联网档案馆)
- 狂吸笑氣成癮 少女神經受損險癱 (页面存档备份,存于互联网档案馆)
- 「笑氣」開趴殺手!1年超過3人猝死 (页面存档备份,存于互联网档案馆)
- Occupational Safety and Health Guideline for Nitrous Oxide
- Paul Crutzen Interview (页面存档备份,存于互联网档案馆) Freeview video of Paul Crutzen Nobel Laureate for his work on decomposition of ozone talking to Harry Kroto Nobel Laureate by the Vega Science Trust.
- National Pollutant Inventory – Oxide of nitrogen fact sheet
- National Institute for Occupational Safety and Health – Nitrous Oxide (页面存档备份,存于互联网档案馆)
- CDC – NIOSH Pocket Guide to Chemical Hazards – Nitrous Oxide (页面存档备份,存于互联网档案馆)
- Nitrous Oxide FAQ (页面存档备份,存于互联网档案馆)
- Erowid article on Nitrous Oxide (页面存档备份,存于互联网档案馆)
- Nitrous oxide fingered as monster ozone slayer (页面存档备份,存于互联网档案馆), Science News
- Dental Fear Central article on the use of nitrous oxide in dentistry (页面存档备份,存于互联网档案馆)










