輪狀病毒
| 輪狀病毒 | |
|---|---|

| |
| 輪狀病毒的電子顯微鏡影像 黑線長度 = 100 nm | |
| 科學分類 | |
| (未分級): | 病毒 Virus |
| 域: | 核糖病毒域 Riboviria |
| 界: | 正核糖病毒界 Orthornavirae |
| 門: | 雙鏈RNA病毒門 Duplornaviricota |
| 綱: | 呼腸孤病毒綱 Resentoviricetes |
| 目: | 呼腸孤病毒目 Reovirales |
| 科: | 呼腸孤病毒科 Reoviridae |
| 亞科: | 無刺突呼腸孤病毒亞科 Sedoreovirinae |
| 屬: | 輪狀病毒屬 Rotavirus |
| 種 | |
| |
| 輪狀病毒腸胃炎 Rotaviral Gastroenteritis | |
|---|---|
| 分類和外部資源 | |
| ICD-11 | XN6N7 |
| ICD-10 | A08.0 |
| ICD-9-CM | 008.61 |
| DiseasesDB | 11667 |
| MedlinePlus | 000252 |
| eMedicine | emerg/401 |
| MeSH | D012400 |
輪狀病毒(Rotavirus,簡稱RV)是一種雙鏈核糖核酸病毒,屬於呼腸孤病毒科。它是引起嬰幼兒腹瀉的最常見原因[1],幾乎每個兒童在約五歲時都經歷至少一次輪狀病毒感染[2]。然而,每一次感染後人體免疫力會逐漸增強,因此之後再次感染的影響就會減輕[3],到成人階段就很少受其影響[4]。輪狀病毒總共有八個種,以英文字母編號為A、B、C、D、E、F、G與H。其中,A種是最為常見的一種,超過90%人類輪狀病毒感染是由該種造成。
輪狀病毒是藉由糞口途徑傳染的。它會感染與小腸壁上的腸黏膜細胞並且產生腸毒素(enterotoxin),腸毒素會引起腸胃炎,導致嚴重的腹瀉,有時候甚至會因為脫水而導致死亡。雖然輪狀病毒於1973年就被由澳洲的露絲·畢夏普所發現[5],而且造成嬰兒與幼兒總計超過50%以上因為嚴重腹瀉而住院治療的案例[6],但是在公共衛生社群中它仍然沒有被廣泛地重視,特別是在開發中國家更是如此[7]。除了對人類健康的影響之外,輪狀病毒也會感染動物,是家畜的病原體之一[8]。
輪狀病毒的治療並不複雜,但每年仍有超過450,000名五歲以下的嬰幼兒因為輪狀病毒的感染而死亡[9],而且每年有幾乎兩百萬以上的兒童因此患重病[7]。在美國實施疫苗施打計畫之前,輪狀病毒每年造成270萬個兒童嚴重腸胃炎的案例,有近60,000名兒童需住院治療,並且每年平均有37個死亡案例[10]。對付輪狀病毒的方式著重於使用口服補液鹽,並且以疫苗接種來防止這種疾病的發生[11]。在疫苗施打實施之後,輪狀病毒的病例即大幅減少[12][13]。
症狀及徵象
[編輯]輪狀病毒腸胃炎是一種中等或重度的急性疾病,會引起噁心、嘔吐、水狀腹瀉,以及低程度的發熱。當兒童受到這類病毒感染時,在症狀發生前大約會有兩天的潛伏期[14]。症狀通常是從嘔吐開始,接著是四到八天的大量腹瀉。輪狀病毒感染比起其他細菌性腸胃炎更容易引起脫水的現象,也是輪狀病毒感染的最常見的死因[15]。
每個人終其一生都可能受到A種輪狀病毒的感染。初次感染通常會產生症狀,再次感染則通常只產生輕微症狀或沒有症狀[4][16],因為免疫系統提供了部分的保護機制[2][17]。所以,感染症狀發生的比例於兩歲以下的兒童最高,之後漸漸降低直到45歲為止[18][19][20]。雖然新生兒感染的機會很常見,但是通常都是溫和的症狀或是無症狀疾病[21][22];最嚴重的症狀都會發生在比較大一點的出生六個月到兩歲的小孩,以及發生在有免疫缺陷的小孩身上。大部分的成人因童年時期獲得的免疫力,因此對於輪狀病毒感染影響不大;成人發生的腸胃炎通常是因為其他病因而非輪狀病毒,但是成人的無症狀感染依然在社群中帶有感染症的傳染性[23]。有症狀的再感染通常因為感染了不同血清型的輪狀病毒A種[3][24]。
傳染途徑
[編輯]
輪狀病毒是由糞口路徑(fecal-oral route)所傳染的,藉由與接觸弄髒的手、弄髒的表面以及弄髒的物體來傳染[25],而且有可能經由呼吸路徑傳染[1]。受感染病患的糞便每克可以包含超過10兆[26]個有傳染性的病毒顆粒[4];而其中只要10顆到100顆就可以藉由傳播而感染另一個人[27]。
輪狀病毒在自然環境中是穩定的,也可以在河口的樣本中發現,其樣本大概每美制加侖可以發現1至5顆有傳染性的輪狀病毒顆粒[28]。消滅細菌與寄生蟲的衛生設備似乎對於輪狀病毒的控制是無效的,因為在高衛生水平與低衛生水平的國家中,輪狀病毒感染的發病率是相似的[1]。
致病機轉
[編輯]
腹瀉是肇因於輪狀病毒的多重活動。輪狀病毒主要複製於消化道[29],並感染腸絨毛的腸細胞,造成上皮組織結構和功能上的改變[30],遭到該病毒的破壞而導致吸收不良。產生腸毒素的病毒蛋白質NSP4製造了倚賴鈣離子的氯化分泌物,破壞了鈉-葡萄糖協同運輸蛋白1(sodium-glucose transport 1,SGLT1)載體[31]居中調節的水份再吸收,這個顯然降低了刷狀緣(brush border)薄膜雙醣酵素(disaccharidase)的活動,而且可能激化腸神經系統中依賴鈣離子的分泌(secretion)的反射作用[32][33]。健康的腸黏膜細胞會分泌乳糖酶進入小腸;所以因乳糖酶缺乏而造成的乳糖不耐症也是輪狀病毒感染經常出現的症狀[34][35],這個症狀可以持續數週[36]。乳糖不耐症的再次發生通常與牛奶再次引入兒童的日常飲食有關,因為細菌發酵了在肚子內的雙醣乳糖[37]。
診斷與檢測
[編輯]輪狀病毒感染的診斷一般都伴隨著有嚴重的腹瀉症狀的腸胃炎。大部分的因為腸胃炎進入醫院的兒童病患都被檢測出輪狀病毒A種[38][39]。對於輪狀病毒A種傳染病的專門診斷方式是對病患的糞便利用酵素免疫分析法去作病毒的識別。目前市場上已經有幾種核准的監測設備,這些監測設備對於輪狀病毒A種的所有血清型都可以敏感,個別的檢測出來[40][41]。其他的檢驗方法,如電子顯微鏡法或是凝膠電泳法,則是使用在研究實驗室之中[42]。逆轉錄聚合酶鏈鎖反應(RT-PCR)可以檢測並識別所有種與所有血清型的人類輪狀病毒[43]。
治療與預後
[編輯]劇烈的輪狀病毒感染症的治療方法並不特別,這包括了症狀的控制與最重要的補充水分(Rehydration)[11]。如果沒有治療,兒童可能會因為嚴重脫水而死亡[44]。依據腹瀉的嚴重度,治療包含使用口服補液鹽作為口服補液療法。[45]。有一些感染症狀較為嚴重,足以住院治療,住院治療時這些液體則是經由靜脈滴入或是經由鼻胃管(nasogastric tube)進入病童身體,而病童的電解質與血糖必須要特別注意[38]。
輪狀病毒感染很少造成其他的併發症,而且對於症狀控制良好的兒童來說,預後是極佳的[46][47]。極少數的報告有出現在中樞神經系統(CNS)的併發症案例,在中樞神經系統中的液體中發現了輪狀病毒,並且引起了腦炎與腦膜炎[48][49][50],而近期的研究結果也確認了輪狀病毒並不會永遠只限制在內臟裡,還可能會引起病毒血症(viremia)[51]。
流行病學
[編輯]
在全世界各地流行的輪狀病毒A種據統計是人類輪狀病毒腸胃炎案例中超過90%以上的病媒[52],每年輪狀病毒在開發中國家造成上億的腹瀉案例,有接近200萬的病患住院治療[7],而且據估計有611,000的死亡案例[53]。單獨就美國而言,平均每年就發生超過270萬件輪狀病毒腸胃炎的案例,約60,000的病童必須住院治療,而且有37名病童因為這個病毒感染症而死亡[10]。而輪狀病毒是引起腹瀉的主要角色並沒有受到廣泛的被公共衛生社群所承認,特別是開發中國家[7]。幾乎每個兒童在五歲以前都曾感染過輪狀病毒[53]。它是嬰兒與幼兒嚴重腹瀉的主要單一原因,其中大約20%的嬰幼兒腹瀉案例是歸因於此,而統計大約50%的案例需要住院治療[7]。男孩住院治療的案例為女孩住院治療的兩倍[6][54]。
| 國家 | 死亡率或其範圍 | 資料年份 | 資料來源 |
|---|---|---|---|
| 越南 | 1/61 至 1/113 | 2006 | [55] |
| 孟加拉 | 1/390 至 1/660 | 2007 | [56] |
| 委內瑞拉 | 1/1800 | 2007 | [57] |
| 歐盟 | 1/20433 | 2006 | [58] |
| 美國 | 1/21675 | 2007 | [10] |
在溫帶地區,輪狀病毒感染症主要發生於冬季,但是在熱帶地區則是一年全年都會發生[59];其中的不同之處有部分可以用溫帶地區溫度與溼度季節性的變化來解釋[60][61]。對於可歸因食物污染的數據尚未清楚[62]。
輪狀病毒A種腹瀉經常在醫院的嬰兒、參加托兒所的幼兒,以及在照養中心的老人之間爆發。1981年在美國科羅拉多州發生一次因為市區飲用水遭到污染而爆發大規模輪狀病毒感染[63]。而在2005年期間,紀錄上最大的腹瀉大規模傳染病疫情發生在尼加拉瓜。這次不尋常大且嚴重的疫情爆發是伴隨著輪狀病毒A種基因突變,也許這幫助了病毒逃離了民眾體內普遍免疫力的保護[64]。另外一次類似的流行性大爆發則是發生在1977年的巴西[65]。
輪狀病毒B種,也稱為成人腹瀉輪狀病毒(adult diarrhoea rotavirus,ADRV),造成影響上千名中國各年齡層人民的嚴重腹瀉大規模傳染病。這些已經發生的傳染病都是因為污水污染了飲用水的結果[66][67]。輪狀病毒B種感染也發生在1998年的印度;這次成因的病毒株被命名為CAL,不像ADRV,CAL病毒株是地方性的[68][69]。目前為止,因為輪狀病毒B種引起的流行病已經被限制在中國大陸,但是研究指出美國普遍缺乏對於該種病毒的免疫力[70]。
輪狀病毒C種出現在許多國家中的小孩腹瀉的極少數偶發案例中,但是在日本與英格蘭曾經爆發過大規模流行[71][72]。
預防方法
[編輯]於2006年,兩種對抗輪狀病毒A種感染的疫苗已經證明對兒童是安全而且有效的:分別是由葛蘭素史克製造的「羅特律」(Rotarix)[73]與由默克大藥廠製造的「輪達停」(RotaTeq)[74]。兩種疫苗皆是用口服接種,並且都包含了無作用力的活病毒。輪狀病毒疫苗目前在澳洲[75]、歐洲、加拿大[76]、巴西[77]、埃及、印度、以色列、台灣、南非[78]、巴拿馬、阿根廷與美國[79]等地都可以取得。
輪狀病毒疫苗計畫(Rotavirus Vaccine Program)是一個適宜衛生科技組織(Program for Appropriate Technology in Health,簡寫為 PATH)、世界衛生組織與美國疾病控制與預防中心的合作計畫,該計畫由全球疫苗與免疫聯盟(GAVI Alliance)資助。該計畫的目的是藉由製造可以讓開發中國家使用的輪狀病毒疫苗,來降低兒童因為痢疾而產生的疾病與兒童死亡率[80]。
動物的感染
[編輯]輪狀病毒也會感染年幼的動物並造成腹瀉。各項研究顯示,輪狀病毒會感染哺乳動物(如:猿猴[81]、牛[82]、豬[83]、羊[8]、田鼠[84]、貓與狗[85]、家鼠[86]、馬[87]與兔子[88]等)以及鳥類(雞與火雞等)[89]等。這些感染動物的輪狀病毒是有與感染人類的輪狀病毒產生基因交換的潛在可能性。目前已經證明感染動物的輪狀病毒也可以感染人類,感染途徑包括病毒的直接傳染以及提供感染人類的病毒株一段或是數段的核糖核酸片段來進行基因重整(reassortment)[90][91]。輪狀病毒是家畜的病原體之一,並且治療的費用、家畜的高罹病率與高死亡率都會造成農人的經濟損失[8]。
病毒學
[編輯]輪狀病毒的種類
[編輯]輪狀病毒總共有七種,分別以英文字母編號為A、B、C、D、E、F與G等。人類主要是受到輪狀病毒A種、B種與C種的感染,而其中最常見的是輪狀病毒A種的感染。而這七種輪狀病毒都會在其他動物身上造成疾病[92]。
在輪狀病毒A種之中有不同的病毒株,稱之為血清變異株(serovar)[93]。與流行性感冒病毒類似,輪狀病毒使用了雙重的分類系統,這樣分類法是依據這個病毒體表面的兩個結構性蛋白質來作分類的。糖蛋白VP7定義了G型而對於蛋白酶敏感的蛋白質VP4則定義了P型(這些蛋白質的細節請見下文)。P型會以一個數字來標示出P血清型,並用方括弧內部的一個數字來標示所對應的P基因型。G血清型的表示方法很類似,但是G基因型的數字會與G血清型的數字相同。舉個例來說,「輪狀病毒Wa病毒株」(rotavirus strain Wa)就會被標示成「P1A[8]G1」[94]。因為這兩個決定G型跟P型的基因可以被分開傳送而產生後代,所以兩基因不同的組合就會產生各種不同的病毒株[95]。
結構
[編輯]輪狀病毒的基因組包括了11條獨特的核糖核酸雙螺旋分子,這11條中總共有18,555個核苷鹼基對。每一條螺旋或是分段即是一個基因,並且依照分子尺寸由大到小依次編號為1到11。每一個基因都可以編碼成一種蛋白質,而其中第9基因與第11基因比較特別,它們都可以編碼成兩種蛋白質[96]。核糖核酸外圍則是包圍了三層二十面體的蛋白質殼體。病毒顆粒大約直徑76.5 nm[97][98],並且並沒有病毒包膜(Viral envelope)。
蛋白質
[編輯]有六個病毒蛋白質(viral protein,VP)架構了整個病毒顆粒(病毒體)。這些「結構性」的蛋白質分別被稱為VP1、VP2、VP3、VP4、VP6與VP7。除了這些結構性蛋白質之外,還有六個非結構性蛋白質(nonstructural protein,NSP),這六個蛋白質僅僅在輪狀病毒感染的細胞中製造,而沒有構成病毒體的結構。這六個非結構性蛋白質分別稱為NSP1、NSP2、NSP3、NSP4、NSP5與NSP6。
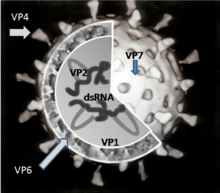
由輪狀病毒基因組所編碼的12個蛋白質中,至少6個會與核糖核酸結合[99]。這些蛋白質在輪狀病毒複製時所扮演的角色目前還沒有完全被了解;它們的功用被認為有可能是與病毒體內核糖核酸的合成與包裝相關,或是與將信使核糖核酸輸送至基因體複製現場相關,或是與信使核糖核酸轉譯與基因表現調節相關[100]。
結構性蛋白
[編輯]VP1蛋白質位於病毒體核心,是一種核糖核酸聚合酶[101]。在被感染的細胞中,這種酶會產生病毒蛋白質合成所需的信使核糖核酸轉錄複本,以及產生輪狀病毒基因體核糖核酸片段拷貝來提供新產生的病毒體使用。
VP2蛋白質形成病毒體的核心層,並且結合核糖核酸基因體[102]。
VP3蛋白質是病毒體內核的一部分,而且是一種稱為鳥苷酸轉移酶(guanylyl transferase)的酶。這種酶是一種加帽酶(Capping enzyme),也就是製作信使核糖核酸轉錄後修飾時候所用的5'端帽的酶[103]。這個5'端帽保護病毒的信使核糖核酸免受核酸酶(以核酸為底物的水解酶)水解,使之能夠保持穩定。
VP4蛋白質位於病毒體的表面,突出來而成為一個刺突(spike)[104]。它連接細胞表面的受體分子,並且驅使病毒進入那個細胞[105]。在病毒有傳染性之前,VP4蛋白質會被一種可以在內臟發現的蛋白酶改變成VP5*蛋白質與VP8*蛋白質[106]。VP4蛋白質決定了該病毒的毒性(Virulence),而它也決定了該病毒的P型[107]。

VP6蛋白質形成殼體的體積。它是抗原性強的蛋白質,並且可以被用來分辨輪狀病毒的種類[4]。這個蛋白質被實驗室用來進行輪狀病毒A種感染症的各種測試上[41]。
VP7蛋白質是一種建立病毒體外層表面的糖蛋白。扣除掉它在病毒結構上的功用之外,它也決定該病毒珠的G型。VP7蛋白質跟VP4蛋白質一樣,都被免疫力(immunity)當作是防止感染的途徑[97]。
病毒的非結構性蛋白
[編輯]NSP1蛋白質是第5號基因的產物,是一種非結構性蛋白質,而且也是核糖核酸結合蛋白質(RNA-binding protein)[108]。
NSP2蛋白質是一種核糖核酸結合蛋白質,此種蛋白質會堆積於細胞質內含物(即病毒質,viroplasm)之中,並且是一種基因體複製時所需的蛋白質[109][110]。
NSP3蛋白質受到感染細胞中的病毒信使核糖核酸影響,它負責停止細胞蛋白質合成的工作[111]。
NSP4蛋白質是一種病毒性腸毒素(enterotoxin),會引起腹瀉的症狀。此蛋白質是首種發現的病毒性腸毒素[112]。
NSP5蛋白質是由輪狀病毒A種基因體第11號基因編碼的產物。而在受病毒感染的細胞中,NSP5蛋白質堆積在病毒質中[113]。
NSP6蛋白質是一個結合核酸的蛋白質[114],是由第11號基因於開放閱讀框架階段的編碼產物[115]。
| 核糖核酸片段 (基因) |
尺寸 (鹼基對數) |
蛋白質 | 分子量 (kDa) |
所在位置 | 功用 |
|---|---|---|---|---|---|
| 1 | 3302 | VP1 | 125 | 位於核心的頂點 | 核醣核酸依賴性的核醣核酸聚合酶(RdRp) |
| 2 | 2690 | VP2 | 102 | 形成核心的內殼 | 刺激病毒的核糖核酸複製酶 |
| 3 | 2591 | VP3 | 88 | 位於核心的頂點 | 鳥苷酸轉移酶,信使核糖核酸加帽酶 |
| 4 | 2362 | VP4 | 87 | 表面刺突 | 細胞附著,毒性 |
| 5 | 1611 | NSP1 | 59 | 非結構性 | 對於病毒成長非必須 |
| 6 | 1356 | VP6 | 45 | 內殼體 | 結構性與物種特殊性的抗原 |
| 7 | 1104 | NSP3 | 37 | 非結構性 | 強化病毒信使核糖核酸的活性,並停止受感染細胞的蛋白質合成 |
| 8 | 1059 | NSP2 | 35 | 非結構性 | 包含在核糖核酸包裝中的核苷三磷酸酶(NTPase) |
| 9 | 1062 | VP71 VP72 |
38 34 |
表面 | 結構性與中和抗原 |
| 10 | 751 | NSP4 | 20 | 非結構性 | 腸毒素 |
| 11 | 667 | NSP5 NSP6 |
22 | 非結構性 | 結合NSP2調節因子的單鏈核糖核酸與雙鏈核糖核酸 |
該表的資料是基於感染類人猿的輪狀病毒SA11病毒株所編寫[116][117]。在不同的病毒株中,核糖核酸與蛋白質之間的編碼預測會有所不同。
複製
[編輯]
輪狀病毒感染小腸絨毛(villi)的腸黏膜細胞,改變上皮組織的結構與功能[30]。輪狀病毒的三重蛋白質外層使它們可以抵抗胃中的胃酸以及消化系統中的消化酶(digestive enzyme)。
病毒藉由受體媒介的內吞作用進入細胞,並且形成一個稱作核內體(endosome)的囊泡。輪狀病毒第三層的蛋白質(即VP7與VP4刺突)會分解核內體的外膜,而創造一個鈣濃度不同的外膜。這個改變導致了VP7蛋白質三聚體破裂為一個單一蛋白質的子單元,留下圍繞在病毒雙鏈核糖核酸外面的VP2與VP6蛋白質,形成雙層構造的病毒顆粒(DLP)。
七條雙鏈核糖核酸鏈依舊維持兩層蛋白質層,並提供病毒核醣核酸依賴性的核醣核酸聚合酶(RNA replicase或RNA-dependent RNA polymerase,RdRp)創造雙鏈病毒基因體的信使核糖核酸轉錄複本的保護。藉由把病毒核醣核酸保持於病毒核心,病毒核醣核酸躲避了先天宿主的免疫反應。這個免疫反應稱為核醣核酸干擾,會因為雙鏈核糖核酸鏈的表現而觸發。
在感染的過程中,輪狀病毒產生信使核糖核酸來生物合成蛋白質並且進行基因複製。大部分的輪狀病毒蛋白質都堆積在病毒質中,病毒質也是核糖核酸複製的地方,以及雙層構造病毒顆粒組裝的地方。病毒質於病毒感染細胞約兩個小時之內就會快速地在細胞核周圍形成,而組成所謂的「病毒工廠」,這個病毒工廠是由兩個病毒非結構性蛋白質(NSP5與NSP2)所製成。NSP5蛋白質如果因為核醣核酸干擾而被壓抑功能,會明顯地減弱輪狀病毒複製功能。新生的雙層構造病毒顆粒則會移動到內質網,它們將在此處獲得它們第三層外層(由VP7與VP4蛋白質所構成)。最後,這些後代病毒就會經由細胞裂解(lysis)釋放到細胞之外[118][119]。
發現歷史
[編輯]
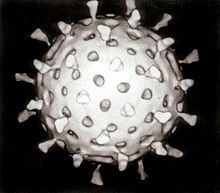
1943年,雅各·萊特(Jacob Light)與荷瑞西·赫德斯(Horace Hodes)證明了在感染傳染性腹瀉的小孩身上有一種濾過性的病媒,這個病媒也會造成家畜腹瀉[120]。30年後,被保存下來的病媒樣本證明此病媒是輪狀病毒[121]。從1943年到1973年間,研究發現老鼠[122]身上的病毒與引起成腹瀉的病毒間有相關性[123]。1973年,位於澳洲的露絲·畢夏普(Ruth Bishop)在兒童腸胃炎的研究報告上描述出類似的病毒[5][124]。
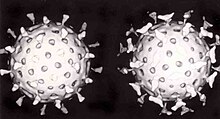
1974年,湯瑪斯·亨利·費留特(Thomas Henry Flewett)在通過電子顯微鏡觀察過這類病毒之後,建議將其命名為「輪狀病毒」(rotavirus),因為輪狀病毒的顆粒看起來很像輪子,而拉丁文中「rota」的意思即為「輪狀」[125][126];這個名稱四年後經由國際病毒分類委員會(International Committee on Taxonomy of Viruses)正式認可[127]。1976年,相關類似的病毒也在許多其他種動物的研究上被描述到[123]。這些被報告描述的病毒,通通都會導致急性腸胃炎,並且被認定為影響全世界人類與動物的集體病原體[125]。輪狀病毒的血清型於1980年首次發表[128],而在隔年,來自人體的輪狀病毒藉由添加胰蛋白酶(一種發現於哺乳動物十二指腸的酶,目前已知是輪狀病毒複製所必須的物質)首次在從自然環境中猴子腎臟取得的細胞培養中成功栽培[129]。成功培養輪狀病毒的能力加速了研究的腳步,且在1980年代中期,首批候選的疫苗已經開始進行評估[130]。
1998年,首種輪狀病毒疫苗(Rotavirus vaccine)[131]獲得在美國使用的執照。在美國、芬蘭與委內瑞拉的臨床試驗發現該疫苗可以對於成功預防輪狀病毒A種所產生的嚴重腹瀉比率高達80%至100%,而研究者也沒有發現顯著的嚴重藥物不良反應[132][133]。然而,在該疫苗被發現會增加腸套疊(即腸梗阻(bowel obstruction)的一種)的風險之後,疫苗製造商在1999年將疫苗從市場上全部撤回,研究顯示每12,000注射過疫苗的嬰兒有一個會有腸套疊的症狀[134]。這次經驗也引發了關於輪狀病毒疫苗的相關風險與益處的激烈爭論[135]。2006年,兩種對抗輪狀病毒A種的新疫苗被證明對兒童是安全而且是有效預防的[136]。
參見
[編輯]- 腸胃炎
- 嬰兒死亡(infant mortality)
- 輪狀病毒轉譯(rotavirus translation)
- 輪狀病毒順式複製元件(rotavirus cis-acting replication element,rotavirus CRE)
注釋與參考文獻
[編輯]- ^ 1.0 1.1 1.2 Dennehy PH. Transmission of rotavirus and other enteric pathogens in the home. Pediatr. Infect. Dis. J. 2000, 19 (10 Suppl): S103–5. PMID 11052397. doi:10.1097/00006454-200010001-00003.
- ^ 2.0 2.1 Velázquez FR, Matson DO, Calva JJ, Guerrero L, Morrow AL, Carter-Campbell S, Glass RI, Estes MK, Pickering LK, Ruiz-Palacios GM. Rotavirus infections in infants as protection against subsequent infections. N. Engl. J. Med. 1996, 335 (14): 1022–8 [2008-12-19]. PMID 8793926. doi:10.1056/NEJM199610033351404. (原始內容存檔於2009-05-18).
- ^ 3.0 3.1 Linhares AC, Gabbay YB, Mascarenhas JD, Freitas RB, Flewett TH, Beards GM. Epidemiology of rotavirus subgroups and serotypes in Belem, Brazil: a three-year study. Ann. Inst. Pasteur Virol. 1988, 139 (1): 89–99. PMID 2849961. doi:10.1016/S0769-2617(88)80009-1.
- ^ 4.0 4.1 4.2 4.3 Bishop RF. Natural history of human rotavirus infection. Arch. Virol. Suppl. 1996, 12: 119–28. PMID 9015109.
- ^ 5.0 5.1 Bishop RF, Davidson GP, Holmes IH, Ruck BJ. Virus particles in epithelial cells of duodenal mucosa from children with acute non-bacterial gastroenteritis. Lancet. 1973, 2 (7841): 1281–3. PMID 4127639. doi:10.1016/S0140-6736(73)92867-5.
- ^ 6.0 6.1 Rheingans RD, Heylen J, Giaquinto C. Economics of rotavirus gastroenteritis and vaccination in Europe: what makes sense?. Pediatr. Infect. Dis. J. 2006, 25 (1 Suppl): S48–55. PMID 16397429. doi:10.1097/01.inf.0000197566.47750.3d.
- ^ 7.0 7.1 7.2 7.3 7.4 Simpson E, Wittet S, Bonilla J, Gamazina K, Cooley L, Winkler JL. Use of formative research in developing a knowledge translation approach to rotavirus vaccine introduction in developing countries. BMC Public Health. 2007, 7: 281 [2008-12-19]. PMID 17919334. doi:10.1186/1471-2458-7-281. (原始內容存檔於2015-09-24).
- ^ 8.0 8.1 8.2 Holland RE. Some infectious causes of diarrhea in young farm animals. Clin. Microbiol. Rev. 1990, 3 (4): 345–75 [2008-12-19]. PMID 2224836. (原始內容 (PDF)存檔於2011-09-28).
- ^ Tate JE, Burton AH, Boschi-Pinto C, Steele AD, Duque J, Parashar UD. 2008 estimate of worldwide rotavirus-associated mortality in children younger than 5 years before the introduction of universal rotavirus vaccination programmes: a systematic review and meta-analysis. Lancet Infect Dis. February 2012, 12 (2): 136–141. PMID 22030330. doi:10.1016/S1473-3099(11)70253-5.
- ^ 10.0 10.1 10.2 Fischer TK, Viboud C, Parashar U; et al. Hospitalizations and deaths from diarrhea and rotavirus among children <5 years of age in the United States, 1993–2003. J. Infect. Dis. 2007, 195 (8): 1117–25. PMID 17357047. doi:10.1086/512863.
- ^ 11.0 11.1 Diggle L. Rotavirus diarrhoea and future prospects for prevention. Br. J. Nurs. 2007, 16 (16): 970–4. PMID 18026034.
- ^ Giaquinto C, Dominiak-Felden G, Van Damme P, Myint TT, Maldonado YA, Spoulou V, Mast TC, Staat MA. Summary of effectiveness and impact of rotavirus vaccination with the oral pentavalent rotavirus vaccine: a systematic review of the experience in industrialized countries. Human Vaccines. July 2011, 7 (7): 734–48 [2016-04-17]. PMID 21734466. doi:10.4161/hv.7.7.15511. (原始內容存檔於2020-05-04).
- ^ Jiang V, Jiang B, Tate J, Parashar UD, Patel MM. Performance of rotavirus vaccines in developed and developing countries. Human Vaccines. July 2010, 6 (7): 532–42 [2016-04-17]. PMC 3322519
 . PMID 20622508. doi:10.4161/hv.6.7.11278. (原始內容存檔於2020-06-04).
. PMID 20622508. doi:10.4161/hv.6.7.11278. (原始內容存檔於2020-06-04).
- ^ Hochwald C, Kivela L. Rotavirus vaccine, live, oral, tetravalent (RotaShield). Pediatr. Nurs. 1999, 25 (2): 203–4, 207. PMID 10532018.
- ^ Maldonado YA, Yolken RH. Rotavirus. Baillieres Clin. Gastroenterol. 1990, 4 (3): 609–25. PMID 1962726. doi:10.1016/0950-3528(90)90052-I.
- ^ Glass RI, Parashar UD, Bresee JS, Turcios R, Fischer TK, Widdowson MA, Jiang B, Gentsch JR. Rotavirus vaccines: current prospects and future challenges. Lancet. July 2006, 368 (9532): 323–32. PMID 16860702. doi:10.1016/S0140-6736(06)68815-6.
- ^ Offit PA. Gastroenteritis viruses. New York: Wiley. 2001: 106–124. ISBN 0-471-49663-4.
- ^ Ramsay M and Brown D. Desselberger, U.; Gray, James , 編. Rotaviruses: methods and protocols. Totowa, NJ: Humana Press. 2000: 217. ISBN 0-89603-736-3.Free ebook [1] (頁面存檔備份,存於網際網路檔案館)
- ^ Bernstein DI, Sander DS, Smith VE, Schiff GM, Ward RL. Protection from rotavirus reinfection: 2-year prospective study. J. Infect. Dis. 1991, 164 (2): 277–83. PMID 1649875.
- ^ Koopman JS, Monto AS. The Tecumseh Study. XV: Rotavirus infection and pathogenicity. Am. J. Epidemiol. 1989, 130 (4): 750–9. PMID 2549788.
- ^ Cameron DJ, Bishop RF, Veenstra AA, Barnes GL. Noncultivable viruses and neonatal diarrhea: Fifteen-month survey in a newborn special care nursery. J. Clin. Microbiol. 1978, 8 (1): 93–8 [2008-12-20]. PMID 209058. (原始內容 (PDF)存檔於2011-09-27).
- ^ Grillner L, Broberger U, Chrystie I, Ransjö U. Rotavirus infections in newborns: an epidemiological and clinical study. Scand. J. Infect. Dis. 1985, 17 (4): 349–55. PMID 3003889.
- ^ Hrdy DB. Epidemiology of rotaviral infection in adults. Rev. Infect. Dis. 1987, 9 (3): 461–9. PMID 3037675.
- ^ De Champs C, Laveran H, Peigue-Lafeuille H; et al. Sequential rotavirus infections: characterization of serotypes and electrophoretypes. Res. Virol. 1991, 142 (1): 39–45. PMID 1647052. doi:10.1016/0923-2516(91)90026-Y.
- ^ Butz AM, Fosarelli P, Dick J, Cusack T, Yolken R. Prevalence of rotavirus on high-risk fomites in day-care facilities. Pediatrics. 1993, 92 (2): 202–5. PMID 8393172.
- ^ 即1013
- ^ Graham DY, Dufour GR, Estes MK. Minimal infective dose of rotavirus. Arch. Virol. 1987, 92 (3–4): 261–71. PMID 3028333. doi:10.1007/BF01317483.
- ^ Rao VC, Seidel KM, Goyal SM, Metcalf TG, Melnick JL. Isolation of enteroviruses from water, suspended solids, and sediments from Galveston Bay: survival of poliovirus and rotavirus adsorbed to sediments. Appl. Environ. Microbiol. 1984, 48 (2): 404–9 [2008-12-21]. PMID 6091548. (原始內容 (PDF)存檔於2011-09-27).
- ^ Greenberg HB, Estes MK. Rotaviruses: from pathogenesis to vaccination. Gastroenterology. 2009, 136 (6): 1939–51. PMC 3690811
 . PMID 19457420. doi:10.1053/j.gastro.2009.02.076.
. PMID 19457420. doi:10.1053/j.gastro.2009.02.076.
- ^ 30.0 30.1 Greenberg HB, Clark HF, Offit PA. Rotavirus pathology and pathophysiology. Ramig RF (編). Rotaviruses. Current Topics in Microbiology and Immunology 185. New York: Springer. 1994: 255–83. ISBN 9783540567615. PMID 8050281. doi:10.1007/978-3-642-78256-5_9.
- ^ 即膜運輸蛋白(membrane transport protein)
- ^ Ball JM, Mitchell DM, Gibbons TF, Parr RD. Rotavirus NSP4: a multifunctional viral enterotoxin. Viral Immunol. 2005, 18 (1): 27–40. PMID 15802952. doi:10.1089/vim.2005.18.27.
- ^ Lorrot M, Vasseur M. How do the rotavirus NSP4 and bacterial enterotoxins lead differently to diarrhea?. Virol. J. 2007, 4: 31 [2008-12-21]. PMID 17376232. doi:10.1186/1743-422X-4-31. (原始內容存檔於2011-09-28).
- ^ Jourdan N, Brunet JP, Sapin C; et al. Rotavirus infection reduces sucrase-isomaltase expression in human intestinal epithelial cells by perturbing protein targeting and organization of microvillar cytoskeleton. J. Virol. 1998, 72 (9): 7228–36 [2008-12-21]. PMID 9696817. (原始內容存檔於2011-09-28).
- ^ Davidson GP, Barnes GL. Structural and functional abnormalities of the small intestine in infants and young children with rotavirus enteritis. Acta. Paediatr. Scand. 1979, 68 (2): 181–6. PMID 217231. doi:10.1111/j.1651-2227.1979.tb04986.x.
- ^ Ouwehand A, Vesterlund S. Health aspects of probiotics. IDrugs. 2003, 6 (6): 573–80. PMID 12811680.
- ^ Arya SC. Rotaviral infection and intestinal lactase level. J. Infect. Dis. 1984, 150 (5): 791. PMID 6436397.
- ^ 38.0 38.1 Patel MM, Tate JE, Selvarangan R; et al. Routine laboratory testing data for surveillance of rotavirus hospitalizations to evaluate the impact of vaccination. Pediatr. Infect. Dis. J. 2007, 26 (10): 914–9. PMID 17901797.
- ^ The Pediatric ROTavirus European CommitTee (PROTECT). The paediatric burden of rotavirus disease in Europe. Epidemiol. Infect. 2006, 134 (5): 908–16. PMID 16650331. doi:10.1017/S0950268806006091.
- ^ Smith TF, Wold AD, Espy MJ, Marshall WF. New developments in the diagnosis of viral diseases. Infect. Dis. Clin. North Am. 1993, 7 (2): 183–201. PMID 8345165.
- ^ 41.0 41.1 Beards GM, Campbell AD, Cottrell NR, Peiris JS, Rees N, Sanders RC, Shirley JA, Wood HC, Flewett TH. Enzyme-linked immunosorbent assays based on polyclonal and monoclonal antibodies for rotavirus detection. J. Clin. Microbiol. 1984, 19 (2): 248–54 [2008-12-21]. PMID 6321549. (原始內容 (PDF)存檔於2011-09-27).
- ^ Beards GM. Laboratory diagnosis of viral gastroenteritis. Eur. J. Clin. Microbiol. Infect. Dis. 1988, 7 (1): 11–3. PMID 3132369. doi:10.1007/BF01962164.
- ^ Fischer TK, Gentsch JR. Rotavirus typing methods and algorithms. Rev. Med. Virol. 2004, 14 (2): 71–82. PMID 15027000. doi:10.1002/rmv.411.
- ^ Alam NH, Ashraf H. Treatment of infectious diarrhea in children. Paediatr. Drugs. 2003, 5 (3): 151–65. PMID 12608880.
- ^ Sachdev HP. Oral rehydration therapy. Journal of the Indian Medical Association. 1996, 94 (8): 298–305. PMID 8855579.
- ^ Haffejee IE. The pathophysiology, clinical features and management of rotavirus diarrhoea. Q. J. Med. 1991, 79 (288): 289–299 [2008-12-21]. PMID 1649479. (原始內容存檔於2008-12-18).
- ^ Ramig RF. Systemic rotavirus infection. Expert review of anti-infective therapy. 2007, 5 (4): 591–612. PMID 17678424. doi:10.1586/14787210.5.4.591.
- ^ Goto T, Kimura H, Numazaki K; et al. A case of meningoencephalitis associated with G1P[8] rotavirus infection in a Japanese child. Scand. J. Infect. Dis. 2007, 39 (11): 1067–70. PMID 17852929. doi:10.1080/00365540701466249.
- ^ Kehle J, Metzger-Boddien C, Tewald F, Wald M, Schüürmann J, Enders G. First case of confirmed rotavirus meningoencephalitis in Germany. Pediatr. Infect. Dis. J. 2003, 22 (5): 468–70. PMID 12797316. doi:10.1097/00006454-200305000-00020.
- ^ Pager C, Steele D, Gwamanda P, Driessen M. A neonatal death associated with rotavirus infection—detection of rotavirus dsRNA in the cerebrospinal fluid. S. Afr. Med. J. 2000, 90 (4): 364–5. PMID 10957919.
- ^ Widdowson MA, Bresee JS, Gentsch JR, Glass RI. Rotavirus disease and its prevention. Curr. Opin. Gastroenterol. 2005, 21 (1): 26–31 [2008-12-21]. PMID 15687881. (原始內容存檔於2012-02-09).
- ^ Leung AK, Kellner JD, Davies HD. Rotavirus gastroenteritis. Adv. Ther. 2005, 22 (5): 476–87. PMID 16418157. doi:10.1007/BF02849868.
- ^ 53.0 53.1 Parashar UD, Gibson CJ, Bresse JS, Glass RI. Rotavirus and severe childhood diarrhea. Emerging Infect. Dis. 2006, 12 (2): 304–6. PMID 16494759.
- ^ Ryan MJ, Ramsay M, Brown D, Gay NJ, Farrington CP, Wall PG. Hospital admissions attributable to rotavirus infection in England and Wales. J. Infect. Dis. 1996,. 174 Suppl 1: S12–8. PMID 8752285.
- ^ Anh DD, Thiem VD, Fischer TK, Canh DG, Minh TT, Tho le H, Van Man N, Luan le T, Kilgore P, von Seidlein L, Glass RI. The burden of rotavirus diarrhea in Khanh Hoa Province, Vietnam: baseline assessment for a rotavirus vaccine trial. Pediatr. Infect. Dis. J. 2006, 25 (1): 37–40. PMID 16395100. doi:10.1097/01.inf.0000195635.05186.52.
- ^ Tanaka G, Faruque AS, Luby SP, Malek MA, Glass RI, Parashar UD. Deaths from rotavirus disease in Bangladeshi children: estimates from hospital-based surveillance. Pediatr. Infect. Dis. J. 2007, 26 (11): 1014–8. PMID 17984808.
- ^ Pérez-Schael I, Salinas B, González R, Salas H, Ludert JE, Escalona M, Alcalá A, Rosas MA, Materán M. Rotavirus mortality confirmed by etiologic identification in Venezuelan children with diarrhea. Pediatr. Infect. Dis. J. 2007, 26 (5): 393–7. PMID 17468648. doi:10.1097/01.inf.0000260252.48129.86.
- ^ Soriano-Gabarró M, Mrukowicz J, Vesikari T, Verstraeten T. Burden of rotavirus disease in European Union countries. Pediatr. Infect. Dis. J. 2006, 25 (1 Suppl): S7–S11. PMID 16397431. doi:10.1097/01.inf.0000197622.98559.01.
- ^ Cook SM, Glass RI, LeBaron CW, Ho MS. Global seasonality of rotavirus infections. Bull. World Health Organ. 1990, 68 (2): 171–7. PMID 1694734.
- ^ Moe K, Harper GJ. The effect of relative humidity and temperature on the survival of bovine rotavirus in aerosol. Arch. Virol. 1983, 76 (3): 211–6. PMID 6307226. doi:10.1007/BF01311105.
- ^ Moe K, Shirley JA. The effects of relative humidity and temperature on the survival of human rotavirus in faeces. Arch. Virol. 1982, 72 (3): 179–86. PMID 6287970. doi:10.1007/BF01348963.
- ^ Koopmans M, Brown D. Seasonality and diversity of Group A rotaviruses in Europe. Acta paediatrica (Oslo, Norway : 1992). Supplement. 1999, 88 (426): 14–9. PMID 10088906. doi:10.1111/j.1651-2227.1999.tb14320.x.
- ^ Hopkins RS, Gaspard GB, Williams FP, Karlin RJ, Cukor G, Blacklow NR. A community waterborne gastroenteritis outbreak: evidence for rotavirus as the agent. American Journal of Public Health. 1984, 74 (3): 263–5. PMID 6320684.[失效連結]
- ^ Bucardo F, Karlsson B, Nordgren J; et al. Mutated G4P[8] rotavirus associated with a nationwide outbreak of gastroenteritis in Nicaragua in 2005. J. Clin. Microbiol. 2007, 45 (3): 990–7 [2008-12-21]. PMID 17229854. doi:10.1128/JCM.01992-06. (原始內容存檔於2011-09-27).
- ^ Linhares AC, Pinheiro FP, Freitas RB, Gabbay YB, Shirley JA, Beards GM. An outbreak of rotavirus diarrhea among a non-immune, isolated South American Indian community. Am. J. Epidemiol. 1981, 113 (6): 703–10. PMID 6263087.
- ^ Hung T, Chen GM, Wang CG; et al. Waterborne outbreak of rotavirus diarrhea in adults in China caused by a novel rotavirus. Lancet. 1984, 1 (8387): 1139–42. PMID 6144874.
- ^ Fang ZY, Ye Q, Ho MS; et al. Investigation of an outbreak of adult diarrhea rotavirus in China. J. Infect. Dis. 1989, 160 (6): 948–53. PMID 2555422.
- ^ Kelkar SD, Zade JK. Group B rotaviruses similar to strain CAL-1, have been circulating in Western India since 1993. Epidemiol. Infect. 2004, 132 (4): 745–9. PMID 15310177. doi:10.1017/S0950268804002171.
- ^ Ahmed MU, Kobayashi N, Wakuda M, Sanekata T, Taniguchi K, Kader A, Naik TN, Ishino M, Alam MM, Kojima K, Mise K, Sumi A. Genetic analysis of group B human rotaviruses detected in Bangladesh in 2000 and 2001. J. Med. Virol. 2004, 72 (1): 149–55. PMID 14635024. doi:10.1002/jmv.10546.
- ^ Penaranda ME, Ho MS, Fang ZY; et al. Seroepidemiology of adult diarrhea rotavirus in China, 1977 to 1987. J. Clin. Microbiol. 1989, 27 (10): 2180–3 [2008-12-21]. PMID 2479654. (原始內容 (PDF)存檔於2011-09-27).
- ^ Kuzuya M, Fujii R, Hamano M, Nishijima M, Ogura H. Detection and molecular characterization of human group C rotaviruses in Okayama Prefecture, Japan, between 1986 and 2005. J. Med. Virol. 2007, 79 (8): 1219–28. PMID 17596825. doi:10.1002/jmv.20910.
- ^ Brown DW, Campbell L, Tomkins DS, Hambling MH. School outbreak of gastroenteritis due to atypical rotavirus. Lancet. 1989, 2 (8665): 737–8. PMID 2570978. doi:10.1016/S0140-6736(89)90794-0.
- ^ O'Ryan M. Rotarix (RIX4414): an oral human rotavirus vaccine. Expert review of vaccines. 2007, 6 (1): 11–9. PMID 17280473. doi:10.1586/14760584.6.1.11.
- ^ Matson DO. The pentavalent rotavirus vaccine, RotaTeq. Seminars in paediatric infectious diseases. 2006, 17 (4): 195–9. PMID 17055370. doi:10.1053/j.spid.2006.08.005.
- ^ Rotarix vaccine launched in Australia (新聞稿). GlaxoSmithKline. 2006-05-14 [2008-08-18]. (原始內容存檔於2013-04-29).
- ^ RotaTeq Is Approved In Canada (PDF) (新聞稿). Merck Frosst Canada. 2006-08-23 [2008-08-18]. (原始內容 (PDF)存檔於2008-10-02).
- ^ Gurgel RQ, Cunliffe NA, Nakagomi O, Cuevas LE. Rotavirus genotypes circulating in Brazil before national rotavirus vaccination: a review. J. Clin. Virol. September 2008, 43 (1): 1–8 [2008-12-04]. PMID 18567534. doi:10.1016/j.jcv.2008.04.010. (原始內容存檔於2021-02-12).
- ^ The Introduction of Rotavirus Vaccines in South Africa. National Center for Communicable Disease, Johannesburg, South Africa. 2006 [2008-12-21]. (原始內容存檔於2016-08-06).
- ^ Tom-Revzon C. Rotavirus live, oral, pentavalent vaccine. Clin. Ther. 2007, 29 (12): 2724–37. PMID 18201590. doi:10.1016/j.clinthera.2007.12.018.
- ^ Accelerating access to rotavirus vaccines PATH, access date July 22 2008. [2008-12-21]. (原始內容存檔於2009-05-06).
- ^ Ashley CR, Caul EO, Clarke SK, Corner BD, Dunn S. Rotavirus infections of apes. Lancet. 1978, 2 (8087): 477. PMID 79844. doi:10.1016/S0140-6736(78)91485-X.
- ^ Wani SA, Bhat MA, Ishaq SM, Ashrafi MA. Determination of bovine rotavirus G genotypes in Kashmir, India. Rev. - Off. Int. Epizoot. 2004, 23 (3): 931–6. PMID 15861888.
- ^ Saif LJ. Enteric viral infections of pigs and strategies for induction of mucosal immunity. Advances in veterinary medicine. 1999, 41: 429–46. PMID 9890034. doi:10.1016/S0065-3519(99)80033-0.
- ^ Pérez-Cano FJ, Castell M, Castellote C, Franch A. Characterization of Clinical and Immune Response in a Rotavirus Diarrhea Model in Suckling Lewis Rats. Pediatr Res. 2007. PMID 17957154.
- ^ Enriquez C, Nwachuku N, Gerba CP. Direct exposure to animal enteric pathogens. Reviews on environmental health. 2001, 16 (2): 117–31. PMID 11512628.
- ^ Feng N, Franco MA, Greenberg HB. Murine model of rotavirus infection. Adv. Exp. Med. Biol. 1997, 412: 233–40. PMID 9192019.
- ^ Hardy ME, Woode GN, Xu ZC; et al. Analysis of serotypes and electropherotypes of equine rotaviruses isolated in the United States. J. Clin. Microbiol. May 1991, 29 (5): 889–93 [2008-12-22]. PMC 269902
 . PMID 1647407. (原始內容存檔於2011-05-25).
. PMID 1647407. (原始內容存檔於2011-05-25).
- ^ Thouless ME, DiGiacomo RF, Deeb BJ, Howard H. Pathogenicity of rotavirus in rabbits. J. Clin. Microbiol. 1988, 26 (5): 943–7 [2008-12-22]. PMID 2838507. (原始內容 (PDF)存檔於2011-09-27).
- ^ Guy JS. Virus infections of the gastrointestinal tract of poultry. Poult. Sci. 1998, 77 (8): 1166–75. PMID 9706084. (原始內容 (PDF)存檔於2008-12-25).
- ^ Müller H, Johne R. Rotaviruses: diversity and zoonotic potential—a brief review. Berl. Munch. Tierarztl. Wochenschr. 2007, 120 (3–4): 108–12. PMID 17416132.
- ^ Cook N, Bridger J, Kendall K, Gomara MI, El-Attar L, Gray J. The zoonotic potential of rotavirus. J. Infect. 2004, 48 (4): 289–302. PMID 15066329. doi:10.1016/j.jinf.2004.01.018.
- ^ Beards GM, Brown DW. The antigenic diversity of rotaviruses: Significance to epidemiology and vaccine strategies. Eur. J. Epidemiol. 1988, 4 (1): 1–11. PMID 2833405. doi:10.1007/BF00152685.
- ^ Santos N, Hoshino Y. Global distribution of rotavirus serotypes/genotypes and its implication for the development and implementation of an effective rotavirus vaccine. Rev. Med. Virol. 2005, 15 (1): 29–56. PMID 15484186. doi:10.1002/rmv.448.
- ^ Desselberger U, Iturriza-Gómara M, Gray JJ. Rotavirus epidemiology and surveillance. Novartis Found. Symp. 2001, 238: 125–47; discussion 147–52. PMID 11444024. doi:10.1002/0470846534.ch9.
- ^ Desselberger U, Wolleswinkel-van den Bosch J, Mrukowicz J, Rodrigo C, Giaquinto C, Vesikari T. Rotavirus types in Europe and their significance for vaccination. Pediatr. Infect. Dis. J. 2006, 25 (1 Suppl.): S30–41 [2008-12-22]. PMID 16397427. doi:10.1097/01.inf.0000197707.70835.f3. (原始內容存檔於2013-05-11).
- ^ Chan WK, Penaranda ME, Crawford SE, Estes MK. Two glycoproteins are produced from the rotavirus neutralization gene. Virology. 1986, 151 (2): 243–52. PMID 3010552. doi:10.1016/0042-6822(86)90046-2.
- ^ 97.0 97.1 Pesavento JB, Crawford SE, Estes MK, Prasad BV. Rotavirus proteins: structure and assembly. Curr. Top. Microbiol. Immunol. 2006, 309: 189–219. PMID 16913048. doi:10.1007/3-540-30773-7_7.
- ^ Prasad BV, Chiu W. Structure of rotavirus. Curr. Top. Microbiol. Immunol. 1994, 185: 9–29. PMID 8050286.
- ^ Patton JT. Structure and function of the rotavirus RNA-binding proteins. J. Gen. Virol. 1995,. 76 (Pt 11): 2633–44. PMID 7595370. doi:10.1099/0022-1317-76-11-2633. (原始內容 (PDF)存檔於2012-12-09).
- ^ Patton JT. Rotavirus RNA replication and gene expression. Novartis Found. Symp. 2001, 238: 64–77; discussion 77–81. PMID 11444036. doi:10.1002/0470846534.ch5.
- ^ Vásquez-del Carpió R, Morales JL, Barro M, Ricardo A, Spencer E. Bioinformatic prediction of polymerase elements in the rotavirus VP1 protein. Biol. Res. 2006, 39 (4): 649–59 [2008-12-22]. PMID 17657346. (原始內容存檔於2017-12-01).
- ^ Arnoldi F, Campagna M, Eichwald C, Desselberger U, Burrone OR. Interaction of rotavirus polymerase VP1 with nonstructural protein NSP5 is stronger than that with NSP2. J. Virol. 2007, 81 (5): 2128–37 [2008-12-22]. PMID 17182692. doi:10.1128/JVI.01494-06. (原始內容存檔於2011-09-28).
- ^ Fresco LD, Buratowski S. Active site of the mRNA-capping enzyme guanylyltransferase from Saccharomyces cerevisiae: similarity to the nucleotidyl attachment motif of DNA and RNA ligases (PDF). Proc. Natl. Acad. Sci. U.S.A. 1994, 91 (14): 6624–8. PMID 8022828. doi:10.1073/pnas.91.14.6624.
- ^ Gardet A, Breton M, Fontanges P, Trugnan G, Chwetzoff S. Rotavirus spike protein VP4 binds to and remodels actin bundles of the epithelial brush border into actin bodies. J. Virol. 2006, 80 (8): 3947–56 [2008-12-22]. PMID 16571811. doi:10.1128/JVI.80.8.3947-3956.2006. (原始內容存檔於2011-09-28).
- ^ Arias CF, Isa P, Guerrero CA, Méndez E, Zárate S, López T, Espinosa R, Romero P, López S. Molecular biology of rotavirus cell entry. Arch. Med. Res. 2002, 33 (4): 356–61. PMID 12234525. doi:10.1016/S0188-4409(02)00374-0.
- ^ Konno T, Suzuki H, Kitaoka S, Sato T, Fukuhara N, Yoshie O, Fukudome K, Numazaki Y. Proteolytic enhancement of human rotavirus infectivity. Clin. Infect. Dis. 1993,. 16 Suppl 2: S92–7. PMID 8384014.
- ^ Hoshino Y, Jones RW, Kapikian AZ. Characterization of neutralization specificities of outer capsid spike protein VP4 of selected murine, lapine, and human rotavirus strains. Virology. 2002, 299 (1): 64–71. PMID 12167342. doi:10.1006/viro.2002.1474.
- ^ Hua J, Mansell EA, Patton JT. Comparative analysis of the rotavirus NS53 gene: conservation of basic and cysteine-rich regions in the protein and possible stem-loop structures in the RNA. Virology. 1993, 196 (1): 372–8. PMID 8395125. doi:10.1006/viro.1993.1492.
- ^ Kattoura MD, Chen X, Patton JT. The rotavirus RNA-binding protein NS35 (NSP2) forms 10S multimers and interacts with the viral RNA polymerase. Virology. 1994, 202 (2): 803–13. PMID 8030243. doi:10.1006/viro.1994.1402.
- ^ Taraporewala ZF, Patton JT. Nonstructural proteins involved in genome packaging and replication of rotaviruses and other members of the Reoviridae. Virus Res. 2004, 101 (1): 57–66. PMID 15010217. doi:10.1016/j.virusres.2003.12.006.
- ^ Poncet D, Aponte C, Cohen J. Rotavirus protein NSP3 (NS34) is bound to the 3' end consensus sequence of viral mRNAs in infected cells. J. Virol. 1993, 67 (6): 3159–65 [2008-12-23]. PMID 8388495. (原始內容 (PDF)存檔於2011-09-28).
- ^ Dong Y, Zeng CQ, Ball JM, Estes MK, Morris AP. The rotavirus enterotoxin NSP4 mobilizes intracellular calcium in human intestinal cells by stimulating phospholipase C-mediated inositol 1,4,5-trisphosphate production. Proc. Natl. Acad. Sci. U.S.A. 1997, 94 (8): 3960–5 [2008-12-23]. PMID 9108087. doi:10.1073/pnas.94.8.3960. (原始內容存檔於2021-02-12).
- ^ Afrikanova I, Miozzo MC, Giambiagi S, Burrone O. Phosphorylation generates different forms of rotavirus NSP5. J. Gen. Virol. 1996,. 77 ( Pt 9): 2059–65. PMID 8811003. doi:10.1099/0022-1317-77-9-2059. (原始內容存檔於2012-05-26).
- ^ Rainsford EW, McCrae MA. Characterization of the NSP6 protein product of rotavirus gene 11. Virus Res. 2007, 130 (1–2): 193–201. PMID 17658646. doi:10.1016/j.virusres.2007.06.011.
- ^ Mohan KV, Atreya CD. Nucleotide sequence analysis of rotavirus gene 11 from two tissue culture-adapted ATCC strains, RRV and Wa. Virus Genes. 2001, 23 (3): 321–9. PMID 11778700. doi:10.1023/A:1012577407824.
- ^ Desselberger U. Rotavirus: basic facts. In Rotaviruses Methods and Protocols. Ed. Gray, J. and Desselberger U. Humana Press, 2000, pp. 1–8. ISBN 0-89603-736-3
- ^ Patton JT. Rotavirus RNA replication and gene expression. In Novartis Foundation. Gastroenteritis Viruses, Humana Press, 2001, pp. 64–81. ISBN 0-471-49663-4
- ^ Jayaram H, Estes MK, Prasad BV. Emerging themes in rotavirus cell entry, genome organization, transcription and replication. Virus Res. 2004, 101 (1): 67–81. PMID 15010218. doi:10.1016/j.virusres.2003.12.007.
- ^ Patton JT, Vasquez-Del Carpio R, Spencer E. Replication and transcription of the rotavirus genome. Curr. Pharm. Des. 2004, 10 (30): 3769–77. PMID 15579070. doi:10.2174/1381612043382620.
- ^ Light JS, Hodes HL. Studies on epidemic diarrhea of the new-born: Isolation of a Filtrable Agent Causing Diarrhea in Calves. Am. J. Public Health Nations Health. 1943, 33 (12): 1451–1454 [2008-12-20]. PMID 18015921. (原始內容存檔於2019-12-16).
- ^ Mebus CA, Wyatt RG, Sharpee RL; et al. Diarrhea in gnotobiotic calves caused by the reovirus-like agent of human infantile gastroenteritis. Infect. Immun. 1976, 14 (2): 471–4 [2008-12-20]. PMID 184047. (原始內容 (PDF)存檔於2011-09-29).
- ^ Rubenstein D, Milne RG, Buckland R, Tyrrell DA. The growth of the virus of epidemic diarrhoea of infant mice (EDIM) in organ cultures of intestinal epithelium. British journal of experimental pathology. 1971, 52 (4): 442–45. PMID 4998842.
- ^ 123.0 123.1 Woode GN, Bridger JC, Jones JM, Flewett TH, Davies HA, Davis HA, White GB. Morphological and antigenic relationships between viruses (rotaviruses) from acute gastroenteritis in children, calves, piglets, mice, and foals. Infect. Immun. 1976, 14 (3): 804–10 [2008-12-20]. PMID 965097. (原始內容 (PDF)存檔於2011-09-29).
- ^ Bishop RF, Davidson GP, Holmes IH, Ruck BJ. Letter: Evidence for viral gastroenteritis. N. Engl. J. Med. 1973, 289 (20): 1096–7. PMID 4742237.
- ^ 125.0 125.1 Flewett TH, Woode GN. The rotaviruses. Arch. Virol. 1978, 57 (1): 1–23. PMID 77663. doi:10.1007/BF01315633.
- ^ Flewett TH, Bryden AS, Davies H, Woode GN, Bridger JC, Derrick JM. Relation between viruses from acute gastroenteritis of children and newborn calves. Lancet. 1974, 2 (7872): 61–3. PMID 4137164. doi:10.1016/S0140-6736(74)91631-6.
- ^ Matthews RE. Third report of the International Committee on Taxonomy of Viruses. Classification and nomenclature of viruses. Intervirology. 1979, 12 (3-5): 129–296. PMID 43850.
- ^ Beards GM, Pilfold JN, Thouless ME, Flewett TH. Rotavirus serotypes by serum neutralisation. J. Med. Virol. 1980, 5 (3): 231–7. PMID 6262451. doi:10.1002/jmv.1890050307.
- ^ Urasawa T, Urasawa S, Taniguchi K. Sequential passages of human rotavirus in MA-104 cells. Microbiol. Immunol. 1981, 25 (10): 1025–35. PMID 6273696.
- ^ Vesikari T, Isolauri E, Delem A; et al. Clinical efficacy of the RIT 4237 live attenuated bovine rotavirus vaccine in infants vaccinated before a rotavirus epidemic. J. Pediatr. 1985, 107 (2): 189–94. PMID 3894608. doi:10.1016/S0022-3476(85)80123-2.
- ^ 即惠氏大藥廠(Wyeth)所製造的「輪盾」(Rotashield®)
- ^ Rotavirus vaccine for the prevention of rotavirus gastroenteritis among children. Recommendations of the Advisory Committee on Immunization Practices (ACIP). MMWR Recomm Rep. 1999, 48 (RR-2): 1–20. PMID 10219046.
- ^ Kapikian AZ. A rotavirus vaccine for prevention of severe diarrhoea of infants and young children: development, utilization and withdrawal. Novartis Found. Symp. 2001, 238: 153–71; discussion 171–9. PMID 11444025. doi:10.1002/0470846534.ch10.
- ^ Bines JE. Rotavirus vaccines and intussusception risk. Curr. Opin. Gastroenterol. 2005, 21 (1): 20–5 [2008-12-20]. PMID 15687880. (原始內容存檔於2013-05-11).
- ^ Bines J. Intussusception and rotavirus vaccines. Vaccine. 2006, 24 (18): 3772–6. PMID 16099078. doi:10.1016/j.vaccine.2005.07.031.
- ^ Dennehy PH. Rotavirus vaccines: an overview. Clin. Microbiol. Rev. 2008, 21 (1): 198–208 [2008-12-20]. PMID 18202442. doi:10.1128/CMR.00029-07. (原始內容存檔於2011-09-28).
