肝性脑病
| 肝性脑病 | |
|---|---|
| 又称 | 门体性脑病(Portosystemic encephalopathy), 肝昏迷(hepatic coma),[1]肝性昏迷(coma hepaticum) |
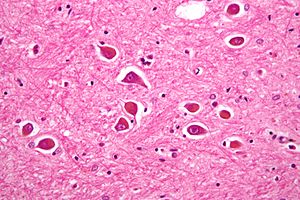 | |
| 由显微照相显示,在肝性脑病患者大脑标本的阿兹海默病二型星形胶质细胞 | |
| 症状 | 意识状态改变、情绪改变、个性改变及行动困难[2] |
| 类型 | 急性,反复出现,持续性[3] |
| 病因 | 肝衰竭[2] |
| 风险因素 | 感染、消化道出血、便秘、电解质不平衡及摄取某些药物[4] |
| 诊断方法 | 根据症状,透过把其他潜在的原因排除后以确定[2][5] |
| 鉴别诊断 | 韦尼克-科尔萨科夫症候群 (WKS)、 震颤性谵妄、低血糖、头部外伤及低血钠症[1] |
| 治疗 | 对症治疗、处理病症触发因素、乳果糖及肝脏移植[1][3] |
| 预后 | 重症者平均预期寿命短于一年。[1] |
| 患病率 | 肝硬化的患者有4成以上会发展出此病症。[6] |
| 分类和外部资源 | |
| 医学专科 | 胃肠学 |
| ICD-11 | DB99.5 |
| ICD-9-CM | 572.2 |
| MedlinePlus | 000302 |
| eMedicine | 186101、182208 |
肝性脑病(英语:Hepatic encephalopathy,HE) 是肝衰竭导致的意识状态改变。[2]发作形式或是渐进,或是突然。[2]其他症状包括行动困难、情绪变化或是性格变化。[2]到晚期阶段,患者会进入昏迷状态。[3]
HE会发生在患有急性,或是慢性肝病的患者身上。[3]感染、消化道出血、便秘、电解质不平衡或是某些药物都可能会引起发作。[4]据信潜在的机制是氨(一种通常透过肝脏可排除的物质)在血液中累积的结果。[2]诊断方式通常是把其他潜在的原因排除后而确定。[2][5]这种症状可经由检查血液中氨的水准、脑电图、或是大脑的电脑断层扫描(CT scan)取得支持的证据。[3][5]
HE通常透过对症治疗和处理病症的触发因素来设法逆转。[1][3]通常会使用乳果糖来降低氨的水准。[1]某些抗生素(如利福昔明)和益生菌是其他的可能选择。[1]肝脏移植可把重症患者的预后改善。[1]
超过40%的肝硬化患者会发展出HE。[6]超过一半的肝硬化,加上有严重HE的患者,其寿命会短于一年。[1]有机会接受肝脏移植的患者中,移植后五年内的死亡率低于30%。[1]这种病症最晚在1860年就曾被描述过。[1]
医学征象
[编辑]最轻微的HE很难透过临床方式发现,但可透过神经心理测试来显示。表现的病征为健忘、轻度意识模糊、和易怒。第一级(I)HE的特征为睡眠周期颠倒(白天睡眠,夜间清醒),第二级(II)是嗜睡和性格改变。第三级(III)是意识模糊状况恶化。第四级(IV)是逐步陷入昏迷。[3]
更严重的HE会造成意识水准恶化,从嗜睡进展为昏睡,最终是昏迷。在其中的阶段,患者的四肢会有特征性抽动(扑翼样震颤(四肢抽搐),或称“肝性摆颤(liver flap)”);四肢抽搐会随著昏睡的加重而消失。然后出现定向障碍和失忆症,可能会出现不恰当的行为。进入第三级时,神经系统检查会显示阵挛和阳性的巴宾斯基反射。到末期时出现昏迷和癫痫发作;最后会因为发生脑水肿而死亡。[3]
脑病常与肝衰竭的其他医学征象同时发生,这些征象包括黄疸、腹水、和外周性水肿。足底腱反射的程度可能加大,巴宾斯基反射可能异常(严重脑病的患者的足部反应是伸展而非弯曲)。这类患者呼气时会散发出特殊的气味(肝病性口臭)。[7]
原因
[编辑]在一小部分病例中,脑病直接由肝衰竭引起;尤其是由于急性肝衰竭。更常见的是在慢性肝病患者中,HE常由其他原因所引发,能够识别这些触发因素变得很重要,因为将可针对这种发病提供有效治疗。[3]
| Type | 原因[3][7][8] |
|---|---|
| 过量 氨负荷 |
吸收大量蛋白质、消化道血管(例如{{le|食道静脉曲张|esophageal varices)破裂,富含蛋白质的血液重新被肠道吸收的结果)、肾功能衰竭(无法排除含氨的废弃物,如尿素)以及便秘 |
| 电解质 不平衡 |
采用利尿剂处理腹水情况的患者,通常会出现低血钠症和低钾血症,另有碱中毒、缺氧及脱水的情况 |
| 药物 治疗 |
如苯二氮䓬类药物的镇静剂(通常用来治疗酒精戒断症候群,或是焦虑症)、麻醉药物(当作镇痛药,或用来治疗物质滥用症状)、抗精神病药及治疗酒精中毒药物 |
| 感染 | 肺炎、泌尿道感染、自发性细菌性腹膜炎及其他感染 |
| 其他 | 外科手术、肝病进一步恶化、其他导致肝脏受损的因素(例如酒精性肝炎,A型肝炎) |
| 不明原因 | 此类病例中,有20% - 30%查不出原因。 |
在建立经颈静脉肝内门脉系统静脉分流术 (TIPS,简称门体分流,用于治疗难治性腹水、食道静脉曲张出血、和肝肾症候群)后也可能发生HE。占病例中的百分比有30%,在以前曾患过脑病、高龄、女性、和非酒精引起的肝病患者群组中,有较高的发生率。[8]
发病
[编辑]
肝功能障碍或是门体分流会导致脑病的原因有好几种解释。在健康的个人,由肠道而来含有氨的复合物(由肠道菌群从食物中制造)经由肝门静脉输送到肝脏,这些氨复合物中有80-90%在肝脏的尿素循环中迅速被代谢或是排出。但这种过程在所有HE的亚型中均受到破坏 - 因为肝细胞无法代谢废物,不然因为门静脉血液经由侧支循环或是医学构建的分流而绕过肝脏的缘故。含氨废物在身体循环系统中积累(因此以前将此症状称为“门体性脑病”)。废物中最重要的的是氨(NH3)。这种小分子穿过血脑屏障,受到星形胶质细胞吸收和代谢,星形胶质细胞是大脑中的细胞,占大脑皮质体积的30%。星形胶质细胞把谷氨酸合成为谷氨酰胺时会使用到氨。增加的谷氨酰胺导致星形胶质细胞渗透压增加而变得肿胀。有抑制功能的γ-氨基丁酸(GABA)系统活性因而增加,而把提供给其他细胞的能量减少。这可当作是种“细胞毒性”类型脑积水的例子。[9]
虽然有很多研究证明氨的核心作用,但这种物质的水准并不一定与脑病的严重程度相关;有人怀疑这表示血清内氨的水准相对较低的严重症状患者中,有更多的氨已经被吸收进入大脑之中[3][7][7]。与HE有关的其他废物包括硫醇、短链脂肪酸和苯酚。[7]
另有许多HE的异常状况受到描述,但这些如何导致疾病的方式尚未被确定。谷氨酸转运蛋白基因表达的丧失(尤其是兴奋性氨基酸转运蛋白2)已确定是由急性肝衰竭造成。[10]患者也显现出苯二氮䓬类化合物水准升高以及GABA神经递质系统异常。也发生芳香族氨基酸(苯丙氨酸、异亮氨酸和酪氨酸)和支链氨基酸(亮氨酸、异亮氨酸、和缬氨酸)之间的失衡的现象;这会导致伪神经递质(如章胺和苯基乙醇胺)的产生。也有血清素系统失调的报导。可能是锌的消耗和锰的积累发生的作用。[3][7]身体其他部位的发炎可能透过细胞因子和细菌脂多糖对星形胶质细胞的作用而诱发脑病。[8]
诊断
[编辑]
调查
[编辑]因为HE症状与其他脑病变相似,诊断只能透过有确诊的肝病(A型肝炎和C型肝炎)或实施过门体分流手术(B型肝炎)的情况下确定。要做区别,需要透过异常肝功能测试和/或医学超音波检查,最好是透过肝脏穿刺检查以确定是否有肝脏疾病。[3][7]HE的症状也可能由其他情况引起,例如脑内出血和癫痫发作(这两种情况在慢性肝病中较常见)。透过脑部CT扫描可把脑内出血的情况排除,如果怀疑是癫痫发作,可透过脑电图做判断。[3]脑病的罕见类似症状有脑膜炎、脑炎、韦尼克氏脑病、和威尔森氏症;这些因素可能会在临床上受到怀疑,必须透过调查加以证实。[7][11]
当其他导致意识模糊或昏迷的原因受到排除,在临床诊断上会认为是HE;没任何测试可完全把诊断确定或是排除。90%的患者血清氨水准会升高,但并非所有高氨血症与脑病有关。[3][7]对大脑做CT扫描,除非是脑病到达IV级的程度,通常不会被发现异常,此时脑肿胀(脑水肿)可能会被察觉。[7]其他神经成像方式,例如磁共振成像(MRI),虽然可能会显示出异常,但目前不被认为有帮助。[11]在0级,脑电图没显示明显的异常,即使当时已有轻微的脑病存在;在 I、II、和III级的时候,额叶上有以5Hz振荡的三相波,在IV级有缓慢的delta 波活动。[3]然而这些脑电图的变化不足以把HE和其他疾病做区别。[11]
一旦做出脑病的诊断,就要努力排除潜在的原因(如上面“原因”中所列出)。这需要做血液检查(尿素和电解质、全血细胞计数、肝功能测试),通常包含胸部X光, 和尿液分析。如果有腹水, 可能需要进行诊断性腔液穿刺术以确定是否有自发性细菌性腹膜炎 (SBP)的感染发生。[3]
分类
[编辑]West Haven分级
[编辑]HE的严重程度可运用West Haven分级法做分类;[12]这是根据患者自主性受损程度、意识改变、智力功能、行为和对治疗的依赖来判断。[3][13]
- 0级 - 除了智力和协调能力可能轻度下降外,没明显变化
- 1级 - 轻微缺乏意识;欣快或是焦虑;注意力持续的时间缩短;数学加法或减法能力受损
- 2级 - 嗜睡或是冷漠;轻微失去时间或地点的感觉;微妙的性格变化;不适当行为
- 3级 - 昏睡到半木僵,但对语言刺激有反应;意识模糊;严重失去方向感
- 4级 - 昏迷
类型
[编辑]
HE的分类在1998年维也纳举行的世界胃肠学大会(World Congress of Gastroenterology 1998)被提出。根据这项分类,HE因潜在原因被细分为A、B、和C型。[11]
- A型(= 急性)描述与急性肝衰竭相关的HE,通常与脑水肿相关
- B型(= 分流)是由门静脉系统分流所引起,并无相关的内在肝病
- C型(= 肝硬化)发生在有肝硬化的患者身上 - 这类型细分为发作性、持续性、和轻微脑病
轻微脑病 (MHE) 被定义为不会导致临床上明显的认知功能障碍的脑病,但可透过神经心理学研究来证实。[11][14]这算是种重大的发现,因为患有MHE会损害生活品质和增加交通事故的风险。[15]
轻微脑病
[编辑]根据定义,轻微HE的诊断需要神经心理学测试。较早的测试包括“数字连接测试”A和B(测量一个人可连接随机分散的数字1到20所需的时间)、“方块设计测试”和“数字符号替换测试“。[11] 一个专家小组在2009年得出结论,在测量认知功能多个领域的神经心理学测试,采用一组包含多种的测试,通常比单一测试的结果更为可靠,并且往往与功能状态有更强的相关性。有两组测试方法 - Repeatable Battery for the Assessment of Neuropsychological Status(RBANS)[16]和PSE-Syndrom-Test[17]可供采用。[14]在德国开发并在其他几个欧洲国家验证过的PSE-Syndrom-Test测试方法也把旧的评估工具,例如数字连接测试包含在内。[14][15][17]
治疗
[编辑]如果脑病属于严重的人(第3和第4级),由于咽反射等保护性反射减弱,可能会发生呼吸道受到阻塞的风险,而会导致呼吸停止。因此通常需要把患者转移到较高级别的护理机构(例如加护病房),并实施气道插管,以防止危及生命的并发症(例如吸入性肺炎或呼吸衰竭)产生。[7][18]而采用鼻胃管可安全施用营养素和药物。[3]
治疗HE取决于推断的潜在病因(A、B或C型)以及是否有这些潜在病因的存在。如果脑病是由急性肝衰竭(A型)造成,即使是轻度(1-2级),也表明可能需要做肝脏移植,建议最好转移到专科部门处理。[18]接受TIPS(分流)手术的患者可能会出现B型HE;在大多数情况下,这情况会自行解决,或是透过下面讨论的医学治疗解决,但有大约5%的病例,需要把分流关闭来解决症状。[8]
对于C型HE,初始治疗的的重点是找出替代治疗方式,或是确定实际潜在原因。[7][8][15]有鉴于感染频率是潜在原因,通常是根据经验疗法而采用抗生素(虽然尚不知确切的感染来源和性质)。[3][8]一旦脑病发作得到有效治疗之后,可能就需要决定是否准备进行肝脏移植。[15]
饮食
[编辑]以往人们认为即使摄入正常水准的蛋白质也会把HE的风险提高。但此看法已被证明不正确。而且一般罹患长期肝病的患者会有营养不良的情况,因此需要足够的蛋白质以维持体重。建议患者的饮食内容该含有足够的蛋白质和能量。[3][8]
在患者膳食中补充支链氨基酸,可改善脑病和其他肝硬化并发症。[3][8]
一些研究显示患者摄取益生菌有益。[8]
乳果糖/乳糖醇
[编辑]乳果糖和乳糖醇属于二糖(双糖),不会被人体消化道所吸收。这种糖类被认为可减少细菌产生氨的数量,而且把氨转化为不被吸收的(NH4+)形式的离子,经过肠道转运转为为废弃物。通常每天给药3次,每次15-30毫升的剂量;希望达到每天排泄3-5次软便,或在某些情况下,粪便的pH值达到<6.0的水准。[7][8][15]乳果糖也可透过灌肠方式施用,特别是在病情严重的时候。[15]较常见的是使用磷酸钠灌肠。这种做法可缓解便秘(脑病的原因之一),并增加肠道通便容易度。[3]
采用乳果糖和乳糖醇,有助于治疗脑病,这类做法被建议当做为一线治疗方式。[3][19]而在治疗时,乳糖醇似乎较乳果糖为有效。[19]乳果糖和乳糖醇的副作用包括可能会有腹泻、腹部胀气、放屁、和恶心。[19]对于急性肝衰竭的情况时,尚不清楚乳果糖是否有益。腹部胀气可能会对肝脏移植手术产生干扰。[18]
抗生素
[编辑]对于复发性脑病患者,除了乳果糖外,另推荐加用利福昔明。[1]利福昔明是种不可吸收的利福霉素类抗生素。这种抗生素被认为可发挥类似新霉素或是甲硝唑的功效,但不会产生并发症。由于使用乳果糖的历史悠久且成本较低,利福昔明通常在如患者对于果乳果糖耐受性差或无效时,仅用作二线治疗方式之用。当同时采用乳果糖和利福昔明时,效果会比单独使用任何一项会高。[3]利福昔明的成本比乳果糖更高,但这种成本可能会因为患者较少的住院次数而被抵消。[15]
新霉素和甲硝唑也是用于治疗HE的抗生素。[20]使用的基本原理是肠道细菌会产生和转化氨和其他废物,杀死这些细菌将可减少废物的产生。选择新霉素是因为它的肠道吸收率低,如果利用注射的方式施用新霉素和类似的胺基糖苷类抗生素,可能会导致患者的听力损失和肾功能衰竭。后来的研究显示口服式的新霉素确能被肠道吸收,而导致并发症。甲硝唑同样不常被使用,因为长期使用时,除对消化系统产生副作用外,还会导致周边神经病变。[3]
L-鸟氨酸和L-天冬氨酸
[编辑]采用L-鸟氨酸和L-天冬氨酸 (LOLA) 组合可降低患者血液中氨的水准。[21]有非常弱的临床试验证据显示使用LOLA治疗可能对于HE患者有益。[21]LOLA透过尿素循环增加而产生尿素,把氨的水准降低,这是一种把氨转化为如尿素的中性物质,而把氨代谢排除的途径。[22]LOLA可与乳果糖和/或利福昔明联合使用,单独使用任何一种,在控制症状方面的效果不好。[3]
流行病学和预后
[编辑]肝硬化患者中,每年会发生HE的风险为20%,并且在任何时候,大约有30-45%的肝硬化患者会出现明显的脑病。而透过正式的神经心理测试,可侦测的轻微HE比率高达60-80%;有轻微HE情况,会把未来发展为明显脑病的可能性增高。[15]一旦患者发展出HE,预后主要取决于肝衰竭的其他标识,例如白蛋白(一种肝脏产生的蛋白质)水准、凝血酶原时间(评估患者血液的凝血能力,依赖肝脏中产生的蛋白质进行)、有腹水以及胆红素(一种由肝脏结合和排泄的血红蛋白分解物)的水准。连同脑病的严重程度,这些标识被纳入Child-Pugh分期系统;系统评分可决定患者具有一年和两年的生存期,有助于做出肝脏移植的决定。[11]
在急性肝衰竭的案例,严重脑病的出现清楚预测出有短期内死亡的可能,和确定肝衰竭根本原因以制定预后计划,两者几乎一样重要。历史上供肝脏移植广泛使用的标准,例如伦敦国王学院标准的用途有限,最近的指南不鼓励过度依赖这些标准。威尔森氏症(遗传性体内铜积累)和蘑菇中毒患者发生的肝性脑病表明迫切需要进行肝脏移植。[18]
历史
[编辑]被现代人誉为医学之父的古希腊医师希波克拉底(生卒约为公元前460年及370年)可能已描述过出现异常行为的黄疸患者。[17][23]1世纪的凯尔苏斯和3世纪的盖伦也认出这种情况。许多把肝病与神经精神症做出联系的现代描述是在18和19世纪出现;例如,义大利的乔瓦尼· 莫尔加尼 (生1682年,卒1771年) 在1761年报告说这是一种渐进式的疾病。[23]
在1950年代,有几项报告把先前提出的众多异常列举,并把先前阐明的理论予以证实,即代谢障碍和门体分流是HE背后的潜在机制,富含氮的化合物来自肠道。[17][24]女爵士谢拉·夏洛克教授 (生1918年,卒2001年) 在伦敦皇家学士后医学院和随后的皇家自由医院进行许多此类研究。同一小组也对膳食蛋白质的限制[23]和新霉素做过研究。[25]
West Haven分级法是由耶鲁大学的Harold Conn教授 (生1925年,卒2011年)[26] 及其同事在研究乳果糖的治疗功效时所制定。[11][27][28]
参见
[编辑]参考文献
[编辑]- ^ 1.00 1.01 1.02 1.03 1.04 1.05 1.06 1.07 1.08 1.09 1.10 1.11 Wijdicks, EF. Hepatic Encephalopathy.. The New England Journal of Medicine. 2016-10-27, 375 (17): 1660–1670. PMID 27783916. doi:10.1056/NEJMra1600561.
- ^ 2.0 2.1 2.2 2.3 2.4 2.5 2.6 2.7 Hepatic encephalopathy. GARD. 2016 [2017-07-30]. (原始内容存档于2017-07-05) (英语).
- ^ 3.00 3.01 3.02 3.03 3.04 3.05 3.06 3.07 3.08 3.09 3.10 3.11 3.12 3.13 3.14 3.15 3.16 3.17 3.18 3.19 3.20 3.21 3.22 3.23 3.24 3.25 3.26 Cash WJ, McConville P, McDermott E, McCormick PA, Callender ME, McDougall NI. Current concepts in the assessment and treatment of hepatic encephalopathy. QJM. January 2010, 103 (1): 9–16. PMID 19903725. doi:10.1093/qjmed/hcp152
 .
.
- ^ 4.0 4.1 Starr, SP; Raines, D. Cirrhosis: diagnosis, management, and prevention.. American Family Physician. 2011-12-15, 84 (12): 1353–9. PMID 22230269.
- ^ 5.0 5.1 5.2 Portosystemic Encephalopathy - Hepatic and Biliary Disorders. Merck Manuals Professional Edition. [2019-09-25]. (原始内容存档于2020-04-22) (加拿大英语).
- ^ 6.0 6.1 Ferri, Fred F. Ferri's Clinical Advisor 2018 E-Book: 5 Books in 1. Elsevier Health Sciences. 2017: 577. ISBN 9780323529570. (原始内容存档于2017-07-30) (英语).
- ^ 7.00 7.01 7.02 7.03 7.04 7.05 7.06 7.07 7.08 7.09 7.10 7.11 7.12 Chung RT, Podolsky DK. Cirrhosis and its complications. Kasper DL, Braunwald E, Fauci AS, et al (编). Harrison's Principles of Internal Medicine
 16th. New York, NY: McGraw-Hill. 2005: 1858–69. ISBN 978-0-07-139140-5.
16th. New York, NY: McGraw-Hill. 2005: 1858–69. ISBN 978-0-07-139140-5.
- ^ 8.00 8.01 8.02 8.03 8.04 8.05 8.06 8.07 8.08 8.09 Sundaram V, Shaikh OS. Hepatic encephalopathy: pathophysiology and emerging therapies. Med. Clin. North Am. July 2009, 93 (4): 819–36, vii. PMID 19577116. doi:10.1016/j.mcna.2009.03.009.
- ^ Ryan JM, Shawcross DL. Hepatic encephalopathy. Medicine. 2011, 39 (10): 617–620. doi:10.1016/j.mpmed.2011.07.008.
- ^ Thumburu, KK; Dhiman, RK; Vasishta, RK; Chakraborti, A; Butterworth, RF; Beauchesne, E; Desjardins, P; Goyal, S; Sharma, N; Duseja, A; Chawla, Y. Expression of astrocytic genes coding for proteins implicated in neural excitation and brain edema is altered after acute liver failure.. Journal of Neurochemistry. Mar 2014, 128 (5): 617–27. PMID 24164438. S2CID 21367707. doi:10.1111/jnc.12511
 .
.
- ^ 11.0 11.1 11.2 11.3 11.4 11.5 11.6 11.7 Ferenci P, Lockwood A, Mullen K, Tarter R, Weissenborn K, Blei A. Hepatic encephalopathy--definition, nomenclature, diagnosis, and quantification: final report of the working party at the 11th World Congresses of Gastroenterology, Vienna, 1998. Hepatology. 2002, 35 (3): 716–21 [18 December2021]. PMID 11870389. doi:10.1053/jhep.2002.31250. (原始内容存档于2022-10-15). }}
- ^ Weissenborn, Karin. Hepatic Encephalopathy: Definition, Clinical Grading and Diagnostic Principles. Drugs. [2021-12-18]. doi:10.1007/s40265-018-1018-z. (原始内容存档于2022-10-14).
- ^ Hepatic Encephalopathy. The Lecturio Medical Concept Library. [2021-07-09]. (原始内容存档于2022-10-19).
- ^ 14.0 14.1 14.2 Randolph C, Hilsabeck R, Kato A, et al. Neuropsychological assessment of hepatic encephalopathy: ISHEN practice guidelines. Liver Int. May 2009, 29 (5): 629–35. PMID 19302444. S2CID 30313260. doi:10.1111/j.1478-3231.2009.02009.x
 .
.
- ^ 15.0 15.1 15.2 15.3 15.4 15.5 15.6 15.7 Bajaj JS. Review article: the modern management of hepatic encephalopathy. Aliment. Pharmacol. Ther. March 2010, 31 (5): 537–47. PMID 20002027. S2CID 10976362. doi:10.1111/j.1365-2036.2009.04211.x.
- ^ Randolph C, Tierney MC, Mohr E, Chase TN. The Repeatable Battery for the Assessment of Neuropsychological Status (RBANS): preliminary clinical validity. J Clin Exp Neuropsychol. June 1998, 20 (3): 310–9. PMID 9845158. doi:10.1076/jcen.20.3.310.823.
- ^ 17.0 17.1 17.2 17.3 Weissenborn K, Ennen JC, Schomerus H, Rückert N, Hecker H. Neuropsychological characterization of hepatic encephalopathy. J. Hepatol. May 2001, 34 (5): 768–73. PMID 11434627. doi:10.1016/S0168-8278(01)00026-5.
- ^ 18.0 18.1 18.2 18.3 Polson J, Lee WM. AASLD position paper: the management of acute liver failure. Hepatology. May 2005, 41 (5): 1179–97. PMID 15841455. S2CID 6216605. doi:10.1002/hep.20703. (原始内容存档于2012-12-16).
- ^ 19.0 19.1 19.2 Gluud, Lise Lotte; Vilstrup, Hendrik; Morgan, Marsha Y. Non-absorbable disaccharides versus placebo/no intervention and lactulose versus lactitol for the prevention and treatment of hepatic encephalopathy in people with cirrhosis. The Cochrane Database of Systematic Reviews. 2016-05-06, (5): CD003044. ISSN 1469-493X. PMC 7004252
 . PMID 27153247. doi:10.1002/14651858.CD003044.pub4.
. PMID 27153247. doi:10.1002/14651858.CD003044.pub4.
- ^ Ferenci, P. Hepatic encephalopathy.. Gastroenterology Report. May 2017, 5 (2): 138–147. PMC 5421503
 . PMID 28533911. doi:10.1093/gastro/gox013.
. PMID 28533911. doi:10.1093/gastro/gox013.
- ^ 21.0 21.1 Goh, Ee Teng; Stokes, Caroline S.; Sidhu, Sandeep S.; Vilstrup, Hendrik; Gluud, Lise Lotte; Morgan, Marsha Y. L-ornithine L-aspartate for prevention and treatment of hepatic encephalopathy in people with cirrhosis (PDF). The Cochrane Database of Systematic Reviews. 2018-05-15, 5 (6): CD012410 [2022-10-19]. ISSN 1469-493X. PMC 6494563
 . PMID 29762873. doi:10.1002/14651858.CD012410.pub2. (原始内容存档 (PDF)于2019-04-30).
. PMID 29762873. doi:10.1002/14651858.CD012410.pub2. (原始内容存档 (PDF)于2019-04-30).
- ^ Kircheiscorresponding, G; Lüth, S. Pharmacokinetic and Pharmacodynamic Properties of l-Ornithine l-Aspartate (LOLA) in Hepatic Encephalopathy. Springer: Drugs. 2019, 79 (1): 23–29. PMC 6416235
 . PMID 30706424. doi:10.1007/s40265-018-1023-2.
. PMID 30706424. doi:10.1007/s40265-018-1023-2.
- ^ 23.0 23.1 23.2 Summerskill WH, Davidson EA, Sherlock S, Steiner RE. The neuropsychiatric syndrome associated with hepatic cirrhosis and an extensive portal collateral circulation. Q. J. Med. April 1956, 25 (98): 245–66. PMID 13323252.
- ^ Sherlock S, Summerskill WH, White LP, Phear EA. Portal-systemic encephalopathy; neurological complications of liver disease. Lancet. September 1954, 264 (6836): 453–7. PMID 13193045. doi:10.1016/S0140-6736(54)91874-7.
- ^ Last PM, Sherlock S. Systemic absorption of orally administered neomycin in liver disease. N. Engl. J. Med. February 1960, 262 (8): 385–9. PMID 14414396. doi:10.1056/NEJM196002252620803.
- ^ In Memoriam: Harold O. Conn, M.D.. Yale University School of Medicine New Haven, CT. [2021-12-16]. (原始内容存档于2022-10-14).
- ^ Conn HO, Leevy CM, Vlahcevic ZR, et al. Comparison of lactulose and neomycin in the treatment of chronic portal-systemic encephalopathy. A double blind controlled trial. Gastroenterology. 1977, 72 (4 Pt 1): 573–83. PMID 14049. doi:10.1016/S0016-5085(77)80135-2
 .
.
- ^ Boyer JL, Garcia-Tsao G, Groszmann RJ. In Memoriam: Harold O. Conn, M.D.. Hepatology. February 2012, 55 (2): 658–9. S2CID 85090164. doi:10.1002/hep.25550
 .
.
