脂類
| 此條目需要精通或熟悉相关主题的编者参与及协助编辑。 (2013年8月23日) |

脂質可以廣義定義為疏水性或雙親性小分子;某些脂質因為其雙親性的特質(兼具親水性與疏水性),能在水溶液環境中形成囊泡、脂質體或膜等構造。生物體內的脂質完全或部分源自兩種截然不同的生物次單元:酮酸基與異戊二烯[7]。由此,脂質可以概分為八類:脂肪酸、甘油酯、甘油磷脂、鞘脂(神經脂質)、醣脂質、聚酮类(由酮乙基次單元聚合而成)、固醇脂类,以及孕烯醇酮脂类(由異戊二烯次單元縮合聚合而成)[5][8]。
脂類包含脂肪,而非其同義詞;脂肪只是一種稱為三酸甘油酯的脂類。脂類也包括脂肪酸及其衍生物,包括單酸甘油酯、二酸甘油酯、磷脂等,也包括其他含有固醇的代謝產物,像是膽固醇[9]。雖然人類和其他動物有許多不同的代謝方式,可以切斷脂肪鏈及合成脂質,不過仍有一些必需脂質無法自行合成,需要在食物中攝取。
脂質形成原始生命體的細胞膜是生命起源模型中的關鍵步驟[10]。
分类[编辑]
| 1.脂肪酰类,Fatty Acyls, FA |
|---|
| 脂肪酸,Fatty acid,FA |
| (O-酰基)-1-羟基脂肪酸,(O-acyl)-1-hydroxy fatty acid,OAHFA |
| 2.甘油酯类,Glycerolipids, GL |
|---|
| 甘油一酯,Monoglyceride,MG |
| 甘油二酯,Diglyceride,DG |
| 甘油三酯,Triglyceride,TG |
| 氘代甘油二酯,Deuterated diglyceride,D5DG |
| 氘代甘油三酯,Deuterated triglyceride,D5TG |
| 3.甘油磷脂类,Glycerophospholipids,GP |
|---|
| 溶血磷脂酰胆碱,Lyso-phosphatidylcholine,LPC |
| 溶血磷脂酰乙醇胺,Lyso-phosphatidylethanolamine,LPE |
| 溶血磷脂酰肌醇,Lyso-phosphatidylinositol,LPI |
| 溶血磷脂酰甘油,Lyso-phosphatidylglycerol,LPG |
| 溶血磷脂酰丝氨酸,Lyso-phosphatidylserine,LPS |
| 溶血磷脂酸,Lyso-phosphatidic acid,LPA |
| 溶血磷脂酰乙醇,Lyso-phosphatidylethanol,LPEt |
| 溶血磷脂酰乙醇,Lyso-phosphatidylmethanol,LPMe |
| 溶血二甲基磷脂酰乙醇胺,Lysodimethylphosphatidylethanolamine,LdMePE |
| 磷脂酰胆碱,Phosphatidylcholine,PC |
| 磷脂酰乙醇胺,Phosphatidylethanolamine,PE |
| 磷脂酰肌醇,Phosphatidylinositol,PI, PIP, PIP2, PIP3 |
| 磷脂酰甘油,Phosphatidylglycerol,PG |
| 磷脂酰丝氨酸,Phosphatidylserine,PS |
| 磷脂酸,Phosphatidic acid,PA |
| 血小板活化因子,Platelet-activating factor,PAF |
| 磷脂酰乙醇,Phosphatidylethanol,PEt |
| 磷脂酰甲醇,Phosphatidylmethanol,PMe |
| 环磷脂酸,Cyclic phosphatidic acid,cPA |
| 二甲基磷脂酰乙醇胺,Dimethylphosphatidylethanolamine,dMePE |
| 心磷脂,Cardiolipin,CL |
| 4.鞘脂类,Sphingolipids, SP |
|---|
| 鞘磷脂,Sphingomyelin,SM |
| 溶血鞘磷脂,Lysosphingomyelin,LSM |
| 鞘磷脂(植物鞘氨醇),Sphingomyelin(phytosphingosine),phSM |
| 鞘氨醇,Sphingoshine,So |
| 磷酸鞘氨醇,Sphingoshine phosphate,SoP |
| 神经酰胺,Ceramides,Cer |
| 磷酸神经酰胺,Ceramides phosphate,CerP |
| 神经节苷脂,Gangliosides,GM1, GM2, GM3, GD1a, GD1b, GD2, GD3, GT1a, GT1b, GT1c, GT2, GT3, GQ1b, GQ1c |
| 5.固醇脂类,Sterol Lipids, ST |
|---|
| 胆固醇酯,Cholesteryl Ester,ChE |
| 胆固醇酯,Cholesterylesters,CE |
| 酵母甾醇,Zymosteryl,ZyE |
| 豆甾醇酯,Stigmasteryl ester,StE |
| 谷甾醇酯,Sitosteryl ester,SiE |
| 氘代胆固醇酯,Deuterated Cholesteryl Ester,D7ChE |
| 6.孕烯醇酮脂类,Prenol Lipids, PR |
|---|
| 辅酶,Coenzyme,Co |
| 7.糖脂类,葡萄糖鞘氨醇,Glucosylsphingoshine,SoG1 |
|---|
| (Saccharolipids, SL),单糖基神经酰胺,Monogylcosylceramide,CerG1 |
| 双糖基神经酰胺,Diglycosylceramide,CerG2 |
| 三糖基神经酰胺,Triglycosyl-ceramide,CerG3 |
| 糖基神经酰胺系列,Simple Glc series,CerG2GNAc1, CerG2GNAc2, CerG2GNAc3 |
| 单半乳糖单酰甘油酯,Monogalactosylmonoacylglycerol,MGMG |
| 单半乳糖二酰甘油酯,Monogalactosyldiacylglycerol,MGDG |
| 双半乳糖基单酰甘油酯,Digalactosylmonoacylglycerol,DGMG |
| 双半乳糖基二酰甘油酯,Digalactosyldiacylglycerol,DGDG |
| 硫代异鼠李糖甘油一酯,Sulfoquinovosylmonoacylglycerol,SQMG |
| 硫代异鼠李糖甘油二酯,Sulfoquinovosyldiacylglycerol,SQDG |
| 8.聚酮类,Polyketides,PK |
|---|
| 抗生素,Antibiotic,ABX |
| 真菌霉素,Mycotoxins,MT |
| 天然色素,NaturalPigments,NP |
脂肪酸类[编辑]


脂肪酸,或是脂質中的脂肪酸殘留部份,是由乙醯輔酶A和丙二醯輔酶A及甲基丙二酸單醯輔酶A合成的許多不同種類的分子,合成的反應稱為脂肪酸合成[12][13]。脂肪酸是由尾端為羧酸官能基的碳鏈組成,因此分子會有有極性且親水的一端,另一端則是非極性且疏水的。脂肪酸結構是生物脂質中最基本的結構,常用來建構更複雜脂質[14]。碳鏈長度一般介於4到24個碳之間[15],可能是飽和化合物或是不饱和化合物,也可能連結其他含有氧、鹵素、氮或是硫的官能基。若脂肪酸中含有雙鍵,則可能會有順式及反式的顺反异构,對分子組態有很大的影響。顺式的雙鍵會使碳鏈彎曲,若是分子中有多個雙鍵,反應會更明顯。18個碳的亚麻酸中有三個雙鍵,是植物的类囊体膜中最豐富的脂肪酸酰基链,因此在環境低溫時,仍可以使囊膜有高度的流動性[16]。大部份天然的(有雙鍵的)脂肪酸是順式的,不過有些天然的脂肪酸是反式的,而人工氫化的脂肪和油類也是反式的[17]。
在生物中重要的脂肪酸包括主要衍生自花生四烯酸的类花生酸,另一種為二十碳五烯酸(EPA),包括前列腺素、白三烯、血栓素等。二十二碳六烯酸(DHA)對生物體也相當的重要,尤其是在生物的視覺上[18][19]。其他重要的脂肪酸類脂質包括脂肪酸酯及脂肪酸胺,脂肪酸酯包括重要的生物化學中間產物,例如蜡酯、及脂肪酸硫酯辅酶A衍生物、脂肪酸硫酯醯基載體蛋白衍生物、及脂肪酸肉碱。脂肪酸胺包括N-脂肪酰基胺,例如大麻素中的神經傳導物質花生四烯酸乙醇胺[20]。
甘油酯类[编辑]

甘油酯中包括單酸、二酸及三酸甘油酯[21],分別是甘油和一、二、三個脂肪酸形成的酯類,其中最為人知的是三酸甘油酯,其中甘油 的三個羥基和脂肪酸反應,多半會是三種不同的脂肪酸。動物會用脂質儲存能量,而這些脂質也會儲存在動物的脂肪組織中。在代謝脂肪時三酸甘油酯的酯鍵會斷裂,分解為甘油和脂肪酸[22]。
甘油酯类中的化合物還包括甘油葡糖苷(glycosylglycerol),是甘油和單醣由糖苷键鍵結的化合物,例如在植物薄膜中常見的二半乳糖基二脂酰甘油(digalactosyldiacylglycerol)[23],或是哺乳類精子中常見的精脂[24]。
甘油磷脂类[编辑]
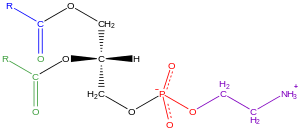
甘油磷脂一般簡稱為磷脂,是含有磷酸的脂類,出現在自然界及細胞的磷脂雙分子層中[25],和新陳代謝和細胞信號傳送有關[26]。神經組織(包括大腦)含有大量的磷脂,其成份的改變意味著有可能有神經的病變[27]。磷脂可以分為兩類,真核生物及細菌中的磷脂,其極性的分子團連結在甘油的sn-3位上,而古菌中的磷脂,其極性的分子團連結在甘油的sn-1位上[28]。
生物膜中常見的磷脂有磷脂醯膽鹼(也稱為PC、GPCho或卵磷脂)、磷脂酰乙醇胺(PE或GPEtn)及磷脂絲胺酸(也稱為PS或GPSer)。磷脂除了作為細胞膜的主要成份,以及結合細胞內或細胞間蛋白質外。有些真核生物细胞中的磷脂是細胞膜衍生的第二信使系統或是其前驅體,這類磷脂有磷脂酰肌醇及磷脂酸[29]。一般而言甘油的一或兩個羥基會連接長鏈的脂肪酸,不過也有連接烷基或是1Z-烯基(缩醛磷脂的磷脂,例如古菌中的二烷基醚变体[30]。
鞘脂类[编辑]
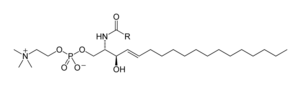
鞘脂是一組複雜化合物的統稱[31],有共同的鞘氨醇碱(sphingoid base)骨架,是由絲胺酸和長脂肪鏈的醯基輔酶A從頭合成,之後轉換為神經醯胺、磷鞘脂、糖鞘脂和其它化合物。哺乳動物的鞘氨醇碱一般是指鞘氨醇。神經醯胺是常見的鞘氨醇碱衍生物,有一個連接酰胺基的脂肪酸。其脂肪酸多半是飽和脂肪酸或是單元不飽和脂肪酸,碳鏈長度約為16至26個碳原子[32]
哺乳類體內的鞘脂主要以鞘磷脂為主[33].而昆蟲體內則主要是磷酸乙醇胺神经酰胺[34],真菌體內有植物神經磷酸肌醇及含有甘露糖的鞘脂[35]。糖鞘脂是鞘脂和糖以糖苷键連結的化合物,例如構造簡單的腦苷脂以及較複雜的神經節苷脂。
固醇类[编辑]
固醇包括膽固醇及其衍生物,和甘油磷脂、鞘磷脂同為組成生物膜的重要成份[36]。固醇都有相同的四環結構,是身體中的激素及細胞信號傳送,有著不同的角色。18個碳的固醇包括雌激素,C19的固醇包括雄激素,例如睾酮及雄甾酮。C21的固醇包括孕激素、糖皮質激素及鹽皮質激素[37]。开环类固醇包括許多不同形式的維生素D,其特徵是固醇主結構中B環的开环[38]其他的固醇有胆汁酸及其共軛鹼[39],是哺乳類氧化膽固醇後的衍生物,在肝臟中生成。植物中的固醇稱為植物固醇,例如β-谷固醇、豆固醇及菜籽固醇,後者也是判斷藻類生長的生物標記[40]。真菌細胞膜中主要的固醇為麥角固醇[41]。
異戊烯醇脂类[编辑]
異戊烯醇酯是由五碳異戊烯基二磷酸及二甲基烯丙基二磷酸合成,主要是透過甲羥戊酸路徑[42]。簡單的类异戊二烯是由C5單元的連續加成所形成,依照萜烯的數量來分類。超過40個碳的萜稱為多萜。類胡蘿蔔素是重要的簡單类异戊二烯,是抗氧化剂,也是維生素A的前驅體[43]。另一種重要的分子是醌及对苯二酚[44]。維生素E、維生素K及辅酶Q10也屬於這一類。原核生物會合成聚異戊二烯醇(细菌萜醇),連接在氧原子上的終端異戊二烯是未飽和的,而動物產生的聚異戊二烯醇(多萜醇)其終端異戊二烯已被還原[45]。
醣脂类[编辑]
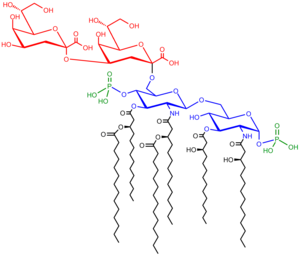
醣脂是指脂肪酸直接連結到醣的骨架,產生和雙層脂膜相容的結構。由單糖取代了甘油酯和磷脂中甘油的骨架角色。最常見的醣脂是脂质A的前體,是革兰氏阴性菌中脂多糖之成份之一。典型的脂质A分子有葡萄糖胺雙醣,是加了七個脂肪酸鏈的衍生物。大腸桿菌生長需要的最小多醣脂為Kdo2-Lipid A,是葡萄糖胺的六酰化二糖,其中有二個糖基化的3-脱氧-D-甘露-2-辛酮糖(Kdo)殘基[46]。
聚酮类[编辑]
聚酮是由乙醯基及丙醯輔酶A的子單位組成,藉由經典的酶聚合的產物。其中包括大量動物、植物、細菌、真菌及海洋生物的次級代謝產物及天然產物,在結構上有很大的不同[47][48]。 許多聚酮是有環的分子,其主結構經醣基化、甲基化、羥基化、氧化或是其他化學反應。許多常用的抗菌藥、抗寄生物药及抗癌藥物是聚酮或其衍生物,例如红霉素、四環素類抗生素、阿佛菌素及抗腫瘤的埃皮霉素[49]。
生物功能[编辑]
生物膜[编辑]
真核細胞用生物膜分隔成數個細胞器,各自有不同的生物機能。甘油磷脂是生物膜的主要成份,像細胞膜和細胞器的細胞內Intracellular,動物細胞是由細胞膜分隔細胞內和細胞外的環境。甘油磷脂是兩親分子,分子中同時具有親水性及親脂性的基團,其中以甘油為中心,藉由酯鍵連結到二個脂肪基的親脂性「尾巴」,另外一個酯鍵連結到一個磷酸的親水性「頭」。生物膜主要是以甘油磷脂為主,但也有一些沒有甘油的脂類,像鞘磷脂、膽固醇[50]。在植物及藻類中,缺少磷酸基的磺酸基异鼠李糖基二脂酰基甘油(sulfoquinovosyldiacylglycerol)是葉綠體以其他有關細胞器膜的主要成份,也是高等植物、藻類及一些細菌的光合組織中最豐富的脂類。
植物的類囊體膜含有形成非雙層膜的單半乳糖甘油二酯(MGDG),且是其中比例最多的脂質,其中也有少量的磷脂。而葉綠體類囊體膜中用磁共振及電子顯微鏡也發現有動態的脂質雙層膜基質[51]。
雙層膜發現有高度的雙折射,可以用双偏振极化干涉测量及圓二色性來量測雙層膜的規則性或變型程度。
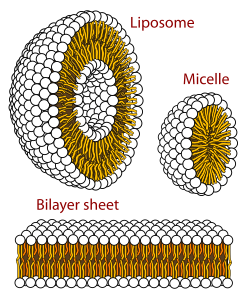
生物膜是種層狀相的磷脂雙分子層,若磷脂是在水溶液的環境中,磷脂雙分子層的形成是能量考量偏好的過程[52]。這稱為疏水效應。在水溶液中,磷脂極性的頭朝向極性的水分子,而疏水的尾巴減少對水的接觸,彼此距離更加緊密,形成囊泡。依脂質浓度的不同,會生成脂質體、膠束(micelle)及脂質雙分子層。也觀察到有其他聚合的形式,都是兩親分子的脂質多態性的一部份,這是生物物理學學術研究的主題之一[53][54]。在極性介質中生成脂質體及膠束的過程稱為疏水效應[55]。當在極性環境中溶解兩親性或是親脂性的物質,因此這些分子的極性分子(例如水溶液中的水)會更加有序。所以在水溶液的環境中,在親脂性分子附近會有有序的晶籠結構[56]。
能量儲存[编辑]
動植物體內的三酸甘油酯儲存在脂肪組織內,是動植物的主要能量來源之一。脂肪細胞設計為可連續生成或分解三酸甘油酯,而其分解主要是透過由荷爾蒙驅動的脂酶來啟動[57]。脂肪酸的完整氧化可以產生高熱量,約為9 kcal/g,而醣和蛋白質氧化只能產生4 kcal/g的熱量,鳥類之所以可以在不進食的條件下長期間飛行,就是利用體內三酸甘油酯儲存的熱量[58]。
信號傳送[编辑]
最近幾年的研究發現脂質信號傳送是細胞信號傳送中基本的一部份[59][60]。脂質信號傳送可以由G蛋白偶聯受體或是核受體啟動,而且已發現許多不同種類的脂質是信號分子或是第二信使系統的一部份[61]。這類脂質包括1-磷酸鞘氨醇,由神經酰胺衍生的鞘脂,是鈣調節[62]、細胞生長及凋亡有關的信息分子[63],二酸甘油酯(DAG)及磷酸磷脂酰肌醇(PIPs)和蛋白激酶C以鈣來引導的活化有關[64],前列腺素是一種脂肪酸衍生的類二十烷酸,和炎症和免疫有關[65],甾體荷爾蒙包括雌激素、睾酮及皮質醇,調節像生殖、代謝及血壓等機能,像25-羟基胆固醇等氧化膽固醇是肝X受體的激動劑[66]。
其他功能[编辑]
脂溶性維生素(如維生素A、D、E、K)是萜烯的脂質,是人體必需的營養素,儲存在肝臟及脂肪組織中,有許多不同的功能。肉鹼和脂肪酸的運輸及代謝時,進出線粒體有關,其中會進行β-氧化[67]。在運輸寡糖進出細胞膜的過程中,聚異戊二烯和其磷酸化的衍生物也起到重要的作用的。聚異戊二烯醇的磷酸糖及二磷酸糖在細胞質外的糖基化反應、細胞外的生物多醣合成(例如細菌進行的肽聚醣聚合)及真核蛋白質的N-糖基化中都有其作用[68][69]。心磷脂是一種含有四個酰基及三個甘油基團的甘油酰磷脂,在線粒體內膜中相當豐富[70][71][72]。一般認為他們可以活化和氧化磷酸化有關的酶[73]。脂質也是形成甾體荷爾蒙的原料[74]。
代謝體學[编辑]
人類和其他動物食物常見的脂質有動物及植物的三酸甘油酯、固醇,和生物膜的磷脂。脂質代謝的過程可以合成及降解儲存的脂質,並產生個別組織需要的結構性及機能性的脂質。
生物合成[编辑]
動物若攝取了過量的醣類,過量的醣類會轉換為三酸甘油酯,過程中包括由乙酰辅酶A合成脂肪酸,以及將脂肪酸酯化形成三酸甘油酯,後者稱為脂肪生成[75]。脂肪酸合酶合成脂肪酸的過程是先聚合,再還原乙酰辅酶A單元。脂肪酸中的酰鏈是在一連串的反應中延長,一開始先加入乙酰基,還原後得到醇類,脫水得到烯類,再還原後得到烷類。生物合成脂肪酸的酶分為二類,在動物及真菌中,脂肪酸的合成反應是由單一的多功能蛋白質實現[76],而在植物色素體及細菌體內是由不同的酶分工進行[77][78]。脂肪酸會轉換為三酸甘油酯,包裹在脂蛋白中,並在肝臟中釋出。
不飽和脂肪酸的生成需要脂肪酸去饱和反應,在脂肪醯基中引入雙鍵酸。在人體身內,硬脂酸透過固醇辅酶A去饱和酶1會變成油酸,是單元不飽和脂肪酸。但人體組織無法生成有二個雙鍵的亚油酸及三個雙鍵的Α-亞麻酸,因此這些多元不飽和脂肪酸需在飲食中攝取,稱為必需脂肪酸[79]。
三酸甘油酯的生成是在內質網中進行,其中在乙酰辅酶A中的酰基轉換為甘油-3-磷酸及二酸甘油酯中的羥基[80]。
萜烯和類萜(如類胡蘿蔔素)的生成是由異戊二烯單元的組合和修飾,異戊二烯單元是由活性的前驅體焦磷酸異戊烷及焦磷酸二甲基烯丙酯提供[81]。前驅體的生成方式有許多種:在動物及古菌中會透過甲羟戊酸途径,由乙酰辅酶A產生這些化合物[82],而在植物和細菌中非甲羟戊酸途径用丙酮酸及甘油醛3-磷酸來產生[81][83]。會用到這些化合物的一種重要反應為甾體生成反應,其中會結合異戊二烯單元,生成鲨烯,再摺疊產生甾體環,生成羊毛固醇[84]。羊毛固醇可以生成像膽固醇及麥角固醇等固醇[84][85]。
降解[编辑]
脂肪酸的代謝是透過在粒線體或/及過氧化體中進行的β-氧化反應,產生乙醯輔酶A。大部份的情形中,脂肪酸氧化的機制類似脂肪酸合成的逆反應。在脱氢、水合及氧化反應後,脂肪酸會脫落二個碳,藉由硫解產生酮酸。乙醯輔酶A最後會由三羧酸循環及電子傳遞鏈,轉換為三磷酸腺苷(ATP)、CO2及H2O。
若體內沒有葡萄糖或是含量不多時,三羧酸循環可以由乙醯輔酶A開始,並且分解脂肪以產生能量。
脂肪酸棕櫚酸酯在完全氧化後,可產生對應106個ATP的能量[86]。不飽和脂肪酸及奇數鏈長的脂肪酸需要額外的酶反應才能降解。
营养和健康[编辑]
大部份食物中的脂質是三酸甘油酯、甾醇和磷脂。若食物中有一些脂質,有助於脂溶性的維生素(如維生素A、D、E、K)及類胡蘿蔔素的吸收[87]。人類和其他哺乳類因為無法合成一些特定的脂肪酸,需要藉由食物攝取,稱為必需脂肪酸,例如ω-6脂肪酸的亚油酸及ω-3脂肪酸的α-亞麻酸[79] 。上述兩種脂肪酸都是18個碳的多元不飽和脂肪酸,但雙鍵的數量和位置有所不同。大部份的植物油含有大量的亚油酸,像是紅花油、葵花籽油及玉米油等。α-亞麻酸則主要是在植物的葉子及以一些特定的種子、核果及豆類中,例如亞麻、油菜籽、核桃及大豆[88]。魚油中有大量長鏈的ω-3脂肪酸,例如二十碳五烯酸(EPA)和二十二碳六烯酸(DHA)。[89]許多研究顯示攝取ω-3脂肪酸對於嬰兒發展、癌症及心血管疾病的預防,以及像抑鬱症,注意力缺陷多動障礙和癡呆等精神疾病的預防都有幫助[90][91]。相反的,攝取由植物油部份氫化產生的反式脂肪是可能造成心血管疾病的危險因子[92][93][94]。
許多研究指出每日脂肪的攝取量和肥胖症[95][96]及糖尿病[97][98]的風險有正相關。不過也有許多研究指出脂肪的攝取量和這些疾病沒有相關性,這些研究包括女性健康行动針對約五萬名婦女為期八年的饮食调整试验、護士健康研究以及衛生專業人員的隨訪研究等[99][100][101]。這些研究認為熱量中來自脂肪的比例和癌症、心臟疾病和體重的增加沒有關係。哈佛公共衛生學院營養系的網站Nutrition Source總結了飲食中總脂肪量對人體的影響:「詳細的研究(其中大部份是在哈佛進行)指出,飲食中總脂肪量和體重的變化或是疾病沒有關係。」[102]。
相關條目[编辑]
参考文献[编辑]
- ^ Maitland, Jr Jones. Organic Chemistry. W W Norton & Co Inc (Np). 1998: 139. ISBN 0-393-97378-6.
- ^ Stryer et al., p. 328.
- ^ Stryer et al., p. 330.
- ^ 生物1 必修 分子与细胞. 人民教育出版社. 2007: 32–33. ISBN 978-7-107-17670-8.
- ^ 5.0 5.1 Fahy E, Subramaniam S, Murphy R, Nishijima M, Raetz C, Shimizu T, Spener F, Van Meer G, Wakelam M and Dennis E.A. Update of the LIPID MAPS comprehensive classification system for lipids. Journal of Lipid Research. 2009, 50 (Supplement): S9–S14. PMC 2674711
 . PMID 19098281. doi:10.1194/jlr.R800095-JLR200.
. PMID 19098281. doi:10.1194/jlr.R800095-JLR200.
- ^ Subramaniam S, Fahy E, Gupta S, Sud M, Byrnes RW, Cotter D, Dinasarapu AR, Maurya MR. Bioinformatics and systems biology of the lipidome. Chemical Reviews. October 2011, 111 (10): 6452–6490. PMC 3383319
 . PMID 21939287. doi:10.1021/cr200295k.
. PMID 21939287. doi:10.1021/cr200295k.
- ^ Fahy E, Subramaniam S, Brown HA; et al. A comprehensive classification system for lipids. Journal of Lipid Research. 2005, 46 (5): 839–61. PMID 15722563. doi:10.1194/jlr.E400004-JLR200.
- ^ 蔡潭溪、刘平生、杨福全、杨福愉. 脂质组学研究进展 (PDF). 生物化学与生物物理进展. 2010, 37 (2): 121–128 [2013-04-11]. (原始内容存档 (PDF)于2016-03-05).
- ^ Michelle A, Hopkins J, McLaughlin CW, Johnson S, Warner MQ, LaHart D, Wright JD. Human Biology and Health. Englewood Cliffs, New Jersey, USA: Prentice Hall. 1993. ISBN 0-13-981176-1. OCLC 32308337.
- ^ Segré D, Ben-Eli D, Deamer DW, Lancet D. The lipid world (PDF). Origins of Life and Evolution of the Biosphere. 2001, 31 (1–2): 119–45 [2022-02-13]. Bibcode:2001OLEB...31..119S. PMID 11296516. S2CID 10959497. doi:10.1023/A:1006746807104. (原始内容 (PDF)存档于2008-09-11).
- ^ Mashaghi S., Jadidi T., Koenderink G., Mashaghi A. Lipid Nanotechnology. Int. J. Mol. Sci. 2013, 2013 (14): 4242–4282 [2013-04-11]. doi:10.3390/ijms14024242. (原始内容存档于2019-09-03).
- ^ Vance JE, Vance DE. Biochemistry of Lipids, Lipoproteins and Membranes. Amsterdam: Elsevier. 2002. ISBN 0-444-51139-3. OCLC 51001207.
- ^ Brown HA (编). Lipodomics and Bioactive Lipids: Mass Spectrometry Based Lipid Analysis, Volume 432 (Methods in Enzymology). Boston: Academic Press. 2007. ISBN 0-12-373895-4. OCLC 166624879.
- ^ Mandal, Ananya. Types of Lipids. news-medical.net. [2014-07-08]. (原始内容存档于2016-01-10).
- ^ Hunt SM, Groff JL, Gropper SAS. Advanced Nutrition and Human Metabolism. Belmont, CA: West Pub. Co. 1995: 98. ISBN 0-314-04467-1.
- ^ YashRoy R.C. (1987) 13-C NMR studies of lipid fatty acyl chains of chloroplast membranes. Indian Journal of Biochemistry and Biophysics, vol. 24(6), pp. 177-178.https://www.researchgate.net/publication/230822408_13-C_NMR_studies_of_lipid_fatty_acyl_chains_of_chloroplast_membranes?ev=prf_pub (页面存档备份,存于互联网档案馆)
- ^ Hunter JE. Dietary trans fatty acids: review of recent human studies and food industry responses. Lipids. November 2006, 41 (11): 967–92. PMID 17263298. doi:10.1007/s11745-006-5049-y.
- ^ A Long Lipid, a Long Name: Docosahexaenoic Acid. The Lipid Chronicles. [2011-12-31]. (原始内容存档于2016-03-28).
- ^ DHA FOR OPTIMAL BRAIN AND VISUAL FUNCTIONING. DHA/EPA Omega-3 Institute. [2014-07-08]. (原始内容存档于2016-03-10).
- ^ Fezza F, De Simone C, Amadio D, Maccarrone M. Fatty acid amide hydrolase: a gate-keeper of the endocannabinoid system. Subcellular Biochemistry. Subcellular Biochemistry. 2008, 49: 101–32. ISBN 978-1-4020-8830-8. PMID 18751909. doi:10.1007/978-1-4020-8831-5_4.
- ^ Coleman RA, Lee DP. Enzymes of triglyceride synthesis and their regulation. Progress in Lipid Research. 2004, 43 (2): 134–76. PMID 14654091. doi:10.1016/S0163-7827(03)00051-1.
- ^ van Holde and Mathews, p. 630–31.
- ^ Hölzl G, Dörmann P. Structure and function of glycoglycerolipids in plants and bacteria. Progress in Lipid Research. 2007, 46 (5): 225–43. PMID 17599463. doi:10.1016/j.plipres.2007.05.001.
- ^ Honke K, Zhang Y, Cheng X, Kotani N, Taniguchi N. Biological roles of sulfoglycolipids and pathophysiology of their deficiency. Glycoconjugates Journal. 2004, 21 (1–2): 59–62. PMID 15467400. doi:10.1023/B:GLYC.0000043749.06556.3d.
- ^ The Structure of a Membrane. The Lipid Chronicles. [2011-12-31]. (原始内容存档于2016-06-10).
- ^ Berridge MJ, Irvine RF. Inositol phosphates and cell signalling. Nature Journal. 1989, 341 (1): 197–205. doi:10.1038/341197a0.
- ^ Farooqui AA, Horrocks LA, Farooqui T. Glycerophospholipids in brain: their metabolism, incorporation into membranes, functions, and involvement in neurological disorders. Chemistry and Physics of Lipids. 2000, 106 (1): 1–29. PMID 10878232. doi:10.1016/S0009-3084(00)00128-6.
- ^ Ivanova PT, Milne SB, Byrne MO, Xiang Y, Brown HA. Glycerophospholipid identification and quantitation by electrospray ionization mass spectrometry. Methods in Enzymology. Methods in Enzymology. 2007, 432: 21–57. ISBN 9780123738950. PMID 17954212. doi:10.1016/S0076-6879(07)32002-8.
- ^ van Holde and Mathews, p. 844.
- ^ Paltauf F. Ether lipids in biomembranes. Chemistry and Physics of Lipids. 1994, 74 (2): 101–39. PMID 7859340. doi:10.1016/0009-3084(94)90054-X.
- ^ Merrill AH, Sandhoff K. (2002). "Sphingolipids: metabolism and cell signaling" (页面存档备份,存于互联网档案馆), Ch. 14 in New Comprehensive Biochemistry: Biochemistry of Lipids, Lipoproteins, and Membranes, Vance, D.E. and Vance, J.E., eds. Elsevier Science, NY, ISBN 978-0-12-182212-5.
- ^ Devlin, pp. 421–22.
- ^ Hori T, Sugita M. Sphingolipids in lower animals. Prog. Lipid Res. 1993, 32 (1): 25–45. PMID 8415797. doi:10.1016/0163-7827(93)90003-F.
- ^ Wiegandt H. Insect glycolipids. Biochimica et Biophysica Acta. 1992, 1123 (2): 117–26. PMID 1739742. doi:10.1016/0005-2760(92)90101-Z.
- ^ Guan X, Wenk MR. Biochemistry of inositol lipids. Frontiers in Bioscience. 2008, 13 (13): 3239–51. PMID 18508430. doi:10.2741/2923.
- ^ Bach D, Wachtel E. Phospholipid/cholesterol model membranes: formation of cholesterol crystallites. Biochim Biophys Acta. 2003, 1610 (2): 187–97. PMID 12648773. doi:10.1016/S0005-2736(03)00017-8.
- ^ Stryer et al., p. 749.
- ^ Bouillon R, Verstuyf A, Mathieu C, Van Cromphaut S, Masuyama R, Dehaes P, Carmeliet G. Vitamin D resistance. Best Practice & Research. Clinical Endocrinology & Metabolism. 2006, 20 (4): 627–45. PMID 17161336. doi:10.1016/j.beem.2006.09.008.
- ^ Russell DW. The enzymes, regulation, and genetics of bile acid synthesis. Annual Review of Biochemistry. 2003, 72: 137–74. PMID 12543708. doi:10.1146/annurev.biochem.72.121801.161712.
- ^ Villinski JC, Hayes JM, Brassell SC, Riggert VL, Dunbar RB. Sedimentary sterols as biogeochemical indicators in the Southern Ocean. Organic Geochemistry. 2008, 39 (5): 567–88. doi:10.1016/j.orggeochem.2008.01.009.
- ^ Deacon J. Fungal Biology. Cambridge, MA: Blackwell Publishers. 2005: 342. ISBN 1-4051-3066-0.
- ^ Kuzuyama T, Seto H. Diversity of the biosynthesis of the isoprene units. Natural Product Reports. 2003, 20 (2): 171–83. PMID 12735695. doi:10.1039/b109860h.
- ^ Rao AV, Rao LG. Carotenoids and human health. Pharmacological Research : the Official Journal of the Italian Pharmacological Society. 2007, 55 (3): 207–16. PMID 17349800. doi:10.1016/j.phrs.2007.01.012.
- ^ Brunmark A, Cadenas E. Redox and addition chemistry of quinoid compounds and its biological implications. Free Radical Biology & Medicine. 1989, 7 (4): 435–77. PMID 2691341. doi:10.1016/0891-5849(89)90126-3.
- ^ Swiezewska E, Danikiewicz W. Polyisoprenoids: structure, biosynthesis and function. Progress in Lipid Research. 2005, 44 (4): 235–58. PMID 16019076. doi:10.1016/j.plipres.2005.05.002.
- ^ 46.0 46.1 Raetz CR, Garrett TA, Reynolds CM, Shaw WA, Moore JD, Smith DC Jr, Ribeiro AA, Murphy RC,Ulevitch RJ, Fearns C, Reichart D, Glass CK, Benner C, Subramaniam S, Harkewicz R, Bowers-Gentry RC, Buczynski MW, Cooper JA, Deems RA, Dennis EA. Kdo2-Lipid A of Escherichia coli, a defined endotoxin that activates macrophages via TLR-4. Journal of Lipid Research. 2006, 47 (5): 1097–111. PMID 16479018. doi:10.1194/jlr.M600027-JLR200.
- ^ Walsh CT. Polyketide and nonribosomal peptide antibiotics: modularity and versatility. Science. 2004, 303 (5665): 1805–10. PMID 15031493. doi:10.1126/science.1094318.
- ^ Caffrey P, Aparicio JF, Malpartida F, Zotchev SB. Biosynthetic engineering of polyene macrolides towards generation of improved antifungal and antiparasitic agents. Current Topics in Medicinal Chemistry. 2008, 8 (8): 639–53 [2009-04-12]. PMID 18473889. doi:10.2174/156802608784221479.[永久失效連結]
- ^ Minto RE, Blacklock BJ. Biosynthesis and function of polyacetylenes and allied natural products. Progress in Lipid Research. 2008, 47 (4): 233–306. PMC 2515280
 . PMID 18387369. doi:10.1016/j.plipres.2008.02.002.
. PMID 18387369. doi:10.1016/j.plipres.2008.02.002.
- ^ Stryer et al., pp. 329–331
- ^ YashRoy R.C. (1990) Magnetic resonance studies of the dynamic organisation of lipids of chloroplast membranes. Journal of Biosciences, vol. 15(4), pp. 281-288.https://www.researchgate.net/publication/225688482_Magnetic_resonance_studies_of_dynamic_organisation_of_lipids_in_chloroplast_membranes?ev=prf_pub
- ^ Stryer et al., pp. 333–34.
- ^ van Meer G, Voelker DR, Feigenson GW. Membrane lipids: where they are and how they behave. Nature Reviews Molecular Cell Biology. 2008, 9 (2): 112–24. PMC 2642958
 . PMID 18216768. doi:10.1038/nrm2330.
. PMID 18216768. doi:10.1038/nrm2330.
- ^ Feigenson GW. Phase behavior of lipid mixtures. Nature Chemical Biology. 2006, 2 (11): 560–63. PMC 2685072
 . PMID 17051225. doi:10.1038/nchembio1106-560.
. PMID 17051225. doi:10.1038/nchembio1106-560.
- ^ Wiggins PM. Role of water in some biological processes. Microbiological Reviews. 1990, 54 (4): 432–49. PMC 372788
 . PMID 2087221.
. PMID 2087221.
- ^ Raschke TM, Levitt M. Nonpolar solutes enhance water structure within hydration shells while reducing interactions between them. Proceedings of the National Academy of Sciences of the United States of America. 2005, 102 (19): 6777–82. PMC 1100774
 . PMID 15867152. doi:10.1073/pnas.0500225102.
. PMID 15867152. doi:10.1073/pnas.0500225102.
- ^ Brasaemle DL. Thematic review series: adipocyte biology. The perilipin family of structural lipid droplet proteins: stabilization of lipid droplets and control of lipolysis. J. Lipid Res. December 2007, 48 (12): 2547–59 [2014-07-11]. PMID 17878492. doi:10.1194/jlr.R700014-JLR200. (原始内容存档于2010-07-06).
- ^ Stryer et al., p. 619.
- ^ Wang X. Lipid signaling. Current Opinion in Plant Biology. 2004, 7 (3): 329–36. PMID 15134755. doi:10.1016/j.pbi.2004.03.012.
- ^ Dinasarapu AR,Saunders B,Ozerlat I,Azam K, and Subramaniam S. Signaling gateway molecule pages—a data model perspective. Bioinformatics. 2011, 27 (12): 1736–1738. PMC 3106186
 . PMID 21505029. doi:10.1093/bioinformatics/btr190.
. PMID 21505029. doi:10.1093/bioinformatics/btr190.
- ^ Eyster KM. The membrane and lipids as integral participants in signal transduction. Advances in Physiology Education. 2007, 31 (1): 5–16. PMID 17327576. doi:10.1152/advan.00088.2006.
- ^ Hinkovska-Galcheva V, VanWay SM, Shanley TP, Kunkel RG. The role of sphingosine-1-phosphate and ceramide-1-phosphate in calcium homeostasis. Current Opinion in Investigational Drugs. 2008, 9 (11): 1192–205. PMID 18951299.
- ^ Saddoughi SA, Song P, Ogretmen B. Roles of bioactive sphingolipids in cancer biology and therapeutics. Subcellular Biochemistry. Subcellular Biochemistry. 2008, 49: 413–40. ISBN 978-1-4020-8830-8. PMC 2636716
 . PMID 18751921. doi:10.1007/978-1-4020-8831-5_16.
. PMID 18751921. doi:10.1007/978-1-4020-8831-5_16.
- ^ Klein C, Malviya AN. Mechanism of nuclear calcium signaling by inositol 1,4,5-trisphosphate produced in the nucleus, nuclear located protein kinase C and cyclic AMP-dependent protein kinase. Frontiers in Bioscience. 2008, 13 (13): 1206–26 [2014-07-12]. PMID 17981624. doi:10.2741/2756. (原始内容存档于2021-02-07).
- ^ Boyce JA. Eicosanoids in asthma, allergic inflammation, and host defense. Current Molecular Medicine. 2008, 8 (5): 335–49. PMID 18691060. doi:10.2174/156652408785160989.
- ^ Bełtowski J. Liver X receptors (LXR) as therapeutic targets in dyslipidemia. Cardiovascular Therapy. 2008, 26 (4): 297–316. PMID 19035881. doi:10.1111/j.1755-5922.2008.00062.x.
- ^ Indiveri C, Tonazzi A, Palmieri F. Characterization of the unidirectional transport of carnitine catalyzed by the reconstituted carnitine carrier from rat liver mitochondria. Biochim. Biophys. Acta. October 1991, 1069 (1): 110–6. PMID 1932043. doi:10.1016/0005-2736(91)90110-T.
- ^ Parodi AJ, Leloir LF. The role of lipid intermediates in the glycosylation of proteins in the eucaryotic cell. Biochim. Biophys. Acta. April 1979, 559 (1): 1–37. PMID 375981. doi:10.1016/0304-4157(79)90006-6.
- ^ Helenius A, Aebi M. Intracellular functions of N-linked glycans. Science. 2001, 291 (5512): 2364–69. PMID 11269317. doi:10.1126/science.291.5512.2364.
- ^ Nowicki, M. and Frentzen, M. Cardiolipin synthase of Arabidopsis thaliana. FEBS Letters. 2005, 579 (10): 2161–2165. PMID 15811335. doi:10.1016/j.febslet.2005.03.007.
- ^ Nowicki, M. Characterization of the Cardiolipin Synthase from Arabidopsis thaliana. Ph.D. thesis, RWTH-Aachen University. 2006 [2014-07-12]. (原始内容存档于2011-10-05).
- ^ Gohil VM, Greenberg ML. Mitochondrial membrane biogenesis: phospholipids and proteins go hand in hand. Journal of Cell Biology. 2009, 184 (4): 469–72. PMC 2654137
 . PMID 19237595. doi:10.1083/jcb.200901127.
. PMID 19237595. doi:10.1083/jcb.200901127.
- ^ Hoch FL. Cardiolipins and biomembrane function. Biochimica et Biophysica Acta. 1992, 1113 (1): 71–133. PMID 10206472. doi:10.1016/0304-4157(92)90035-9.
- ^ Steroids 互联网档案馆的存檔,存档日期2011-10-23.. Elmhurst.edu. Retrieved on 2013-10-10.
- ^ Stryer et al., p. 634.
- ^ Chirala S, Wakil S. Structure and function of animal fatty acid synthase. Lipids. 2004, 39 (11): 1045–53. PMID 15726818. doi:10.1007/s11745-004-1329-9.
- ^ White S, Zheng J, Zhang Y. The structural biology of type II fatty acid biosynthesis. Annual Review of Biochemistry. 2005, 74: 791–831. PMID 15952903. doi:10.1146/annurev.biochem.74.082803.133524.
- ^ Ohlrogge J, Jaworski J. Regulation of fatty acid synthesis. Annual Review of Plant Physiology and Plant Molecular Biology. 1997, 48: 109–136. PMID 15012259. doi:10.1146/annurev.arplant.48.1.109.
- ^ 79.0 79.1 Stryer et al., p. 643.
- ^ Stryer et al., pp. 733–39.
- ^ 81.0 81.1 Kuzuyama T, Seto H. Diversity of the biosynthesis of the isoprene units. Natural Product Reports. 2003, 20 (2): 171–83. PMID 12735695. doi:10.1039/b109860h.
- ^ Grochowski L, Xu H, White R. Methanocaldococcus jannaschii uses a modified mevalonate pathway for biosynthesis of isopentenyl diphosphate. Journal of Bacteriology. 2006, 188 (9): 3192–98. PMC 1447442
 . PMID 16621811. doi:10.1128/JB.188.9.3192-3198.2006.
. PMID 16621811. doi:10.1128/JB.188.9.3192-3198.2006.
- ^ Lichtenthaler H. The 1-Dideoxy-D-xylulose-5-phosphate pathway of isoprenoid biosynthesis in plants. Annual Review of Plant Physiology and Plant Molecular Biology. 1999, 50: 47–65. PMID 15012203. doi:10.1146/annurev.arplant.50.1.47.
- ^ 84.0 84.1 Schroepfer G. Sterol biosynthesis. Annual Review of Biochemistry. 1981, 50: 585–621. PMID 7023367. doi:10.1146/annurev.bi.50.070181.003101.
- ^ Lees N, Skaggs B, Kirsch D, Bard M. Cloning of the late genes in the ergosterol biosynthetic pathway of Saccharomyces cerevisiae—a review. Lipids. 1995, 30 (3): 221–26. PMID 7791529. doi:10.1007/BF02537824.
- ^ Stryer et al., pp. 625–26.
- ^ Bhagavan, p. 903.
- ^ Russo GL. Dietary n-6 and n-3 polyunsaturated fatty acids: from biochemistry to clinical implications in cardiovascular prevention. Biochemical Pharmacology. 2009, 77 (6): 937–46. PMID 19022225. doi:10.1016/j.bcp.2008.10.020.
- ^ Bhagavan, p. 388.
- ^ Riediger ND, Othman RA, Suh M, Moghadasian MH. A systemic review of the roles of n-3 fatty acids in health and disease. Journal of the American Dietetic Association. 2009, 109 (4): 668–79. PMID 19328262. doi:10.1016/j.jada.2008.12.022.
- ^ Galli C, Risé P. Fish consumption, omega 3 fatty acids and cardiovascular disease. The science and the clinical trials. Nutrition and Health (Berkhamsted, Hertfordshire). 2009, 20 (1): 11–20. PMID 19326716. doi:10.1177/026010600902000102.
- ^ Micha R, Mozaffarian D. Trans fatty acids: effects on cardiometabolic health and implications for policy. Prostaglandins, Leukotrienes, and Essential Fatty Acids. 2008, 79 (3–5): 147–52. PMC 2639783
 . PMID 18996687. doi:10.1016/j.plefa.2008.09.008.
. PMID 18996687. doi:10.1016/j.plefa.2008.09.008.
- ^ Dalainas I, Ioannou HP. The role of trans fatty acids in atherosclerosis, cardiovascular disease and infant development. International Angiology: a Journal of the International Union of Angiology. 2008, 27 (2): 146–56. PMID 18427401.
- ^ Mozaffarian D, Willett WC. Trans fatty acids and cardiovascular risk: a unique cardiometabolic imprint?. Current Atherosclerosis Reports. 2007, 9 (6): 486–93. PMID 18377789. doi:10.1007/s11883-007-0065-9.
- ^ Astrup A, Dyerberg J, Selleck M, Stender S. Nutrition transition and its relationship to the development of obesity and related chronic diseases. Obesity Review. 2008,. 9 Suppl 1: 48–52. PMID 18307699. doi:10.1111/j.1467-789X.2007.00438.x.
- ^ Astrup A. The role of dietary fat in obesity. Seminars in Vascular Medicine. 2005, 5 (1): 40–47. PMID 15968579. doi:10.1055/s-2005-871740.
- ^ Ma Y.; Olendzki, Barbara C.; Hafner, Andrea R.; Chiriboga, David E.; Culver, Annie L.; Andersen, Victoria A.; Merriam, Philip A.; Pagoto, Sherry L.; et al. Low-carbohydrate and high-fat intake among adult patients with poorly controlled type 2 diabetes mellitus. Nutrition. 2006, 22 (11–12): 1129–1136. PMC 2039705
 . PMID 17027229. doi:10.1016/j.nut.2006.08.006.
. PMID 17027229. doi:10.1016/j.nut.2006.08.006.
- ^ Astrup A. Dietary management of obesity. JPEN Journal of Parenteral and Enteral Nutrition. 2008, 32 (5): 575–77. PMID 18753397. doi:10.1177/0148607108321707.
- ^ Beresford SA, Johnson KC, Ritenbaugh C; et al. Low-fat dietary pattern and risk of colorectal cancer: the Women's Health Initiative Randomized Controlled Dietary Modification Trial. JAMA: the Journal of the American Medical Association. 2006, 295 (6): 643–54. PMID 16467233. doi:10.1001/jama.295.6.643.
- ^ Howard BV, Manson JE, Stefanick ML; et al. Low-fat dietary pattern and weight change over 7 years: the Women's Health Initiative Dietary Modification Trial. JAMA: the Journal of the American Medical Association. 2006, 295 (1): 39–49. PMID 16391215. doi:10.1001/jama.295.1.39.
- ^ Howard BV, Van Horn L, Hsia J; et al. Low-fat dietary pattern and risk of cardiovascular disease: the Women's Health Initiative Randomized Controlled Dietary Modification Trial. JAMA : the Journal of the American Medical Association. 2006, 295 (6): 655–66. PMID 16467234. doi:10.1001/jama.295.6.655.
- ^ Fats and Cholesterol: Out with the Bad, In with the Good — What Should You Eat? – The Nutrition Source — Harvard School of Public Health. [2009-05-12]. (原始内容存档于2011-04-27).
外部連結[编辑]
- 入門
- 脂質相關網站列表 (英文)
- 天然脂質學入口網站 (页面存档备份,存于互联网档案馆) - 近期脂質研究之摘要 (英文)
- 脂質資料庫 - 脂質化學與生物化學之文獻 (英文)
- Cyberlipid.org (页面存档备份,存于互联网档案馆) - 脂質相關歷史與資源 (英文)
- 電腦模擬分子 (页面存档备份,存于互联网档案馆) - 膜脂模型 (英文)
- 脂質、膜和囊泡運輸 - 生物化學和細胞生物學的虛擬圖書館 (英文)
- 命名
- IUPAC命名法:脂質 (页面存档备份,存于互联网档案馆) (英文)
- IUPAC詞彙表:脂質類分子 (英文)
- 数据库
- LIPID MAPS (页面存档备份,存于互联网档案馆) - 脂質及其相關之基因/蛋白質資料 (英文)
- LipidBank (页面存档备份,存于互联网档案馆) - 脂質與其相關性質、光譜數據及文獻 (日語)
- LIPIDAT (页面存档备份,存于互联网档案馆) - 磷脂和相關熱力學資訊 (英文)
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
