代谢:修订间差异
小 機器人 新增: ast:Metabolismu |
內容擴充 |
||
| 第1行: | 第1行: | ||
[[Image:ATP-3D-vdW.png|thumb|right|280px|[[ |
[[Image:ATP-3D-vdW.png|thumb|right|280px|[[辅酶]][[三磷酸腺苷]]的结构,它是能量代谢的核心中间物。]] |
||
'''代谢'''是[[生物体]]内所发生的用于维持[[生命]]的一系列[[化学反应]]的总称。这些反应进程使得生物体能够生长和[[繁殖]]、保持它们的结构以及对外界环境做出反应。代谢通常被分为两类:[[分解代谢]]可以对大的分子进行分解以获得能量(如[[细胞呼吸]]);[[合成代谢]]则可以利用能量来合成细胞中的各个组分,如[[蛋白质]]和[[核酸]]等。代谢可以被认为是[[生物体]]不断进行[[物质]]和[[能量]]交换的过程,一旦物质和能量的交换停止,生物体的结构和系统就会解体。 |
|||
代谢中的化学反应可以被归纳为[[代谢途径]],通过一系列[[酶]]的作用将一种化学物质转化为另一种化学物质。酶对于代谢来说是至关重要的,因为它们的[[催化]]作用使得生物体可以进行[[热力学]]上难以发生的反应。当外界环境发生变化或接受来自其他[[细胞]]的[[信号转导|信号]]时,细胞也需要通过酶来实现对代谢途径的调控,从而对这些变化和信号做出反应。 |
|||
'''代谢''',有时也用'''[[新陳代謝]]'''来指代,是指[[生物体]]不断同[[外界]]环境进行[[物质]]和[[能量]]交换的过程。生物体是一个[[结构]]和[[功能]]都严整有序的[[开放系统]]。它的严整有序性是靠不断同外界环境进行[[物质]]和[[能量]]的[[交换]]来维持的,一旦物质和能量的交换停止,结构和系统就会解体。 |
|||
一个生物体的代谢机制决定了哪些物质对于此生物体是[[营养|有营养的]],而哪些是[[毒物|有毒的]]。例如,一些[[原核生物]]利用[[硫化氢]]作为营养物质,但这种气体对于[[动物]]来说却是致命的。<ref>{{en}}{{cite journal en|author=Friedrich C |title=Physiology and genetics of sulfur-oxidizing bacteria |journal=Adv Microb Physiol |volume=39 |issue= |pages=235-89 |year=1998 |pmid=9328649}}</ref>代谢速度,或者说[[代谢率]],也影响了一个生物体对于食物的需求量。 |
|||
各种生物都有代谢。代谢包括[[同化作用]]和[[异化作用]]。同化作用是形成[[有机物]]和贮存能量的过程;异化作用是分解有机物、释放能量的过程。代谢是一系列极其复杂的、有精确顺序的[[酶促反应]]的总和。各种生物的基本代谢途径相似,各个相应步骤所需的[[酶]]相同。各种生物都以[[三磷酸腺苷]]([[ATP]])为其贮能和放能的中心物质。 |
|||
代谢的一个很大的特点是:即使是差异巨大的不同物种,它们之间的基本代谢途径也还是相似的。例如,[[羧酸]],作为[[柠檬酸循环]]中的最为人们所知的中间产物,存在于所有的生物体中,无论是[[微生物|单细胞]]的[[细菌]]还是巨大的[[多细胞生物|多细胞]]生物如[[大象]]。<ref name=SmithE>{{en}}{{cite journal en|author=Smith E, Morowitz H |title=Universality in intermediary metabolism |url=http://www.pubmedcentral.nih.gov/articlerender.fcgi?tool=pubmed&pubmedid=15340153 |journal=Proc Natl Acad Sci U S A |volume=101 |issue=36 |pages=13168-73 |year=2004 |pmid=15340153}}</ref>代谢中所存在的这样的相似性很可能是由于相关代谢途径的高效率以及在进化史早期就出现的结果。<ref name=Ebenhoh>{{en}}{{cite journal en|author=Ebenhöh O, Heinrich R |title=Evolutionary optimization of metabolic pathways. Theoretical reconstruction of the stoichiometry of ATP and NADH producing systems |journal=Bull Math Biol |volume=63 |issue=1 |pages=21–55 |year=2001 |pmid=11146883}}</ref><ref name=Cascante>{{en}}{{cite journal en|author=Meléndez-Hevia E, Waddell T, Cascante M |title=The puzzle of the Krebs citric acid cycle: assembling the pieces of chemically feasible reactions, and opportunism in the design of metabolic pathways during evolution |journal=J Mol Evol |volume=43 |issue=3 |pages=293–303 |year=1996 |pmid=8703096}}</ref> |
|||
==外部連結== |
|||
*[http://www2.ufp.pt/~pedros/bq/integration.htm Overview of the Major metabolic pathways (英文)] |
|||
==历史== |
|||
主要的代谢过程有: |
|||
{{see also|生物化学史|分子生物学史}} |
|||
* [[醣代谢]] |
|||
[[Image:SantoriosMeal.jpg|thumb|right|150px|[[:en:Santorio Santorio|桑托里奥]]在他的秤中,摘自《''Ars de statica medecina''》,1614年首次出版。]] |
|||
* [[蛋白质代谢]] |
|||
对于代謝的科学研究已经跨越了数个世纪,从早期对于动物整体代谢的研究一直到现代生物化学中对于单个代谢反应机制的探索。代谢的概念的出现可以追溯到13世纪,[[阿拉伯]]医学家[[伊本·纳菲斯]]([[:en:Ibn al-Nafis|Ibn al-Nafis]])提出“身体和它的各个部分是处于一个分解和接受营养的连续状态,因此它们不可避免地一直发生着变化”。<ref name=Roubi>{{en}}Dr. Abu Shadi Al-Roubi (1982), "Ibn Al-Nafis as a philosopher", ''Symposium on Ibn al Nafis'', Second International Conference on Islamic Medicine: Islamic Medical Organization, Kuwait ([[cf.]] [http://www.islamset.com/isc/nafis/drroubi.html Ibnul-Nafees As a Philosopher], ''Encyclopedia of Islamic World'').</ref>第一个关于人体代谢的实验由意大利人[[桑托里奥·桑托里奥]]([[:en:Santorio Santorio|Santorio Santorio]])于1614年完成并发表在他的著作《医学统计方法》(''Ars de statica medecina'')中。<ref>{{en}}{{cite journal en|author=Eknoyan G |title=Santorio Sanctorius (1561–1636) - founding father of metabolic balance studies |journal=Am J Nephrol |volume=19 |issue=2 |pages=226-33 |year=1999 |pmid=10213823}}</ref>在书中,他描述了他如何在进食、睡觉、工作、性生活、斋戒、饮酒以及排泄等各项活动前后对自己的体重进行秤量;他发现大多数他所摄入的食物最终都通过他所称的“无知觉排汗”被消耗掉了。 |
|||
* [[脂肪代谢]] |
|||
* [[核酸代谢]] |
|||
在这些早期研究中,代谢进程的机制还没有被揭示,人们普遍认为存在一种“[[活力论|活力]]”可以活化器官。<ref>{{en}}Williams, H. S. (1904) [http://etext.lib.virginia.edu/toc/modeng/public/Wil4Sci.html A History of Science: in Five Volumes. Volume IV: Modern Development of the Chemical and Biological Sciences] Harper and Brothers (New York) 2008年6月29日查阅</ref>到了19世纪,在对糖被[[酵母]][[发酵|酵解]]为[[酒精]]的研究中,法国科学家[[路易斯·巴斯德]]总结出酵解过程是由酵母细胞内他称为“酵素”的物质来催化的。他写道:“酒精酵解是一种与生命以及酵母细胞的组织相关的,而与细胞的死亡和腐化无关的一种行为。”<ref>{{en}}{{cite journal en|author=Dubos J.|year=1951 |title= Louis Pasteur: Free Lance of Science, Gollancz. Quoted in Manchester K. L. (1995) Louis Pasteur (1822 – 1895)—chance and the prepared mind.|journal= Trends Biotechnol| volume=13 |issue=12 |pages=511–515 |id= PMID 8595136}}</ref>这一发现与[[弗里德里希·维勒]]在1828年发表的关于[[尿素]]的化学合成<ref>{{en}}{{cite journal en|author=Kinne-Saffran E, Kinne R |title=Vitalism and synthesis of urea. From Friedrich Wöhler to Hans A. Krebs |journal=Am J Nephrol |volume=19 |issue=2 |pages=290-4 |year=1999 |pmid=10213830}}</ref>证明了细胞中发现的化学反应和有机物与其他化学无异,都遵循化学的基本原则。 |
|||
20世纪初,[[酶]]首次被[[爱德华·比希纳]]所发现,这一发现使得对代谢中化学反应的研究从对细胞的生物学研究中独立出来,同时这也标志着生物化学研究的开始。<ref>{{en}}爱德华·比希纳在1907年[http://nobelprize.org/nobel_prizes/chemistry/laureates/1907/buchner-lecture.html 诺贝尔颁奖典礼上的演讲],2008年6月29日查阅</ref>从20世纪初开始,人们对于生物化学的了解迅速增加。在现代生物化学家中,[[汉斯·阿道夫·克雷布斯|汉斯·克雷布斯]]是最多产的研究者之一,他对代谢的研究做出了重大的贡献:<ref>{{en}}{{cite journal en|author=Kornberg H |title=Krebs and his trinity of cycles |journal=Nat Rev Mol Cell Biol |volume=1 |issue=3 |pages=225-8 |year=2000 |pmid=11252898}}</ref>他发现了尿素循环,随后又与[[汉斯·科恩伯格]]([[:en:Hans Kornberg|Hans Kornberg]])合作发现了三羧酸循环和乙醛酸循环。<ref>{{en}}Krebs H A, Henseleit K (1932) "Untersuchungen über die Harnstoffbildung im tierkorper." ''Z. Physiol. Chem.'' 210, 33 – 66. {{cite journal en|author=Krebs H, Johnson W |title=Metabolism of ketonic acids in animal tissues |url=http://www.pubmedcentral.nih.gov/articlerender.fcgi?tool=pubmed&pubmedid=16746382 |journal=Biochem J |volume=31 |issue=4 |pages=645-60 |year=1937 |pmid=16746382}}</ref><ref name=Kornberg/>现代生物化学研究受益于大量新技术的应用,诸如[[色谱分析]]、[[X射线晶体学]]、[[蛋白质核磁共振谱学|核磁共振]]、[[电子显微学]]、[[同位素标记]]、[[质谱|质谱分析]]和[[分子动力学]]模拟等。这些技术使得研究者可以发现并具体分析细胞中与代谢途径相关的分子。 |
|||
==关键的生化物质== |
|||
{{see also|生物大分子|细胞|生物化学}} |
|||
动植物和微生物的大部分组成结构是由三类基本生物分子所构成,这三类分子是[[氨基酸]]、[[糖类]]和[[脂类]](通常为称为[[脂肪]])。由于这些分子是维持生命所必需的,代谢既制造这些分子以用于构建细胞和组织,又在摄入食物后将食物中的这些分子消化降解以提供维持生命所需的能量。许多重要的生化物质可以聚合在一起形成[[多聚体]],如[[DNA]]和[[蛋白质]]。这些[[生物大分子]]对于所有的生物体都是必要的组分。下表中列出了一些最常见的生物大分子。 |
|||
{| class="wikitable" style="margin-left: auto; margin-right: auto;" |
|||
!分子类型 |
|||
![[单体]]形式的名称 |
|||
![[多聚体]]形式的名称 |
|||
!多聚体形式的例子 |
|||
|- |
|||
|align="center" |[[氨基酸]] |
|||
|align="center" |氨基酸 |
|||
|align="center" |[[蛋白质]](或[[多肽]]) |
|||
|align="center" |[[纤维蛋白]]和[[球蛋白]] |
|||
|- |
|||
|align="center" |[[糖类]] |
|||
|align="center" |[[单糖]] |
|||
|align="center" |[[多糖]] |
|||
|align="center" |[[淀粉]]、[[糖原]]和[[纤维素]] |
|||
|- |
|||
|align="center" |[[核酸]] |
|||
|align="center" |[[核苷酸]] |
|||
|align="center" |[[多聚核苷酸]] |
|||
|align="center" |[[DNA]]和[[RNA]] |
|||
|} |
|||
[[Image:GLO1 Homo sapiens small fast.gif|thumb|200px|right|人源I型[[乙二醛酶]]的结构。]] |
|||
===氨基酸和蛋白质=== |
|||
[[蛋白质]]是由线性排列[[氨基酸]]所组成,氨基酸之间通过[[肽键]]相互连接。酶是最常见的蛋白质,它们[[催化]]代谢中的各类化学反应。一些蛋白质具有结构或机械功能,如参与形成[[细胞骨架]]以维持细胞形态。<ref>{{en}}{{cite journal en|author=Michie K, Löwe J |title=Dynamic filaments of the bacterial cytoskeleton |journal=Annu Rev Biochem |volume=75 |issue= |pages=467-92 |year=2006 |pmid=16756499}}</ref>还有许多蛋白质在[[信号传导|细胞信号传导]]、[[免疫反应]]、[[细胞黏附]]和[[细胞周期|细胞周期调控]]中扮演重要角色。<ref name=Nelson>{{en}}{{cite book | last = Nelson | first = David L. | coauthors = Michael M. Cox | title = Lehninger Principles of Biochemistry | publisher = W. H. Freeman and company | date = 2005 | location = New York | pages = 841 | isbn = 0-7167-4339-6}}</ref> |
|||
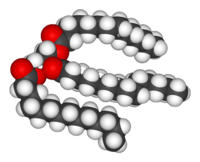
[[Image:Trimyristin-3D-vdW.png|left|thumb|200px|[[三酸甘油酯]]的结构。]] |
|||
===脂类=== |
|||
[[脂类]]是类别最多的生物分子。它们主要的结构用途是形成[[生物膜]],如[[细胞膜]];此外,它们也可以作为机体能量来源。<ref name=Nelson/>脂类通常被定义为[[疏水性]]或[[两性分子|两性]]生物分子,可溶于诸如[[苯]]或[[氯仿]]等[[有机溶剂]]中。<ref>{{en}}{{cite journal en|author=Fahy E, Subramaniam S, Brown H, Glass C, Merrill A, Murphy R, Raetz C, Russell D, Seyama Y, Shaw W, Shimizu T, Spener F, van Meer G, VanNieuwenhze M, White S, Witztum J, Dennis E |title=A comprehensive classification system for lipids |url=http://www.jlr.org/cgi/content/full/46/5/839 |journal=J Lipid Res |volume=46 |issue=5 |pages=839-61 |year=2005 |pmid=15722563}}</ref>[[脂肪]]是由[[脂肪酸]]基团和[[甘油]]基团所组成的一大类脂类化合物;其结构为一个甘油分子上以[[酯]]键连接了三个脂肪酸分子形成[[甘油三酯]]。<ref>{{en}}{{cite web | title=Nomenclature of Lipids |publisher=IUPAC-IUB Commission on Biochemical Nomenclature (CBN) | url=http://www.chem.qmul.ac.uk/iupac/lipid/ |accessdate=2007-03-08}}</ref>在此基本结构基础上,还存在有多种变型,包括不同大小长度的疏水骨架(如[[鞘脂类]]中的[[神经鞘氨醇]]基团)和不同类型的[[亲水性|亲水]]基团(如[[磷脂]]中的[[磷酸盐]]基团)。[[类固醇]](如[[胆固醇]])是另一类由细胞合成的主要的脂类分子。<ref>{{en}}{{cite journal en|author=Hegardt F |title=Mitochondrial 3-hydroxy-3-methylglutaryl-CoA synthase: a control enzyme in ketogenesis |url=http://www.pubmedcentral.nih.gov/picrender.fcgi?artid=1220089&blobtype=pdf |journal=Biochem J |volume=338 (Pt 3) |issue= |pages=569-82 |year=1999 |pmid=10051425}}</ref> |
|||
[[Image:Glucose Fisher to Haworth.gif|thumb|200px|right||[[葡萄糖]]可以以直线型和环形两种形式存在。]] |
|||
===糖类=== |
|||
[[糖类]]为带有大量[[羟基]]的[[醛]]或[[酮]],可以以直链或环的形式存在。糖类是含量最为分赴的生物分子,其具有多种功能,如储存和运输能量(例如[[淀粉]]、[[糖原]])以及作为结构性组分(植物中的[[纤维素]]和动物中的[[几丁质]])。<ref name=Nelson/>糖类的基本组成单位为[[单糖]],包括[[半乳糖]]、[[果糖]]以及十分重要的[[葡萄糖]]。单糖可以通过糖苷键连接在一起形成多糖,而连接的方式极为多样,也就造成了多糖种类的多样性。<ref>{{en}}{{cite journal en|author=Raman R, Raguram S, Venkataraman G, Paulson J, Sasisekharan R |title=Glycomics: an integrated systems approach to structure-function relationships of glycans |journal=Nat Methods |volume=2 |issue=11 |pages=817-24 |year=2005 |pmid=16278650}}</ref> |
|||
[[Image:DNA double helix 45.PNG|thumb|200px|left|[[DNA]]双螺旋結構。]] |
|||
===核苷酸和核酸=== |
|||
[[DNA]]和[[RNA]]是主要的两类[[核酸]],它们都是由[[核苷酸]]连接形成的直链分子。核酸分子对于遗传信息的储存和利用是必不可少的,通过[[转录]]和[[翻译 (遗传学)|翻译]]来完成从遗传信息到蛋白质的过程。<ref name=Nelson/>这些遗传信息由[[DNA修复]]机制来进行保护,并通过[[DNA复制]]来进行扩增。一些[[病毒]](如[[HIV]])含有RNA[[基因组]],它们可以利用[[逆转录]]来从病毒RNA合成DNA模板。<ref>{{en}}{{cite journal en|author=Sierra S, Kupfer B, Kaiser R |title=Basics of the virology of HIV-1 and its replication |journal=J Clin Virol |volume=34 |issue=4 |pages=233-44 |year=2005 |pmid=16198625}}</ref>[[核酶]](如[[剪切体]]和[[核糖体]])中的RNA还具有类似酶的特性,可以催化化学反应。单个核苷酸是由一个[[核糖]]分子连接上一个[[碱基]]来形成。其中,碱基是含氮的[[杂环化合物|杂环]],可以被分为两类:[[嘌呤]]和[[嘧啶]]。核苷酸也可以作为[[辅酶]]参与代谢基团的转移反应。<ref name=Wimmer>{{en}}{{cite journal |author=Wimmer M, Rose I |title=Mechanisms of enzyme-catalyzed group transfer reactions |journal=Annu Rev Biochem |volume=47 |issue= |pages=1031–78 |year=1978 |pmid=354490}}</ref> |
|||
[[Image:Acetyl-CoA-2D.svg|thumb|right|300px|[[乙酰辅酶A]]的结构。可以被转移的[[乙酰基]]结合在最左端的硫原子上。]] |
|||
===辅酶=== |
|||
{{see also|辅酶}} |
|||
代谢中包含了种类广泛的化学反应,但其中大多数反应都属于几类基本的含有功能性基团的转移的反应类型。<ref>{{en}}{{cite journal en|author=Mitchell P |title=The Ninth Sir Hans Krebs Lecture. Compartmentation and communication in living systems. Ligand conduction: a general catalytic principle in chemical, osmotic and chemiosmotic reaction systems |journal=Eur J Biochem |volume=95 |issue=1 |pages=1–20 |year=1979 |pmid=378655}}</ref>这些反应中,细胞利用一系列小分子代谢中间物来在不同的反应之间携带化学基团。<ref name=Wimmer/>这些基团转移的中间物被称为[[辅酶]]。每一类基团转移反应都由一个特定的辅酶来执行,辅酶同时是合成它和消耗它的一系列酶的[[底物]]。这些辅酶不断地被生成、消耗、再被回收利用。<ref name=Dimroth>{{en}}{{cite journal en|author=Dimroth P, von Ballmoos C, Meier T |title=Catalytic and mechanical cycles in F-ATP synthases. Fourth in the Cycles Review Series |url=http://www.pubmedcentral.nih.gov/articlerender.fcgi?tool=pubmed&pubmedid=16607397 |journal=EMBO Rep |volume=7 |issue=3 |pages=276-82 |year=2006 |pmid=16607397}}</ref> |
|||
[[三磷酸腺苷]](ATP)是生命体中最重要的辅酶之一,它是细胞中能量流通的普遍形式。ATP被用于在不同的化学反应之间进行[[化学能]]的传递。虽然细胞中只有少量的ATP存在,但它被不断地合成,人体一天所消耗的ATP的量积累起来可以达到自身的体重。<ref name=Dimroth/>ATP是连接[[合成代谢]]和[[分解代谢]]的桥梁:分解代谢反应生成ATP,而合成代谢反应消耗ATP。它也可以作为磷酸基团的携带者参与[[磷酸化]]反应。 |
|||
[[维生素]]是一类生命所需的微量有机化合物,但细胞自身无法合成。在人类[[营养学]]中,大多数的维生素可以在被修饰后发挥辅酶的功能;例如,细胞所利用的所有的水溶性维生素都是被磷酸化或偶联到核苷酸上的。<ref>{{en}}{{Citation | last1 = Coulston | first1 = Ann | last2 = Kerner | first2 = John | last3 = Hattner | first3 = JoAnn | last4 = Srivastava | first4 = Ashini | contribution = Nutrition Principles and Clinical Nutrition | title = Stanford School of Medicine Nutrition Courses | publisher = SUMMIT | year = 2006 }}</ref>[[烟酰胺腺嘌呤二核苷酸]](NAD,还原形式为NADH)是维生素B<sub>3</sub>(俗称[[烟酸]])的一种衍生物,它也是一种重要的辅酶,可以作为氢受体。数百种不同类型的[[脱氢酶]]可以从它们的底物上移去电子,同时将NAD<sup>+</sup>还原为NADH。而后,这种还原形式便可以作为任何一个[[还原酶]]的辅酶,用于为酶底物的还原提供电子。<ref>{{en}}{{cite journal en|author=Pollak N, Dölle C, Ziegler M |title=The power to reduce: pyridine nucleotides—small molecules with a multitude of functions |journal=Biochem J |volume=402 |issue=2 |pages=205-18 |year=2007 |pmid=17295611}}</ref>烟酰胺腺嘌呤二核苷酸在细胞中存在两种不同的形式:NADH和NADPH。NAD<sup>+</sup>/NADH多在分解代谢反应中发挥重要作用,而NADP<sup>+</sup>/NADPH则多用于合成代谢反应中。 |
|||
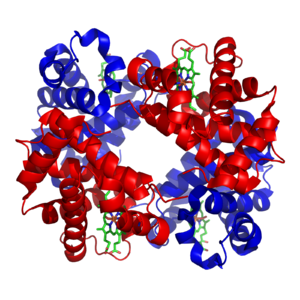
[[Image:1GZX Haemoglobin.png|thumb|300px|left|[[血红蛋白]]的结构。[[蛋白质亚基]]显示为红色和蓝色,结合铁的[[血红素]]显示为绿色。来自{{PDB|1GZX}}。]] |
|||
===矿物质和辅因子=== |
|||
{{see also|生理学|生物无机化学|辅因子|铁质}} |
|||
无机元素在代谢中也发挥着重要的作用;其中一些在机体内含量丰富(如[[钠]]和[[钾]]),而另一些则为微量元素。大约99%的哺乳动物的质量为[[碳]]、[[氮]]、[[钙]]、[[钠]]、[[氯]]、[[钾]]、[[氢]]、[[磷]]、[[氧]]和[[硫]]元素。<ref name=Heymsfield>{{en}}{{cite journal en|author=Heymsfield S, Waki M, Kehayias J, Lichtman S, Dilmanian F, Kamen Y, Wang J, Pierson R |title=Chemical and elemental analysis of humans in vivo using improved body composition models |journal=Am J Physiol |volume=261 |issue=2 Pt 1 |pages=E190-8 |year=1991 |pmid=1872381}}</ref>绝大多数的碳和氮存在于有机物(如蛋白质、脂类和糖类)中,而氢和氧则主要存在于水中。<ref name=Heymsfield/> |
|||
含量丰富的无机元素都是作为电解质的离子。体内最重要的离子有[[钠]]、[[钾]]、[[钙]]、[[镁]]等金属离子和[[氯]]离子、[[磷酸根]]离子以及有机的[[碳酸氢根]]离子。在[[细胞膜]]的内外维持准确的[[离子梯度]],可以保持[[渗透压]]和[[pH]]值的稳定。<ref>{{en}}{{cite journal en|author=Sychrová H |title=Yeast as a model organism to study transport and homeostasis of alkali metal cations |url=http://www.biomed.cas.cz/physiolres/pdf/53%20Suppl%201/53_S91.pdf |journal=Physiol Res |volume=53 Suppl 1 |issue= |pages=S91-8 |year=2004 |pmid=15119939}}</ref>离子对于[[神经]]和[[肌肉]]组织也同样不可缺少,这是因为这些组织中的[[动作电位]](可以引起神经信号和[[肌肉收缩]])是由[[细胞外液]]和细胞[[原生质]]之间的电解质交换来产生的。<ref>{{en}}{{cite journal en|author=Levitan I |title=Modulation of ion channels in neurons and other cells |journal=Annu Rev Neurosci |volume=11 |issue= |pages=119-36 |year=1988 |pmid=2452594}}</ref>电解质进入和离开细胞是通过细胞膜上的[[离子通道]]蛋白来完成的。例如,肌肉收缩依赖于位于细胞膜和[[横行小管]]([[:en:T-tubule|T-tubule]])上的离子通道对于钙离子、钾离子和钠离子的流动的控制。<ref>{{en}}{{cite journal en|author=Dulhunty A |title=Excitation-contraction coupling from the 1950s into the new millennium |journal=Clin Exp Pharmacol Physiol |volume=33 |issue=9 |pages=763-72 |year=2006 |pmid=16922804}}</ref> |
|||
[[过渡金属]]在生物体体内通常是作为[[微量元素]]存在的,其中[[锌]]和[[铁]]的含量最为丰富。<ref>{{en}}{{cite journal en|author=Mahan D, Shields R |title=Macro- and micromineral composition of pigs from birth to 145 kilograms of body weight |url=http://jas.fass.org/cgi/reprint/76/2/506 |journal=J Anim Sci |volume=76 |issue=2 |pages=506-12 |year=1998 |pmid=9498359}}</ref><ref name=Husted>{{en}}{{cite journal en|author=Husted S, Mikkelsen B, Jensen J, Nielsen N |title=Elemental fingerprint analysis of barley (Hordeum vulgare) using inductively coupled plasma mass spectrometry, isotope-ratio mass spectrometry, and multivariate statistics |journal=Anal Bioanal Chem |volume=378 |issue=1 |pages=171-82 |year=2004 |pmid=14551660}}</ref>这些金属元素被一些蛋白质用作[[辅因子]]或者对于酶活性的发挥具有关键作用,例如携氧的[[血红蛋白]]和[[过氧化氢酶]]。<ref>{{en}}{{cite journal en|author=Finney L, O'Halloran T |title=Transition metal speciation in the cell: insights from the chemistry of metal ion receptors |journal=Science |volume=300 |issue=5621 |pages=931-6 |year=2003 |pmid=12738850}}</ref>这些辅因子可以与特定蛋白质紧密结合;虽然酶的辅因子会在催化过程中被修饰,这些辅因子总是能够在催化完成后回到起始状态。<ref>{{en}}{{cite journal en|author=Cousins R, Liuzzi J, Lichten L |title=Mammalian zinc transport, trafficking, and signals |url=http://www.jbc.org/cgi/content/full/281/34/24085 |journal=J Biol Chem |volume=281 |issue=34 |pages=24085-9 |year=2006 |pmid=16793761}}</ref><ref>{{en}}{{cite journal en|author=Dunn L, Rahmanto Y, Richardson D |title=Iron uptake and metabolism in the new millennium |journal=Trends Cell Biol |volume=17 |issue=2 |pages=93–100 |year=2007 |pmid=17194590}}</ref> |
|||
==分解代谢== |
|||
{{main|分解代谢}} |
|||
'''分解代谢'''(又称为'''同化作用''')是一系列裂解大分子的反应过程的总称,包括裂解和氧化食物分子。分解代谢反应的目的是为合成代谢反应提供所需的能量和反应物。分解代谢的机制在生物体中不尽相同,如[[有机营养菌]]分解[[有机物|有机分子]]来获得能量,而[[无机营养菌]]利用[[无机物]]作为能量来源,[[光能利用菌]]则能够吸收[[阳光]]并转化为可利用的[[化学能]]。然而,所有这些代谢形式都需要[[氧化还原]]反应的参与,反应主要是将[[电子]]从还原性的供体分子(如有机分子、[[水]]、[[氨]]、[[硫化氢]]、[[亚铁离子]]等)转移到受体分子(如[[氧气]]、[[硝酸盐]]、[[硫酸盐]]等)。<ref>{{en}}{{cite journal en|author=Nealson K, Conrad P |title=Life: past, present and future |url=http://www.pubmedcentral.nih.gov/articlerender.fcgi?tool=pubmed&pubmedid=10670014 |journal=Philos Trans R Soc Lond B Biol Sci |volume=354 |issue=1392 |pages=1923–39 |year=1999 |pmid=10670014}}</ref>在动物中,这些反应还包括将复杂的有机分子分解为简单分子(如[[二氧化碳]]和水)。在[[光合作用|光合]]生物(如植物和[[藍藻]])中,这些电子转移反应并不释放能量,而是用作储存所吸收光能的一种方式。<ref name=Nelson>{{en}}{{cite journal en|author=Nelson N, Ben-Shem A |title=The complex architecture of oxygenic photosynthesis |journal=Nat Rev Mol Cell Biol |volume=5 |issue=12 |pages=971-82 |year=2004 |pmid=15573135}}</ref> |
|||
动物中最普遍的分解代谢反应可以被分为三个主要步骤:首先,大分子有机化合物,如蛋白质、多糖或脂类被消化分解为小分子组分;然后,这些小分子被细胞摄入并被转化为更小的分子,通常为[[乙酰辅酶A]],此过程中会释放出部分能量;最后,辅酶A上的[[乙酰]]基团通过[[柠檬酸循环]]和[[电子传递链]]被氧化为水和二氧化碳,并释放出能量,这些能量可以通过将[[烟酰胺腺嘌呤二核苷酸]](NAD<sup>+</sup>)还原为NADH而以化学能的形式被储存起来。 |
|||
===消化=== |
|||
{{main|消化|消化系统}} |
|||
淀粉、蛋白质和纤维素等大分子多聚体不能很快被细胞所吸收,需要先被分解为小分子[[单体]]然后才能被用于细胞代谢。有多种消化性酶能够降解这些多聚体,如[[蛋白酶]]可以将但蛋白质降解为多肽片断或氨基酸,[[糖苷水解酶]]可以将多糖分解为单糖。 |
|||
微生物只是简单地分泌消化性酶到周围环境中,<ref>{{en}}{{cite journal en|author=Häse C, Finkelstein R |title=Bacterial extracellular zinc-containing metalloproteases |url=http://www.pubmedcentral.nih.gov/articlerender.fcgi?tool=pubmed&pubmedid=8302217 |journal=Microbiol Rev |volume=57 |issue=4 |pages=823-37 |year=1993 |pmid=8302217}}</ref><ref>{{en}}{{cite journal en|author=Gupta R, Gupta N, Rathi P |title=Bacterial lipases: an overview of production, purification and biochemical properties |journal=Appl Microbiol Biotechnol |volume=64 |issue=6 |pages=763-81 |year=2004 |pmid=14966663}}</ref>而动物则只能由其[[消化系统]]中的特定细胞来分泌这些酶。<ref>{{en}}{{cite journal en|author=Hoyle T |title=The digestive system: linking theory and practice |journal=Br J Nurs |volume=6 |issue=22 |pages=1285–91 |year=1997 |pmid=9470654}}</ref>由这些位于细胞外的酶分解获得的氨基酸或单糖接着通过[[主动运输]]蛋白被运送到细胞内。<ref>{{en}}{{cite journal en|author=Souba W, Pacitti A |title=How amino acids get into cells: mechanisms, models, menus, and mediators |journal=JPEN J Parenter Enteral Nutr |volume=16 |issue=6 |pages=569-78 |year=1992 |pmid=1494216}}</ref><ref>{{en}}{{cite journal en|author=Barrett M, Walmsley A, Gould G |title=Structure and function of facilitative sugar transporters |journal=Curr Opin Cell Biol |volume=11 |issue=4 |pages=496–502 |year=1999 |pmid=10449337}}</ref> |
|||
[[Image:Catabolism schematic zh.svg|thumb|left|300px|[[蛋白质]]、[[糖类]]、[[脂肪]]的代谢简化图。]] |
|||
===来自有机物的能量=== |
|||
{{see also|呼吸作用|发酵|糖代谢|脂代谢|蛋白质代谢}} |
|||
糖类的分解代谢即是将糖链分解为更小的单位。通常一旦糖链被分解为单糖后就可以被细胞所吸收。<ref>{{en}}{{cite journal en|author=Bell G, Burant C, Takeda J, Gould G |title=Structure and function of mammalian facilitative sugar transporters |journal=J Biol Chem |volume=268 |issue=26 |pages=19161-4 |year=1993 |pmid=8366068}}</ref>进入细胞内的糖,如葡萄糖和果糖,就会通过[[糖酵解]]途径被转化为[[丙酮酸|丙酮酸盐]]并产生部分的ATP。<ref name=Bouche>{{en}}{{cite journal en|author=Bouché C, Serdy S, Kahn C, Goldfine A |title=The cellular fate of glucose and its relevance in type 2 diabetes |url=http://edrv.endojournals.org/cgi/content/full/25/5/807 |journal=Endocr Rev |volume=25 |issue=5 |pages=807-30 |year=2004 |pmid=15466941}}</ref>丙酮酸盐是多个代谢途径的中间物,但其大部分会被转化为乙酰辅酶A并进入柠檬酸循环。虽然柠檬酸循环能够产生ATP,但其最重要的产物是NADH——由乙酰辅酶A被氧化来提供电子并由NAD生成,同时释放出无用的二氧化碳。在无氧条件下,糖酵解过程会生成[[乳酸|乳酸盐]],即由[[乳酸脱氢酶]]将丙酮酸盐转化为乳酸盐,同时将NADH又氧化为NAD<sup>+</sup>,使得NAD可以被循环利用于糖酵解中。另一中降解葡萄糖的途径是[[磷酸戊糖途径]],该途径可以将辅酶[[烟酰胺腺嘌呤二核苷酸磷酸]](NADP<sup>+</sup>)还原为NADPH,并生成[[戊糖]],如[[核糖]](合成核苷酸的重要组分)。 |
|||
[[脂肪]]是通过[[水解]]作用分解为[[脂肪酸]]和[[甘油]]。甘油可以进入糖酵解途径,通过[[β-氧化]]被分解并释放出乙酰辅酶A,而乙酰辅酶A如上所述进入柠檬酸循环。脂肪酸同样通过氧化被分解;在氧化过程中脂肪酸可以释放出比糖类更多的能量,这是因为糖类结构的含氧比例较高。 |
|||
[[氨基酸]]既可以被用于合成蛋白质或其他生物分子,又可以被氧化为尿素和二氧化碳以提供能量。<ref>{{en}}{{cite journal en|author=Sakami W, Harrington H |title=Amino acid metabolism |journal=Annu Rev Biochem |volume=32 |issue= |pages=355-98 |year=1963 |pmid=14144484}}</ref>氧化的第一步是由[[转氨酶]]将氨基酸上的[[氨基]]除去,氨基随后被送入[[尿素循环]],而留下的脱去氨基的碳骨架以[[酮酸]]的形式存在。有多种酮酸(如[[α-酮戊二酸]],由脱去氨基的[[谷氨酸]]所形成)是柠檬酸循环的中间物。<ref>{{en}}{{cite journal en|author=Brosnan J |title=Glutamate, at the interface between amino acid and carbohydrate metabolism |url=http://jn.nutrition.org/cgi/content/full/130/4/988S |journal=J Nutr |volume=130 |issue=4S Suppl |pages=988S-90S |year=2000 |pmid=10736367}}</ref>此外,[[生糖氨基酸]]([[:en:glucogenic amino acid|glucogenic amino acid]])能够通过[[糖异生]]作用被转化为葡萄糖(具体内容见下文)。<ref>{{en}}{{cite journal en|author=Young V, Ajami A |title=Glutamine: the emperor or his clothes? |url=http://jn.nutrition.org/cgi/content/full/131/9/2449S |journal=J Nutr |volume=131 |issue=9 Suppl |pages=2449S-59S; discussion 2486S-7S |year=2001 |pmid=11533293}}</ref> |
|||
==能量转换== |
|||
===氧化磷酸化=== |
|||
[[Image:ATPsynthase labelled.png|right|thumb|280px|[[ATP合成酶]]的结构。其质子通道和转动轴显示为蓝色,合成酶亚基显示为红色,固定亚基显示为黄色。]] |
|||
{{main|氧化磷酸化}}{{see also|化学渗透|线粒体}} |
|||
氧化磷酸化中,通过如柠檬酸循环等代谢途径,电子从被消化吸收的食物分子上转移到氧气上,并将产生的能量以ATP的方式储存起来。在[[真核生物]]中,这一过程是由位于[[线粒体]]膜上的一系列[[膜蛋白]]来完成的,被称为[[电子传递链]]。而在[[原核生物]]中,对应的蛋白质则位于细胞内膜上。<ref>{{en}}{{cite journal en|author=Hosler J, Ferguson-Miller S, Mills D |title=Energy transduction: proton transfer through the respiratory complexes |journal=Annu Rev Biochem |volume=75 |issue= |pages=165-87 |year=2006 |pmid=16756489}}</ref>这些蛋白质利用从电子还原性分子(如[[NAD|NADH]])传递到氧气的反应所产生的能量将[[质子]]进行跨膜运输。<ref>{{en}}{{cite journal en|author=Schultz B, Chan S |title=Structures and proton-pumping strategies of mitochondrial respiratory enzymes |journal=Annu Rev Biophys Biomol Struct |volume=30 |issue= |pages=23–65 |year=2001 |pmid=11340051}}</ref>将质子泵出线粒体的结果就会在线粒体膜的两边产生质子的浓度差,从而在膜的两边形成一个[[电化学梯度]]。<ref>{{en}}{{cite journal en|author=Capaldi R, Aggeler R |title=Mechanism of the F(1)F(0)-type ATP synthase, a biological rotary motor |journal=Trends Biochem Sci |volume=27 |issue=3 |pages=154-60 |year=2002 |pmid=11893513}}</ref>通过电化学梯度所产生的驱动力使得质子通过线粒体膜上的[[ATP合成酶]]重新进入线粒体。这样的一个质子流会促使ATP合成酶的stalk[[蛋白质亚基|亚基]]发生转动,并进一步带动合成酶[[结构域]]上的[[活性位点]]发生形变并将[[腺苷二磷酸]](ADP)磷酸化,最终产生ATP。<ref name=Dimroth/> |
|||
===来自无机物的能量=== |
|||
{{see also|微生物代谢|氮循环}} |
|||
[[化能自养菌|化能无机营养]]是一种发现于一些原核生物中的代谢类型,这些原核生物通过氧化[[无机物]]来获得能量。它们能够利用[[氢气]],<ref>{{en}}{{cite journal en|author=Friedrich B, Schwartz E |title=Molecular biology of hydrogen utilization in aerobic chemolithotrophs |journal=Annu Rev Microbiol |volume=47 |issue= |pages=351-83 |year=1993 |pmid=8257102}}</ref>还原性的含硫化合物(如[[硫化物]]、[[硫化氢]]和[[硫代硫酸盐]])<ref>{{en}}{{cite journal en|author=Friedrich C |title=Physiology and genetics of sulfur-oxidizing bacteria |journal=Adv Microb Physiol |volume=39 |issue= |pages=235-89 |year=1998 |pmid=9328649}}</ref>,[[氧化亚铁|二价铁化合物]]<ref>{{en}}{{cite journal en|author=Weber K, Achenbach L, Coates J |title=Microorganisms pumping iron: anaerobic microbial iron oxidation and reduction |journal=Nat Rev Microbiol |volume=4 |issue=10 |pages=752-64 |year=2006 |pmid=16980937}}</ref>或[[氨]]<ref>{{en}}{{cite journal en|author=Jetten M, Strous M, van de Pas-Schoonen K, Schalk J, van Dongen U, van de Graaf A, Logemann S, Muyzer G, van Loosdrecht M, Kuenen J |title=The anaerobic oxidation of ammonium |journal=FEMS Microbiol Rev |volume=22 |issue=5 |pages=421-37 |year=1998 |pmid=9990725}}</ref>作为还原能的来源;这些还原性物质氧化过程的电子受体常常为氧气或[[亚硝酸盐]]。<ref>{{en}}{{cite journal en|author=Simon J |title=Enzymology and bioenergetics of respiratory nitrite ammonification |journal=FEMS Microbiol Rev |volume=26 |issue=3 |pages=285–309 |year=2002 |pmid=12165429}}</ref>这些进程对于整体的[[生物地質化學循環]],如[[乙酸生成作用]](acetogenesis)以及[[硝化]]和[[反硝化作用]]都很重要,并且对土壤的肥沃十分关键。<ref>{{en}}{{cite journal en|author=Conrad R |title=Soil microorganisms as controllers of atmospheric trace gases (H2, CO, CH4, OCS, N2O, and NO) |url=http://www.pubmedcentral.nih.gov/articlerender.fcgi?tool=pubmed&pubmedid=8987358 |journal=Microbiol Rev |volume=60 |issue=4 |pages=609-40 |year=1996 |pmid=8987358}}</ref><ref>{{en}}{{cite journal en|author=Barea J, Pozo M, Azcón R, Azcón-Aguilar C |title=Microbial co-operation in the rhizosphere |url=http://jxb.oxfordjournals.org/cgi/content/full/56/417/1761 |journal=J Exp Bot |volume=56 |issue=417 |pages=1761–78 |year=2005 |pmid=15911555}}</ref> |
|||
===来自光的能量=== |
|||
{{see also|光合细菌|電子傳遞鏈|叶绿体}} |
|||
太阳光中的能量可以被[[植物]]、[[蓝藻]]、[[紫细菌]]、[[綠菌門|绿菌]]和一些[[原生生物]]所捕获。这一获取光能的进程常常与二氧化碳转化为有机物(即“[[碳固定]]”)相偶联,成为[[光合作用]]的一部分。光能获取和碳固定系统在原核生物中却能够分开运行的,因为紫细菌和绿菌无论在碳固定或是在有机物酵解之时,都可以利用阳光作为能量来源。<ref>{{en}}{{cite journal en|author=van der Meer M, Schouten S, Bateson M, Nübel U, Wieland A, Kühl M, de Leeuw J, Sinninghe Damsté J, Ward D |title=Diel variations in carbon metabolism by green nonsulfur-like bacteria in alkaline siliceous hot spring microbial mats from Yellowstone National Park |url=http://www.pubmedcentral.nih.gov/articlerender.fcgi?tool=pubmed&pubmedid=16000812 |journal=Appl Environ Microbiol |volume=71 |issue=7 |pages=3978–86 |year=2005 |pmid=16000812}}</ref><ref>{{en}}{{cite journal en|author=Tichi M, Tabita F |title=Interactive control of Rhodobacter capsulatus redox-balancing systems during phototrophic metabolism |url=http://www.pubmedcentral.nih.gov/articlerender.fcgi?tool=pubmed&pubmedid=11591679 |journal=J Bacteriol |volume=183 |issue=21 |pages=6344–54 |year=2001 |pmid=11591679}}</ref> |
|||
捕获太阳能的过程与氧化磷酸化在本质上是相似的,因为两者都包括了能量以质子浓度梯度形式存在以及这种浓度差所驱动的ATP的合成。<ref name=Dimroth/>用于驱动电子传递链的电子是来自于被称为[[光合反应中心]]的捕光蛋白。根据所含的[[光合色素]]类型的不同,可以将反应中心体分为两类:[[叶绿素|去镁叶绿素]]-[[醌]]型和铁-硫型;大多数的光合细菌只含有一类反应中心体,而植物和蓝藻则含有两类。<ref>{{cite journal |author=Allen J, Williams J |title=Photosynthetic reaction centers |journal=FEBS Lett |volume=438 |issue=1–2 |pages=5–9 |year=1998 |pmid=9821949}}</ref> |
|||
此外,[[光系统]]是在光合作用中发挥主要作用的[[蛋白质复合物]],包括光系统I和II。在植物中,光系统II可以利用光能从水中获得电子,并释放出氧气。电子随后流入[[细胞色素b6f复合物]],该复合物用能量将质子泵出[[类囊体]](位于[[叶绿体]]中)膜。<ref>{{en}}{{cite journal en|author=Nelson N, Ben-Shem A |title=The complex architecture of oxygenic photosynthesis |journal=Nat Rev Mol Cell Biol |volume=5 |issue=12 |pages=971-82 |year=2004 |pmid=15573135}}</ref>被泵出的质子又通过膜回到类囊体内,从而驱动ATP的合成(类似于氧化磷酸化中的ATP的合成)。当电子继续流过光系统I时,它们可以被用于还原辅酶NADP<sup>+</sup>、用于[[卡尔文循环]]或回收后用于合成更多的ATP。<ref>{{en}}{{cite journal en|author=Munekage Y, Hashimoto M, Miyake C, Tomizawa K, Endo T, Tasaka M, Shikanai T |title=Cyclic electron flow around photosystem I is essential for photosynthesis |journal=Nature |volume=429 |issue=6991 |pages=579-82 |year=2004 |pmid=15175756}}</ref> |
|||
==合成代谢== |
|||
{{main|合成代谢}} |
|||
'''合成代谢'''(又称为'''异化作用''')是一系列合成型代谢进程(即利用分解代谢所释放的能量来合成复杂分子)的总称。一般而言,用于组成细胞结构的复杂分子都是从小且简单的前体一步一步地构建而来。合成代谢包括三个基本阶段:首先生成前体分子,如[[氨基酸]]、[[单糖]]、[[类萜|类异戊二烯]]和[[核苷酸]];其次,利用ATP水解所提供的能量,这些分子被激活而形成活性形式;最后,它们被组装成复杂的分子,如[[蛋白质]]、[[多糖]]、[[脂类]]和[[核酸]]。 |
|||
不同的生物体所需要合成的各类复杂分子也互不相同。[[自养生物]],如植物,可以在细胞中利用简单的小分子,如二氧化碳和水,来合成复杂的有机分子如多糖和蛋白质。[[异养生物]]则需要更复杂的物质来源,如单糖和氨基酸,来生产对应的复杂分子。生物体还可以根据它们所获得的能量来源的不同而被细分为:获取光能的光能自养生物和光能异养生物,以及从无机物氧化过程或的能量的化能自养生物和化能异养生物。 |
|||
===碳固定=== |
|||
{{main|碳固定}} |
|||
{{see also|光合作用|化能合成作用}} |
|||
[[Image:Chloroplasten.jpg|frame|植物细胞(其周围环绕的为紫色的细胞壁)中充满了光合作用的“工厂”──[[叶绿体]](绿色)。]] |
|||
光合作用是利用阳光、二氧化碳(CO<sub>2</sub>)和水来合成糖类并释放出氧气的过程。这一过程利用[[光合反应中心]]所产生的ATP和NADPH将CO<sub>2</sub>转化为[[3-磷酸甘油酸]],并继续将3-磷酸甘油酸转化为生物体所需的葡萄糖,因此该过程被称为[[碳固定]]。碳固定反应作为[[卡尔文循环|卡尔文-本森循环]]的一部分,由[[1,5-二磷酸核酮糖羧化酶/加氧酶|RuBisCO]]酶来进行催化。<ref>{{en}}{{cite journal en|author=Miziorko H, Lorimer G |title=Ribulose-1,5-bisphosphate carboxylase-oxygenase |journal=Annu Rev Biochem |volume=52 |issue= |pages=507-35 |year=1983 |pmid=6351728}}</ref>发生在植物中的光合作用分为三种:[[:en:C3 carbon fixation|C3碳固定]]、[[:en:C4 carbon fixation|C4碳固定]]和[[景天酸代謝|CAM光合作用]]。这些光合作用种类之间的差异在于当二氧化碳进入卡尔文循环的途径不同:C3型植物可以直接对CO<sub>2</sub>进行固定;而C4和CAM型则先将CO<sub>2</sub>合并到其他化合物上,这是对强光照和干旱环境的一种适应。<ref>{{en}}{{cite journal en|author=Dodd A, Borland A, Haslam R, Griffiths H, Maxwell K |title=Crassulacean acid metabolism: plastic, fantastic |url=http://jxb.oxfordjournals.org/cgi/content/full/53/369/569 |journal=J Exp Bot |volume=53 |issue=369 |pages=569-80 |year=2002 |pmid=11886877}}</ref> |
|||
在光合型原核生物中,碳固定的机制只见差异性更大。例如,二氧化碳可以经由卡尔文-本森循环(一种[[:en:Reverse Krebs cycle|反式柠檬酸循环]])<ref>{{en}}{{cite journal en|author=Hügler M, Wirsen C, Fuchs G, Taylor C, Sievert S |title=Evidence for autotrophic CO2 fixation via the reductive tricarboxylic acid cycle by members of the epsilon subdivision of proteobacteria |url=http://www.pubmedcentral.nih.gov/articlerender.fcgi?tool=pubmed&pubmedid=15838028 |journal=J Bacteriol |volume=187 |issue=9 |pages=3020–7 |year=2005 |pmid=15838028}}</ref>或者乙酰辅酶A的[[羧化作用]]<ref>{{en}}{{cite journal en|author=Strauss G, Fuchs G |title=Enzymes of a novel autotrophic CO2 fixation pathway in the phototrophic bacterium Chloroflexus aurantiacus, the 3-hydroxypropionate cycle |journal=Eur J Biochem |volume=215 |issue=3 |pages=633-43 |year=1993 |pmid=8354269}}</ref><ref>{{en}}{{cite journal en|author=Wood H |title=Life with CO or CO2 and H2 as a source of carbon and energy |url=http://www.fasebj.org/cgi/reprint/5/2/156 |journal=FASEB J |volume=5 |issue=2 |pages=156-63 |year=1991 |pmid=1900793}}</ref>而被固定。此外,原核的[[化能自养生物|化能自养菌]]也可以通过卡尔文-本森循环来固定CO<sub>2</sub>,但却使用来自无机化合物的能量来驱动反应。<ref>{{en}}{{cite journal en|author=Shively J, van Keulen G, Meijer W |title=Something from almost nothing: carbon dioxide fixation in chemoautotrophs |journal=Annu Rev Microbiol |volume=52 |issue= |pages=191–230 |year=1998 |pmid=9891798}}</ref> |
|||
===糖类和聚糖=== |
|||
{{see also|糖异生|乙醛酸循环|糖原生成|糖基化}} |
|||
糖类的合成代谢中,简单的有机酸可以被转化为[[单糖]](如葡萄糖),然后单糖再聚合在一起形成[[多糖]](如[[淀粉]])。从包括[[丙酮酸|丙酮酸盐]]、[[乳酸|乳酸盐]]、[[甘油]]、[[3-磷酸甘油酸]]和[[氨基酸]]在内的化合物来生成葡萄糖的过程被称为[[糖异生]]。糖异生将丙酮酸盐通过一系列的中间物转化为[[葡萄糖-6-磷酸]],其中的许多中间物可以与[[糖酵解]]过程共享。<ref name=Bouche/>然而,糖异生过程不是简单的糖酵解过程的逆反应,其中多个步骤是由不在糖酵解中发挥作用的酶来催化的。这样就使得葡萄糖的合成和分解可以被分别调控,以防止这两个途径进入[[无效循环]]([[:en:futile cycle|futile cycle]])。<ref>{{en}}{{cite journal en|author=Boiteux A, Hess B |title=Design of glycolysis |journal=Philos Trans R Soc Lond B Biol Sci |volume=293 |issue=1063 |pages=5–22 |year=1981 |pmid=6115423}}</ref><ref>{{en}}{{cite journal en|author=Pilkis S, el-Maghrabi M, Claus T |title=Fructose-2,6-bisphosphate in control of hepatic gluconeogenesis. From metabolites to molecular genetics |journal=Diabetes Care |volume=13 |issue=6 |pages=582-99 |year=1990 |pmid=2162755}}</ref> |
|||
虽然脂肪是通用的储存能量的方式,但在[[脊椎动物]],如[[人类]]中,储存的脂肪酸不能通过糖异生作用而被转化为葡萄糖,因为这些生物体无法将乙酰辅酶A转变为丙酮酸盐(植物具有必要的酶,而动物则没有)。<ref name=Ensign>{{en}}{{cite journal en|author=Ensign S |title=Revisiting the glyoxylate cycle: alternate pathways for microbial acetate assimilation |journal=Mol Microbiol |volume=61 |issue=2 |pages=274-6 |year=2006 |pmid=16856935}}</ref> 因此,在长期饥饿后,脊椎动物需要从脂肪酸来制造[[酮体]]来代替组织中的葡萄糖,因为像脑这样的组织不能够代谢脂肪酸。<ref>{{en}}{{cite journal en|author=Finn P, Dice J |title=Proteolytic and lipolytic responses to starvation |journal=Nutrition |volume=22 |issue=7–8 |pages=830-44 |year=2006 |pmid=16815497}}</ref>在其它生物体,如植物和细菌中,由于存在[[乙醛酸循环]],可以跳过柠檬酸循环中的[[脱羧反应]],使得乙酰辅酶A可以被转化为[[草酰乙酸盐]],而草酰乙酸盐可以被用于葡萄糖的生产,因此解决了脊椎动物中存在的这一代谢问题。<ref name=Kornberg>{{en}}{{cite journal en|author=Kornberg H, Krebs H |title=Synthesis of cell constituents from C2-units by a modified tricarboxylic acid cycle |journal=Nature |volume=179 |issue=4568 |pages=988-91 |year=1957 |pmid=13430766}}</ref><ref name=Ensign/> |
|||
多糖和[[聚糖]]是通过逐步加入单糖来合成的,加入单糖的过程是由[[糖基转移酶]]将糖基从一个活化的糖-磷酸供体(如[[尿苷二磷酸葡萄糖]])上转移到作为受体的[[羟基]](位于延长中的多糖链)上。由于糖环上的任一羟基都可以作为受体,因此多糖链可以是直链结构,也可以含有多个支链。<ref>{{en}}{{cite journal en|author=Rademacher T, Parekh R, Dwek R |title=Glycobiology |journal=Annu Rev Biochem |volume=57 |issue= |pages=785–838 |year=1988 |pmid=3052290}}</ref>这些生成的多糖自身可以具有结构或代谢功能,或者可以在寡糖链转移酶的作用下被转接到脂类和蛋白质上。<ref>{{en}}{{cite journal en|author=Opdenakker G, Rudd P, Ponting C, Dwek R |title=Concepts and principles of glycobiology |url=http://www.fasebj.org/cgi/reprint/7/14/1330 |journal=FASEB J |volume=7 |issue=14 |pages=1330–7 |year=1993 |pmid=8224606}}</ref><ref>{{en}}{{cite journal en|author=McConville M, Menon A |title=Recent developments in the cell biology and biochemistry of glycosylphosphatidylinositol lipids (review) |journal=Mol Membr Biol |volume=17 |issue=1 |pages=1–16 |year=2000 |pmid=10824734}}</ref> |
|||
===脂肪酸、萜类化合物和类固醇=== |
|||
{{see also|脂肪酸合成|类固醇代谢}} |
|||
[[Image:Sterol synthesis.svg|thumb|right|350px|[[类固醇代谢]]途径的简化图。其中包括了中间物[[异戊烯焦磷酸]](isopentenyl pyrophosphate,IPP)、[[二甲基丙烯焦磷酸酯]](dimethylallyl pyrophosphate,DMAPP)、[[焦磷酸香叶酯]](geranyl pyrophosphate,GPP)和[[鲨烯]](squalene)。有一些中间物被省略。产物为[[羊毛甾醇]](lanosterol)。]] |
|||
[[脂肪酸合成]]是一个将乙酰辅酶A多聚化并还原的过程。脂肪酸上的乙酰基链是通过一个反应循环来延伸的,包括加入[[乙酰]]基、将其还原为[[乙醇]]和继续还原为[[烷烃]]的过程。在脂肪酸的生物合成中发挥作用的酶可以被分为两类:动物和真菌中,所有的脂肪酸合成反应由一个单一的多功能酶,I型脂肪酸合成酶来完成;<ref>{{en}}{{cite journal en|author=Chirala S, Wakil S |title=Structure and function of animal fatty acid synthase |journal=Lipids |volume=39 |issue=11 |pages=1045–53 |year=2004 |pmid=15726818}}</ref>而在植物[[色素體|质体]]和细菌中,有多个不同的酶分别催化每一个反应,这些酶统称为I型脂肪酸合成酶。<ref>{{en}}{{cite journal en|author=White S, Zheng J, Zhang Y |title=The structural biology of type II fatty acid biosynthesis |journal=Annu Rev Biochem |volume=74 |issue= |pages=791–831 |year=2005 |pmid=15952903}}</ref><ref>{{en}}{{cite journal en|author=Ohlrogge J, Jaworski J |title=Regulation of fatty acid synthesis |journal=Annu Rev Plant Physiol Plant Mol Biol |volume=48 |issue= |pages=109–136 |year=1997 |pmid=15012259}}</ref> |
|||
[[萜烯]]和[[萜类化合物|异戊二烯类]]化合物(包括[[类胡萝卜素]]在内)是脂类中的一个大家族,它们组成了植物[[天然化合物]]中的最大的一类。<ref>{{en}}{{cite journal en|author=Dubey V, Bhalla R, Luthra R |title=An overview of the non-mevalonate pathway for terpenoid biosynthesis in plants |url=http://www.ias.ac.in/jbiosci/sep2003/637.pdf |journal=J Biosci |volume=28 |issue=5 |pages=637-46 |year=2003 |pmid=14517367}}</ref>这些化合物是以[[异戊二烯]]为单位,聚合和修饰而成的;其中,异戊二烯是由具反应活性的前体,[[异戊烯焦磷酸]](isopentenyl pyrophosphate)和[[二甲烯丙基焦磷酸]](dimethylallyl pyrophosphate)提供的。<ref name=Kuzuyama>{{en}}{{cite journal en|author=Kuzuyama T, Seto H |title=Diversity of the biosynthesis of the isoprene units |journal=Nat Prod Rep |volume=20 |issue=2 |pages=171-83 |year=2003 |pmid=12735695}}</ref>这两个前体可以在不同的途径中被合成。动物和古菌利用[[甲瓦龙酸途径]](mevalonate pathway)来从乙酰辅酶A生产这两个化合物;<ref>{{en}}{{cite journal en|author=Grochowski L, Xu H, White R |title=Methanocaldococcus jannaschii uses a modified mevalonate pathway for biosynthesis of isopentenyl diphosphate |url=http://www.pubmedcentral.nih.gov/articlerender.fcgi?tool=pubmed&pubmedid=16621811 |journal=J Bacteriol |volume=188 |issue=9 |pages=3192–8 |year=2006 |pmid=16621811}}</ref>而植物和细菌则通过[[非甲瓦龙酸途径]]利用丙酮酸和[[甘油醛-3-磷酸]]作为底物来生产它们。<ref>{{en}}{{cite journal en|author=Lichtenthaler H |title=The 1-Ddeoxy-D-xylulose-5-phosphate pathway of isoprenoid biosynthesis in plants |journal=Annu Rev Plant Physiol Plant Mol Biol |volume=50 |issue= |pages=47–65 |year=1999 |pmid=15012203}}</ref><ref name=Kuzuyama/>另一个利用这些活化的异戊二烯供体的重要反应是[[类固醇生物合成|类固醇的生物合成]]。其中,异戊二烯单位连接在一起聚成[[角鲨烯]](squalene),然后折叠起来形成一系列的环而得到[[羊毛脂甾醇]](lanosterol)。<ref name=Schroepfer>{{en}}{{cite journal en|author=Schroepfer G |title=Sterol biosynthesis |journal=Annu Rev Biochem |volume=50 |issue= |pages=585–621 |year=1981 |pmid=7023367}}</ref>而羊毛脂甾醇能够被继续转化为其他类固醇,如[[胆固醇]]和[[麦角甾醇]](ergosterol)。<ref>{{en}}{{cite journal en|author=Lees N, Skaggs B, Kirsch D, Bard M |title=Cloning of the late genes in the ergosterol biosynthetic pathway of Saccharomyces cerevisiae—a review |journal=Lipids |volume=30 |issue=3 |pages=221-6 |year=1995 |pmid=7791529}}</ref><ref name=Schroepfer/> |
|||
===蛋白质=== |
|||
{{see also|蛋白质合成|氨基酸合成}} |
|||
生物体之间合成20种[[标准氨基酸列表|基本氨基酸]]的能力各不相同。大多数的细菌和植物可以合成所有这20种氨基酸,而哺乳动物只能合成10种非必需氨基酸。<ref name=Nelson/>因此对于包括人在内的哺乳动物,获取[[必需氨基酸]]的途径只能是摄入富含这些氨基酸的食物。所有氨基酸都可以从糖酵解、柠檬酸循环或磷酸戊糖循环中的中间产物生成。其中,合成过程所需的氮由[[谷氨酸]]和[[谷氨酰胺]]来提供。氨基酸合成需要先有适当的α-酮酸形成,然后通过[[转氨酶|转氨]]作用形成氨基酸。<ref>{{en}}{{cite book en| last = Guyton | first = Arthur C. | coauthors = John E. Hall | title = Textbook of Medical Physiology | publisher = Elsevier | date = 2006 | location = Philadelphia | pages = 855-6 | isbn = 0-7216-0240-1}}</ref> |
|||
氨基酸是通过[[肽键]]连接在一起并进一步形成蛋白质。每种不同的蛋白质都对应着自己独特的氨基酸序列(又被称为[[一级结构]])。如同20多个字母就能排列组合成数以万计的单词一般,不同的氨基酸连接在一起能够形成数量庞大的蛋白质种类。氨基酸通过连接到对应[[转运RNA]](tRNA)分子上形成[[氨酰tRNA]]而被激活,然后才可以被连接在一起。这种氨酰tRNA前体是通过一个ATP依赖的反应(将tRNA与正确的氨基酸相连接)来合成,该反应由[[氨酰tRNA合成酶]]进行催化。<ref>{{en}}{{cite journal en| author = Ibba M, Söll D | title = The renaissance of aminoacyl-tRNA synthesis | url=http://www.molcells.org/home/journal/include/downloadPdf.asp?articleuid={A158E3B4-2423-4806-9A30-4B93CDA76DA0} | journal = EMBO Rep | volume = 2 | issue = 5 | pages = 382-7 | year = 2001 | pmid = 11375928}}</ref>然后,以[[信使RNA]]中的序列信息为指导,带有正确氨基酸的氨酰tRNA分子就可以结合到[[核糖体]]的对应位置,在核糖体的作用下将氨基酸连接到正在延长的蛋白质链上。<ref>{{en}}{{cite journal en| author = Lengyel P, Söll D | title = Mechanism of protein biosynthesis | url=http://www.pubmedcentral.nih.gov/picrender.fcgi?artid=378322&blobtype=pdf | journal = Bacteriol Rev | volume = 33 | issue = 2 | pages = 264–301 | year = 1969 | pmid = 4896351}}</ref> |
|||
===核苷酸=== |
|||
{{see also|核苷酸补救|嘧啶合成|嘌呤代谢}} |
|||
[[核苷酸]]是由氨基酸、二氧化碳以及[[甲酸]]来合成的。<ref name=Rudolph>{{en}}{{cite journal en|author=Rudolph F |title=The biochemistry and physiology of nucleotides |journal=J Nutr |volume=124 |issue=1 Suppl |pages=124S-127S |year=1994 |pmid=8283301}} {{cite journal |author=Zrenner R, Stitt M, Sonnewald U, Boldt R |title=Pyrimidine and purine biosynthesis and degradation in plants |journal=Annu Rev Plant Biol |volume=57 |issue= |pages=805-36 |year=2006 |pmid=16669783}}</ref>由于其合成途径需要消耗大量的代谢能量,大多数的生物体内都有有效的系统来进行[[核苷酸补救]]。<ref name=Rudolph/><ref>{{en}}{{cite journal en|author=Stasolla C, Katahira R, Thorpe T, Ashihara H |title=Purine and pyrimidine nucleotide metabolism in higher plants |journal=J Plant Physiol |volume=160 |issue=11 |pages=1271–95 |year=2003 |pmid=14658380}}</ref>[[嘌呤]]是以[[核苷]](即[[碱基]]连接上[[核糖]])为基础合成的。[[腺嘌呤]]和[[鸟嘌呤]]是由前体核苷分子[[肌苷]]单磷酸(即[[次黄苷酸]])衍生而来,而次黄苷酸则是由来自[[甘氨酸]]、[[谷氨酰胺]]和[[谷氨酰胺]]的原子以及从辅酶[[四氢叶酸|四氢叶酸盐]]上转移来的[[甲酸]]基来合成的。[[嘧啶]]是由碱基[[乳清酸|乳清酸盐]]合成的,乳清酸盐则由谷氨酰胺和谷氨酰胺转化而来。<ref>{{en}}{{cite journal en|author=Smith J |title=Enzymes of nucleotide synthesis |journal=Curr Opin Struct Biol |volume=5 |issue=6 |pages=752-7 |year=1995 |pmid=8749362}}</ref> |
|||
==异型生物质代谢和氧化还原代谢== |
|||
{{see also|异型生物质代谢|药物代谢|抗氧化剂}} |
|||
所有的生物体如果持续摄入非食物类物质而没有相应的代谢途径,这些物质就会在细胞中积累并造成危害。这些存在于机体内可能造成损害的物质被称为[[异型生物质]]([[:en:xenobiotic|xenobiotic]])。<ref>{{en}}{{cite journal en|author=Testa B, Krämer S |title=The biochemistry of drug metabolism—an introduction: part 1. Principles and overview |journal=Chem Biodivers |volume=3 |issue=10 |pages=1053-101 |year=2006 |pmid=17193224}}</ref>异型生物质包括[[药物|合成药物]]、[[毒药|天然毒药]]和[[抗生素]],所幸的是它们可以在一系列异型生物质代谢酶的作用下被去毒化。在人体中,细胞色素-P450氧化酶<ref>{{en}}{{cite journal en|author=Danielson P |title=The cytochrome P450 superfamily: biochemistry, evolution and drug metabolism in humans |journal=Curr Drug Metab |volume=3 |issue=6 |pages=561-97 |year=2002 |pmid=12369887}}</ref>、尿苷二磷酸葡醛酸转移酶(UDP-glucuronosyltransferases)<ref>{{en}}{{cite journal en|author=King C, Rios G, Green M, Tephly T |title=UDP-glucuronosyltransferases |journal=Curr Drug Metab |volume=1 |issue=2 |pages=143-61 |year=2000 |pmid=11465080}}</ref>和[[谷胱苷肽转移酶]]([[:en:glutathione S-transferase|glutathione S-transferase]])<ref>{{en}}{{cite journal en|author=Sheehan D, Meade G, Foley V, Dowd C |title=Structure, function and evolution of glutathione transferases: implications for classification of non-mammalian members of an ancient enzyme superfamily |url=http://www.pubmedcentral.nih.gov/articlerender.fcgi?tool=pubmed&pubmedid=11695986 |journal=Biochem J |volume=360 |issue=Pt 1 |pages=1–16 |year=2001 |pmid=11695986}}</ref>都属于这类酶。这一酶系统的功能发挥有三个阶段:首先氧化异型生物质,然后在该物质分子上连接一个水溶性基团,最后修饰过的含水溶性基团的异型生物质被运出细胞(在多细胞生物体中,还可以被进一步代谢并被排出体外)。在[[生态学]]中,这些反应对于污染物的[[生物降解|微生物降解]]和污染土壤(特别是石油污染)的[[生物修复]]具有极为重要的作用。<ref>{{en}}{{cite journal en|author=Galvão T, Mohn W, de Lorenzo V |title=Exploring the microbial biodegradation and biotransformation gene pool |journal=Trends Biotechnol |volume=23 |issue=10 |pages=497–506 |year=2005 |pmid=16125262}}</ref>许多这样的微生物反应在多细胞生物体中也同样存在,但由于微生物种类的多样性使得它们能够代谢的物质比多细胞生物体要广泛的多,它们甚至可以降解包括[[有机氯]]([[:en:organochloride|organochloride]])在内的[[持久性有机污染物]]。<ref>{{en}}{{cite journal en|author=Janssen D, Dinkla I, Poelarends G, Terpstra P |title=Bacterial degradation of xenobiotic compounds: evolution and distribution of novel enzyme activities |journal=Environ Microbiol |volume=7 |issue=12 |pages=1868–82 |year=2005 |pmid=16309386}}</ref> |
|||
在[[需氧生物]]中还存在[[氧化应激]]的问题。<ref name=Davies>{{en}}{{cite journal en|author=Davies K |title=Oxidative stress: the paradox of aerobic life |journal=Biochem Soc Symp |volume=61 |issue= |pages=1–31 |year=1995 |pmid=8660387}}</ref>其中,需要对包括氧化磷酸化和蛋白质折叠中二硫键形成所产生的[[活性氧]](如[[过氧化氢]])进行处理。<ref>{{en}}{{cite journal en|author=Tu B, Weissman J |title=Oxidative protein folding in eukaryotes: mechanisms and consequences |url=http://www.jcb.org/cgi/content/full/164/3/341 |journal=J Cell Biol |volume=164 |issue=3 |pages=341-6 |year=2004 |pmid=14757749}}</ref>这些能够损害机体的氧化活性物质由[[抗氧化剂|抗氧化]]代谢物(如[[谷胱甘肽]])和相关酶(如[[过氧化氢酶]]和[[辣根过氧化物酶]])来清除。<ref name=Sies>{{en}}{{cite journal en|author=Sies H |title=Oxidative stress: oxidants and antioxidants |url=http://ep.physoc.org/cgi/reprint/82/2/291.pdf |journal=Exp Physiol |volume=82 |issue=2 |pages=291-5 |year=1997 |pmid=9129943}}</ref><ref name=Vertuani>{{en}}{{cite journal en|author=Vertuani S, Angusti A, Manfredini S |title=The antioxidants and pro-antioxidants network: an overview |journal=Curr Pharm Des |volume=10 |issue=14 |pages=1677–94 |year=2004 |pmid=15134565}}</ref> |
|||
==生物体的热力学== |
|||
{{main|生物热力学}} |
|||
生物体也必须遵守[[热力学定律]](描述[[功]]和[[内能|热]]之间的转移关系)。[[热力学第二定律]]指出,在任何[[封闭系统]]中,[[熵 (熱力學)|熵]]值总是趋向于增加。虽然生物体的高度复杂性看起来似乎与这一定律相反,但生物体实际上是[[开放系统]],能够与周围环境进行物质和能量交换;因此,生命系统不是处于[[热力学平衡|平衡]]之中,而是表现为[[耗散结构]]来维持它们的高度复杂性,同时增加周围环境的熵值。<ref>{{en}}{{cite journal en|author=von Stockar U, Liu J |title=Does microbial life always feed on negative entropy? Thermodynamic analysis of microbial growth |journal=Biochim Biophys Acta |volume=1412 |issue=3 |pages=191–211 |year=1999 |pmid=10482783}}</ref>细胞中的代谢则是通过将分解代谢的[[自发过程]]([[:en:spontaneous process|spontaneous process]])和合成代谢的非自发过程偶联来达到保持复杂性的目的。用[[非平衡态热力学|热力学]]来解释,代谢实际上就是通过制造无序来保持有序。<ref>{{en}}{{cite journal en|author=Demirel Y, Sandler S |title=Thermodynamics and bioenergetics |journal=Biophys Chem |volume=97 |issue=2–3 |pages=87–111 |year=2002 |pmid=12050002}}</ref> |
|||
==调控机制== |
|||
{{see also|代谢途径|代谢控制分析|荷尔蒙|信号转导}} |
|||
由于生物体的外界环境处于不断的变化之中,因此代谢反应必须能够被精确的调控,以保持细胞内各组分的稳定,即[[体内平衡]]。<ref>{{en}}{{cite journal en|author=Albert R |title=Scale-free networks in cell biology |url=http://jcs.biologists.org/cgi/content/full/118/21/4947 |journal=J Cell Sci |volume=118 |issue=Pt 21 |pages=4947–57 |year=2005 |pmid=16254242}}</ref><ref>{{en}}{{cite journal en|author=Brand M |title=Regulation analysis of energy metabolism |url=http://jeb.biologists.org/cgi/reprint/200/2/193 |journal=J Exp Biol |volume=200 |issue=Pt 2 |pages=193–202 |year=1997 |pmid=9050227}}</ref>代谢调控也使得生物体能够对外界信号产生反馈并能够与其周围环境进行互动。<ref>{{en}}{{cite journal en|author=Soyer O, Salathé M, Bonhoeffer S |title=Signal transduction networks: topology, response and biochemical processes |journal=J Theor Biol |volume=238 |issue=2 |pages=416-25 |year=2006 |pmid=16045939}}</ref>其中,两个紧密联系的概念对于了解代谢途径的调控机制非常重要:其一,一个酶在代谢途径中的'''调节'''就是它的酶活性是如何根据信号来增加或降低的;其二,由这个酶所施加的'''控制'''即是它的活性的变化对于代谢途径整体速率(途径的[[通量]])的影响。<ref name=Salter>{{en}}{{cite journal en|author=Salter M, Knowles R, Pogson C |title=Metabolic control |journal=Essays Biochem |volume=28 |issue= |pages=1–12 |year=1994 |pmid=7925313}}</ref>例如,一个酶可以在活性上发生很大的变化(比如被高度调控),但如果这些变化对于其所在的代谢途径的通量基本没有影响,那么这个酶就不能够对于这一途径发挥控制作用。<ref>{{en}}{{cite journal en|author=Westerhoff H, Groen A, Wanders R |title=Modern theories of metabolic control and their applications (review) |journal=Biosci Rep |volume=4 |issue=1 |pages=1–22 |year=1984 |pmid=6365197}}</ref> |
|||
[[Image:Insulin glucose metabolism ZP zh.svg|thumb|right|300px|'''胰岛素对于葡萄糖吸收和代谢的影响'''。(1)胰岛素结合到对应受体上,(2)受体激活许多蛋白级联反应,其中包括(3)Glut-4运输蛋白转运到质膜上使葡萄糖可以进入细胞、(4)[[糖原]]合成、(5)[[糖酵解]]、(6)[[脂肪酸]]合成。]] |
|||
代谢调控可分为多个层次。在自身调节中,代谢途径可以自调节以对底物或产物水平的变化做出反应;例如,产物量降低可以引起途径通量的增加,从而使产物量得到补偿。<ref name=Salter/>这种类型的调节包含对于途径中多个酶的活性的[[变构调节]]。<ref>{{en}}{{cite journal en|author=Fell D, Thomas S |title=Physiological control of metabolic flux: the requirement for multisite modulation |url=http://www.pubmedcentral.nih.gov/articlerender.fcgi?tool=pubmed&pubmedid=7575476 |journal=Biochem J |volume=311 (Pt 1) |issue= |pages=35-9 |year=1995 |pmid=7575476}}</ref>多细胞生物中,细胞在接收到来自其他细胞的信号后作出反应来改变它的代谢情况,而这就属于外部调控。这些信号通常是通过可溶性分子(“信使”)来传递的,如[[激素]]和[[生长因子]],它们能够特异性地与细胞表面特定的[[受体]]分子结合。<ref>{{en}}{{cite journal en|author=Hendrickson W |title=Transduction of biochemical signals across cell membranes |journal=Q Rev Biophys |volume=38 |issue=4 |pages=321-30 |year=2005 |pmid=16600054}}</ref>在与受体结合之后,信号就会通过[[第二信使系统]]被传递到细胞内部,此过程中通常含有蛋白质的[[磷酸化]]。<ref>{{en}}{{cite journal en|author=Cohen P |title=The regulation of protein function by multisite phosphorylation—a 25 year update |journal=Trends Biochem Sci |volume=25 |issue=12 |pages=596–601 |year=2000 |pmid=11116185}}</ref> |
|||
由[[胰岛素]]调节的葡萄糖代谢是一个研究得比较透彻的外部调控的例子。<ref>{{en}}{{cite journal en|author=Lienhard G, Slot J, James D, Mueckler M |title=How cells absorb glucose |journal=Sci Am |volume=266 |issue=1 |pages=86–91 |year=1992 |pmid=1734513}}</ref>机体合成胰岛素是用于对[[血糖|血液中葡萄糖水平]]的升高做出反应。胰岛素与细胞表面的[[胰岛素受体]]结合,然后激活一系列[[蛋白激酶]]级联反应,使细胞能够摄入葡萄糖并将其转化为能量储存分子,如[[脂肪酸]]和[[糖原]]。<ref>{{en}}{{cite journal en|author=Roach P |title=Glycogen and its metabolism |journal=Curr Mol Med |volume=2 |issue=2 |pages=101-20 |year=2002 |pmid=11949930}}</ref>糖原的代谢是由[[磷酸化酶]]和[[糖原合成酶]]来控制的,前者可以降解糖原,而后者可以合成糖原。这些酶是相互调控的:磷酸化作用可以抑制糖原合成酶的活性,却激活磷酸化酶的活性。胰岛素通过激活[[磷酸酶|蛋白磷酸酶]]而降低酶的磷酸化,从而使糖原得以合成。<ref>{{en}}{{cite journal en|author=Newgard C, Brady M, O'Doherty R, Saltiel A |title=Organizing glucose disposal: emerging roles of the glycogen targeting subunits of protein phosphatase-1 |url=http://diabetes.diabetesjournals.org/cgi/reprint/49/12/1967.pdf |journal=Diabetes |volume=49 |issue=12 |pages=1967–77 |year=2000 |pmid=11117996}}</ref> |
|||
==进化== |
|||
{{see also|分子进化|种系发生学}} |
|||
[[Image:Tree of life int zh.svg|thumb|left|500px|[[系統發生樹|进化树]]显示所有来自生物三[[域 (生物)|域]]中的生物体有着共同的祖先。[[细菌]]显示为蓝色,[[真核生物]]显示为红色,而[[古菌]]显示为绿色。一些生物[[门 (生物)|门]]的相对位置也都在进化树周围标示出来。]] |
|||
如前所述,代谢的中心途径,如糖酵解和三羧酸循环,存在于[[三域系統|三域]]中的所有生物体中,也曾存在于“[[最后的共同祖先]]”中。<ref>{{en}}{{cite journal en|author=Romano A, Conway T |title=Evolution of carbohydrate metabolic pathways |journal=Res Microbiol |volume=147 |issue=6–7 |pages=448-55 |year=1996 |pmid=9084754}}</ref><ref name=SmithE/>共同祖先细胞是[[原核生物]],并且很可能是一种具有广泛的氨基酸、糖类和脂类代谢的[[产甲烷菌]]。<ref>{{en}}{{cite journal en|author=Koch A |title=How did bacteria come to be? |journal=Adv Microb Physiol |volume=40 |pages=353-99 |year=1998 |pmid=9889982}}</ref><ref>{{en}}{{cite journal en|author=Ouzounis C, Kyrpides N |title=The emergence of major cellular processes in evolution |journal=FEBS Lett |volume=390 |issue=2 |pages=119-23 |year=1996 |pmid=8706840}}</ref>这些古老的代谢途径之所以没有进一步[[进化]],其原因可能是途径中的反应对于特定的代谢问题已经是一个优化的解决办法,可以以很少的步骤达而到很高的效率。<ref name=Ebenhoh/><ref name=Cascante/>第一个基于酶的代谢途径(现在可能已经成为嘌呤核苷酸代谢中的一部分)和之前的代谢途径是原始的[[RNA世界學說|RNA世界]]的组成部分。<ref>{{en}}{{cite journal en|author=Caetano-Anolles G, Kim HS, Mittenthal JE |title=The origin of modern metabolic networks inferred from phylogenomic analysis of protein architecture |journal=Proc Natl Acad Sci USA |volume=104 |issue=22 |pages=9358-63 |year=2007 |pmid=17517598}}</ref> |
|||
研究者们提出了多种模型来描述新的代谢途径是如何进化而来的:如添加新的酶到一个较短的原始途径,或是复制而后分化整个途径,并将已存在的酶和它们的复合体带入新的反应途径中。<ref>{{en}}{{cite journal en|author=Schmidt S, Sunyaev S, Bork P, Dandekar T |title=Metabolites: a helping hand for pathway evolution? |journal=Trends Biochem Sci |volume=28 |issue=6 |pages=336-41 |year=2003 |pmid=12826406}}</ref>这些进化机制中,哪一种更为重要目前还不清楚,但基因组研究显示在同一个途径中的酶可能具有一个共同“祖先”,这就提示许多途径是通过一步接一步的演化方式利用已存在的反应步骤来获得新的功能。<ref>{{en}}{{cite journal en|author=Light S, Kraulis P |title=Network analysis of metabolic enzyme evolution in Escherichia coli |journal=BMC Bioinformatics |volume=5 |issue= |pages=15 |year=2004 |pmid=15113413}}</ref><ref>{{en}}{{cite journal en|author=Alves R, Chaleil R, Sternberg M |title=Evolution of enzymes in metabolism: a network perspective |journal=J Mol Biol |volume=320 |issue=4 |pages=751-70 |year=2002 |pmid=12095253}}</ref>另一种较为合理的模型来自于对代谢网络中蛋白质结构的演化研究,其结果提示酶具有普适性,同样的酶能够在不同的代谢途径中被利用并发挥相似的作用。<ref>{{en}}{{cite journal en|author=Kim HS, Mittenthal JE, Caetano-Anolles G|title=MANET: tracing evolution of protein architecture in metabolic networks |journal=BMC Bioinformatics|volume=19 |issue=7 |pages=351 |year=2006 |pmid=16854231}}</ref>这些利用的进程就导致进化,酶在途径中以类似于马赛克排列的方式进行拼接。<ref>{{en}}{{cite journal en|author=Teichmann SA, Rison SC, Thornton JM, Riley M, Gough J, Chothia C|title=Small-molecule metabolsim: an enzyme mosaic |journal=Trends Biotechnol|volume=19 |issue=12 |pages=482-6 |year=2001 |pmid=11711174}}</ref>第三种可能性是代谢中的一些部分可以以“模块”的方式存在,而模块可以被用于不同的途径并对不同的分子执行相似的功能。<ref>{{en}}{{cite journal en|author=Spirin V, Gelfand M, Mironov A, Mirny L |title=A metabolic network in the evolutionary context: multiscale structure and modularity |url=http://www.pubmedcentral.nih.gov/articlerender.fcgi?tool=pubmed&pubmedid=16731630 |journal=Proc Natl Acad Sci U S A |volume=103 |issue=23 |pages=8774–9 |year=2006 |pmid=16731630}}</ref> |
|||
在进化出新的代谢途径的同时,进化也可能造成代谢功能的降低或丧失。例如,一些[[寄生|寄生物]]失去了对于生存非关键的代谢进程,代之以直接从[[宿主]]体内获取氨基酸、核苷酸和糖类。<ref>{{en}}{{cite journal en|author=Lawrence J |title=Common themes in the genome strategies of pathogens |journal=Curr Opin Genet Dev |volume=15 |issue=6 |pages=584-8 |year=2005 |pmid=16188434}}</ref><ref>{{en}}{{cite journal en|author=Wernegreen J |title=For better or worse: genomic consequences of intracellular mutualism and parasitism |journal=Curr Opin Genet Dev |volume=15 |issue=6 |pages=572-83 |year=2005 |pmid=16230003}}</ref>类似的代谢能力退化的现象在一些[[内共生体|内共生]]生物体中也被观察到。<ref>{{en}}{{cite journal en|author=Pál C, Papp B, Lercher M, Csermely P, Oliver S, Hurst L |title=Chance and necessity in the evolution of minimal metabolic networks |journal=Nature |volume=440 |issue=7084 |pages=667-70 |year=2006 |pmid=16572170}}</ref> |
|||
==相关的研究分析== |
|||
{{see also|蛋白质研究方法|蛋白质组学|代谢物组学|代谢网络建模}} |
|||
[[Image:A thaliana metabolic network.png|thumb|300px|right|[[拟南芥]](''Arabidopsis thaliana'')中[[三羧酸循环]]的[[代谢网络]]。[[酶]]和[[代謝物]]用红色方块来表示,它们之间的相互作用用黑线来表示。]] |
|||
代谢的经典研究方法是[[还原论|还原法]],即对单个代谢途径进行研究。[[放射性示踪]]([[:en:radioactive tracer|radioactive tracer]])是一个非常有用的研究手段,它通过定位放射性标记的中间物和产物来追踪代谢过程,从而可以在整个生物体、组织或细胞等不同水平上对代谢进行研究。<ref>{{en}}{{cite journal en|author=Rennie M |title=An introduction to the use of tracers in nutrition and metabolism |journal=Proc Nutr Soc |volume=58 |issue=4 |pages=935-44 |year=1999 |pmid=10817161}}</ref>随后,对催化这些化学反应的酶进行[[蛋白质纯化|纯化]],并鉴定它们的[[酶动力学|动力学]]性质和对应的[[酶抑制剂|抑制剂]]。另一种研究方法是在一个细胞或组织中鉴定代谢相关的小分子,其中所有的这些小分子被称为一个[[组织细胞代谢组|代谢组]](Metabolome)。综上,这些研究给出了单个代谢途径的组成结构和功能;但这些方法却无法有效应用于更为复杂的系统,如一个完整细胞中的所有代谢。<ref>{{en}}{{cite journal en|author=Phair R |title=Development of kinetic models in the nonlinear world of molecular cell biology |journal=Metabolism |volume=46 |issue=12 |pages=1489–95 |year=1997 |pmid=9439549}}</ref> |
|||
细胞中代谢网络(含有数千种不同的酶)的复杂性由右图(图中仅仅只含有43个蛋白质和40个代谢物之间的相互作用)可知是极高的。但现在,利用基因组数据来构建完整的代谢化学反应网络并生成更[[整体论|整体化]]的数学模型来解释和预测各种代谢行为已经成为可能。<ref>{{en}}{{cite journal en|author=Borodina I, Nielsen J |title=From genomes to in silico cells via metabolic networks |journal=Curr Opin Biotechnol |volume=16 |issue=3 |pages=350-5 |year=2005 |pmid=15961036}}</ref>特别是将从经典研究方法中所获得的代谢途径和代谢物的数据以及从[[蛋白质组学]]和[[DNA微阵列]]研究中获得的数据整合到这些数学模型中,则可以极大地完善这些模型。<ref>{{en}}{{cite journal en|author=Gianchandani E, Brautigan D, Papin J |title=Systems analyses characterize integrated functions of biochemical networks |journal=Trends Biochem Sci |volume=31 |issue=5 |pages=284-91 |year=2006 |pmid=16616498}}</ref>利用所有这些技术,一个人体代谢模型已经被提出,这一模型将对未来的药物和生物化学研究提供指导。<ref>{{en}}{{cite journal en|author=Duarte NC, Becker SA, Jamshidi N, ''et al'' |title=Global reconstruction of the human metabolic network based on genomic and bibliomic data |journal=Proc. Natl. Acad. Sci. U.S.A. |volume=104 |issue=6 |pages=1777–82 |year=2007 |month=February |pmid=17267599 |doi=10.1073/pnas.0610772104 |url=http://www.pnas.org/cgi/pmidlookup?view=long&pmid=17267599}}</ref> |
|||
代谢信息的一项主要的技术应用是[[代谢工程]]。在代谢工程中,诸如酵母、植物和细菌等生物体被[[遗传工程]]改造为[[生物技术]]中的高效工具,用于包括[[抗生素]]在内的药物或工业用化学品(如[[1,3-丙二醇]]和[[莽草酸]])的生产。<ref>{{en}}{{cite journal en|author=Thykaer J, Nielsen J |title=Metabolic engineering of beta-lactam production |journal=Metab Eng |volume=5 |issue=1 |pages=56–69 |year=2003 |pmid=12749845}} |
|||
</ref><ref>{{en}}{{cite journal en|author=González-Pajuelo M, Meynial-Salles I, Mendes F, Andrade J, Vasconcelos I, Soucaille P |title=Metabolic engineering of Clostridium acetobutylicum for the industrial production of 1,3-propanediol from glycerol |journal=Metab Eng |volume=7 |issue=5–6 |pages=329-36 |year=2005 |pmid=16095939}}</ref><ref>{{en}}{{cite journal en|author=Krämer M, Bongaerts J, Bovenberg R, Kremer S, Müller U, Orf S, Wubbolts M, Raeven L |title=Metabolic engineering for microbial production of shikimic acid |journal=Metab Eng |volume=5 |issue=4 |pages=277-83 |year=2003 |pmid=14642355}}</ref>这些改造通常有助于降低产物合成中的能量消耗,增加产量和减少废物的产生。<ref>{{en}}{{cite journal en|author=Koffas M, Roberge C, Lee K, Stephanopoulos G |title=Metabolic engineering |journal=Annu Rev Biomed Eng |volume=1 |issue= |pages=535-57 |year=1999 |pmid=11701499}}</ref> |
|||
==参见== |
|||
{{wikibooks}}{{Wiktionary}} |
|||
* [[基础代谢率]] |
|||
* [[量热法]] |
|||
* [[遗传性代谢病]] |
|||
* [[铁硫世界理论]],一种关于[[生命起源]]的理论。 |
|||
* [[呼吸运动计量法]] |
|||
* [[食物热效应]] |
|||
* [[水代谢]] |
|||
==参考文献== |
|||
{{reflist|2}} |
|||
==延伸阅读== |
|||
'''入门级''' |
|||
* {{en}}{{aut|Rose, S.}} and {{aut|Mileusnic, R.}}, ''The Chemistry of Life.'' (Penguin Press Science, 1999), ISBN 0-14027-273-9 |
|||
* {{en}}{{aut|Schneider, E. D.}} and {{aut|Sagan, D.}}, ''Into the Cool: Energy Flow, Thermodynamics, and Life.'' (University Of Chicago Press, 2005), ISBN 0-22673-936-8 |
|||
* {{en}}{{aut|Lane, N.}}, ''Oxygen: The Molecule that Made the World.'' (Oxford University Press, USA, 2004), ISBN 0-19860-783-0 |
|||
'''进阶级''' |
|||
* {{en}}{{aut|Price, N.}} and {{aut|Stevens, L.}}, ''Fundamentals of Enzymology: Cell and Molecular Biology of Catalytic Proteins.'' (Oxford University Press, 1999), ISBN 0-19850-229-X |
|||
* {{en}}{{aut|Berg, J.}} {{aut|Tymoczko, J.}} and {{aut|Stryer, L.}}, ''Biochemistry.'' (W. H. Freeman and Company, 2002), ISBN 0-71674-955-6 |
|||
* {{en}}{{aut|Cox, M.}} and {{aut|Nelson, D. L.}}, ''Lehninger Principles of Biochemistry.'' (Palgrave Macmillan, 2004), ISBN 0-71674-339-6 |
|||
* {{en}}{{aut|Brock, T. D.}} {{aut|Madigan, M. T.}} {{aut|Martinko, J.}} and {{aut|Parker J.}}, ''Brock's Biology of Microorganisms.'' (Benjamin Cummings, 2002), ISBN 0-13066-271-2 |
|||
* {{en}}{{aut|Da Silva, J.J.R.F.}} and {{aut|Williams, R. J. P.}}, ''The Biological Chemistry of the Elements: The Inorganic Chemistry of Life.'' (Clarendon Press, 1991), ISBN 0-19855-598-9 |
|||
* {{en}}{{aut|Nicholls, D. G.}} and {{aut|Ferguson, S. J.}}, ''Bioenergetics.'' (Academic Press Inc., 2002), ISBN 0-12518-121-3 |
|||
==外部链接== |
|||
'''一般性介绍''' |
|||
* {{en}}[http://www.biochemweb.org/metabolism.shtml 代谢、呼吸作用和光合作用] |
|||
* {{zh}}[http://www.lmbe.seu.edu.cn/biology/bess/biology/chapt12/index.htm 能量获得与转换],现代生命科学导论 |
|||
* {{en}}[http://www.rpi.edu/dept/bcbp/molbiochem/MBWeb/mb1/MB1index.html 代谢中的生物化学] |
|||
* {{en}}[http://www.stthomas.edu/biol/ecophys/homepage/homepage.html 高级动物代谢计算器/互动式学习工具] |
|||
* {{en}}[http://www.slic2.wsu.edu:82/hurlbert/micro101/pages/Chap7.html 微生物代谢] |
|||
* {{en}}[http://www.gwu.edu/~mpb/ 生物化学中的代谢途径] |
|||
* {{en}}[http://www.chemsoc.org/networks/LearnNet/cfb/contents.htm 生物学家的化学] |
|||
* {{en}}[http://www.sparknotes.com/testprep/books/sat2/biology/ Sparknotes SAT 生物化学] |
|||
* {{en}}[http://www.sciencegateway.org/resources/biologytext/index.html MIT生物在线书籍] |
|||
* {{en}}[http://www.britannica.com/eb/article-9109831/metabolism Encyclopœdia Britannica上关于代谢的文章] |
|||
'''词汇表和词典''' |
|||
* {{en}}[http://biology.clc.uc.edu/scripts/glossary.pl 生化词汇表] |
|||
* {{en}}[http://www.portlandpress.com/pp/books/online/glick/default.htm 另一生化词汇表] |
|||
* {{en}}[http://www.biology-online.org/dictionary.asp 在线生物词典] |
|||
'''人体代谢''' |
|||
* {{en}}[http://library.med.utah.edu/NetBiochem/titles.htm 医学生物化学中的话题] |
|||
* {{en}}[http://themedicalbiochemistrypage.org/ 医学生物化学] |
|||
'''数据库''' |
|||
* {{en}}[http://BioCyc.org/ BioCyc Collection上的基因组和通路数据库] |
|||
* {{en}}[http://www.expasy.org/cgi-bin/show_thumbnails.pl 代谢途径流程图] |
|||
* {{en}}[http://www.genome.ad.jp/kegg/ KEGG通路数据库] |
|||
* {{en}}[http://www.sigmaaldrich.com/img/assets/4202/MetabolicPathways_6_17_04_.pdf IUBMB-Nicholson代谢通路图] |
|||
* {{en}}[http://www.reactome.org/ Reactome生物进程数据库] |
|||
'''代谢途径''' |
|||
* {{en}}[http://www2.ufp.pt/~pedros/bq/integration.htm Interactive 主要代谢通路的流程图] |
|||
* {{en}}[http://biotech.icmb.utexas.edu/glycolysis/glycohome.html 糖酵解] |
|||
* {{en}}[http://www.oxygraphics.co.uk/cds.htm 光合作用] |
|||
* {{en}}[http://photoscience.la.asu.edu/photosyn/education/learn.html 什么是光合作用] |
|||
* {{zh}}[http://www.ymcn.gx.cn/yysh/Article/ShowArticle.asp?ArticleID=153 糖、脂、氨基酸代谢途径间的相互联系] |
|||
{{metabolism}} |
|||
{{Biochemical families}} |
|||
{{Wiktionary}} |
|||
{{Link FA|he}} |
{{Link FA|he}} |
||
{{Link FA|en}} |
{{Link FA|en}} |
||
2008年7月24日 (四) 06:35的版本

代谢是生物体内所发生的用于维持生命的一系列化学反应的总称。这些反应进程使得生物体能够生长和繁殖、保持它们的结构以及对外界环境做出反应。代谢通常被分为两类:分解代谢可以对大的分子进行分解以获得能量(如细胞呼吸);合成代谢则可以利用能量来合成细胞中的各个组分,如蛋白质和核酸等。代谢可以被认为是生物体不断进行物质和能量交换的过程,一旦物质和能量的交换停止,生物体的结构和系统就会解体。
代谢中的化学反应可以被归纳为代谢途径,通过一系列酶的作用将一种化学物质转化为另一种化学物质。酶对于代谢来说是至关重要的,因为它们的催化作用使得生物体可以进行热力学上难以发生的反应。当外界环境发生变化或接受来自其他细胞的信号时,细胞也需要通过酶来实现对代谢途径的调控,从而对这些变化和信号做出反应。
一个生物体的代谢机制决定了哪些物质对于此生物体是有营养的,而哪些是有毒的。例如,一些原核生物利用硫化氢作为营养物质,但这种气体对于动物来说却是致命的。[1]代谢速度,或者说代谢率,也影响了一个生物体对于食物的需求量。
代谢的一个很大的特点是:即使是差异巨大的不同物种,它们之间的基本代谢途径也还是相似的。例如,羧酸,作为柠檬酸循环中的最为人们所知的中间产物,存在于所有的生物体中,无论是单细胞的细菌还是巨大的多细胞生物如大象。[2]代谢中所存在的这样的相似性很可能是由于相关代谢途径的高效率以及在进化史早期就出现的结果。[3][4]
历史

对于代謝的科学研究已经跨越了数个世纪,从早期对于动物整体代谢的研究一直到现代生物化学中对于单个代谢反应机制的探索。代谢的概念的出现可以追溯到13世纪,阿拉伯医学家伊本·纳菲斯(Ibn al-Nafis)提出“身体和它的各个部分是处于一个分解和接受营养的连续状态,因此它们不可避免地一直发生着变化”。[5]第一个关于人体代谢的实验由意大利人桑托里奥·桑托里奥(Santorio Santorio)于1614年完成并发表在他的著作《医学统计方法》(Ars de statica medecina)中。[6]在书中,他描述了他如何在进食、睡觉、工作、性生活、斋戒、饮酒以及排泄等各项活动前后对自己的体重进行秤量;他发现大多数他所摄入的食物最终都通过他所称的“无知觉排汗”被消耗掉了。
在这些早期研究中,代谢进程的机制还没有被揭示,人们普遍认为存在一种“活力”可以活化器官。[7]到了19世纪,在对糖被酵母酵解为酒精的研究中,法国科学家路易斯·巴斯德总结出酵解过程是由酵母细胞内他称为“酵素”的物质来催化的。他写道:“酒精酵解是一种与生命以及酵母细胞的组织相关的,而与细胞的死亡和腐化无关的一种行为。”[8]这一发现与弗里德里希·维勒在1828年发表的关于尿素的化学合成[9]证明了细胞中发现的化学反应和有机物与其他化学无异,都遵循化学的基本原则。
20世纪初,酶首次被爱德华·比希纳所发现,这一发现使得对代谢中化学反应的研究从对细胞的生物学研究中独立出来,同时这也标志着生物化学研究的开始。[10]从20世纪初开始,人们对于生物化学的了解迅速增加。在现代生物化学家中,汉斯·克雷布斯是最多产的研究者之一,他对代谢的研究做出了重大的贡献:[11]他发现了尿素循环,随后又与汉斯·科恩伯格(Hans Kornberg)合作发现了三羧酸循环和乙醛酸循环。[12][13]现代生物化学研究受益于大量新技术的应用,诸如色谱分析、X射线晶体学、核磁共振、电子显微学、同位素标记、质谱分析和分子动力学模拟等。这些技术使得研究者可以发现并具体分析细胞中与代谢途径相关的分子。
关键的生化物质
动植物和微生物的大部分组成结构是由三类基本生物分子所构成,这三类分子是氨基酸、糖类和脂类(通常为称为脂肪)。由于这些分子是维持生命所必需的,代谢既制造这些分子以用于构建细胞和组织,又在摄入食物后将食物中的这些分子消化降解以提供维持生命所需的能量。许多重要的生化物质可以聚合在一起形成多聚体,如DNA和蛋白质。这些生物大分子对于所有的生物体都是必要的组分。下表中列出了一些最常见的生物大分子。
| 分子类型 | 单体形式的名称 | 多聚体形式的名称 | 多聚体形式的例子 |
|---|---|---|---|
| 氨基酸 | 氨基酸 | 蛋白质(或多肽) | 纤维蛋白和球蛋白 |
| 糖类 | 单糖 | 多糖 | 淀粉、糖原和纤维素 |
| 核酸 | 核苷酸 | 多聚核苷酸 | DNA和RNA |
氨基酸和蛋白质
蛋白质是由线性排列氨基酸所组成,氨基酸之间通过肽键相互连接。酶是最常见的蛋白质,它们催化代谢中的各类化学反应。一些蛋白质具有结构或机械功能,如参与形成细胞骨架以维持细胞形态。[14]还有许多蛋白质在细胞信号传导、免疫反应、细胞黏附和细胞周期调控中扮演重要角色。[15]
脂类
脂类是类别最多的生物分子。它们主要的结构用途是形成生物膜,如细胞膜;此外,它们也可以作为机体能量来源。[15]脂类通常被定义为疏水性或两性生物分子,可溶于诸如苯或氯仿等有机溶剂中。[16]脂肪是由脂肪酸基团和甘油基团所组成的一大类脂类化合物;其结构为一个甘油分子上以酯键连接了三个脂肪酸分子形成甘油三酯。[17]在此基本结构基础上,还存在有多种变型,包括不同大小长度的疏水骨架(如鞘脂类中的神经鞘氨醇基团)和不同类型的亲水基团(如磷脂中的磷酸盐基团)。类固醇(如胆固醇)是另一类由细胞合成的主要的脂类分子。[18]

糖类
糖类为带有大量羟基的醛或酮,可以以直链或环的形式存在。糖类是含量最为分赴的生物分子,其具有多种功能,如储存和运输能量(例如淀粉、糖原)以及作为结构性组分(植物中的纤维素和动物中的几丁质)。[15]糖类的基本组成单位为单糖,包括半乳糖、果糖以及十分重要的葡萄糖。单糖可以通过糖苷键连接在一起形成多糖,而连接的方式极为多样,也就造成了多糖种类的多样性。[19]

核苷酸和核酸
DNA和RNA是主要的两类核酸,它们都是由核苷酸连接形成的直链分子。核酸分子对于遗传信息的储存和利用是必不可少的,通过转录和翻译来完成从遗传信息到蛋白质的过程。[15]这些遗传信息由DNA修复机制来进行保护,并通过DNA复制来进行扩增。一些病毒(如HIV)含有RNA基因组,它们可以利用逆转录来从病毒RNA合成DNA模板。[20]核酶(如剪切体和核糖体)中的RNA还具有类似酶的特性,可以催化化学反应。单个核苷酸是由一个核糖分子连接上一个碱基来形成。其中,碱基是含氮的杂环,可以被分为两类:嘌呤和嘧啶。核苷酸也可以作为辅酶参与代谢基团的转移反应。[21]

辅酶
代谢中包含了种类广泛的化学反应,但其中大多数反应都属于几类基本的含有功能性基团的转移的反应类型。[22]这些反应中,细胞利用一系列小分子代谢中间物来在不同的反应之间携带化学基团。[21]这些基团转移的中间物被称为辅酶。每一类基团转移反应都由一个特定的辅酶来执行,辅酶同时是合成它和消耗它的一系列酶的底物。这些辅酶不断地被生成、消耗、再被回收利用。[23]
三磷酸腺苷(ATP)是生命体中最重要的辅酶之一,它是细胞中能量流通的普遍形式。ATP被用于在不同的化学反应之间进行化学能的传递。虽然细胞中只有少量的ATP存在,但它被不断地合成,人体一天所消耗的ATP的量积累起来可以达到自身的体重。[23]ATP是连接合成代谢和分解代谢的桥梁:分解代谢反应生成ATP,而合成代谢反应消耗ATP。它也可以作为磷酸基团的携带者参与磷酸化反应。
维生素是一类生命所需的微量有机化合物,但细胞自身无法合成。在人类营养学中,大多数的维生素可以在被修饰后发挥辅酶的功能;例如,细胞所利用的所有的水溶性维生素都是被磷酸化或偶联到核苷酸上的。[24]烟酰胺腺嘌呤二核苷酸(NAD,还原形式为NADH)是维生素B3(俗称烟酸)的一种衍生物,它也是一种重要的辅酶,可以作为氢受体。数百种不同类型的脱氢酶可以从它们的底物上移去电子,同时将NAD+还原为NADH。而后,这种还原形式便可以作为任何一个还原酶的辅酶,用于为酶底物的还原提供电子。[25]烟酰胺腺嘌呤二核苷酸在细胞中存在两种不同的形式:NADH和NADPH。NAD+/NADH多在分解代谢反应中发挥重要作用,而NADP+/NADPH则多用于合成代谢反应中。
矿物质和辅因子
无机元素在代谢中也发挥着重要的作用;其中一些在机体内含量丰富(如钠和钾),而另一些则为微量元素。大约99%的哺乳动物的质量为碳、氮、钙、钠、氯、钾、氢、磷、氧和硫元素。[26]绝大多数的碳和氮存在于有机物(如蛋白质、脂类和糖类)中,而氢和氧则主要存在于水中。[26]
含量丰富的无机元素都是作为电解质的离子。体内最重要的离子有钠、钾、钙、镁等金属离子和氯离子、磷酸根离子以及有机的碳酸氢根离子。在细胞膜的内外维持准确的离子梯度,可以保持渗透压和pH值的稳定。[27]离子对于神经和肌肉组织也同样不可缺少,这是因为这些组织中的动作电位(可以引起神经信号和肌肉收缩)是由细胞外液和细胞原生质之间的电解质交换来产生的。[28]电解质进入和离开细胞是通过细胞膜上的离子通道蛋白来完成的。例如,肌肉收缩依赖于位于细胞膜和横行小管(T-tubule)上的离子通道对于钙离子、钾离子和钠离子的流动的控制。[29]
过渡金属在生物体体内通常是作为微量元素存在的,其中锌和铁的含量最为丰富。[30][31]这些金属元素被一些蛋白质用作辅因子或者对于酶活性的发挥具有关键作用,例如携氧的血红蛋白和过氧化氢酶。[32]这些辅因子可以与特定蛋白质紧密结合;虽然酶的辅因子会在催化过程中被修饰,这些辅因子总是能够在催化完成后回到起始状态。[33][34]
分解代谢
分解代谢(又称为同化作用)是一系列裂解大分子的反应过程的总称,包括裂解和氧化食物分子。分解代谢反应的目的是为合成代谢反应提供所需的能量和反应物。分解代谢的机制在生物体中不尽相同,如有机营养菌分解有机分子来获得能量,而无机营养菌利用无机物作为能量来源,光能利用菌则能够吸收阳光并转化为可利用的化学能。然而,所有这些代谢形式都需要氧化还原反应的参与,反应主要是将电子从还原性的供体分子(如有机分子、水、氨、硫化氢、亚铁离子等)转移到受体分子(如氧气、硝酸盐、硫酸盐等)。[35]在动物中,这些反应还包括将复杂的有机分子分解为简单分子(如二氧化碳和水)。在光合生物(如植物和藍藻)中,这些电子转移反应并不释放能量,而是用作储存所吸收光能的一种方式。[15]
动物中最普遍的分解代谢反应可以被分为三个主要步骤:首先,大分子有机化合物,如蛋白质、多糖或脂类被消化分解为小分子组分;然后,这些小分子被细胞摄入并被转化为更小的分子,通常为乙酰辅酶A,此过程中会释放出部分能量;最后,辅酶A上的乙酰基团通过柠檬酸循环和电子传递链被氧化为水和二氧化碳,并释放出能量,这些能量可以通过将烟酰胺腺嘌呤二核苷酸(NAD+)还原为NADH而以化学能的形式被储存起来。
消化
淀粉、蛋白质和纤维素等大分子多聚体不能很快被细胞所吸收,需要先被分解为小分子单体然后才能被用于细胞代谢。有多种消化性酶能够降解这些多聚体,如蛋白酶可以将但蛋白质降解为多肽片断或氨基酸,糖苷水解酶可以将多糖分解为单糖。
微生物只是简单地分泌消化性酶到周围环境中,[36][37]而动物则只能由其消化系统中的特定细胞来分泌这些酶。[38]由这些位于细胞外的酶分解获得的氨基酸或单糖接着通过主动运输蛋白被运送到细胞内。[39][40]

来自有机物的能量
糖类的分解代谢即是将糖链分解为更小的单位。通常一旦糖链被分解为单糖后就可以被细胞所吸收。[41]进入细胞内的糖,如葡萄糖和果糖,就会通过糖酵解途径被转化为丙酮酸盐并产生部分的ATP。[42]丙酮酸盐是多个代谢途径的中间物,但其大部分会被转化为乙酰辅酶A并进入柠檬酸循环。虽然柠檬酸循环能够产生ATP,但其最重要的产物是NADH——由乙酰辅酶A被氧化来提供电子并由NAD生成,同时释放出无用的二氧化碳。在无氧条件下,糖酵解过程会生成乳酸盐,即由乳酸脱氢酶将丙酮酸盐转化为乳酸盐,同时将NADH又氧化为NAD+,使得NAD可以被循环利用于糖酵解中。另一中降解葡萄糖的途径是磷酸戊糖途径,该途径可以将辅酶烟酰胺腺嘌呤二核苷酸磷酸(NADP+)还原为NADPH,并生成戊糖,如核糖(合成核苷酸的重要组分)。
脂肪是通过水解作用分解为脂肪酸和甘油。甘油可以进入糖酵解途径,通过β-氧化被分解并释放出乙酰辅酶A,而乙酰辅酶A如上所述进入柠檬酸循环。脂肪酸同样通过氧化被分解;在氧化过程中脂肪酸可以释放出比糖类更多的能量,这是因为糖类结构的含氧比例较高。
氨基酸既可以被用于合成蛋白质或其他生物分子,又可以被氧化为尿素和二氧化碳以提供能量。[43]氧化的第一步是由转氨酶将氨基酸上的氨基除去,氨基随后被送入尿素循环,而留下的脱去氨基的碳骨架以酮酸的形式存在。有多种酮酸(如α-酮戊二酸,由脱去氨基的谷氨酸所形成)是柠檬酸循环的中间物。[44]此外,生糖氨基酸(glucogenic amino acid)能够通过糖异生作用被转化为葡萄糖(具体内容见下文)。[45]
能量转换
氧化磷酸化
氧化磷酸化中,通过如柠檬酸循环等代谢途径,电子从被消化吸收的食物分子上转移到氧气上,并将产生的能量以ATP的方式储存起来。在真核生物中,这一过程是由位于线粒体膜上的一系列膜蛋白来完成的,被称为电子传递链。而在原核生物中,对应的蛋白质则位于细胞内膜上。[46]这些蛋白质利用从电子还原性分子(如NADH)传递到氧气的反应所产生的能量将质子进行跨膜运输。[47]将质子泵出线粒体的结果就会在线粒体膜的两边产生质子的浓度差,从而在膜的两边形成一个电化学梯度。[48]通过电化学梯度所产生的驱动力使得质子通过线粒体膜上的ATP合成酶重新进入线粒体。这样的一个质子流会促使ATP合成酶的stalk亚基发生转动,并进一步带动合成酶结构域上的活性位点发生形变并将腺苷二磷酸(ADP)磷酸化,最终产生ATP。[23]
来自无机物的能量
化能无机营养是一种发现于一些原核生物中的代谢类型,这些原核生物通过氧化无机物来获得能量。它们能够利用氢气,[49]还原性的含硫化合物(如硫化物、硫化氢和硫代硫酸盐)[50],二价铁化合物[51]或氨[52]作为还原能的来源;这些还原性物质氧化过程的电子受体常常为氧气或亚硝酸盐。[53]这些进程对于整体的生物地質化學循環,如乙酸生成作用(acetogenesis)以及硝化和反硝化作用都很重要,并且对土壤的肥沃十分关键。[54][55]
来自光的能量
太阳光中的能量可以被植物、蓝藻、紫细菌、绿菌和一些原生生物所捕获。这一获取光能的进程常常与二氧化碳转化为有机物(即“碳固定”)相偶联,成为光合作用的一部分。光能获取和碳固定系统在原核生物中却能够分开运行的,因为紫细菌和绿菌无论在碳固定或是在有机物酵解之时,都可以利用阳光作为能量来源。[56][57]
捕获太阳能的过程与氧化磷酸化在本质上是相似的,因为两者都包括了能量以质子浓度梯度形式存在以及这种浓度差所驱动的ATP的合成。[23]用于驱动电子传递链的电子是来自于被称为光合反应中心的捕光蛋白。根据所含的光合色素类型的不同,可以将反应中心体分为两类:去镁叶绿素-醌型和铁-硫型;大多数的光合细菌只含有一类反应中心体,而植物和蓝藻则含有两类。[58]
此外,光系统是在光合作用中发挥主要作用的蛋白质复合物,包括光系统I和II。在植物中,光系统II可以利用光能从水中获得电子,并释放出氧气。电子随后流入细胞色素b6f复合物,该复合物用能量将质子泵出类囊体(位于叶绿体中)膜。[59]被泵出的质子又通过膜回到类囊体内,从而驱动ATP的合成(类似于氧化磷酸化中的ATP的合成)。当电子继续流过光系统I时,它们可以被用于还原辅酶NADP+、用于卡尔文循环或回收后用于合成更多的ATP。[60]
合成代谢
合成代谢(又称为异化作用)是一系列合成型代谢进程(即利用分解代谢所释放的能量来合成复杂分子)的总称。一般而言,用于组成细胞结构的复杂分子都是从小且简单的前体一步一步地构建而来。合成代谢包括三个基本阶段:首先生成前体分子,如氨基酸、单糖、类异戊二烯和核苷酸;其次,利用ATP水解所提供的能量,这些分子被激活而形成活性形式;最后,它们被组装成复杂的分子,如蛋白质、多糖、脂类和核酸。
不同的生物体所需要合成的各类复杂分子也互不相同。自养生物,如植物,可以在细胞中利用简单的小分子,如二氧化碳和水,来合成复杂的有机分子如多糖和蛋白质。异养生物则需要更复杂的物质来源,如单糖和氨基酸,来生产对应的复杂分子。生物体还可以根据它们所获得的能量来源的不同而被细分为:获取光能的光能自养生物和光能异养生物,以及从无机物氧化过程或的能量的化能自养生物和化能异养生物。
碳固定

光合作用是利用阳光、二氧化碳(CO2)和水来合成糖类并释放出氧气的过程。这一过程利用光合反应中心所产生的ATP和NADPH将CO2转化为3-磷酸甘油酸,并继续将3-磷酸甘油酸转化为生物体所需的葡萄糖,因此该过程被称为碳固定。碳固定反应作为卡尔文-本森循环的一部分,由RuBisCO酶来进行催化。[61]发生在植物中的光合作用分为三种:C3碳固定、C4碳固定和CAM光合作用。这些光合作用种类之间的差异在于当二氧化碳进入卡尔文循环的途径不同:C3型植物可以直接对CO2进行固定;而C4和CAM型则先将CO2合并到其他化合物上,这是对强光照和干旱环境的一种适应。[62]
在光合型原核生物中,碳固定的机制只见差异性更大。例如,二氧化碳可以经由卡尔文-本森循环(一种反式柠檬酸循环)[63]或者乙酰辅酶A的羧化作用[64][65]而被固定。此外,原核的化能自养菌也可以通过卡尔文-本森循环来固定CO2,但却使用来自无机化合物的能量来驱动反应。[66]
糖类和聚糖
糖类的合成代谢中,简单的有机酸可以被转化为单糖(如葡萄糖),然后单糖再聚合在一起形成多糖(如淀粉)。从包括丙酮酸盐、乳酸盐、甘油、3-磷酸甘油酸和氨基酸在内的化合物来生成葡萄糖的过程被称为糖异生。糖异生将丙酮酸盐通过一系列的中间物转化为葡萄糖-6-磷酸,其中的许多中间物可以与糖酵解过程共享。[42]然而,糖异生过程不是简单的糖酵解过程的逆反应,其中多个步骤是由不在糖酵解中发挥作用的酶来催化的。这样就使得葡萄糖的合成和分解可以被分别调控,以防止这两个途径进入无效循环(futile cycle)。[67][68]
虽然脂肪是通用的储存能量的方式,但在脊椎动物,如人类中,储存的脂肪酸不能通过糖异生作用而被转化为葡萄糖,因为这些生物体无法将乙酰辅酶A转变为丙酮酸盐(植物具有必要的酶,而动物则没有)。[69] 因此,在长期饥饿后,脊椎动物需要从脂肪酸来制造酮体来代替组织中的葡萄糖,因为像脑这样的组织不能够代谢脂肪酸。[70]在其它生物体,如植物和细菌中,由于存在乙醛酸循环,可以跳过柠檬酸循环中的脱羧反应,使得乙酰辅酶A可以被转化为草酰乙酸盐,而草酰乙酸盐可以被用于葡萄糖的生产,因此解决了脊椎动物中存在的这一代谢问题。[13][69]
多糖和聚糖是通过逐步加入单糖来合成的,加入单糖的过程是由糖基转移酶将糖基从一个活化的糖-磷酸供体(如尿苷二磷酸葡萄糖)上转移到作为受体的羟基(位于延长中的多糖链)上。由于糖环上的任一羟基都可以作为受体,因此多糖链可以是直链结构,也可以含有多个支链。[71]这些生成的多糖自身可以具有结构或代谢功能,或者可以在寡糖链转移酶的作用下被转接到脂类和蛋白质上。[72][73]
脂肪酸、萜类化合物和类固醇

脂肪酸合成是一个将乙酰辅酶A多聚化并还原的过程。脂肪酸上的乙酰基链是通过一个反应循环来延伸的,包括加入乙酰基、将其还原为乙醇和继续还原为烷烃的过程。在脂肪酸的生物合成中发挥作用的酶可以被分为两类:动物和真菌中,所有的脂肪酸合成反应由一个单一的多功能酶,I型脂肪酸合成酶来完成;[74]而在植物质体和细菌中,有多个不同的酶分别催化每一个反应,这些酶统称为I型脂肪酸合成酶。[75][76]
萜烯和异戊二烯类化合物(包括类胡萝卜素在内)是脂类中的一个大家族,它们组成了植物天然化合物中的最大的一类。[77]这些化合物是以异戊二烯为单位,聚合和修饰而成的;其中,异戊二烯是由具反应活性的前体,异戊烯焦磷酸(isopentenyl pyrophosphate)和二甲烯丙基焦磷酸(dimethylallyl pyrophosphate)提供的。[78]这两个前体可以在不同的途径中被合成。动物和古菌利用甲瓦龙酸途径(mevalonate pathway)来从乙酰辅酶A生产这两个化合物;[79]而植物和细菌则通过非甲瓦龙酸途径利用丙酮酸和甘油醛-3-磷酸作为底物来生产它们。[80][78]另一个利用这些活化的异戊二烯供体的重要反应是类固醇的生物合成。其中,异戊二烯单位连接在一起聚成角鲨烯(squalene),然后折叠起来形成一系列的环而得到羊毛脂甾醇(lanosterol)。[81]而羊毛脂甾醇能够被继续转化为其他类固醇,如胆固醇和麦角甾醇(ergosterol)。[82][81]
蛋白质
生物体之间合成20种基本氨基酸的能力各不相同。大多数的细菌和植物可以合成所有这20种氨基酸,而哺乳动物只能合成10种非必需氨基酸。[15]因此对于包括人在内的哺乳动物,获取必需氨基酸的途径只能是摄入富含这些氨基酸的食物。所有氨基酸都可以从糖酵解、柠檬酸循环或磷酸戊糖循环中的中间产物生成。其中,合成过程所需的氮由谷氨酸和谷氨酰胺来提供。氨基酸合成需要先有适当的α-酮酸形成,然后通过转氨作用形成氨基酸。[83]
氨基酸是通过肽键连接在一起并进一步形成蛋白质。每种不同的蛋白质都对应着自己独特的氨基酸序列(又被称为一级结构)。如同20多个字母就能排列组合成数以万计的单词一般,不同的氨基酸连接在一起能够形成数量庞大的蛋白质种类。氨基酸通过连接到对应转运RNA(tRNA)分子上形成氨酰tRNA而被激活,然后才可以被连接在一起。这种氨酰tRNA前体是通过一个ATP依赖的反应(将tRNA与正确的氨基酸相连接)来合成,该反应由氨酰tRNA合成酶进行催化。[84]然后,以信使RNA中的序列信息为指导,带有正确氨基酸的氨酰tRNA分子就可以结合到核糖体的对应位置,在核糖体的作用下将氨基酸连接到正在延长的蛋白质链上。[85]
核苷酸
核苷酸是由氨基酸、二氧化碳以及甲酸来合成的。[86]由于其合成途径需要消耗大量的代谢能量,大多数的生物体内都有有效的系统来进行核苷酸补救。[86][87]嘌呤是以核苷(即碱基连接上核糖)为基础合成的。腺嘌呤和鸟嘌呤是由前体核苷分子肌苷单磷酸(即次黄苷酸)衍生而来,而次黄苷酸则是由来自甘氨酸、谷氨酰胺和谷氨酰胺的原子以及从辅酶四氢叶酸盐上转移来的甲酸基来合成的。嘧啶是由碱基乳清酸盐合成的,乳清酸盐则由谷氨酰胺和谷氨酰胺转化而来。[88]
异型生物质代谢和氧化还原代谢
所有的生物体如果持续摄入非食物类物质而没有相应的代谢途径,这些物质就会在细胞中积累并造成危害。这些存在于机体内可能造成损害的物质被称为异型生物质(xenobiotic)。[89]异型生物质包括合成药物、天然毒药和抗生素,所幸的是它们可以在一系列异型生物质代谢酶的作用下被去毒化。在人体中,细胞色素-P450氧化酶[90]、尿苷二磷酸葡醛酸转移酶(UDP-glucuronosyltransferases)[91]和谷胱苷肽转移酶(glutathione S-transferase)[92]都属于这类酶。这一酶系统的功能发挥有三个阶段:首先氧化异型生物质,然后在该物质分子上连接一个水溶性基团,最后修饰过的含水溶性基团的异型生物质被运出细胞(在多细胞生物体中,还可以被进一步代谢并被排出体外)。在生态学中,这些反应对于污染物的微生物降解和污染土壤(特别是石油污染)的生物修复具有极为重要的作用。[93]许多这样的微生物反应在多细胞生物体中也同样存在,但由于微生物种类的多样性使得它们能够代谢的物质比多细胞生物体要广泛的多,它们甚至可以降解包括有机氯(organochloride)在内的持久性有机污染物。[94]
在需氧生物中还存在氧化应激的问题。[95]其中,需要对包括氧化磷酸化和蛋白质折叠中二硫键形成所产生的活性氧(如过氧化氢)进行处理。[96]这些能够损害机体的氧化活性物质由抗氧化代谢物(如谷胱甘肽)和相关酶(如过氧化氢酶和辣根过氧化物酶)来清除。[97][98]
生物体的热力学
生物体也必须遵守热力学定律(描述功和热之间的转移关系)。热力学第二定律指出,在任何封闭系统中,熵值总是趋向于增加。虽然生物体的高度复杂性看起来似乎与这一定律相反,但生物体实际上是开放系统,能够与周围环境进行物质和能量交换;因此,生命系统不是处于平衡之中,而是表现为耗散结构来维持它们的高度复杂性,同时增加周围环境的熵值。[99]细胞中的代谢则是通过将分解代谢的自发过程(spontaneous process)和合成代谢的非自发过程偶联来达到保持复杂性的目的。用热力学来解释,代谢实际上就是通过制造无序来保持有序。[100]
调控机制
由于生物体的外界环境处于不断的变化之中,因此代谢反应必须能够被精确的调控,以保持细胞内各组分的稳定,即体内平衡。[101][102]代谢调控也使得生物体能够对外界信号产生反馈并能够与其周围环境进行互动。[103]其中,两个紧密联系的概念对于了解代谢途径的调控机制非常重要:其一,一个酶在代谢途径中的调节就是它的酶活性是如何根据信号来增加或降低的;其二,由这个酶所施加的控制即是它的活性的变化对于代谢途径整体速率(途径的通量)的影响。[104]例如,一个酶可以在活性上发生很大的变化(比如被高度调控),但如果这些变化对于其所在的代谢途径的通量基本没有影响,那么这个酶就不能够对于这一途径发挥控制作用。[105]

代谢调控可分为多个层次。在自身调节中,代谢途径可以自调节以对底物或产物水平的变化做出反应;例如,产物量降低可以引起途径通量的增加,从而使产物量得到补偿。[104]这种类型的调节包含对于途径中多个酶的活性的变构调节。[106]多细胞生物中,细胞在接收到来自其他细胞的信号后作出反应来改变它的代谢情况,而这就属于外部调控。这些信号通常是通过可溶性分子(“信使”)来传递的,如激素和生长因子,它们能够特异性地与细胞表面特定的受体分子结合。[107]在与受体结合之后,信号就会通过第二信使系统被传递到细胞内部,此过程中通常含有蛋白质的磷酸化。[108]
由胰岛素调节的葡萄糖代谢是一个研究得比较透彻的外部调控的例子。[109]机体合成胰岛素是用于对血液中葡萄糖水平的升高做出反应。胰岛素与细胞表面的胰岛素受体结合,然后激活一系列蛋白激酶级联反应,使细胞能够摄入葡萄糖并将其转化为能量储存分子,如脂肪酸和糖原。[110]糖原的代谢是由磷酸化酶和糖原合成酶来控制的,前者可以降解糖原,而后者可以合成糖原。这些酶是相互调控的:磷酸化作用可以抑制糖原合成酶的活性,却激活磷酸化酶的活性。胰岛素通过激活蛋白磷酸酶而降低酶的磷酸化,从而使糖原得以合成。[111]
进化

如前所述,代谢的中心途径,如糖酵解和三羧酸循环,存在于三域中的所有生物体中,也曾存在于“最后的共同祖先”中。[112][2]共同祖先细胞是原核生物,并且很可能是一种具有广泛的氨基酸、糖类和脂类代谢的产甲烷菌。[113][114]这些古老的代谢途径之所以没有进一步进化,其原因可能是途径中的反应对于特定的代谢问题已经是一个优化的解决办法,可以以很少的步骤达而到很高的效率。[3][4]第一个基于酶的代谢途径(现在可能已经成为嘌呤核苷酸代谢中的一部分)和之前的代谢途径是原始的RNA世界的组成部分。[115]
研究者们提出了多种模型来描述新的代谢途径是如何进化而来的:如添加新的酶到一个较短的原始途径,或是复制而后分化整个途径,并将已存在的酶和它们的复合体带入新的反应途径中。[116]这些进化机制中,哪一种更为重要目前还不清楚,但基因组研究显示在同一个途径中的酶可能具有一个共同“祖先”,这就提示许多途径是通过一步接一步的演化方式利用已存在的反应步骤来获得新的功能。[117][118]另一种较为合理的模型来自于对代谢网络中蛋白质结构的演化研究,其结果提示酶具有普适性,同样的酶能够在不同的代谢途径中被利用并发挥相似的作用。[119]这些利用的进程就导致进化,酶在途径中以类似于马赛克排列的方式进行拼接。[120]第三种可能性是代谢中的一些部分可以以“模块”的方式存在,而模块可以被用于不同的途径并对不同的分子执行相似的功能。[121]
在进化出新的代谢途径的同时,进化也可能造成代谢功能的降低或丧失。例如,一些寄生物失去了对于生存非关键的代谢进程,代之以直接从宿主体内获取氨基酸、核苷酸和糖类。[122][123]类似的代谢能力退化的现象在一些内共生生物体中也被观察到。[124]
相关的研究分析

代谢的经典研究方法是还原法,即对单个代谢途径进行研究。放射性示踪(radioactive tracer)是一个非常有用的研究手段,它通过定位放射性标记的中间物和产物来追踪代谢过程,从而可以在整个生物体、组织或细胞等不同水平上对代谢进行研究。[125]随后,对催化这些化学反应的酶进行纯化,并鉴定它们的动力学性质和对应的抑制剂。另一种研究方法是在一个细胞或组织中鉴定代谢相关的小分子,其中所有的这些小分子被称为一个代谢组(Metabolome)。综上,这些研究给出了单个代谢途径的组成结构和功能;但这些方法却无法有效应用于更为复杂的系统,如一个完整细胞中的所有代谢。[126]
细胞中代谢网络(含有数千种不同的酶)的复杂性由右图(图中仅仅只含有43个蛋白质和40个代谢物之间的相互作用)可知是极高的。但现在,利用基因组数据来构建完整的代谢化学反应网络并生成更整体化的数学模型来解释和预测各种代谢行为已经成为可能。[127]特别是将从经典研究方法中所获得的代谢途径和代谢物的数据以及从蛋白质组学和DNA微阵列研究中获得的数据整合到这些数学模型中,则可以极大地完善这些模型。[128]利用所有这些技术,一个人体代谢模型已经被提出,这一模型将对未来的药物和生物化学研究提供指导。[129]
代谢信息的一项主要的技术应用是代谢工程。在代谢工程中,诸如酵母、植物和细菌等生物体被遗传工程改造为生物技术中的高效工具,用于包括抗生素在内的药物或工业用化学品(如1,3-丙二醇和莽草酸)的生产。[130][131][132]这些改造通常有助于降低产物合成中的能量消耗,增加产量和减少废物的产生。[133]
参见
参考文献
- ^ (英文)Friedrich C. Physiology and genetics of sulfur-oxidizing bacteria. Adv Microb Physiol. 1998, 39: 235–89. PMID 9328649.
- ^ 2.0 2.1 (英文)Smith E, Morowitz H. Universality in intermediary metabolism. Proc Natl Acad Sci U S A. 2004, 101 (36): 13168–73. PMID 15340153.
- ^ 3.0 3.1 (英文)Ebenhöh O, Heinrich R. Evolutionary optimization of metabolic pathways. Theoretical reconstruction of the stoichiometry of ATP and NADH producing systems. Bull Math Biol. 2001, 63 (1): 21–55. PMID 11146883.
- ^ 4.0 4.1 (英文)Meléndez-Hevia E, Waddell T, Cascante M. The puzzle of the Krebs citric acid cycle: assembling the pieces of chemically feasible reactions, and opportunism in the design of metabolic pathways during evolution. J Mol Evol. 1996, 43 (3): 293–303. PMID 8703096.
- ^ (英文)Dr. Abu Shadi Al-Roubi (1982), "Ibn Al-Nafis as a philosopher", Symposium on Ibn al Nafis, Second International Conference on Islamic Medicine: Islamic Medical Organization, Kuwait (cf. Ibnul-Nafees As a Philosopher, Encyclopedia of Islamic World).
- ^ (英文)Eknoyan G. Santorio Sanctorius (1561–1636) - founding father of metabolic balance studies. Am J Nephrol. 1999, 19 (2): 226–33. PMID 10213823.
- ^ (英文)Williams, H. S. (1904) A History of Science: in Five Volumes. Volume IV: Modern Development of the Chemical and Biological Sciences Harper and Brothers (New York) 2008年6月29日查阅
- ^ (英文)Dubos J. Louis Pasteur: Free Lance of Science, Gollancz. Quoted in Manchester K. L. (1995) Louis Pasteur (1822 – 1895)—chance and the prepared mind.. Trends Biotechnol. 1951, 13 (12): 511–515. PMID 8595136.
- ^ (英文)Kinne-Saffran E, Kinne R. Vitalism and synthesis of urea. From Friedrich Wöhler to Hans A. Krebs. Am J Nephrol. 1999, 19 (2): 290–4. PMID 10213830.
- ^ (英文)爱德华·比希纳在1907年诺贝尔颁奖典礼上的演讲,2008年6月29日查阅
- ^ (英文)Kornberg H. Krebs and his trinity of cycles. Nat Rev Mol Cell Biol. 2000, 1 (3): 225–8. PMID 11252898.
- ^ (英文)Krebs H A, Henseleit K (1932) "Untersuchungen über die Harnstoffbildung im tierkorper." Z. Physiol. Chem. 210, 33 – 66. Krebs H, Johnson W. Metabolism of ketonic acids in animal tissues. Biochem J. 1937, 31 (4): 645–60. PMID 16746382.
- ^ 13.0 13.1 (英文)Kornberg H, Krebs H. Synthesis of cell constituents from C2-units by a modified tricarboxylic acid cycle. Nature. 1957, 179 (4568): 988–91. PMID 13430766.
- ^ (英文)Michie K, Löwe J. Dynamic filaments of the bacterial cytoskeleton. Annu Rev Biochem. 2006, 75: 467–92. PMID 16756499.
- ^ 15.0 15.1 15.2 15.3 15.4 15.5 (英文)Nelson, David L.; Michael M. Cox. Lehninger Principles of Biochemistry. New York: W. H. Freeman and company. 2005: 841. ISBN 0-7167-4339-6. 引证错误:带有name属性“Nelson”的
<ref>标签用不同内容定义了多次 - ^ (英文)Fahy E, Subramaniam S, Brown H, Glass C, Merrill A, Murphy R, Raetz C, Russell D, Seyama Y, Shaw W, Shimizu T, Spener F, van Meer G, VanNieuwenhze M, White S, Witztum J, Dennis E. A comprehensive classification system for lipids. J Lipid Res. 2005, 46 (5): 839–61. PMID 15722563.
- ^ (英文)Nomenclature of Lipids. IUPAC-IUB Commission on Biochemical Nomenclature (CBN). [2007-03-08].
- ^ (英文)Hegardt F. Mitochondrial 3-hydroxy-3-methylglutaryl-CoA synthase: a control enzyme in ketogenesis. Biochem J. 1999,. 338 (Pt 3): 569–82. PMID 10051425.
- ^ (英文)Raman R, Raguram S, Venkataraman G, Paulson J, Sasisekharan R. Glycomics: an integrated systems approach to structure-function relationships of glycans. Nat Methods. 2005, 2 (11): 817–24. PMID 16278650.
- ^ (英文)Sierra S, Kupfer B, Kaiser R. Basics of the virology of HIV-1 and its replication. J Clin Virol. 2005, 34 (4): 233–44. PMID 16198625.
- ^ 21.0 21.1 (英文)Wimmer M, Rose I. Mechanisms of enzyme-catalyzed group transfer reactions. Annu Rev Biochem. 1978, 47: 1031–78. PMID 354490.
- ^ (英文)Mitchell P. The Ninth Sir Hans Krebs Lecture. Compartmentation and communication in living systems. Ligand conduction: a general catalytic principle in chemical, osmotic and chemiosmotic reaction systems. Eur J Biochem. 1979, 95 (1): 1–20. PMID 378655.
- ^ 23.0 23.1 23.2 23.3 (英文)Dimroth P, von Ballmoos C, Meier T. Catalytic and mechanical cycles in F-ATP synthases. Fourth in the Cycles Review Series. EMBO Rep. 2006, 7 (3): 276–82. PMID 16607397.
- ^ (英文)Coulston, Ann; Kerner, John; Hattner, JoAnn; Srivastava, Ashini, Nutrition Principles and Clinical Nutrition, Stanford School of Medicine Nutrition Courses, SUMMIT, 2006
- ^ (英文)Pollak N, Dölle C, Ziegler M. The power to reduce: pyridine nucleotides—small molecules with a multitude of functions. Biochem J. 2007, 402 (2): 205–18. PMID 17295611.
- ^ 26.0 26.1 (英文)Heymsfield S, Waki M, Kehayias J, Lichtman S, Dilmanian F, Kamen Y, Wang J, Pierson R. Chemical and elemental analysis of humans in vivo using improved body composition models. Am J Physiol. 1991, 261 (2 Pt 1): E190–8. PMID 1872381.
- ^ (英文)Sychrová H. Yeast as a model organism to study transport and homeostasis of alkali metal cations (PDF). Physiol Res. 2004,. 53 Suppl 1: S91–8. PMID 15119939.
- ^ (英文)Levitan I. Modulation of ion channels in neurons and other cells. Annu Rev Neurosci. 1988, 11: 119–36. PMID 2452594.
- ^ (英文)Dulhunty A. Excitation-contraction coupling from the 1950s into the new millennium. Clin Exp Pharmacol Physiol. 2006, 33 (9): 763–72. PMID 16922804.
- ^ (英文)Mahan D, Shields R. Macro- and micromineral composition of pigs from birth to 145 kilograms of body weight. J Anim Sci. 1998, 76 (2): 506–12. PMID 9498359.
- ^ (英文)Husted S, Mikkelsen B, Jensen J, Nielsen N. Elemental fingerprint analysis of barley (Hordeum vulgare) using inductively coupled plasma mass spectrometry, isotope-ratio mass spectrometry, and multivariate statistics. Anal Bioanal Chem. 2004, 378 (1): 171–82. PMID 14551660.
- ^ (英文)Finney L, O'Halloran T. Transition metal speciation in the cell: insights from the chemistry of metal ion receptors. Science. 2003, 300 (5621): 931–6. PMID 12738850.
- ^ (英文)Cousins R, Liuzzi J, Lichten L. Mammalian zinc transport, trafficking, and signals. J Biol Chem. 2006, 281 (34): 24085–9. PMID 16793761.
- ^ (英文)Dunn L, Rahmanto Y, Richardson D. Iron uptake and metabolism in the new millennium. Trends Cell Biol. 2007, 17 (2): 93–100. PMID 17194590.
- ^ (英文)Nealson K, Conrad P. Life: past, present and future. Philos Trans R Soc Lond B Biol Sci. 1999, 354 (1392): 1923–39. PMID 10670014.
- ^ (英文)Häse C, Finkelstein R. Bacterial extracellular zinc-containing metalloproteases. Microbiol Rev. 1993, 57 (4): 823–37. PMID 8302217.
- ^ (英文)Gupta R, Gupta N, Rathi P. Bacterial lipases: an overview of production, purification and biochemical properties. Appl Microbiol Biotechnol. 2004, 64 (6): 763–81. PMID 14966663.
- ^ (英文)Hoyle T. The digestive system: linking theory and practice. Br J Nurs. 1997, 6 (22): 1285–91. PMID 9470654.
- ^ (英文)Souba W, Pacitti A. How amino acids get into cells: mechanisms, models, menus, and mediators. JPEN J Parenter Enteral Nutr. 1992, 16 (6): 569–78. PMID 1494216.
- ^ (英文)Barrett M, Walmsley A, Gould G. Structure and function of facilitative sugar transporters. Curr Opin Cell Biol. 1999, 11 (4): 496–502. PMID 10449337.
- ^ (英文)Bell G, Burant C, Takeda J, Gould G. Structure and function of mammalian facilitative sugar transporters. J Biol Chem. 1993, 268 (26): 19161–4. PMID 8366068.
- ^ 42.0 42.1 (英文)Bouché C, Serdy S, Kahn C, Goldfine A. The cellular fate of glucose and its relevance in type 2 diabetes. Endocr Rev. 2004, 25 (5): 807–30. PMID 15466941.
- ^ (英文)Sakami W, Harrington H. Amino acid metabolism. Annu Rev Biochem. 1963, 32: 355–98. PMID 14144484.
- ^ (英文)Brosnan J. Glutamate, at the interface between amino acid and carbohydrate metabolism. J Nutr. 2000, 130 (4S Suppl): 988S–90S. PMID 10736367.
- ^ (英文)Young V, Ajami A. Glutamine: the emperor or his clothes?. J Nutr. 2001, 131 (9 Suppl): 2449S–59S; discussion 2486S–7S. PMID 11533293.
- ^ (英文)Hosler J, Ferguson-Miller S, Mills D. Energy transduction: proton transfer through the respiratory complexes. Annu Rev Biochem. 2006, 75: 165–87. PMID 16756489.
- ^ (英文)Schultz B, Chan S. Structures and proton-pumping strategies of mitochondrial respiratory enzymes. Annu Rev Biophys Biomol Struct. 2001, 30: 23–65. PMID 11340051.
- ^ (英文)Capaldi R, Aggeler R. Mechanism of the F(1)F(0)-type ATP synthase, a biological rotary motor. Trends Biochem Sci. 2002, 27 (3): 154–60. PMID 11893513.
- ^ (英文)Friedrich B, Schwartz E. Molecular biology of hydrogen utilization in aerobic chemolithotrophs. Annu Rev Microbiol. 1993, 47: 351–83. PMID 8257102.
- ^ (英文)Friedrich C. Physiology and genetics of sulfur-oxidizing bacteria. Adv Microb Physiol. 1998, 39: 235–89. PMID 9328649.
- ^ (英文)Weber K, Achenbach L, Coates J. Microorganisms pumping iron: anaerobic microbial iron oxidation and reduction. Nat Rev Microbiol. 2006, 4 (10): 752–64. PMID 16980937.
- ^ (英文)Jetten M, Strous M, van de Pas-Schoonen K, Schalk J, van Dongen U, van de Graaf A, Logemann S, Muyzer G, van Loosdrecht M, Kuenen J. The anaerobic oxidation of ammonium. FEMS Microbiol Rev. 1998, 22 (5): 421–37. PMID 9990725.
- ^ (英文)Simon J. Enzymology and bioenergetics of respiratory nitrite ammonification. FEMS Microbiol Rev. 2002, 26 (3): 285–309. PMID 12165429.
- ^ (英文)Conrad R. Soil microorganisms as controllers of atmospheric trace gases (H2, CO, CH4, OCS, N2O, and NO). Microbiol Rev. 1996, 60 (4): 609–40. PMID 8987358.
- ^ (英文)Barea J, Pozo M, Azcón R, Azcón-Aguilar C. Microbial co-operation in the rhizosphere. J Exp Bot. 2005, 56 (417): 1761–78. PMID 15911555.
- ^ (英文)van der Meer M, Schouten S, Bateson M, Nübel U, Wieland A, Kühl M, de Leeuw J, Sinninghe Damsté J, Ward D. Diel variations in carbon metabolism by green nonsulfur-like bacteria in alkaline siliceous hot spring microbial mats from Yellowstone National Park. Appl Environ Microbiol. 2005, 71 (7): 3978–86. PMID 16000812.
- ^ (英文)Tichi M, Tabita F. Interactive control of Rhodobacter capsulatus redox-balancing systems during phototrophic metabolism. J Bacteriol. 2001, 183 (21): 6344–54. PMID 11591679.
- ^ Allen J, Williams J. Photosynthetic reaction centers. FEBS Lett. 1998, 438 (1–2): 5–9. PMID 9821949.
- ^ (英文)Nelson N, Ben-Shem A. The complex architecture of oxygenic photosynthesis. Nat Rev Mol Cell Biol. 2004, 5 (12): 971–82. PMID 15573135.
- ^ (英文)Munekage Y, Hashimoto M, Miyake C, Tomizawa K, Endo T, Tasaka M, Shikanai T. Cyclic electron flow around photosystem I is essential for photosynthesis. Nature. 2004, 429 (6991): 579–82. PMID 15175756.
- ^ (英文)Miziorko H, Lorimer G. Ribulose-1,5-bisphosphate carboxylase-oxygenase. Annu Rev Biochem. 1983, 52: 507–35. PMID 6351728.
- ^ (英文)Dodd A, Borland A, Haslam R, Griffiths H, Maxwell K. Crassulacean acid metabolism: plastic, fantastic. J Exp Bot. 2002, 53 (369): 569–80. PMID 11886877.
- ^ (英文)Hügler M, Wirsen C, Fuchs G, Taylor C, Sievert S. Evidence for autotrophic CO2 fixation via the reductive tricarboxylic acid cycle by members of the epsilon subdivision of proteobacteria. J Bacteriol. 2005, 187 (9): 3020–7. PMID 15838028.
- ^ (英文)Strauss G, Fuchs G. Enzymes of a novel autotrophic CO2 fixation pathway in the phototrophic bacterium Chloroflexus aurantiacus, the 3-hydroxypropionate cycle. Eur J Biochem. 1993, 215 (3): 633–43. PMID 8354269.
- ^ (英文)Wood H. Life with CO or CO2 and H2 as a source of carbon and energy. FASEB J. 1991, 5 (2): 156–63. PMID 1900793.
- ^ (英文)Shively J, van Keulen G, Meijer W. Something from almost nothing: carbon dioxide fixation in chemoautotrophs. Annu Rev Microbiol. 1998, 52: 191–230. PMID 9891798.
- ^ (英文)Boiteux A, Hess B. Design of glycolysis. Philos Trans R Soc Lond B Biol Sci. 1981, 293 (1063): 5–22. PMID 6115423.
- ^ (英文)Pilkis S, el-Maghrabi M, Claus T. Fructose-2,6-bisphosphate in control of hepatic gluconeogenesis. From metabolites to molecular genetics. Diabetes Care. 1990, 13 (6): 582–99. PMID 2162755.
- ^ 69.0 69.1 (英文)Ensign S. Revisiting the glyoxylate cycle: alternate pathways for microbial acetate assimilation. Mol Microbiol. 2006, 61 (2): 274–6. PMID 16856935.
- ^ (英文)Finn P, Dice J. Proteolytic and lipolytic responses to starvation. Nutrition. 2006, 22 (7–8): 830–44. PMID 16815497.
- ^ (英文)Rademacher T, Parekh R, Dwek R. Glycobiology. Annu Rev Biochem. 1988, 57: 785–838. PMID 3052290.
- ^ (英文)Opdenakker G, Rudd P, Ponting C, Dwek R. Concepts and principles of glycobiology. FASEB J. 1993, 7 (14): 1330–7. PMID 8224606.
- ^ (英文)McConville M, Menon A. Recent developments in the cell biology and biochemistry of glycosylphosphatidylinositol lipids (review). Mol Membr Biol. 2000, 17 (1): 1–16. PMID 10824734.
- ^ (英文)Chirala S, Wakil S. Structure and function of animal fatty acid synthase. Lipids. 2004, 39 (11): 1045–53. PMID 15726818.
- ^ (英文)White S, Zheng J, Zhang Y. The structural biology of type II fatty acid biosynthesis. Annu Rev Biochem. 2005, 74: 791–831. PMID 15952903.
- ^ (英文)Ohlrogge J, Jaworski J. Regulation of fatty acid synthesis. Annu Rev Plant Physiol Plant Mol Biol. 1997, 48: 109–136. PMID 15012259.
- ^ (英文)Dubey V, Bhalla R, Luthra R. An overview of the non-mevalonate pathway for terpenoid biosynthesis in plants (PDF). J Biosci. 2003, 28 (5): 637–46. PMID 14517367.
- ^ 78.0 78.1 (英文)Kuzuyama T, Seto H. Diversity of the biosynthesis of the isoprene units. Nat Prod Rep. 2003, 20 (2): 171–83. PMID 12735695.
- ^ (英文)Grochowski L, Xu H, White R. Methanocaldococcus jannaschii uses a modified mevalonate pathway for biosynthesis of isopentenyl diphosphate. J Bacteriol. 2006, 188 (9): 3192–8. PMID 16621811.
- ^ (英文)Lichtenthaler H. The 1-Ddeoxy-D-xylulose-5-phosphate pathway of isoprenoid biosynthesis in plants. Annu Rev Plant Physiol Plant Mol Biol. 1999, 50: 47–65. PMID 15012203.
- ^ 81.0 81.1 (英文)Schroepfer G. Sterol biosynthesis. Annu Rev Biochem. 1981, 50: 585–621. PMID 7023367.
- ^ (英文)Lees N, Skaggs B, Kirsch D, Bard M. Cloning of the late genes in the ergosterol biosynthetic pathway of Saccharomyces cerevisiae—a review. Lipids. 1995, 30 (3): 221–6. PMID 7791529.
- ^ (英文)Guyton, Arthur C.; John E. Hall. Textbook of Medical Physiology. Philadelphia: Elsevier. 2006: 855–6. ISBN 0-7216-0240-1.
- ^ (英文)Ibba M, Söll D. The renaissance of aminoacyl-tRNA synthesis. EMBO Rep. 2001, 2 (5): 382–7. PMID 11375928.
- ^ (英文)Lengyel P, Söll D. Mechanism of protein biosynthesis. Bacteriol Rev. 1969, 33 (2): 264–301. PMID 4896351.
- ^ 86.0 86.1 (英文)Rudolph F. The biochemistry and physiology of nucleotides. J Nutr. 1994, 124 (1 Suppl): 124S–127S. PMID 8283301. Zrenner R, Stitt M, Sonnewald U, Boldt R. Pyrimidine and purine biosynthesis and degradation in plants. Annu Rev Plant Biol. 2006, 57: 805–36. PMID 16669783.
- ^ (英文)Stasolla C, Katahira R, Thorpe T, Ashihara H. Purine and pyrimidine nucleotide metabolism in higher plants. J Plant Physiol. 2003, 160 (11): 1271–95. PMID 14658380.
- ^ (英文)Smith J. Enzymes of nucleotide synthesis. Curr Opin Struct Biol. 1995, 5 (6): 752–7. PMID 8749362.
- ^ (英文)Testa B, Krämer S. The biochemistry of drug metabolism—an introduction: part 1. Principles and overview. Chem Biodivers. 2006, 3 (10): 1053–101. PMID 17193224.
- ^ (英文)Danielson P. The cytochrome P450 superfamily: biochemistry, evolution and drug metabolism in humans. Curr Drug Metab. 2002, 3 (6): 561–97. PMID 12369887.
- ^ (英文)King C, Rios G, Green M, Tephly T. UDP-glucuronosyltransferases. Curr Drug Metab. 2000, 1 (2): 143–61. PMID 11465080.
- ^ (英文)Sheehan D, Meade G, Foley V, Dowd C. Structure, function and evolution of glutathione transferases: implications for classification of non-mammalian members of an ancient enzyme superfamily. Biochem J. 2001, 360 (Pt 1): 1–16. PMID 11695986.
- ^ (英文)Galvão T, Mohn W, de Lorenzo V. Exploring the microbial biodegradation and biotransformation gene pool. Trends Biotechnol. 2005, 23 (10): 497–506. PMID 16125262.
- ^ (英文)Janssen D, Dinkla I, Poelarends G, Terpstra P. Bacterial degradation of xenobiotic compounds: evolution and distribution of novel enzyme activities. Environ Microbiol. 2005, 7 (12): 1868–82. PMID 16309386.
- ^ (英文)Davies K. Oxidative stress: the paradox of aerobic life. Biochem Soc Symp. 1995, 61: 1–31. PMID 8660387.
- ^ (英文)Tu B, Weissman J. Oxidative protein folding in eukaryotes: mechanisms and consequences. J Cell Biol. 2004, 164 (3): 341–6. PMID 14757749.
- ^ (英文)Sies H. Oxidative stress: oxidants and antioxidants (PDF). Exp Physiol. 1997, 82 (2): 291–5. PMID 9129943.
- ^ (英文)Vertuani S, Angusti A, Manfredini S. The antioxidants and pro-antioxidants network: an overview. Curr Pharm Des. 2004, 10 (14): 1677–94. PMID 15134565.
- ^ (英文)von Stockar U, Liu J. Does microbial life always feed on negative entropy? Thermodynamic analysis of microbial growth. Biochim Biophys Acta. 1999, 1412 (3): 191–211. PMID 10482783.
- ^ (英文)Demirel Y, Sandler S. Thermodynamics and bioenergetics. Biophys Chem. 2002, 97 (2–3): 87–111. PMID 12050002.
- ^ (英文)Albert R. Scale-free networks in cell biology. J Cell Sci. 2005, 118 (Pt 21): 4947–57. PMID 16254242.
- ^ (英文)Brand M. Regulation analysis of energy metabolism. J Exp Biol. 1997, 200 (Pt 2): 193–202. PMID 9050227.
- ^ (英文)Soyer O, Salathé M, Bonhoeffer S. Signal transduction networks: topology, response and biochemical processes. J Theor Biol. 2006, 238 (2): 416–25. PMID 16045939.
- ^ 104.0 104.1 (英文)Salter M, Knowles R, Pogson C. Metabolic control. Essays Biochem. 1994, 28: 1–12. PMID 7925313.
- ^ (英文)Westerhoff H, Groen A, Wanders R. Modern theories of metabolic control and their applications (review). Biosci Rep. 1984, 4 (1): 1–22. PMID 6365197.
- ^ (英文)Fell D, Thomas S. Physiological control of metabolic flux: the requirement for multisite modulation. Biochem J. 1995,. 311 (Pt 1): 35–9. PMID 7575476.
- ^ (英文)Hendrickson W. Transduction of biochemical signals across cell membranes. Q Rev Biophys. 2005, 38 (4): 321–30. PMID 16600054.
- ^ (英文)Cohen P. The regulation of protein function by multisite phosphorylation—a 25 year update. Trends Biochem Sci. 2000, 25 (12): 596–601. PMID 11116185.
- ^ (英文)Lienhard G, Slot J, James D, Mueckler M. How cells absorb glucose. Sci Am. 1992, 266 (1): 86–91. PMID 1734513.
- ^ (英文)Roach P. Glycogen and its metabolism. Curr Mol Med. 2002, 2 (2): 101–20. PMID 11949930.
- ^ (英文)Newgard C, Brady M, O'Doherty R, Saltiel A. Organizing glucose disposal: emerging roles of the glycogen targeting subunits of protein phosphatase-1 (PDF). Diabetes. 2000, 49 (12): 1967–77. PMID 11117996.
- ^ (英文)Romano A, Conway T. Evolution of carbohydrate metabolic pathways. Res Microbiol. 1996, 147 (6–7): 448–55. PMID 9084754.
- ^ (英文)Koch A. How did bacteria come to be?. Adv Microb Physiol. 1998, 40: 353–99. PMID 9889982.
- ^ (英文)Ouzounis C, Kyrpides N. The emergence of major cellular processes in evolution. FEBS Lett. 1996, 390 (2): 119–23. PMID 8706840.
- ^ (英文)Caetano-Anolles G, Kim HS, Mittenthal JE. The origin of modern metabolic networks inferred from phylogenomic analysis of protein architecture. Proc Natl Acad Sci USA. 2007, 104 (22): 9358–63. PMID 17517598.
- ^ (英文)Schmidt S, Sunyaev S, Bork P, Dandekar T. Metabolites: a helping hand for pathway evolution?. Trends Biochem Sci. 2003, 28 (6): 336–41. PMID 12826406.
- ^ (英文)Light S, Kraulis P. Network analysis of metabolic enzyme evolution in Escherichia coli. BMC Bioinformatics. 2004, 5: 15. PMID 15113413.
- ^ (英文)Alves R, Chaleil R, Sternberg M. Evolution of enzymes in metabolism: a network perspective. J Mol Biol. 2002, 320 (4): 751–70. PMID 12095253.
- ^ (英文)Kim HS, Mittenthal JE, Caetano-Anolles G. MANET: tracing evolution of protein architecture in metabolic networks. BMC Bioinformatics. 2006, 19 (7): 351. PMID 16854231.
- ^ (英文)Teichmann SA, Rison SC, Thornton JM, Riley M, Gough J, Chothia C. Small-molecule metabolsim: an enzyme mosaic. Trends Biotechnol. 2001, 19 (12): 482–6. PMID 11711174.
- ^ (英文)Spirin V, Gelfand M, Mironov A, Mirny L. A metabolic network in the evolutionary context: multiscale structure and modularity. Proc Natl Acad Sci U S A. 2006, 103 (23): 8774–9. PMID 16731630.
- ^ (英文)Lawrence J. Common themes in the genome strategies of pathogens. Curr Opin Genet Dev. 2005, 15 (6): 584–8. PMID 16188434.
- ^ (英文)Wernegreen J. For better or worse: genomic consequences of intracellular mutualism and parasitism. Curr Opin Genet Dev. 2005, 15 (6): 572–83. PMID 16230003.
- ^ (英文)Pál C, Papp B, Lercher M, Csermely P, Oliver S, Hurst L. Chance and necessity in the evolution of minimal metabolic networks. Nature. 2006, 440 (7084): 667–70. PMID 16572170.
- ^ (英文)Rennie M. An introduction to the use of tracers in nutrition and metabolism. Proc Nutr Soc. 1999, 58 (4): 935–44. PMID 10817161.
- ^ (英文)Phair R. Development of kinetic models in the nonlinear world of molecular cell biology. Metabolism. 1997, 46 (12): 1489–95. PMID 9439549.
- ^ (英文)Borodina I, Nielsen J. From genomes to in silico cells via metabolic networks. Curr Opin Biotechnol. 2005, 16 (3): 350–5. PMID 15961036.
- ^ (英文)Gianchandani E, Brautigan D, Papin J. Systems analyses characterize integrated functions of biochemical networks. Trends Biochem Sci. 2006, 31 (5): 284–91. PMID 16616498.
- ^ (英文)Duarte NC, Becker SA, Jamshidi N; et al. Global reconstruction of the human metabolic network based on genomic and bibliomic data. Proc. Natl. Acad. Sci. U.S.A. 2007, 104 (6): 1777–82. PMID 17267599. doi:10.1073/pnas.0610772104. 已忽略未知参数
|month=(建议使用|date=) (帮助) - ^ (英文)Thykaer J, Nielsen J. Metabolic engineering of beta-lactam production. Metab Eng. 2003, 5 (1): 56–69. PMID 12749845.
- ^ (英文)González-Pajuelo M, Meynial-Salles I, Mendes F, Andrade J, Vasconcelos I, Soucaille P. Metabolic engineering of Clostridium acetobutylicum for the industrial production of 1,3-propanediol from glycerol. Metab Eng. 2005, 7 (5–6): 329–36. PMID 16095939.
- ^ (英文)Krämer M, Bongaerts J, Bovenberg R, Kremer S, Müller U, Orf S, Wubbolts M, Raeven L. Metabolic engineering for microbial production of shikimic acid. Metab Eng. 2003, 5 (4): 277–83. PMID 14642355.
- ^ (英文)Koffas M, Roberge C, Lee K, Stephanopoulos G. Metabolic engineering. Annu Rev Biomed Eng. 1999, 1: 535–57. PMID 11701499.
延伸阅读
入门级
- (英文)Rose, S. and Mileusnic, R., The Chemistry of Life. (Penguin Press Science, 1999), ISBN 0-14027-273-9
- (英文)Schneider, E. D. and Sagan, D., Into the Cool: Energy Flow, Thermodynamics, and Life. (University Of Chicago Press, 2005), ISBN 0-22673-936-8
- (英文)Lane, N., Oxygen: The Molecule that Made the World. (Oxford University Press, USA, 2004), ISBN 0-19860-783-0
进阶级
- (英文)Price, N. and Stevens, L., Fundamentals of Enzymology: Cell and Molecular Biology of Catalytic Proteins. (Oxford University Press, 1999), ISBN 0-19850-229-X
- (英文)Berg, J. Tymoczko, J. and Stryer, L., Biochemistry. (W. H. Freeman and Company, 2002), ISBN 0-71674-955-6
- (英文)Cox, M. and Nelson, D. L., Lehninger Principles of Biochemistry. (Palgrave Macmillan, 2004), ISBN 0-71674-339-6
- (英文)Brock, T. D. Madigan, M. T. Martinko, J. and Parker J., Brock's Biology of Microorganisms. (Benjamin Cummings, 2002), ISBN 0-13066-271-2
- (英文)Da Silva, J.J.R.F. and Williams, R. J. P., The Biological Chemistry of the Elements: The Inorganic Chemistry of Life. (Clarendon Press, 1991), ISBN 0-19855-598-9
- (英文)Nicholls, D. G. and Ferguson, S. J., Bioenergetics. (Academic Press Inc., 2002), ISBN 0-12518-121-3
外部链接
一般性介绍
- (英文)代谢、呼吸作用和光合作用
- (中文)能量获得与转换,现代生命科学导论
- (英文)代谢中的生物化学
- (英文)高级动物代谢计算器/互动式学习工具
- (英文)微生物代谢
- (英文)生物化学中的代谢途径
- (英文)生物学家的化学
- (英文)Sparknotes SAT 生物化学
- (英文)MIT生物在线书籍
- (英文)Encyclopœdia Britannica上关于代谢的文章
词汇表和词典
人体代谢
- (英文)医学生物化学中的话题
- (英文)医学生物化学
数据库
- (英文)BioCyc Collection上的基因组和通路数据库
- (英文)代谢途径流程图
- (英文)KEGG通路数据库
- (英文)IUBMB-Nicholson代谢通路图
- (英文)Reactome生物进程数据库
代谢途径
- (英文)Interactive 主要代谢通路的流程图
- (英文)糖酵解
- (英文)光合作用
- (英文)什么是光合作用
- (中文)糖、脂、氨基酸代谢途径间的相互联系
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 糖类 | ||
|---|---|---|
| 酯質 | ||
| 核酸 | ||
| 蛋白質 | ||
| 其他 | ||
